HPLC法测定金酸萍颗粒中蒽醌类成分的含量
杜继权 吴春玲 张志君
【摘 要】 目的:建立中成药金酸萍颗粒中大黄素、大黄酚、大黄素甲醚3种蒽醌类成分的HPLC含量测定方法。方法:采用Thermo Hypersill GOLD C18色谱柱(4.6 mm×250 mm,5 μm); 流动相为甲醇-0.1%磷酸水溶液液(85∶15);流速为1.0 mL/min;检测波长选择254 nm;柱温在25 ℃。结果:大黄素、大黄酚以及大黄素甲醚分别在相应的浓度范围内与峰面积的线性关系均良好(r≥0.9999);平均加样回收率分别为96.12%、104.22%和97.41%,RSD分别为2.47%、1.57%和1.96% 。结论:本方法操作方便、准确、重现性好,可用于金酸萍颗粒的质量控制。
【关键词】 金酸萍颗粒;蒽醌类成分;HPLC
【中图分类号】R284.1 【文献标志码】 A 【文章编号】1007-8517(2021)21-0028-04
Determination of Anthraquinones in Jinsuanping Granules by HPLC
DU Jiquan WU Chunling ZHANG Zhijun*
School of Pharmacy, Hubei University of Science and Technology, Xianning 437100, China
Abstract:Objective An HPLC method was established for the simultaneous determination of three anthraquinones (emodin, chrysophanol and physcion) in Jinsuanping Granules (Siphonostegiae Herba, Rumicis acetosae Radix, Marsileae Herba).Method The Thermo Hypersill GOLD(4.6 mm×250 mm,5 μm)was adopted and the mobile phase was methanol-0.1% phosphoric acid aqueous solution(85∶15,V/V) with a flow rate at 1.0mL/min. The detection wavelength was set at 254 nm and the column temperature was kept at 25 ℃.Results Emodin, chrysophanol and physcion showed a good linear relationship with peak areas in the corresponding concentration range ( r≥0.9999 ). Whose average recovery rates were 96.12%, 104.22% and 97.41%, respectively, and the RSD was 2.47%,1.57% and 1.96%, respectively.Conclusion It’s a convenient, accurate and reproducible method , and can be used to control the quality of Jinsuanping Granules.
Key words:Jinsuanping Granules; Anthraquinone; HPLC
中成藥金酸萍颗粒由北刘寄奴(Siphonostegia chinensis Benth.)、酸模(Rumex acetosa L.)、萍(Marsilea quadrifolia L.)3味药组成,具有清热解毒、利湿退黄的功效[1],主要用于治疗急性黄疸型、慢性、重症等类型肝炎,有降低转氨酶、恢复肝功能的作用[2-4]。方中臣药酸模,系蓼科酸模属植物,在我国广泛分布,民间作“土大黄”使用,根主要含有大黄素型蒽醌类化合物,具有清热解毒、凉血止血之功[5-7]。
金酸萍颗粒标准WS3-B-1561-93收载于部颁标准(中药成方制剂第八册),原标准只对性状、酸模的薄层鉴别和通则进行检测[8],而无含量测定项,不能全面反映酸模质量。因此,金酸萍颗粒中3个蒽醌类成分的定量测定方法的建立,为金酸萍颗粒的质量标准修订与提高提供依据,更好的控制金酸萍颗粒的质量。
1 仪器与试药
1.1 仪器 北京清博华LC300型高效液相色谱仪,UV检测器;Hypersill GOLD C18柱(4.6 mm×250 mm,5 μm);超声波清洗器(上海船舶电子设备研究所 );GWP十万分之一分析天平(型号:XS105DU)。
1.2 试药 大黄素对照品(批号:110756-201512)、大黄酚对照品(批号:110757-201607)和大黄素甲醚对照品(批号:110758-201817)均购自中国食品药品检定研究院;金酸萍颗粒(批号:20190204,20200707,20200901,20201001,20201002,20201003,20201004,20201005,20201101,20201102,20201103)和缺酸模的阴性样品均由湖北福人金身药业有限公司提供;甲醇为色谱级(天津欧博凯化工有限公司);实验用水为CM-RO-C2型超纯水机制水,其它试剂为分析纯。
2 方法与结果
2.1 色谱条件 色谱柱: Hypersill GOLD C18柱(4.6mm×250 mm,5 μm);流动相为甲醇(A):0.1%磷酸水溶液(B)=85∶15;流速为:1.0mL/min;UV:254 nm;柱温控制在25 ℃;进样体积20 μL。所检测成分理论塔板数不低于5000。
2.2 溶液的制备 对照品溶液:分别精密称得适量上述对照品于量瓶,加甲醇溶解并定容,得对照品贮备液,4 ℃避光保存。精密移取1.25 mL贮备液于10mL棕色量瓶,定容得浓度为大黄素20 μg/mL、大黄酚9 μg/mL以及大黄素甲醚16 μg/mL的对照品溶液。
供试品溶液:精准称取金酸萍颗粒粉末1 g到具塞锥形瓶中,加25 mL甲醇,超声提取30 min,放冷后用甲醇补重,取5 mL续滤液水浴蒸干,然后依次加入水10 mL、浓盐酸2 mL及二氯甲烷10 mL,热回流水解30 min,待冷确后倒到60 mL分液漏斗中,用少量二氯甲烷洗涤2次,并入分液漏斗中,静置后分取二氯甲烷层,酸液再以二氯甲烷萃取,共2次,每次10 mL,合并并回收二氯甲烷,残渣加适量甲醇溶解,转到10 mL量瓶定容,即得[10-12]。
阴性样品溶液:取阴性样品,其制备操作与供试品处理方法相同,即得。
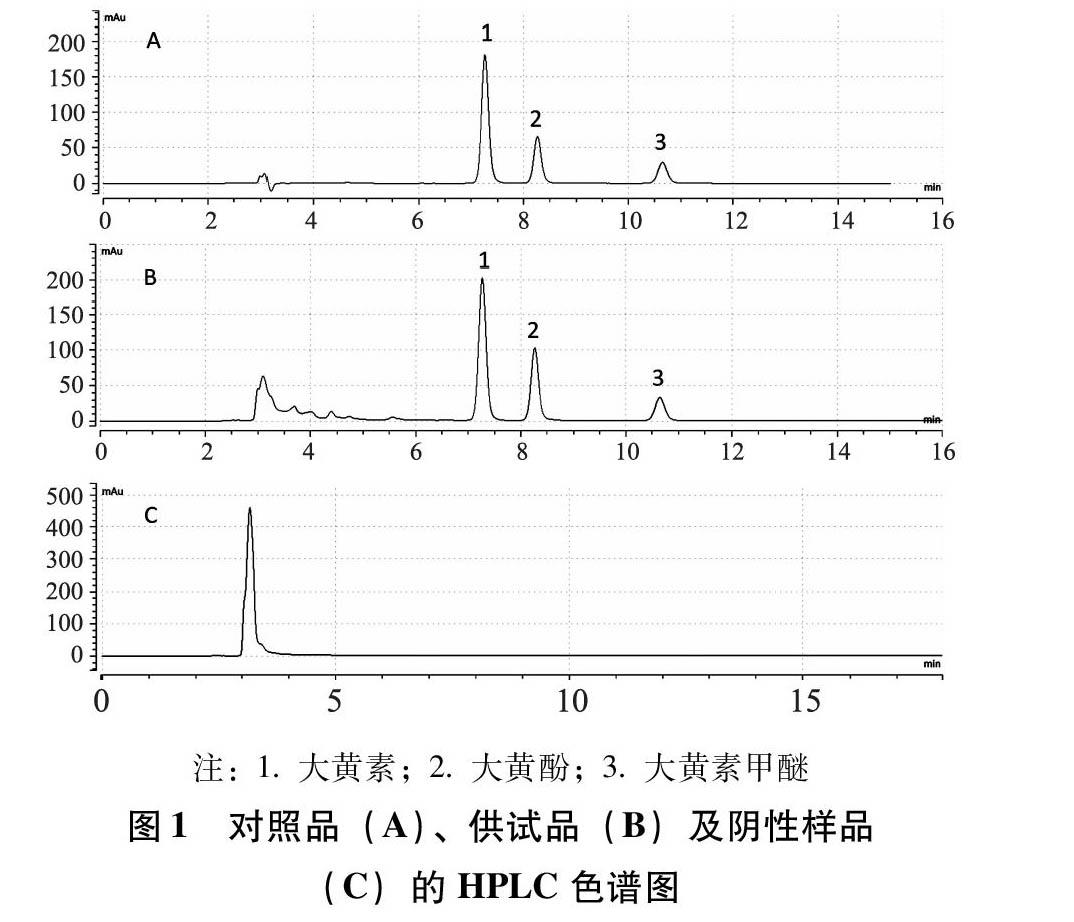
2.3 专属性试验 取“2.2”项下制备的三种溶液,照“2.1”项下条件采集色谱图,结果见图1。由图1可知,在既定色谱条件下, A和B中3个色谱峰的保留时间均能相对应,而C在相应的时间未出峰,说明专属性较强。
2.4 线性关系考察 取6个10 mL棕色量瓶,移液枪依次准确加入0.3125 mL、0.625 mL、1.25mL、2.5 mL、3.75 mL、5 mL对照品贮备液,用甲醇稀释至刻度线,得到6个不同浓度的对照品溶液。在“2.1”项色谱条件下,浓度从低到高依次测定,并对其数据处理。峰面积为Y轴,浓度(μg/mL)为X轴,得到3个成分的标准曲线:大黄素y=82.6569x+36.4847,r=1.0000;大黄酚y=142.3478x+18.1365,r=1.0000;大黄素甲醚y=22.9311x+11.4092,r=0.9999。3个成分依次在5~80 μg/mL, 2.25~36 μg/mL和4~64 μg/mL与峰响应值相关性良好。
2.5 仪器精密度试验 精密吸取20 μL对照品溶液,依“2.1”色谱条件,重复进样6次测定3个成分的峰面积,并计算得大黄素、大黄酚、大黄素甲醚峰面积的RSD分别为0.93%、1.13%和0.61%,说明该仪器精密度较好。
2.6 重复性试验 按“2.2”项制备6份供试品溶液(批号:20190204),照“2.1”项色谱条件,采集峰面积,计算得大黄素、大黄酚、大黄素甲醚含量的RSD分别为1.29%、1.96%、0.88%,表明该法重复性良好。
2.7 稳定性试验 取同一供试品溶液(样品批号:20190204),以“2.1”项色谱条件下,在0~24 h每隔一段时间测定大黄素、大黄酚、大黄素甲醚的峰面积,并计算峰面积的RSD(n=6)分别为0.71%、0.83%、1.14%,表明在24 h内供试品溶液比较稳定。
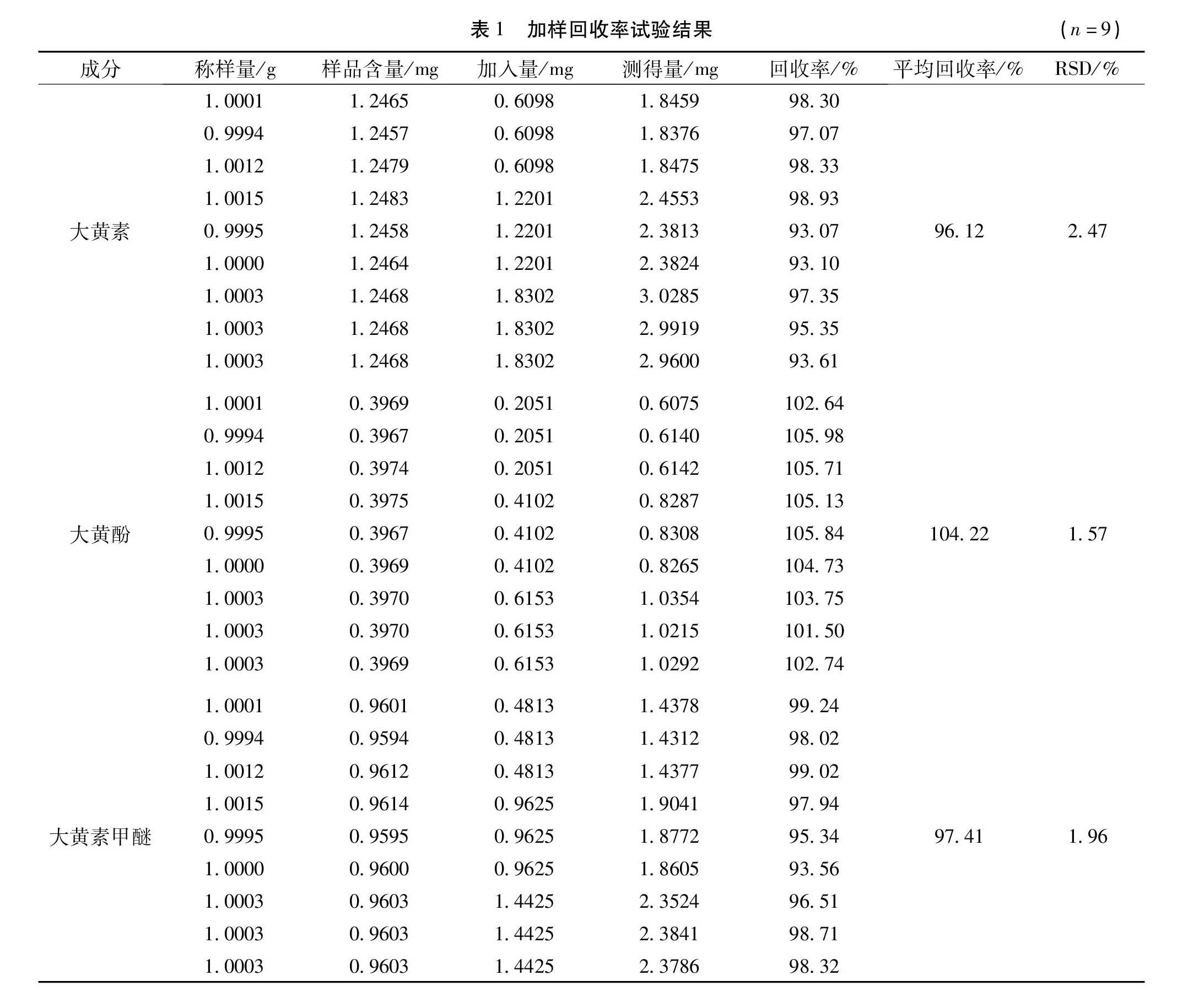
2.8 加样回收率试验 取知道含量的样品(批号:20190204)约1 g,精密称定,以1∶0.5,1∶1,1∶1.5的比例精准加入对照品,再按“2.2”项下方法制备,每个比例平行3份,照“2.1”色谱条件测定峰面积,计算回收率及RSD。大黄素、大黄酚、大黄素甲醚的平均加样回收率分别为96.12%、104.22%和97.41%,RSD分别为2.47%、1.57%和1.96%。结果见表1。
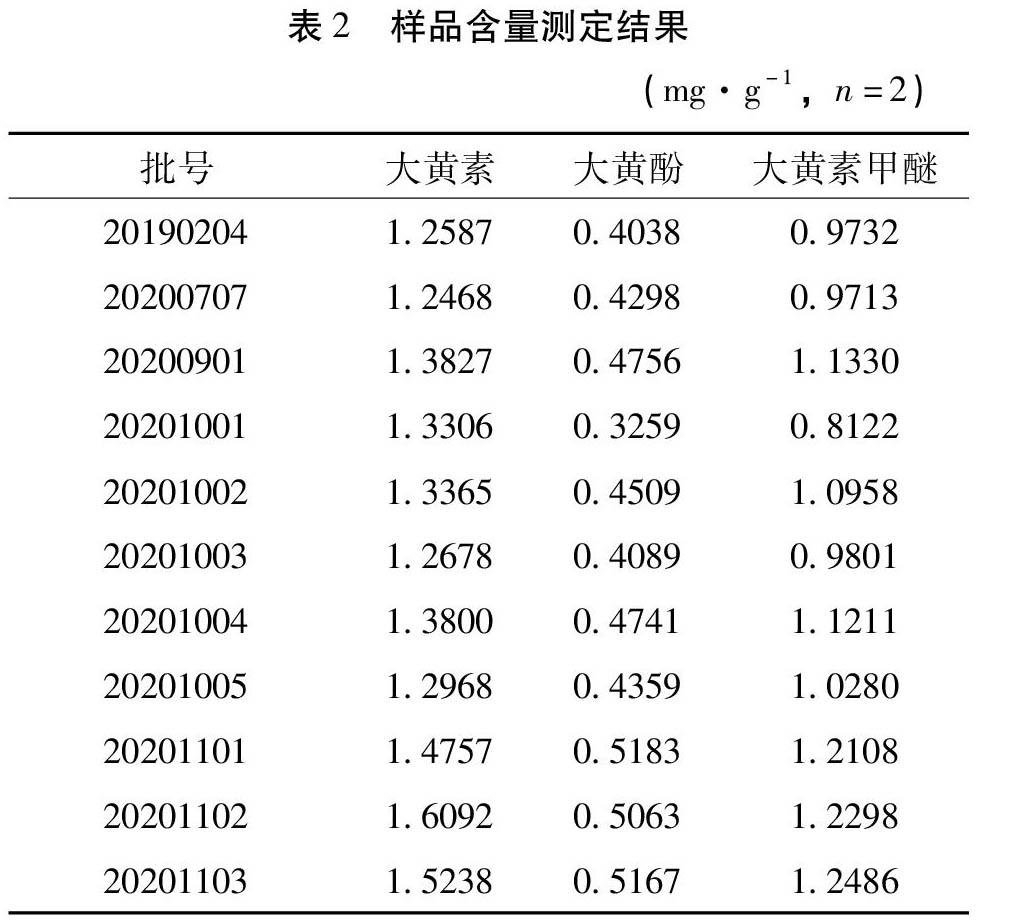
2.9 样品含量测定 取11批次样品,依法制备样品并测定其峰面积,以标准曲线计算样品3个成分的含量(按干燥品计),结果见表2。
3 讨论
3.1 样品提取条件的优化 在制备供试品溶液时,摸索了不同提取方式(超声和加热回流方式分别提取30 min和45 min)、提取溶剂(甲醇、80%甲醇、乙醇、80%乙醇)、溶剂用量(12.5 mL、25mL、50 mL)、盐酸用量(1 mL、2 mL、3 mL)和水解时间(30 min、45 min、60 min)对待测组分含量的影响。结果显示以加入25 mL甲醇,超声30min,加入盐酸2 mL,水解30min的提取条件较佳。
3.2 色谱条件的优化 供试品和对照品溶液的全波长扫描结果显示,两溶液最大吸收波长均在254nm和285 nm附近,同时参考2015版中国药典大黄中蒽醌类成分的含量测定方法 [13],检测波长确定为254 nm。曾对甲醇-0.1%磷酸溶液的比例进行考察,发现以体积比为85∶15时3种成分的保留时间适中,理论塔板数较高,峰形良好,可满足快速定量检验的要求。
3.3 样品测定结果分析 表2含量测定结果显示,样品中大黃素、大黄酚和大黄素甲醚的含量分别为1.2468~1.6092 mg/g、0.3259~0.5183 mg/g、0.8122~1.2486 mg/g,该厂提供的不同批次样品3个蒽醌成分的含量水平波动较大,推测原因可能与原料药的质量差异有关,因此应当严格控制原料药的质量,把控生产环节,以保证药品质量的稳定。
4 结论
本研究建立了金酸萍颗粒中3个大黄素型蒽醌类成分的HPLC含量测定方法,该方法操作简单,专属性强,快速准确,可为金酸萍颗粒的质量控制提供参考依据。
参考文献
[1]王丹.金酸萍颗粒治疗慢性乙型病毒性肝炎(肝胆湿热证)的临床研究[D].武汉:湖北中医学院, 2009.
[2]LI L,ZHENG Y X,CHEN B F. Clinical observation on Bao-Le-An combined with Jin-Suan-Ping granules in treatment of neonatal jaundice[J]. Chinese Journal of Microecology, 2019, 31 (6) :712-714.
[3]张峰,申亚东.金酸萍糖浆治疗药源性转氨酶升高15例临床观[J]. 甘肃中医, 2001, 14(6):24-25.
[4]王春安.中西医结合治疗急性黄疸型病毒性肝炎40例分析[J].青海医药杂志, 2011, 41(3):70-71.
[5]中国科学院中国植物志编辑委员会.中国植物志:第25卷[M].北京:科学出版社,1998:151.
[6]张广庆,赵海鹏,王振月,等.酸模属植物的化学成分与药理活性研究进展[J].世界科学技术-中医药现代化,2008(5):86-93.
[7]国家中医药管理局《中华本草》编委会.中华本草:蒙药卷[M].上海:上海科学技术出版社,2004.
[8]中华人民共和国卫生部药典委员会.药品标准·中药成方制剂(第八册)[S].1993.
[9]熊茉君,徐小平,钱广生,等.HPLC测定金酸萍胶囊中的大黄素[J].华西药学杂志,2017,32(4):427-428.
[10]张立.HPLC法同时测定金酸萍颗粒中大黄素、大黄酚的含量[J].中国药师,2011,14(3):425-426.
[11]肖凌.HPLC测定不同品种酸模中蒽醌类成分的含量[J].中国现代应用药学,2011,28(4):353-356.
[12]金贤武,付彩群,黄道明,等.高效液相色谱法同时测定复方胆通片中5种蒽醌类成分含量[J].中国药业,2018,27(6):7-10.
[13]国家药典委员会. 中国药典(一部)[M].北京:中国医药科技出版社, 2015: 23-24.
(收稿日期:2021-03-15 编辑:刘斌)

