双刺参胶囊总皂苷的提取、含量测定及体外活性
邸松,戴鹂莹,钟方丽,王晓林,郑郡,崔泽伟
吉林化工学院化学与制药工程学院(吉林 132022)
双刺参胶囊由刺玫果、刺五加及人参的醇提物经干燥粉碎后加入少量淀粉制成。刺玫果属蔷薇科植物成熟果实[1]、人参[2]及刺五加[3]均为五加科植物。三者在东北地区分布广泛,且均具有较为丰富的化学成分,如皂苷、黄酮、氨基酸等[4-6]。
由于现今社会发展迅速,繁忙的学习、工作及生活压力使人长期处于疲劳性亚健康状态。该状态是一种处于健康和疾病之间的第三状态[7],其表现大体可以分为躯体性[8]和精神性[9]两大类。长时间处于虚弱、疲劳等亚健康状态下,会发展成为其他疾病[10]。中医学上对于疲劳的论述最早出现在《黄帝内经》[11],经后世医者补充得以完善。中医讲气血耗损所引起的“虚劳”即为疲劳[12],补中益气、固本培元的中药材如人参[13]、党参[14]、刺五加[15]、黄芪[16]等,可以在一定程度上调理疲劳。近年来,受中国饮食、医药文化的影响,药食同源类功能性保健食品受到越来越多人的青睐[17]。经文献查阅,刺玫果[18]、刺五加[19]及人参[20]提取物中的皂苷成分具有较好的抗疲劳作用,且三者均为药食同源类中药材。课题组选用三者,按照一定比例混合后进行提取、干燥、粉碎、制粒、装囊,制备抗疲劳保健食品双刺参胶囊。
研究建立了双刺参胶囊中总皂苷含量的检测方法,并以总皂苷提取率作为指标,采用正交试验的方法优选出提取的最佳工艺,为双刺参胶囊的进一步研究提供了基础数据。
1 材料与方法
1.1 试验材料
齐墩果酸(纯度98.33%,成都曼思特生物科技有限公司);香草醛(天津市光复精细化工研究)所。无水乙醇及其余分析纯试剂(天津大茂化学试剂厂)。
1.2 仪器与设备
真空干燥箱(上海精宏实验设备有限公司);旋转蒸发仪(上海亚荣生化仪器厂);多功能振荡器(金坛市华城开元仪器厂);紫外分光光度计(TU-1950型,北京普析通用仪器有限责任公司)。
1.3 试验方法
1.3.1 溶液的制备
1.3.1.1 供试品溶液
双刺参胶囊内容物供试品溶液的制备:取适量双刺参胶囊内容物,研磨粉碎,精密称取2.0 g,置于烧瓶中,加20 mL甲醇,超声处理(功率200 W,频率53 kHz)30 min,放冷后过滤,用2 mL甲醇洗涤滤渣2次,将滤液及洗涤液转移至25 mL容量瓶中,定容至刻度线,摇匀后取1.3 mL再次定容至25 mL容量瓶中,即得。
提取物供试品溶液的制备:称取2 g干燥至恒质量的双刺参提取物,精密称定。加入适量甲醇,经30 min超声处理(功率200 W,频率53 kHz)后过滤,用少量甲醇洗涤2次后定容至25 mL容量瓶中,取0.5 mL上述溶液定容至10 mL容量瓶中,即得。
1.3.1.2 对照品溶液
取10 mg齐墩果酸,精密称定,加入甲醇溶解并定容至50 mL容量瓶中,置于4 ℃冰箱备用。
1.3.2 测定方法的选择
1.3.2.1 香草醛-冰醋酸-浓硫酸显色法(A法)
参照文献[21]。吸取0.4 mL供试品溶液,于80 ℃水浴蒸干溶剂,加入0.2 mL 5%香草醛-冰醋酸溶液溶解后加入0.8 mL 80%硫酸,于60 ℃水浴振荡15 min,振荡结束后放于冰水浴中冷却10 min,加入10 mL冰醋酸室温静置15 min。
1.3.2.2 香草酸-冰醋酸-高氯酸显色法(B法)[22]
吸取0.4 mL供试品溶液,于80 ℃水浴蒸干溶剂,加入0.2 mL 5%香草醛-冰醋酸溶液溶解后加入0.8 mL高氯酸,于60 ℃水浴振荡15 min,振荡结束后放于冰水浴中冷却10 min,加入10 mL冰醋酸室温静置15 min。
1.3.2.3 香草醛-乙醇-硫酸显色法(C法)
参照文献[23],并进行调整。吸取0.4 mL供试品溶液,于80 ℃水浴蒸干溶剂,加入0.5 mL 8%香草醛-乙醇溶液溶解后加入5 mL 72%硫酸,混合均匀于60℃水浴振荡15 min,振荡结束后放于冰水浴中冷却10 min,在室温下静置15 min。
采用上述3种方法分别对双刺参提取物、双刺参胶囊内容物、齐墩果酸、淀粉进行显色,将显色后的样品、未显色的双刺参胶囊内容物供试品溶液以及对应显色剂在200~800 nm进行全波长扫描,通过对比最大吸收峰的波长及峰型确定检测方法。
1.3.3 方法学考察
1.3.3.1 稳定性试验
吸取双刺参胶囊内容物供试品溶液,分别考察其显色前360 min内及显色后90 min内的稳定性。
1.3.3.2 仪器精密度试验
吸取6份同一双刺参胶囊内容物供试品溶液,按照相应方法进行显色,在同一台紫外分光光度计下测定吸光度,记录并计算测定值的RSD值,应小于3%。
1.3.3.3 中间精密度试验
吸取6份同一双刺参胶囊内容物供试品溶液进行显色,使用2台紫外分光光度计对显色后的供试品溶液进行吸光度测定,计算其RSD值,应小于3%。
1.3.3.4 重现性试验
取同一批次双刺参胶囊内容物,按照双刺参胶囊内容物供试品溶液制备方法制备6份溶液,按照检测方法进行显色后测定吸光度,吸光度的RSD值应小于3%。
1.3.3.5 加样回收率试验
精密称取9份已知总皂苷含量的双刺参胶囊内容物,每份1.0 g。每3份为1组,分别加入总皂苷含量的50%,100%和150%的齐墩果酸对照品,按照选定的显色方法进行显色处理,测定吸光度并计算加样回收率,RSD值应小于3%。
1.3.4 标准曲线的绘制
精密吸取0.1,0.2,0.3,0.4,0.5,0.6和0.7 mL对照品溶液进行显色处理,显色后测定吸光度。以齐墩果酸质量浓度为横坐标,吸光度为纵坐标,绘制标准曲线。
1.3.5 双刺参胶囊内容物总皂苷含量的测定
取若干3个批次的双刺参胶囊,取内容物按供试品溶液制备方法制备供试品溶液,在显色方法下显色后测定吸光度,代入标准曲线方程,计算双刺参胶囊中总皂苷的含量。
1.4 正交试验优选总皂苷提取工艺
1.4.1 正交试验
在预试验中,分别对总皂苷的提取溶剂种类乙醇体积分数、溶剂用量料液比(g/mL)、提取温度及提取时间等可能影响总皂苷提取的因素进行单因素试验考察,最终选择影响较大的3个因素:提取溶剂种类乙醇体积分数(A)、溶剂用量料液比(B)及提取时间(C),以总皂苷的提取率作为指标,进行三因素三水平正交试验,正交因素与水平见表1。

表1 正交因素水平表
1.4.2 验证试验
称取10.5 g过孔径0.180 mm筛的人参粉、21 g刺五加粉及14 g刺玫果粉,混合,共3份,每份均采用正交试验的最优工艺提取2次,合并滤液,减压浓缩后置于真空干燥箱60 ℃干燥至恒质量。按照双刺参提取物供试品溶液制备方法进行溶液制备,经显色,测定吸光度,计算总皂苷提取率。
1.5 提取物体外活性研究
1.5.1 清除ABTS自由基阳离子能力
参考文献[24]配制ABTS自由基阳离子工作液。取0.1 mL不同质量浓度的各种供试品溶液,与3.9 mL ABTS自由基阳离子工作液混合,于23 ℃避光放置6 min,于734 nm测定吸光度(Ay),同法操作,将供试品溶液更换为蒸馏水测得Ak,按式(1)计算自由基清除率,并计算其IC50值。通过对比IC50,比较双刺参提取物与VC体外抗氧化活性。

1.5.2 抗脂质过氧化能力
以抑制率为指标,参照文献[25]的试验方法,对VC、总皂苷提取物的抗卵磷脂脂质过氧化作用进行测试。在具塞试管中依次加入1 mL卵磷脂溶液、1 mL 0.4 mmol/L FeSO4溶液及1 mL供试品溶液混匀。于37℃避光水浴60 min,加入2 mL TCA-TBA-HCl混合液,于90~100 ℃水浴15 min,迅速冷却,以5 000 r/min离心10 min,取上清液在波长535 nm处测定吸光度As。空白管以1 mL重蒸水代替1 mL供试品溶液测得Ac,按式(2)计算抗脂质过氧化抑制率。
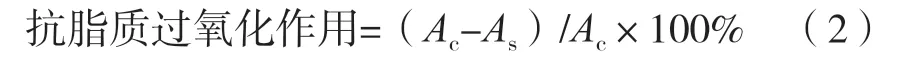
2 结果与分析
2.1 总皂苷含量测定方法的试验结果
2.1.1 总皂苷测定方法
A法双刺参提取物与胶囊内容物在530 nm附近存在吸收峰,齐墩果酸对照品在550 nm处有最大吸收峰。目标峰波长相差较大,且提取物及内容物在470 nm处也存在吸收峰,专属性较差。
B法双刺参提取物与胶囊内容物、齐墩果酸三者的吸收峰均在545 nm附近,但峰型未呈现较为完美的馒头峰,且各样品的最大吸收峰偏差较大。
C法双刺参提取物,胶囊内容物及齐墩果酸对照品的最大吸收峰均在540 nm附近,且相应空白试剂在该处无吸收峰,故该法适用于双刺参胶囊中总皂苷的含量测定。在C显色方法下各供试品全波长扫描图见图1。

图1 C显色方法下供试品全波长扫描谱图
2.1.2 方法学考察
2.1.2.1 稳定性
显色前双刺参胶囊供试品溶液在0,30,60,120,180,240,300和360 min的吸光度分别为0.524,0.536,0.549,0.545,0.543,0.542,0.543和0.563,均在0.544±0.02范围内,显色后其在0,15,30,45,60,75和90 min内吸光度分别为0.587,0.571,0.573,0.572,0.563,0.566和0.579,均在0.575±0.01范围内,显色前后的RSD值分别为2.03%和1.40%,均小于3%,说明双刺参胶囊供试品溶液在显色前360 min内、显色后90 min内稳定。
2.1.2.2 仪器精密度
6份双刺参胶囊内容物供试品溶液的吸光度分别为0.592,0.587,0.584,0.582,0.584和0.583,RSD为0.63%,说明仪器精密度良好。
2.1.2.3 中间精密度
由同一名实验员在相同的试验条件下,分别在2台紫外分光光度计上测定6份双刺参胶囊供试品溶液的吸光度,分别为0.579,0.591,0.577,0.608,0.605,0.588和0.584,0.589,0.583,0.579,0.596,0.581。通过对比,2台分光光度计的测定结果相差不大,且RSD值为1.73%,表明此方法的中间精密度良好。
2.1.2.4 重现性
6份双刺参胶囊供试品溶液显色后的吸光度分别为0.555,0.549,0.551,0.549,0.562和0.550。经计算,RSD值为0.88%,小于3%,说明该方法重现性良好,可用于测定胶囊中总皂苷的含量。
2.1.2.5 加样回收率
称取9份1 g双刺参胶囊内容物,精密称定,加入约已知总皂苷含量50%,100%和150%的齐墩果酸,按含量测定方法制备供试品溶液并进行显色处理,在540 nm处用紫外分光光度仪进行吸光度测定,试验结果见表2。
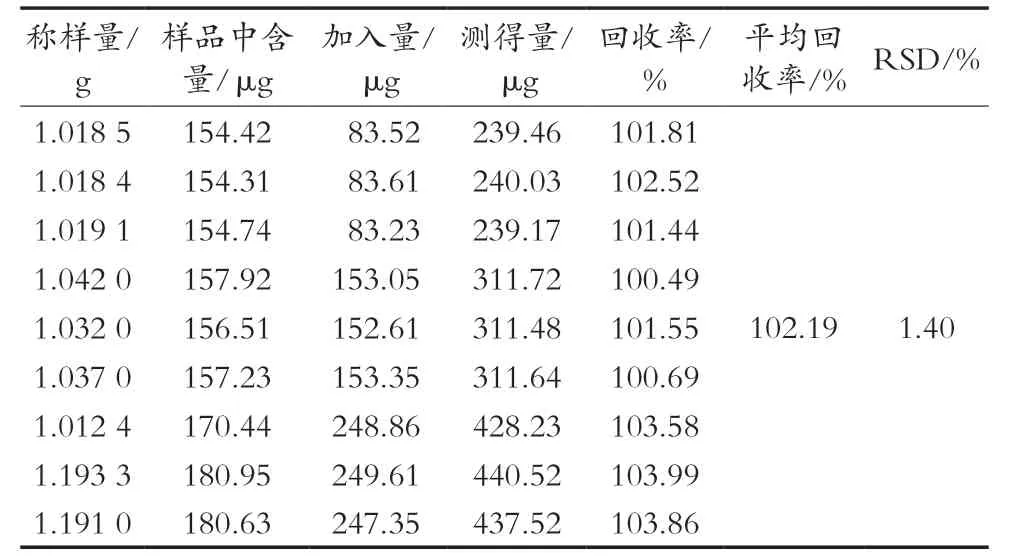
表2 加样回收率试验结果
2.1.3 标准曲线的制备
以齐墩果酸的质量浓度为横坐标,吸光度为纵坐标绘制标准曲线,其线性回归方程为Y=23.01X+0.057 7,R2=0.999 4,表明在4.51~31.56 μg/mL质量浓度范围内线性关系良好。
2.1.4 双刺参胶囊总皂苷含量测定结果
将测得的吸光度代入到标准曲线中进行计算,结果得到3个批次的双刺参胶囊总皂苷平均含量,分别为13.28,13.31和13.36 g/100 g。
2.2 优选总皂苷提取工艺的试验结果
2.2.1 正交试验结果与方差分析
结合表3可以看出,各因素对提取物中总皂苷含量影响最大的是因素C,即提取时间,其次为提取溶剂A,溶剂用量B的影响较小,因此选择提取工艺A3B1C2,即为料液比为1∶5(g/mL),乙醇体积分数为90%,提取时间为1 h。
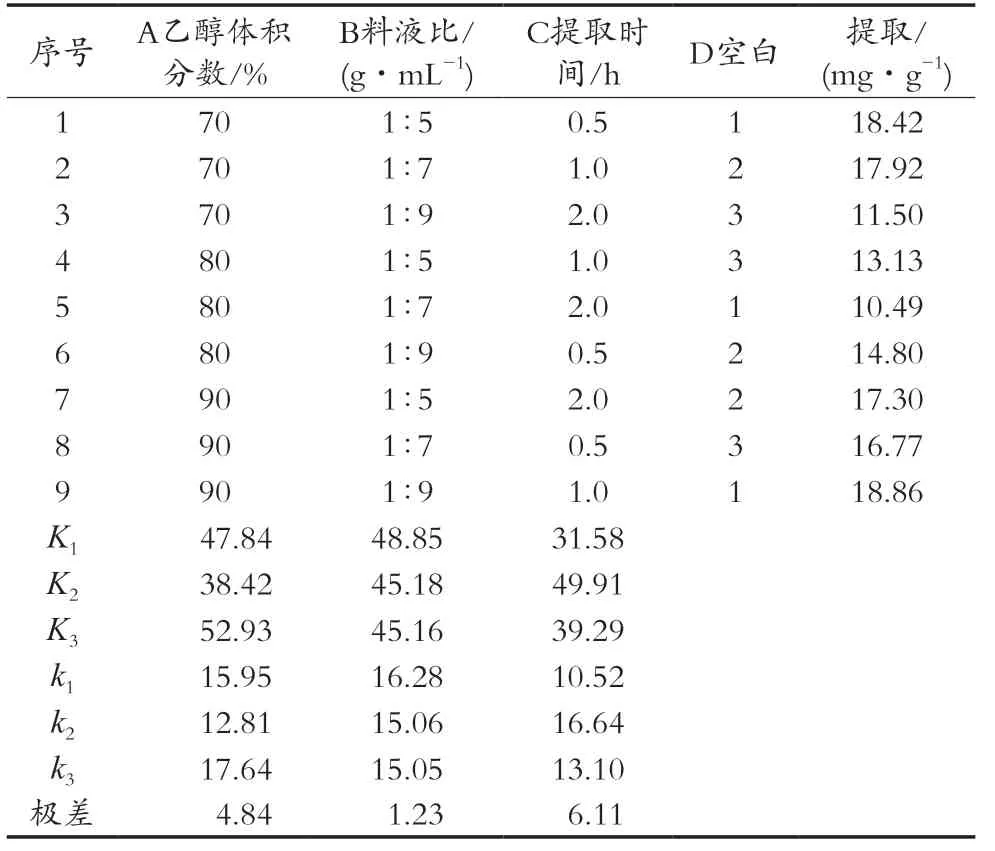
表3 正交试验结果分析表
2.2.2 工艺验证试验结果
采用最佳工艺平行提取3次,总皂苷提取率分别为28.82,29.25和28.46 mg/g,且RSD值为1.08%,说明该工艺合理稳定,可以用于双刺参胶囊总皂苷的提取,且提取效率较高。
2.3 体外抗氧化试验结果
双刺参提取物与VC均能有效地清除ABTS自由基阳离子,抑制脂质的过氧化作用。通过对比两者清除ABTS自由基阳离子能力及抗脂质过氧化能力的半数抑制浓度,结果发现双刺参提取物的抗氧化能力弱于VC,试验结果见表4。

表4 体外抗氧化试验结果
3 结论
研究采用香草醛-冰醋酸-浓硫酸显色法、香草酸-冰醋酸-高氯酸显色法、香草醛-乙醇-硫酸显色法三种显色方法,对供试品溶液进行显色,在200~800 nm波长范围内进行扫描。结果显示,经香草醛-乙醇-硫酸显色法,各供试品溶液在540 nm处均有最大吸收,且专属性较高、稳定性较好,可作为双刺参胶囊总皂苷的含量测定方法。通过正交试验优选得到双刺参总皂苷的最佳提取工艺,即5倍量90%乙醇,于80 ℃水浴提取2次,每次1 h,总皂苷平均提取率为28.84 g/g,该方法简单快捷,总皂苷提取率较高。体外抗氧化试验结果显示,双刺参提取物具有一定的抗氧化能力。此次研究不仅为双刺参胶囊的进一步研究提供了基础数据,同时也为刺玫果、刺五加及人参进一步的开发利用提供了试验基础。

