5-取代基对钴配合物的结构及性能影响*
陈敏玲,陈志胜,刘俊林,欧冠荣,叶添诚,闫 鹏
(肇庆学院环境与化学工程学院,广东 肇庆 526061)
金属-有机框架(MOFs)材料是一种新型多孔晶体材料,由金属离子或多核金属簇与有机配体通过配位键连接而成,也称为多孔配位聚合物。1995年Yaghi等[1]首次提出金属有机框架这一概念,此后在国内外众多学者的关注下,MOFs迅速发展成为材料研究的热门领域。MOFs材料结构与功能的多样性在于其金属中心和有机配体的可选择范围广,再结合有机配体中的官能团可调节修饰性,使其具有广阔的应用领域。近年来,其在气体存储与分离[2-6]、催化[7-9]、化学传感[10-11]、生物医药[12]、磁性材料[13]等方面的应用价值日益凸显。
在MOFs材料的实际应用中,其结构的稳定性是一个亟待解决的问题,到目前为止,尽管已有数万种金属有机框架材料被合成出来,但由于结构稳定性差等问题,限制了很多材料的进一步应用。根据文献,结构稳定的MOFs一般具有以下特点:由高价多核金属簇和羧酸配体构建的框架,诸如UiO-66等;由二价金属和唑类配体构建的框架,如ZIF-8等[14]。此外,利用羧酸配体和含氮配体组成混合配体,来构建具有金属-O和金属-N配位键的稳定框架材料,也逐渐受到重视。
间苯二甲酸结构中的两个羧基在空间上间隔约120°,并且其苯环上5-位氢可被不同取代基修饰,因而具有构建新颖框架结构的潜力[15-17]。本工作以5-溴间苯二甲酸、间苯二甲酸-5-磺酸钠、5-甲基间苯二甲酸、5-甲氧基间苯二甲酸为羧酸配体,分别与4,4′-联吡啶组成混合配体,合成了四个钴金属配合物,通过粉末衍射、热重对材料进行了结构对比和热稳定性分析,考察了合成材料对二氧化碳和乙炔的吸附性能,以及对溶液中金属阳离子的荧光识别性能。
1 实 验
1.1 材料与仪器
实验材料:5-溴间苯二甲酸、间苯二甲酸-5-磺酸钠、5-甲基间苯二甲酸、六水合硝酸钴等购自上海阿拉丁生化科技股份有限公司;5-甲氧基间苯二甲酸和4,4′-联吡啶购自梯希爱(上海)化成工业发展有限公司。
主要实验仪器:DGG-9030程序控温烘箱,上海森信;D8 Advance X射线粉末衍射仪,德国布鲁克;DTG-60H热分析仪,日本岛津;Autosorb iQ物理吸附仪,美国康塔;F-7000荧光分光光度计,日本日立。
1.2 配合物合成
分别称取间苯二甲酸-5-磺酸钠(0.3 mmol)、4,4′-联吡啶(0.15 mmol)加入装有乙醇-水混合溶剂(7:3)的水热反应釜内衬中,再称取六水合硝酸钴(0.3 mmol)加入其中,搅拌混合均匀,密封后置于程序控温烘箱中,程序升温至140 ℃,恒温反应72 h,然后降至室温后取出,过滤洗涤得到粉色配合物1。分别用5-溴间苯二甲酸、5-甲基间苯二甲酸、5-甲氧基间苯二甲酸代替间苯二甲酸-5-磺酸钠,其他合成条件不变,可分别得到配合物2~4。
1.3 分析测试
利用X射线粉末衍射仪对合成的配合物1~4样品进行对比分析,光源为Cu靶,测试电压电流为40 kV、40 mA,步进角度0.02,分析角度范围为5°~50°(2θ)。利用热分析仪对各配合物样品进行热稳定性评价,程序升温速率10 ℃/min,测试温度范围为室温-700 ℃,测试气氛N2。
二氧化碳、乙炔气体吸附等温线由Autosorb-iQ全自动物理吸附仪获得,分析前先将粉末样品在180 ℃下进行真空脱气处理8 h,然后于273 K下进行配合物对CO2、C2H2的吸附实验,得到吸附等温线。
分别配制0.001 mol/L的K+、Na+、Mg2+、Ca2+、Cu2+、Al3+、Fe3+等金属盐溶液。分别称取1 mg的配合物3样品,加入3 mL的各种金属阳离子溶液中,超声混合15 min,然后利用荧光分光光度计检测溶液在270 nm的激发波长下的发射光谱。
2 结果与讨论
2.1 合成材料的PXRD分析
配合物1~4的PXRD谱图见图1。由图1可知,羧酸配体中5-取代基不同时,对合成材料的结构影响较大。配合物3(5-CH3)和4(5-OCH3)的衍射峰基本一致,说明二者的结构具有相似性。配合物2(5-Br)的衍射峰比较接近配合物3、4。配合物1的衍射峰与上述三者相比,则有很大差别,这表明其结构差异较大。

图1 合成配合物的XRD谱图
2.2 合成材料的TG分析
图2为配合物1~4的TG曲线。由图2可知,配合物1在室温至150 ℃之间有约20%的失重,这主要由乙醇、水等溶剂分子损失所致,在370 ℃之后框架结构开始快速分解,失重加速。配合物2与配合物1相似,其框架结构在370 ℃之后坍塌,在此之前失重很少,说明其孔道结构中的溶剂分子很少。配合物3、4的热重曲线比较相似,在室温至160 ℃之间有和溶剂分子相关的失重,并且在大约420 ℃之后才开始快速失重,由此可知配合物3、4较1、2的热稳定性更好。
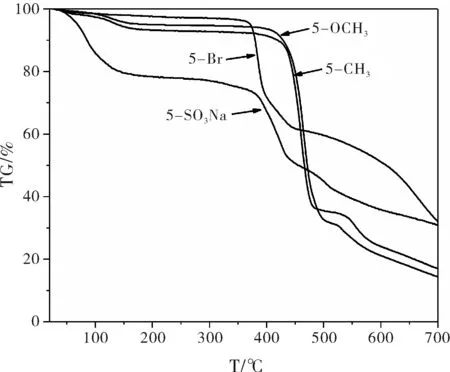
图2 合成配合物的TG曲线
2.3 合成材料的气体吸附性能
图3为配合物1~4对二氧化碳和乙炔的吸附等温线。由图3可知,配合物4对二氧化碳和乙炔的吸附性能均明显高于其他配合物,其次是配合物3,性能最差的是配合物1。在273 K、100 kPa下,配合物4对二氧化碳和乙炔的吸附量分别为44.9 cm3·g-1和35.9 cm3·g-1。在配合物1~4的羧酸配体中,5-甲氧基功能基团较其他基团更有利于构建吸附性能较好的材料,这可能和甲氧基的供电性有关。另外,配合物4对二氧化碳和乙炔的吸附能力差异较大,说明其对二氧化碳具有一定的吸附选择性,这有别于大多数MOFs材料会优先吸附乙炔。
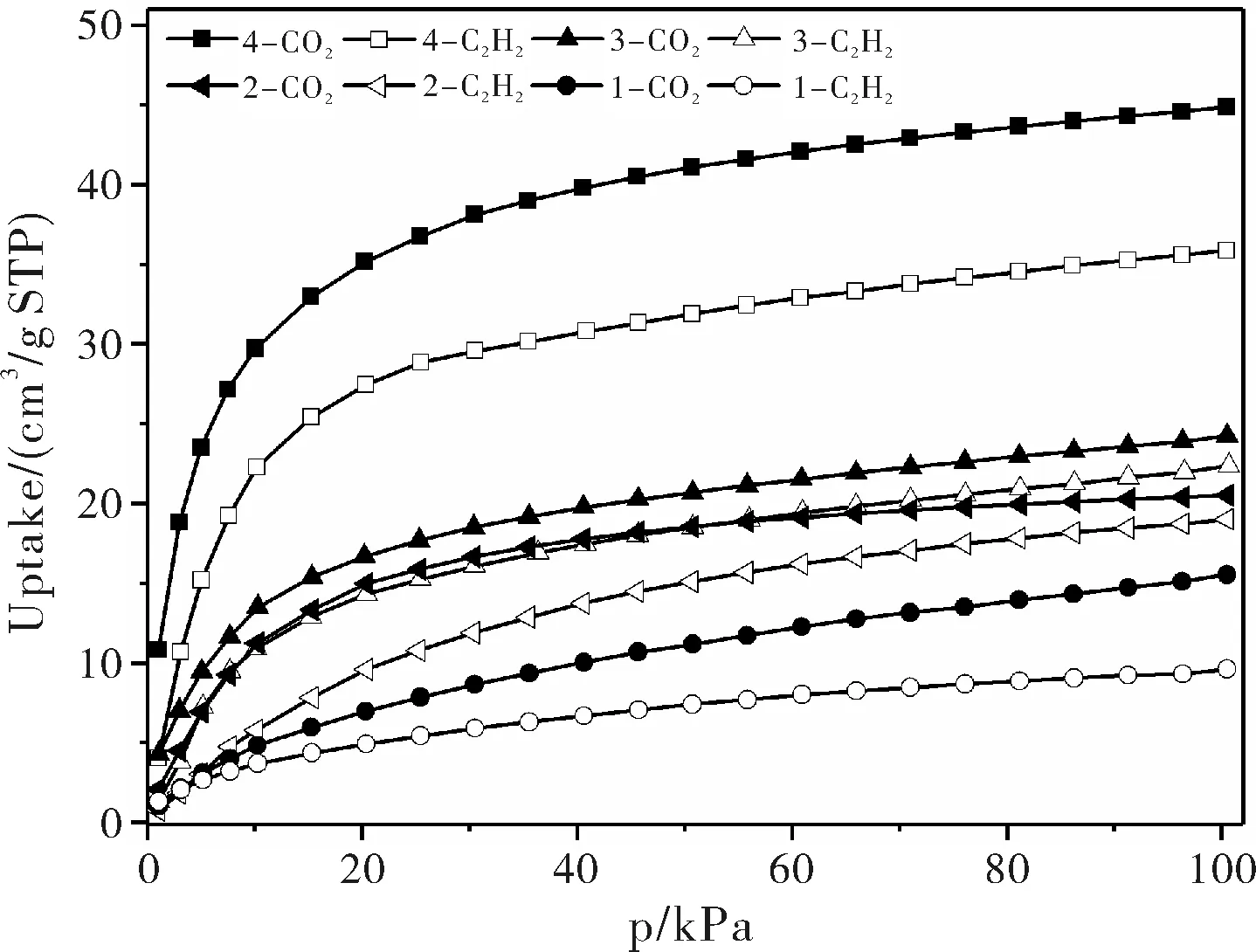
图3 273 K下配合物1~4对二氧化碳和乙炔的吸附性能
2.4 配合物3对金属离子荧光性能的研究
对合成的配合物样品进行荧光性能分析,发现配合物3具有较好荧光性能。图4为配合物3在各种金属阳离子水溶液中的荧光发射图谱,由上而下曲线依次为K+、Cu2+、空白、…、Fe3+。由图4可知,配合物3空白样品在350 nm左右出现明显的特征峰。不同金属阳离子存在下,其特征峰强度会发生变化,K+、Cu2+存在时略有增强,Na+、Mg2+、Ca2+存在时略有减弱,Al3+、Fe3+存在时则会导致明显的荧光猝灭现象,可见配合物3对Al3+、Fe3+具有选择性检测能力。
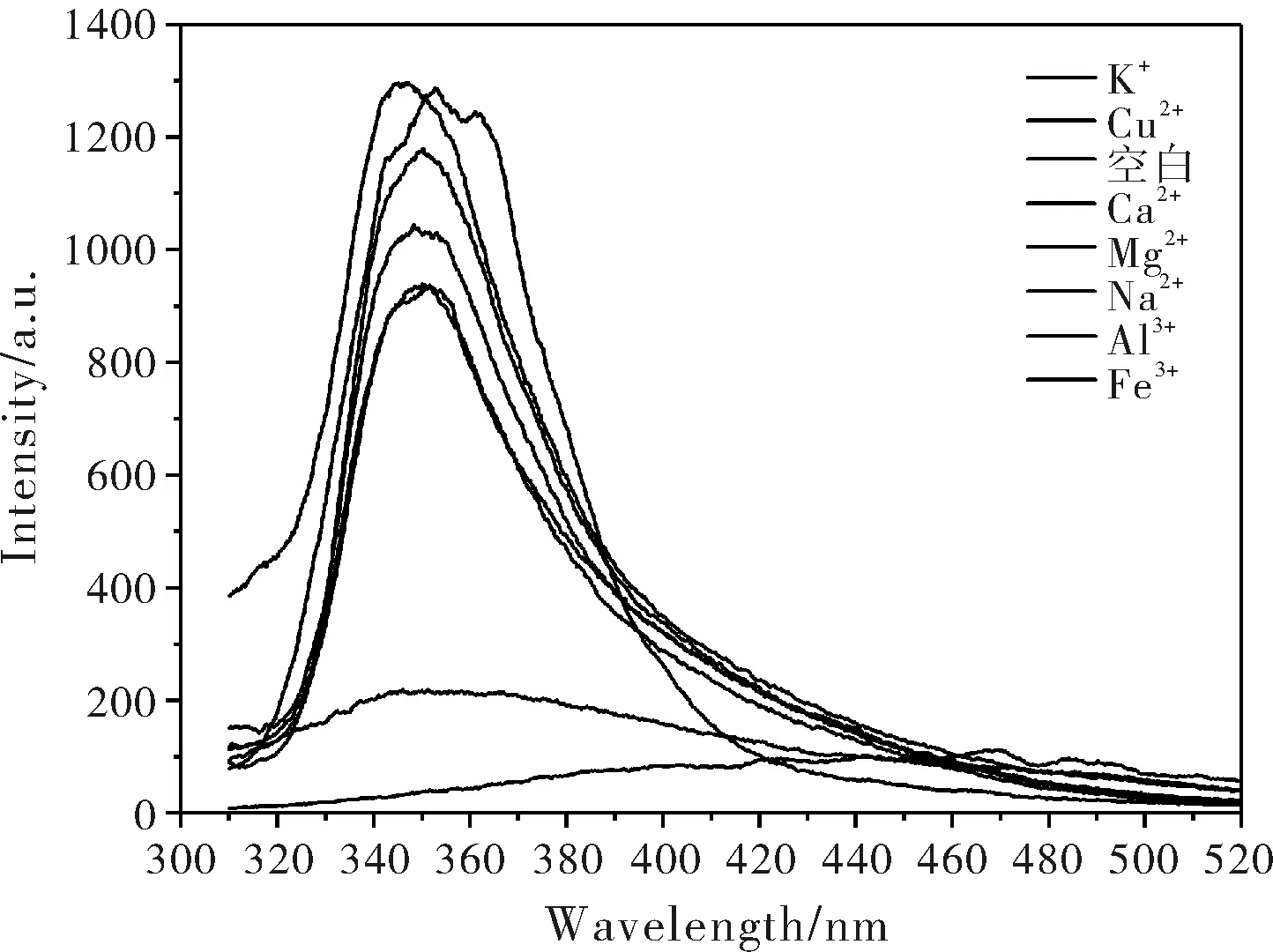
图4 不同金属阳离子条件下配合物3的荧光强度
3 结 论
基于5-取代间苯二甲酸和联吡啶混合配体合成了4个钴配合物,配合物3(5-甲基)和4(5-甲氧基)具有相似的结构,并且其热稳定性优于配合物1和2。配合物4具有较好的二氧化碳和乙炔吸附性能,配合物3对水溶液中的Al3+、Fe3+具有荧光识别能力。

