初中化学理论课融入化学实验的尝试
江苏省徐州市撷秀初级中学(221006) 郭 焘
江苏省徐州市西苑中学(221002) 李德前
化学理论课相对枯燥,而基础教育化学的学科特点是实验,因此在化学理论课中增补一些化学实验,可以帮助学生认识基本概念和基本理论,提高学生的学习兴趣,培养学生理论联系实践的能力。多年来,笔者积极尝试化学理论课融入化学实验的教学方式,取得了显著的教学效果。
1 “混合物性质”实验
现行各个版本的9年级化学教科书均介绍了混合物的性质,即组成混合物的各种成分之间没有发生化学反应,它们各自保持着原来的性质。但是该知识点较为抽象,学生理解起来有一定的困难。我们在教学中借助几种常规仪器设计了有关的化学实验,可以直观而形象地说明“混合物各成分均保持各自原来的性质”。
1.1 实验用品
60 mL集气瓶,20 mL注射器,细的软胶管,澄清石灰水,氧气或一氧化碳气体,二氧化碳气体等。
1.2 实验装置
新设计的实验装置见图1~3。
1.3 实验步骤
(1)取一个60 mL的集气瓶(其实际容积约为80 mL),采用排水法在其中集满氧气。
(2)在20 mL注射器的吸入口接一根长约12 cm的细软胶管,然后吸入10 mL二氧化碳。
(3)将注射器吸入口上的软胶管插入氧气瓶底部,然后缓缓推出注射器针筒里的10 mL二氧化碳(此时集气瓶里含有70 mL氧气和10 mL二氧化碳);再将毛玻璃片盖在集气瓶口,缓缓颠倒集气瓶6~7次,使集气瓶内的氧气与二氧化碳充分混合,即得氧气与二氧化碳体积比为7∶1的混合气。
(4)取下集气瓶口的毛玻璃片,将少许石灰水倒入氧气与二氧化碳的混合气中(见图2),立即在集气瓶口盖上毛玻璃片,轻轻振荡集气瓶,石灰水立刻明显变浑。上述实验现象充分说明,混合气中二氧化碳的化学性质没有变化。

图2 向混合气中注入少许澄清的石灰水
(5)接下来,将带火星的木条伸入集气瓶内,木条立即复燃(见图3)。上述实验现象又说明,混合气中氧气的化学性质没有发生变化。综上可知,混合物中各成分均保持各自原来的性质。
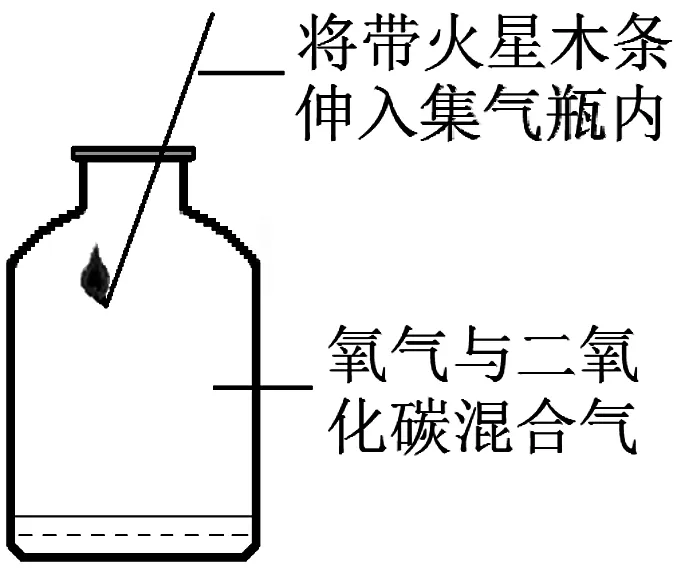
图3 将带火星的木条伸入集气瓶内
(6)实验结束,整理实验用品。
1.4 几点说明
(1)使带火星木条复燃的氧气最低浓度约是40%,使石灰水变浑浊的二氧化碳最低浓度约是1%。因此,在氧气与二氧化碳的混合气中氧气浓度必须大于40%,二氧化碳浓度必须大于1%。
(2)本实验如果使用一氧化碳与二氧化碳体积比为1∶1的混合气,仍然可以得出有关的实验结论。实验时,先使用湿润的黄色氯化钯试纸检验一氧化碳的存在(试纸变蓝色),再使用澄清石灰水检验二氧化碳的存在(石灰水变浑浊);或者先使用澄清石灰水检验二氧化碳的存在(石灰水变浑浊),再使用燃着的木条检验一氧化碳的存在(气体燃烧并产生蓝色火焰)。
2 “钠的化学变化”实验
“化学式的书写”不仅是教学重点,也是教学难点。笔者在有关“化学式的书写”教学中独辟蹊径,引入“钠的化学变化”实验,突出了教学重点,突破了学习难点,促进了初、高中化学的衔接。
2.1 实验用品
250 mL烧杯,镊子,滤纸(或面巾纸),玻璃片,小刀,金属钠,蒸馏水,酚酞溶液,稀盐酸等。
2.2 实验装置
新设计的实验装置见图4。

图4 钠的化学变化系列实验
2.3 实验步骤
(1)准备一个250 mL的烧杯,注入大约150 mL的蒸馏水,备用。
(2)用镊子从试剂瓶里取出一块金属钠,置于玻璃片上,用洁净的滤纸或面巾纸吸干表面的煤油,再用小刀切下绿豆粒大小的一块钠(见图4-A);将切下来的金属钠展示给学生观察,可以发现切口处呈银白色,告诉学生这是金属钠;表面的其他地方呈灰黄色,告诉学生这个是被氧化的金属钠,即氧化钠。
(3)随后,将钠块轻轻投入水中(见图4-B),可以发现金属钠浮在水面上较快的四处游动,并伴随轻微的嘶嘶声,说明钠与水反应产生气体,告诉学生这是氢气;钠与水反应同时放出大量的热(见图4-C),钠块因此由不规则形状而熔为光亮的小球。
(4)向反应后的水中滴入酚酞溶液(见图4-D),发现溶液变红,告诉学生这是因为钠与水反应还生成了氢氧化钠;再向反应后的水中滴入适量的稀盐酸,溶液红色消失(见图4-E),告诉学生这是因为氢氧化钠被盐酸完全反应并生成了氯化钠。
(5)实验结束,整理实验用品。
2.4 几点说明
(1)在切取金属钠后,剩下的钠块要及时放回原瓶中。
(2)将钠投入水中后,要立即将一块大小合适的玻璃片或表面皿盖在烧杯口,以防熔化的金属钠飞溅出来,酿成实验事故。
(3)由于学生化学知识的储备有限,上述实验过程中涉及的反应物、生成物要适时告诉学生,从而为下一步书写化学式做好铺垫。
(4)实验结束后,教师在黑板上分别写出上述实验涉及的几种主要物质,如钠、水、氢气、氢氧化钠、氯化钠等;在这些物质中,有的是由原子构成的(如金属钠),有的是由分子构成的(如氢气和水),有的是有离子构成的(如氢氧化钠、氯化钠);基于这三类不同微粒构成的物质,过渡到化学式的书写,不仅水到渠成而且新颖有趣,也便于提炼化学式书写的规律。
3 “包含4种反应类型的多米诺”实验
“认识几种化学反应”是义务教育课程标准对9年级学生的基本要求。在“认识几种化学反应”的复习课中,为了防止理论课的枯燥无味,避免复习课简单重复热剩饭的弊端,笔者设计了多米诺化学实验,提高了复习效果。
3.1 实验用品
300 mL塑料瓶,250 mL锥形瓶,橡皮塞,小烧杯,导气管,5%的双氧水,二氧化锰丸等。
3.2 实验装置
新设计的实验装置如图5所示。

图5 包含4种反应类型的多米诺实验装置
3.3 实验步骤
(1)提前自制二氧化锰丸。即取少许建筑水泥,在其中加入适量的水,然后将和好的水泥在二氧化锰粉末上滚成大小合适的小球,晾干即得二氧化锰丸。
(2)按图5所示,连好实验装置(A、B、C、D装置里先不装入药品),检查装置气密性,即轻轻挤压塑料瓶,如果小烧杯中冒出气泡,说明该装置不漏气。
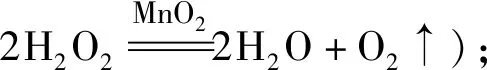
(4)实验结束,整理实验用品。
3.4 几点说明
(1)A中的双氧水、B中的稀盐酸必须足量,使后续的反应可以持续进行。
(2)C装置中的出液管(短导管),要比锥形瓶中的红色液面略高,从而使C装置中的过量盐酸顺利进入D装置中。
(3)在实验过程中,要注意引导学生观察实验现象;在实验结束后,要及时板书有关的化学方程式,并指导学生分析反应的基本类型。
(4)该多米诺化学实验,既可以用来导入情境,也可以作为复习课中间环节的教学素材,从而发挥实验的创设问题情境、激发学习兴趣、深化知识技能等作用。
总之,作为一线化学教师,我们要想方设法开发实验教学资源,尤其是在教育装备条件不断优化的情况下,一定要开齐、开足、开好化学实验,从而充分发挥化学实验的激趣、培智、练技、树人等功能。

