不同种植体上部结构对犬牙龈组织的影响
周美玲,于晋,屈直,王稚英
(锦州医科大学附属第二医院,辽宁 锦州 121000)
烤瓷熔附金属(porcelain fused to metals,PFM)全冠能完整恢复牙体的形态及功能,抗折力强,且颜色、外观逼真,色泽稳定,表面光滑,耐磨性和抗冲击性强,是目前临床上较为常用的固定修复方法。但牙科合金的金属元素释放是一个潜在影响牙科病人的健康问题[1]。众所周知,金属能引起皮肤的过敏或诱导炎症发生反应,而这些都是金属元素被释放的结果,其会造成相邻组织的细胞生物毒性[2-3]。铸造修复体被放置在与口腔组织密切接触的各个不同部位可能会引起接触部位或相邻组织不良反应如牙龈炎和牙周炎。镍离子可以在人类口腔黏膜细胞和角质形成细胞聚集,激活单核细胞和上皮细胞抑制或促进内皮细胞的细胞间黏附分子1表达[4-5]。此外,镍能够诱导表面抗原的表达调控,而高浓度的LPS影响刺激巨噬细胞的基本功能[6-7]。肿瘤坏死因子-α(TNF-α)已被报道与许多骨吸收和炎症相关,导致细胞增殖,细胞迁移,细胞凋亡和坏死。本研究主要研究两种金属全冠修复体对于犬牙龈组织中TNF-α和NF-κB的表达量,用于对临床种植体上的金属全冠的使用提供理论依据。
1 材料与方法
1.1 主要试剂和仪器
金刚砂车针(日本MANI)、硅橡胶印模材(瑞士康特coltene RAPID LINER)、美佳境A+种植体(台湾美佳境)、3M ESPE水门汀粘结剂、环氧树脂(美国3M ESPE公司);镍铬合金(北京乐乐嘉齿科有限公司);钴铬合金(钴不少于25%,钼不少于4%,钴、镍、铬3种加起来不少于85%,北京乐乐嘉齿科有限公司);LEICA EM UC6超薄切片机(德国 LEICA公司);JEM-1200EX 型透射电子显微镜(日本电子公司);ZEISS A1光学显微镜(ZEISS 公司);CIAS-1000型细胞图像分析仪(北京大恒图像视觉有限公司)。
1.2 实验动物选择及分组
选择清洁级、健康成年雄性杂种犬12只,年龄2岁,质量15~18 kg。前期试验中每只犬每侧下颌均有2颗种植体;右侧制作镍铬合金PFM冠,左侧制作钴铬合金PFM冠,上颌同名牙位为正常对照组。实验动物由锦州医科大学实验动物中心提供。实验于2017年9月至2018年2月在锦州医科大学第二临床医院口腔科学实验中心完成。实验动物犬生产许可证号:SCXK(辽)2010-0002。
1.3 标本获取与处理

1.4 牙龈组织病理变化
切取每颗修复体对应的犬牙龈及其上颌同名牙位健康犬牙龈一小块,放入质量浓度为4%多聚甲醛固定液中固定24 h。常规乙醇脱水,石蜡包埋,制成5 μm厚切片,行HE染色。光镜下牙龈组织病理变化。
1.5 Western Blot检测NF-κB、TNF-α的表达
组织蛋白提取,配制SDS-PAGE凝胶进行电泳,将蛋白转移到膜上,转膜结束后,将PVDF膜浸泡于含5%的脱脂乳的PBS中,4 ℃封闭过夜。次日,弃掉封闭液,立即加入一抗(稀释,稀释液为5%的脱脂乳)与PVDF膜一同在37 ℃水平摇床中孵育1 h。弃掉稀释的一抗溶液,PBST漂洗3次,每次5 min,以二抗(稀释,稀释液为5%的脱脂乳)孵育,室温水平摇床中孵育1 h。弃掉二抗,PBST漂洗3次,每次5 min。孵育底物1 min。
1.6 统计学处理
数据采用SPSS 13.0统计分析软件进行方差分析,比较正常对照组与各处理组之间是否有统计学差异。
2 结 果
术后各组犬均成活,精神状态、饮食、活动正常,全冠无脱落进入结果分析。
2.1 术后牙龈组织形态学观察
术后第3个月:光镜下观察到镍铬实验组,钴铬实验组牙龈组织形态均有充血,炎性细胞浸润,细胞空泡,而正常对照组血管充血较轻,炎细胞浸润不明显,见图1A、图1B、图1C。
术后第6个月:镍铬实验组牙龈有充血,炎性细胞浸润,空泡面积比钴铬合金组要多,并且棘层增生明显,而正常对照组炎细胞浸润不明显,见图2A、图2B、图2C。
术后第12个月:镍铬合金牙龈组织的炎症细胞浸润,棘层变化明显,重度异常增生,并突破基底膜向结缔组织侵润生长,钴铬合金组牙龈组织无炎症,无血管充血,正常对照组炎细胞浸润不明显,见图3A、图3B、图3C。
2.2 Western blot检测
2.2.1 NF-kB的表达情况
镍铬合金组在术后3个月有少量表达,与钴铬合金组相有明显差异(P<0.05),术后6个月、12个月与钴铬合金组相比显著表达(P<0.01),在12个月表达量最多,见表1、图4。

A:正常对照组;B:镍铬合金修复体;C:钴铬合金修复体

A:正常对照组;B:镍铬合金修复体;C:钴铬合金修复体

A:正常对照组;B:镍铬合金修复体;C:钴铬合金修复体

表1 NF-kB在不同时期的表达量的灰度值比较
2.2.2 TNF-α的表达情况
镍铬合金组在术后3个月有少量表达,与钴铬合金组相有明显差异(P<0.05),术后6个月12个月与钴铬合金组相比显著表达(P<0.01),在12个月表达量最多,见表2、图4。

表2 TNF-α在不同时期的表达量的灰度值比较
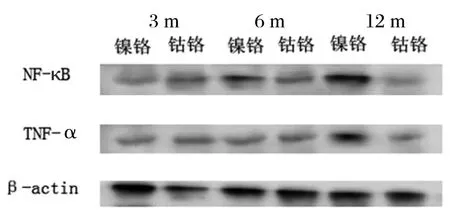
图4 Western blot结果
3 讨 论
近些年的研究发现,口腔中的金属材料在戴用一段时间后,在合金周围的刮片及牙龈中均可发现析出的金属离子,唾液中的离子浓度也会升高,产生不利的生物学效应[8-10],本实验结果发现,在HE染色中,镍铬合金会造成牙龈组织形态学的改变,并且随着时间的延长呈加重趋势,说明这些释放的金属元素和其他的蛋白结合形成有害于局部或者全身的化合物,造成机体损害。有研究显示长期接触低浓度的Ni和Cr离子元素,可能导致在肾脏的积累[11]。
本实验研究发现镍铬合金组会导致有牙龈炎症的发生,导致炎症产生的主要因素常常是炎症前递质的功能紊乱,因此评估合金的生物相容性可以考察其对炎症前递质分泌和表达的影响,其中TNF-α无论对于一般的组织还是牙周组织都是重要的炎性递质。何慧明等[12]研究表明,用LPS刺激不同牙科金属材料,TNF-α、白细胞介素1α等细胞因子会被单核细胞或巨噬细胞分泌。Horowitz等[13]人发现,把钴铬合金和巨噬细胞放到一起培养,可以导致TNF-α的产生,但不会造成明显的TNF-α、IL-6的产生。
口腔上皮组织在炎症和肿瘤的入侵和改造的情况下,病变的炎症或肿瘤组织组织会造成TNF-α激活NF-κB,造成基质TNF-α和NF-κB的过度表达,炎症和肿瘤组织是它们之间链接的通道[14]。NF-κB促进白细胞介素2的转录和介入T细胞的活化及促炎性细胞因子的反应,许多类型的细胞,如TNF、IL-1和细菌脂蛋白[15]。据Alifui-Segbaya等[16]的研究,在炎症过程中激活NF-κB诱发病变的恶变,这种细胞因子参与T细胞的活化从而促进转录的IL-2和促炎细胞因子,如肿瘤坏死因子的反应;在炎性浸润的条件下, NF-κB和TNF-α的过度表达呈正相关关系,本实验研究证实了这一点。
实验Western blot检测表明镍铬合金引起NF-κB和TNF-α分泌的增加在第3个月和第6个月第12个月均有,钴铬合金在第3个月和第6个月均引起NF-κB和TNF-α的增加,但第12个月NF-κB和TNF-α减少,实验结果表明,随着时间的延长,各种金属材料间的刺激性有差异,不同材料对于细胞因子的分泌影响是不同的,并且在相同条件下,NF-κB和TNF-α的表达呈正相关关系。
本实验采用Western blot对镍铬合金和钴铬合金修复后局部牙龈组织的NF-κB及TNF-α的分析结果表明:种植戴用两种修复体3个月后,局部牙龈组织中的NF-κB及TNF-α含量升高,说明戴用两种修复体后,基底合金金属离子会渗透到牙龈组织中,并且HE染色发现细胞核固缩,空泡性变,表明局部有炎症的产生,并且黑白灰度值检测中发现钴铬合金和镍铬合金两者之间有差异,说明两种金属间刺激性不同;戴用6个月后,镍铬合金周围牙龈组织中的NF-κB及TNF-α表达含量持续增高,钴铬合金修复体周围的NF-κB及TNF-α表达含量有所减少,灰度值的检测发现钴铬合金和镍铬合金有明显差异,HE染色图片发现镍铬合金中的上皮棘层组织增生要比钴铬合金明显,说明钴铬合金的炎症逐渐减轻,镍铬合金随着时间的增加有加重趋势;戴用两种修复体12个月后,镍铬合金的NF-κB及TNF-α表达含量持续增多,钴铬合金的NF-κB及TNF-α表达含量持续降低,两者之间的黑白灰度值检测发现,钴铬合金与镍铬合金相对比有显著差异,HE染色结果发现,钴铬合金组上皮组织恢复明显,而镍铬合金组上皮重度异常增生,并突破基底膜向结缔组织侵润生长,说明随着时间的延长,镍铬合金组的刺激明显,炎症因子的表达明显,钴铬合金组随着时间改变,症状逐渐减轻,表明两者虽然刺激性不同,但是钴铬合金明显优于镍铬合金,钴铬合金组的NF-κB及TNF-α表达含量的减少的原因需要今后实验的进一步的研究。

