蔗糖水解制取结晶果糖技术研究
胡瑞云,王智能,杨 柳,杨 婷,应雄美,郭家文,沈石妍,李艳芳
【糖产品研发与检测】
蔗糖水解制取结晶果糖技术研究
胡瑞云,王智能,杨柳,杨婷,应雄美,郭家文,沈石妍*,李艳芳
(云南省农业科学院甘蔗研究所 云南省甘蔗遗传改良重点实验室,云南开远 661699)
为提升制糖产业的综合效益,以白砂糖为原料开发附加值更高的结晶果糖,探讨用蔗糖原料制取高纯度结晶果糖的最优工艺方法。实验以高浓度蔗糖液(55%w/w)为原料,食品酸味剂柠檬酸为水解剂,通过蔗糖水解、脱色、阴阳离子树脂除盐,以钙型树脂分离、纯化果葡糖液,在常温下得到结晶果糖和结晶葡萄糖。实验优化蔗糖最佳水解工艺条件:水解温度80℃,水解时间4.0 h,柠檬酸用量0.50%,蔗糖水解率为100%;果糖结晶工艺条件:在水-乙醇比例为1∶4的体系下,果糖纯度88%以上、糖膏固形物含量87°Bx以上、晶种用量为糖膏总量5%、养晶时间48 h,果糖结晶率达到56.34%;葡萄糖结晶工艺条件:在水-乙醇比例为1∶2的体系下,葡萄糖纯度65%以上、糖膏固形物含量83°Bx以上、晶种用量为糖膏总量5%、养晶时间48 h,葡萄糖结晶率达到63.27%。实验选择高浓度蔗糖液水解及常温下结晶的方式,可降低能源消耗,同时通过将纯度65%以上的葡萄糖液直接结晶分离,使母液中果糖纯度从33.3%提升至60.2%,起到了分离纯化果糖液的效果,有效减轻果葡糖液的分离负荷。
蔗糖;果糖;葡萄糖;水解;分离;结晶
0 引言
果糖甜味纯正,是自然界最甜的单糖,其甜度大约为蔗糖的1.8倍、葡萄糖的3倍[1]。果糖不会掩盖食品的风味,还具有增强食品风味的作用,加之它比蔗糖和葡萄糖具有更大的溶解度和更快的溶解速度,因而,被广泛地应用于饮料和食品行业。果糖不致龋齿,各年龄段的人群均可放心食用。果糖易吸收、代谢快,代谢过程不依赖胰岛素,对人体血糖浓度的影响非常小,是糖尿病患者、肝病患者甜味剂和能量来源的优选[1]。随着人们健康意识的不断提高以及特殊人群对甜味剂的特殊需求,果糖的需求量逐年上升,加之其在医疗领域方面的重要作用,使果糖具有较好的市场前景。
目前果糖工业化生产多以淀粉为原料,通过水解得到葡萄糖,再经固定化葡萄糖异构酶转化为果糖含量42%的果葡糖浆,经树脂分离纯化,最后结晶得到结晶果糖。以白砂糖(蔗糖)为原料经水解、分离、异构、结晶等工序生产结晶果糖是更直接的一种果糖生产方法。我国是世界第3大蔗糖生产国,白砂糖的年产量超过1000万t,但总体来说产品价值较低。结晶果糖售价依纯度不同存在较大差异,大约在1.6~2.4万元/t,比蔗糖高3~4倍,国内白砂糖价格受国际糖价的影响较为严重,市场价格波动较大,在蔗糖生产效益不佳的形势下,以白砂糖为原料开发附加值更高的结晶果糖产品,对提升蔗糖产业的综合效益具有重要的作用[2]。
以蔗糖为原料开发结晶果糖的工艺研究一直受到广大科研工作者的重视,针对生产工艺的优化取得了相应的研究成果。黄立新等[3]对盐酸、柠檬酸、酒石酸等水解剂对蔗糖的水解效果进行对比。结果表明:在浓度为55%的蔗糖溶液中,有机酸用量0.15%(w/w蔗糖)、温度85℃、水解时间150 min,蔗糖转化率约90%。徐珊珊[4]通过2次阴阳离子交换后淀粉质水解糖液的色值从604 IU降低至0 IU,电导率从196 μS/cm降至2 μS/cm。徐珊珊、Tong等[4-5]利用大孔强酸基聚苯乙烯树脂转型为Ga型树脂分离果葡糖浆,通过对吸附和洗脱条件的优化,分离得到的果糖纯度为90%以上。聂圣才[6]模拟结晶果糖的中试放大实验,以6根φ 50 mm×1000 mm的交换柱分离浓度F45果葡糖浆总回收率为60%。杨瑞金等[7]研究发现,果糖在60℃、pH 4.0时结晶果糖比较稳定。李闯等[8]的果糖结晶实验显示,在水-乙醇比例为1∶4的体系下,果糖纯度90%以上、糖膏固形物含量85°Bx以上、晶种用量为固形物总质量10%、养晶时间9~36 h的条件下,果糖结晶率达到60.51%。闫序东[9]优化的果糖结晶工艺条件为:晶种添加量为2%,初始过饱和度为1.02~1.08,乙醇对水的添加量为20%,Span 60用量为100 mg/kg,最终提糖率为56.92%。
实验拟以蔗糖(白砂糖)为原料,选择食品酸味剂柠檬酸替代盐酸为蔗糖水解剂,优化蔗糖水解过程的控制条件。通过HPD 100树脂脱除水解液色素[10],采用D 001 FD强酸性阳离子、D 354弱碱性阴离子树脂进行水解液的脱盐精制,以D 001 FD 钙型树脂实现果糖和葡萄糖的分离,得到了高纯度的果糖液。最终对结晶果糖生产工艺进行了实验室模拟扩大实验,为结晶果糖生产提供技术参考。
1 材料与方法
1.1 实验材料
材料:无水葡萄糖、D-果糖、蔗糖(标准品,上海源叶生物科技有限公司);乙腈(色谱纯,默克股份公司);无水乙醇(色谱纯,天津市致远化学试剂有限公司);柠檬酸(分析纯,天津风船试剂科技有限公司);HPD 100大孔吸附树脂(郑州勤实科技有限公司);D 354 FD弱碱型阴离子树脂,D 001 FD强酸型阳离子树脂(浙江争光实业股份有限公司)。
仪器:φ50 mm×500 mm离子交换柱,锦州新科水处理设备厂;WYA-2S数字阿贝折射仪,上海仪电物理光学仪器有限公司;DDSJ-308A电导仪,上海仪电物理光学仪器有限公司;Waters E2695液相色谱仪,美国Waters公司;BAS 224S 型电子分析天平,赛多利斯科学仪器(北京)有限公司;UV-5800 PC紫外分光光度计,上海元析仪器有限公司;ZD-3A自动电位测定仪,上海本昌科学仪器有限公司;AE-3000旋转蒸发器,上海亚西生化仪器厂;SHZ-95B型循环水真空泵,上海互佳仪器设备有限公司;BT 100 SV2-CE蠕动泵,保定雷弗流体科技有限公司。
1.2 实验方法
1.2.1 蔗糖水解过程色值的变化
配制55%(w/w)蔗糖液,添加蔗糖液质量的1.0%柠檬酸,分别控制水浴温度75、80、85、90、100℃,观测水解时间2.5、3.0、3.5、4.0、4.5 h蔗糖液色值的变化。
1.2.2 蔗糖水解条件优化
配制55%(w/w)蔗糖液,以柠檬酸为水解剂,柠檬酸用量(w/w蔗糖液)参考余小娜[11]、黄立新[3]等实验筛选蔗糖水解条件,结合水解温度、时间对蔗糖色值的影响,初步确定蔗糖三因素四水平正交实验(见表1),以蔗糖水解完成情况为判断依据,确定最优水解条件。
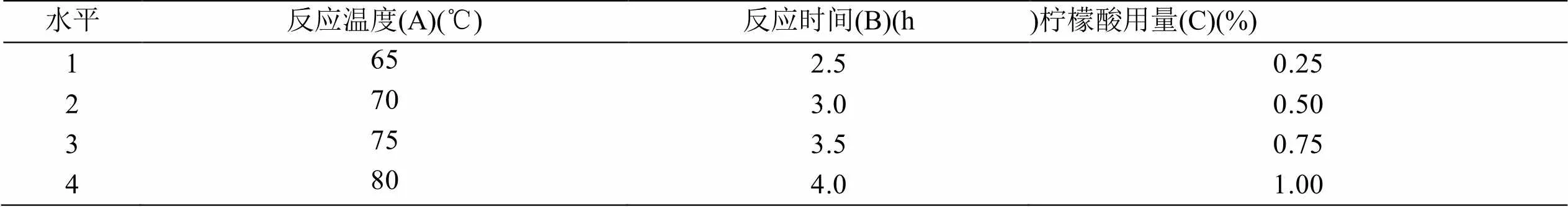
表1 蔗糖水解正交实验因素水平
1.2.3 白砂糖生产结晶果糖模拟实验
(1)脱色、脱盐树脂预处理:预备HPD 100脱色树脂600 mL 1组、D 001 FD强酸型阳离子树脂700 mL 1组、D 354弱碱型阴离子树脂700 mL 1组。使用前均用纯水活化,装入离子交换柱中,纯水冲洗至中性备用,使用一定周期后树脂交换容量不理想时,依次使用4%~5%的HCl以及NaOH溶液再生。
(2)果糖分离树脂预处理:选用D 001 FD强酸型阳离子树脂转型为Ca型树脂分离果葡糖液[4]。将8组离子交换柱串联,每柱装入经纯水活化的树脂800 mL,用1 mol/L CaCl2溶液通过树脂置换转化为Ca型树脂,用清水清洗至中性备用。
(3)蔗糖液的水解、精制:配制55%(w/w)蔗糖液4800g,按优化确定的最佳水解条件于水浴锅中完成水解。将水解液以3 BV/h的速度依次通过HPD 100脱色树脂、D 001 FD强酸型阳离子树脂和D 354 FD弱碱型阴离子树脂进行脱色和2次脱盐,对糖液进行精制。
(4)果葡糖液的分离:常温下将水解糖液以0.6 BV/h(64 mL/min)速度通过串联的8组φ50 mm×500 mm交换柱,当糖液从最末端树脂溢出时停止加料,纯水解吸,分段收集解吸液,据各段样品组分含量情况进行循环分离,直至分离出纯度达88%以上的果糖液和纯度65%以上的葡萄糖液。
(5)果糖和葡萄糖的结晶、分离、干燥:果糖有较大的溶解度,25℃时1 g水可以溶解4.08 g果糖,但只能溶解2.11 g蔗糖和1.11 g葡萄糖。30℃下果糖饱和溶液浓度81.9%,致使果糖饱和溶液的粘度很大,较大的粘度降低了母液的流动性,阻碍结晶过程中的传质,添加乙醇可降低糖液粘度,有利于果糖的结晶与分离。糖液过饱和系数在1.0~1.2,可使存在的晶体长大。实验拟定:纯度88%以上果糖液,调节pH 4~5,于65℃、0.085 MPa真空下浓缩至85~88°Bx,即过饱和系数在1.04~1.07停止浓缩,调整浓缩糖膏中水-乙醇比例为1∶4,当温度低于45℃时加入浓缩糖膏量5% 的果糖粉作为晶种,常温下结晶24 h~72 h后,真空抽滤、醇洗分离结晶体,于65℃真空干燥得到结晶果糖,观测结晶得率以及分离母液中果糖含量的变化。
葡萄糖20℃时100 g水中溶解度为83 g,即20℃葡萄糖饱和溶液浓度为45.4%,溶解度明显低于蔗糖、果糖,同比更易结晶。参考煮制白砂糖的结晶工艺,即相对纯度较高的糖浆,可选用低浓度起晶,反之,则可选用高浓度起晶煮制[12]。因此,葡萄糖结晶采用低纯度,稍高浓度的结晶方式,实验拟定:纯度65% 以上葡萄糖液,调节pH 4~5,于65℃、0.085 MPa真空下浓缩至80~85°Bx,停止浓缩,调整糖膏水-乙醇比例为1∶2,低于45℃加入糖膏量的5%葡萄糖粉起种结晶,常温下结晶24~72 h后,真空抽滤、醇洗分离结晶体,于65℃真空干燥得到结晶葡萄糖,观测结晶得率以及分离母液中果糖含量的变化。
1.2.4 产品指标的检测及计算方法
实验中糖液色值、浊度等指标检测方法依据制糖分析相关方法检测分析[13],果糖、葡萄糖、蔗糖含量的检测方法采用高效液相色谱法检测[14]。果糖、葡萄糖最终产品依据中华人民共和国国家标准GB/T 26762-2011《结晶果糖、固体果葡糖》[15]、GB/T 20880-2018《食用葡萄糖》[16]、中华人民共和国药典2015版2部《果糖》[17]规定的指标和检测方法进行检测。各指标计算依据如下:
果糖(葡萄糖)结晶率(%)=结晶果糖质量/(糖膏质量×固形物含量×果糖(葡萄糖)纯度)×100%·········(1)
果糖(葡萄糖、蔗糖)纯度(%)=果糖(葡萄糖、蔗糖)含量/(果糖含量+葡萄糖含量+蔗糖含量)×100%······(2)
2 结果与分析
2.1 水解温度、时间对蔗糖水解过程色值的影响
从图1看出:水解前蔗糖液色值为95.3 IU,随水解时间的延长,水解温度的升高,糖液色值逐渐加深,当水解温度为85℃时,糖液色值开始变化明显,4.5 h后色值增幅达33.4%;在沸腾状态下,糖液色值显著升高,4.5 h后色值增幅达277.17%;水解温度为80℃时,糖液色值变化非常轻微,4.5 h后色值增幅仅为18.22%。因此,适当降低水解温度对降低糖液色值非常有利,初步确定正交实验水解温度范围为65~80℃。
2.2 蔗糖水解正交实验结果
蔗糖水解三因素四水平正交实验结果见表2。由表中R和K值可知:三因素影响蔗糖转化的主次顺序为A>B>C,各因素的最好水平是A4B4C2,即蔗糖水解影响力为:反应温度>反应时间>柠檬酸用量,各因素的最好水平为:温度80℃、反应时间4 h、柠檬酸用量0.5%。
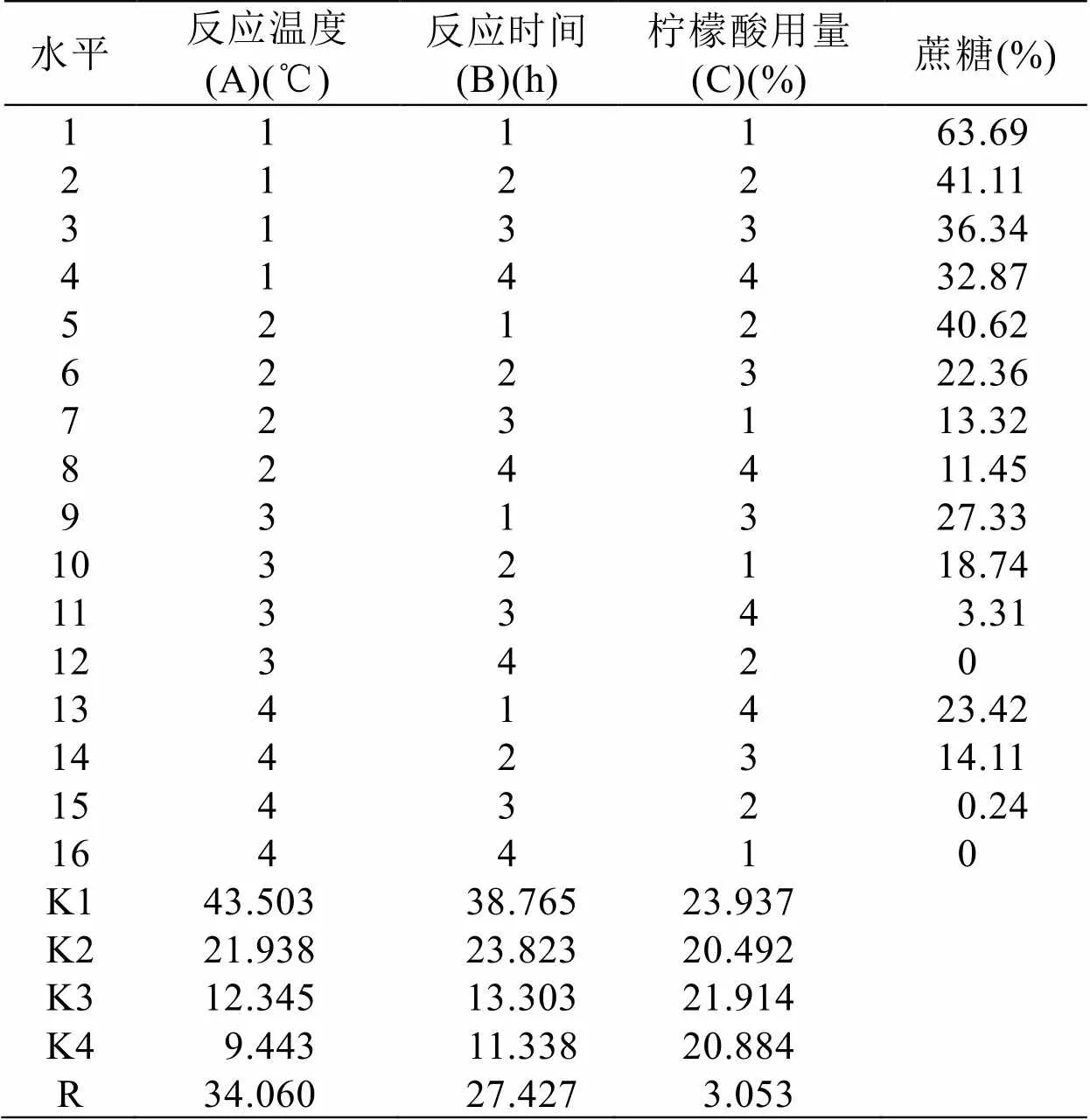
表2 蔗糖水解正交实验结果
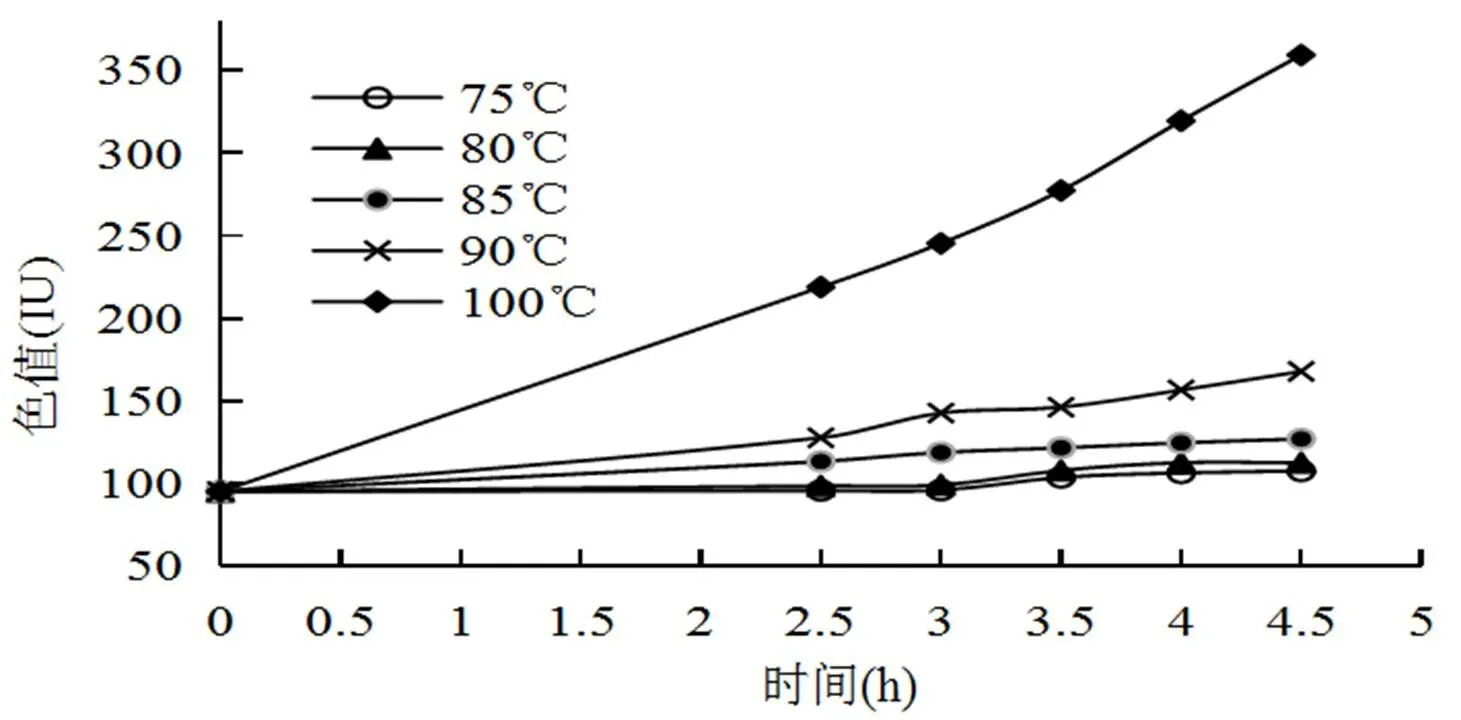
图1 蔗糖水解色值变化图
由方差分析表3可知:A、B、C三因素的显著水平值分别为0、0、0.434,A、B二因素显著水平值均小于0.05,对蔗糖水解结果有显著影响,C因素显著水平值大于0.05,说明柠檬酸用量在0.25%~1.00%期间对蔗糖水解的影响力区别不明显。
综合考虑正交试验结果与后续工艺过程脱色和脱盐的处理负荷,选择较低柠檬酸用量和适当降低水解温度的方式优化水解条件,最终确定的较优水解条件为:水解温度80℃,水解时间4.0 h,柠檬酸用量0.50%(w/w对蔗糖液),此时蔗糖液为pH 2.35,该条件下实验结果显示蔗糖含量测定为0%,蔗糖全部水解,后续模拟水解实验均在此条件下进行。
2.3 制取结晶果糖的模拟实验
2.3.1 蔗糖液的水解、精制
配制浓度55%(w/w)蔗糖液4800 g,添加0.50%柠檬酸(w/w对蔗糖液),控制水解温度80℃,水解时间4.0 h,经检测水解液蔗糖含量为0%,果糖含量49.52%。将水解液以3 BV/h的速度通过脱色和脱盐树脂的精制处理后,得到46.6°Bx糖液5660 g(4380 mL),实验结果如表4所示:色值从115.9 IU降至5.4 IU,浊度从81.9 MAU降至10.0 MAU,电导率从116.8 μS/cm降至4.0 μS/cm,色值、浊度、电导率等指标得到大幅的降低,pH升至7.5,离子交换树脂对糖液起到很好的脱色和脱盐的作用。
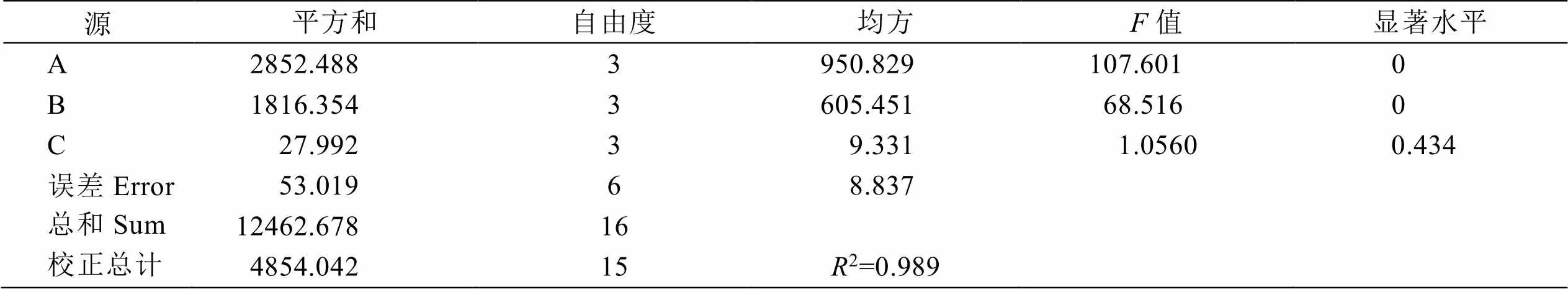
表3 蔗糖水解正交设计方差分析表
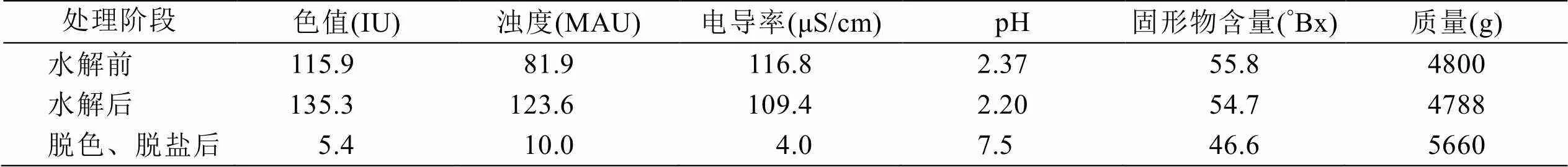
表4 蔗糖水解液指标情况
2.3.2 果葡糖液的分离
精制后水解糖液中果糖、葡萄糖纯度约各占50%,常温下以65 mL/min速度通过8组串联的交换柱,每850 mL收集解吸液一组,至最末组有糖液溢出时终止糖液吸附,此时共吸附46.6°Bx糖液5660 g(4380 mL),以65 mL/min的速度纯水进行解吸,从图2和表5可看出:在解吸初期(葡萄糖富集期)果糖纯度仅为11.5%~43.1%,解吸中期(果糖富集期)果糖纯度达到49.7%~80.4%,解吸后期(纯果糖期)果糖纯度达到84.0%~100%,3个期间果糖平均纯度分别为35.76%、60.6%、88.4%。如图3和表5所示,将中期纯度60.6%高果糖液(36.3°Bx 3400 mL),再次通过7组交换柱分离,每650 mL收集样液一组,解吸初期、中期、后期3个期间果糖平均纯度分别为33.2%、65.0%、90.6%,解吸中期果糖平均含量从表5中的60.6%提高至65.0%。
从图2、图3显示:不同纯度含量的果糖液,解吸分离的特征有所不同,果糖纯度为50%的水解液分离时果糖、葡萄糖分离的组分含量、时间差异不太明显;当果糖纯度从50%提高至60%以上,组分含量差异明显增大,第2次再分离比第1次纯化果糖的含量得到明显提升;按此方法循环分离操作4次后全部糖液完成分离,最终可得到纯度达88%以上的纯果糖液。
2.3.3 果糖、葡萄糖的结晶、分离、干燥
表6中蔗糖水解液经过4次分离得到4个批次纯度88%以上果糖液,第1、2批次糖液于65℃、0.085 MPa真空下浓缩至87°Bx,停止浓缩,加入乙醇使体系中水-乙醇比例为1∶4,冷却至45℃,按糖膏质量221 g加入5%果糖晶种结晶,常温下养晶48 h后,续料补充第3、4批次浓缩纯果糖膏357 g继续养晶,至最末次补料后,养晶48 h结晶完成,真空抽滤分离果糖晶体、醇洗晶体3次,于65℃、0.075 MPa真空下烘干得结晶果糖产品265 g。
从表6看出:蔗糖水解液经过4次分离,得到4个批次纯度65%以上葡萄糖液,第1批次糖液于65℃、0.085 MPa真空下浓缩至83°Bx,停止浓缩,调整糖膏中水-乙醇比例为1∶2的体系下,冷却至45℃,按糖膏质量1260 g加入5%葡萄糖粉起晶,常温下养晶24 h后,分别续料补充第2、3、4批次浓缩葡萄糖膏403 g、386 g继续养晶,至最末次补料后,养晶48 h结晶完成,真空抽滤分离葡萄糖晶体,醇洗晶体3次,于65℃、0.075 MPa真空下烘干得到结晶葡萄糖产品691 g。
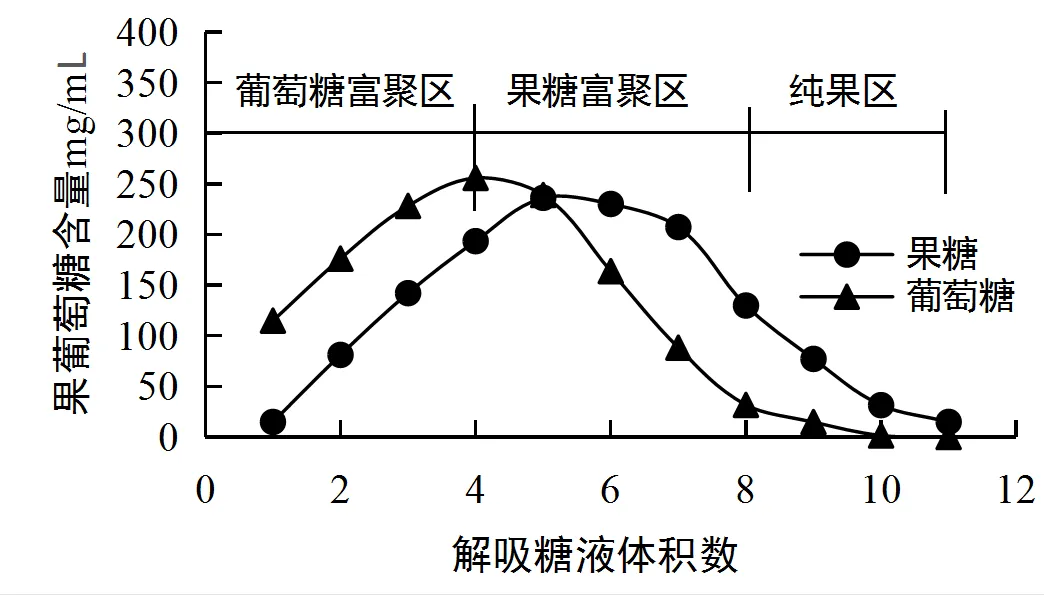
图2 纯度50%果葡糖液解吸图
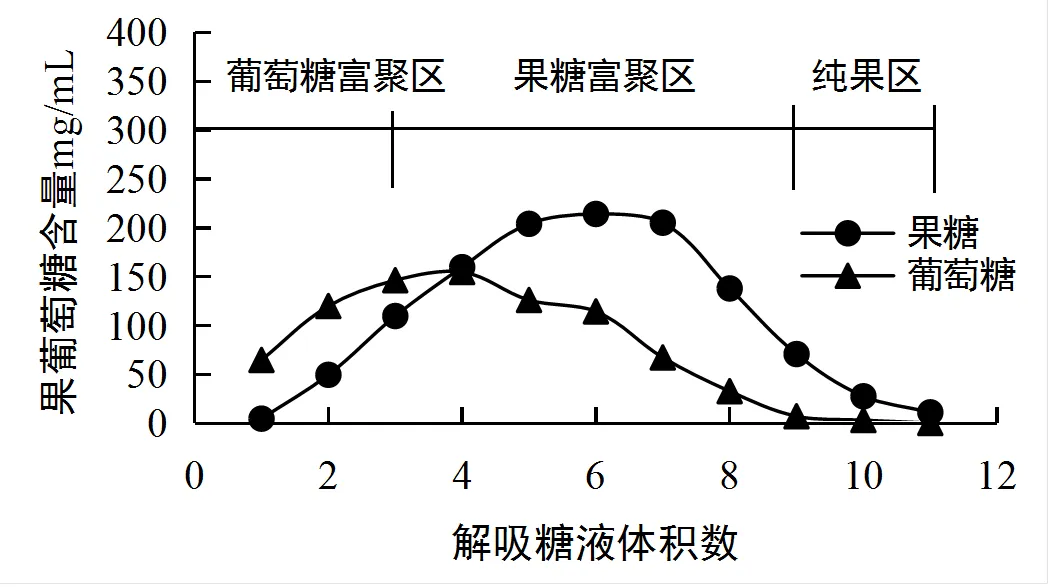
图3 纯度60%果葡糖液解吸图
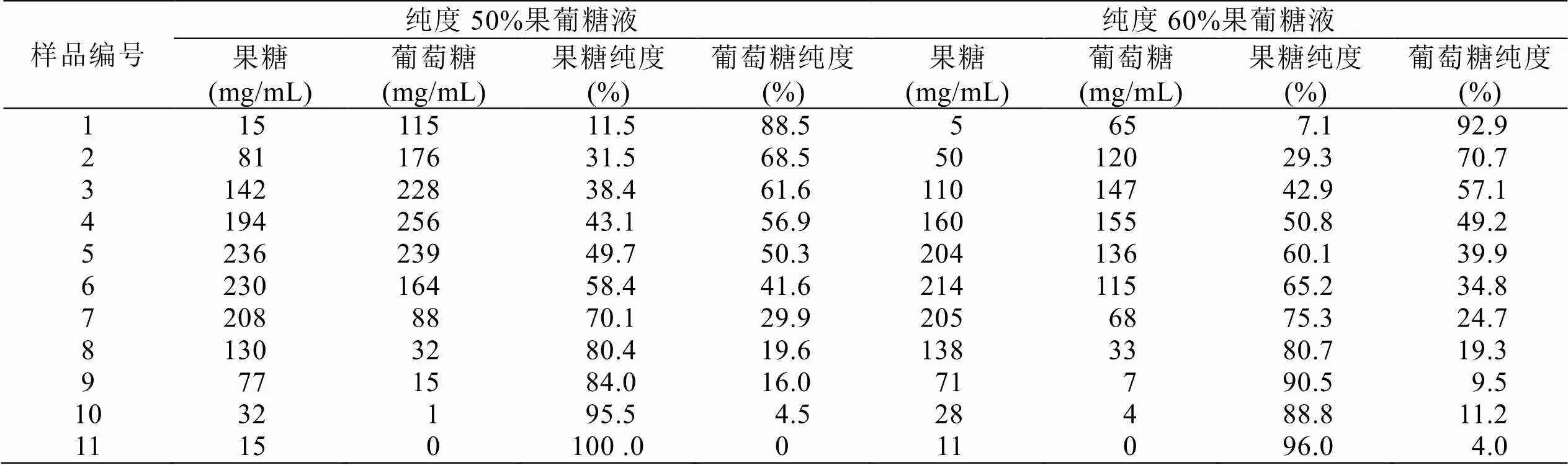
表5 50%和60%纯度果葡糖解吸液组分含量
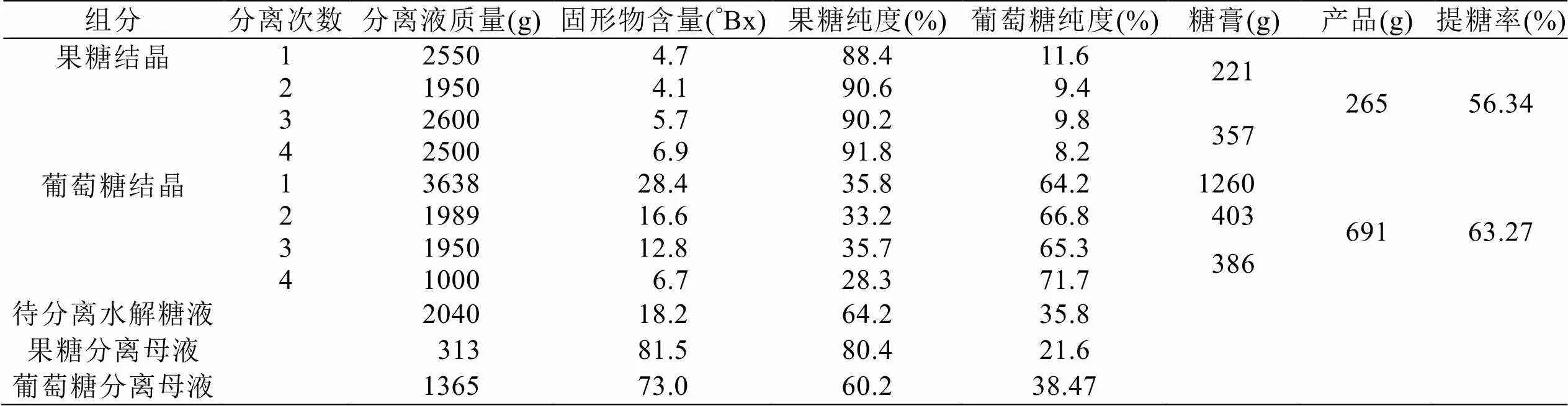
表6 果糖、葡萄糖结晶过程物料指标
从表6可看出:①果糖结晶分离后得到313 g、81.5°Bx的分离母液,母液中果糖的纯度从90.4%降至80.4%;②葡萄糖结晶分离后得到1365 g 73.0°Bx的分离母液,母液中果糖的纯度从33.3%提升至60.2%,起到了分离纯化的效果。
实验投入白砂糖2640 g,果糖、葡萄糖的单次结晶分别得到265 g、691 g,果糖、葡萄糖单次结晶率分别为56.34%、63.27%,尚存待分离果葡糖液2040 g、果糖分离母液313 g、葡萄糖分离母液1365 g;后续把3种在制品混合调制后得到高果糖液3164 g(纯度64.28%,51.3°Bx),再次通过树脂多级分离、浓缩结晶得到结晶果糖、葡萄糖产品1 030 g、584 g;最终投入糖分总回收率达97.4%,有2.6%糖分损失主要为树脂交换过程中较低浓度的糖液未收集以及树脂中残存的糖液等损失。
2.3.4 产品检测结果
从表7可以看出:制备得到的结晶果糖产品检测指标同时到达GB/T 26762-2011《结晶果糖、固体果葡糖》和中华人民共和国中国药典版2015版2部《果糖》的标准要求,说明以蔗糖为原料,采用本实验的工艺方法制取的结晶果糖经阴阳离子交换以及钙型树脂对果葡糖液的不断分离对结晶果糖产品起到了很好的脱色、脱盐和纯化的作用。
依据GB/T 20880-2018《食用葡萄糖》标准检测结果显示:葡萄糖含量(占干物质)液相色谱法:86.75%~97.54%之间(一级品标准≥99.0%);水分:1.06%~8.63%之间(一级品标准≤2.0%);比旋光度:48.13°~51.73°(一级品标准≤52.0°~53.5°);其余指标检测均符合标准要求。检测结果显示:葡萄糖产品含量有一定的波动幅度,适当提高葡萄糖液的结晶纯度及适当加大结晶葡萄糖的醇洗分离可提升葡萄糖产品的含量。葡萄糖产品若用于食品工业,对产品理化指标要求不高的前提下采用此工艺生产葡萄糖可减少葡萄糖分离纯化的环节,降低能源消耗,节约生产成本。
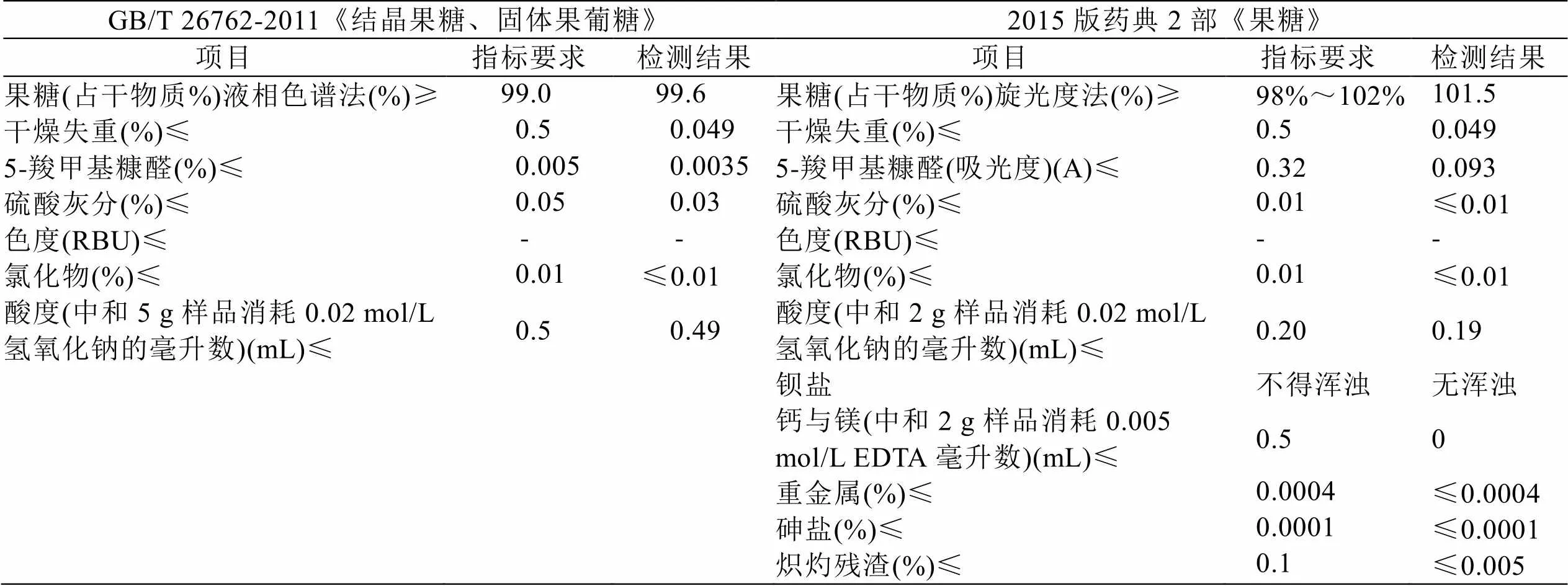
表7 果糖产品指标检测对照表
3 结论与讨论
(1)水解温度和水解时间均对水解糖液的色值有影响,当水解温度为85℃时,水解4.5 h后色值增幅达33.4%;在沸腾状态下,水解4.5 h后色值增幅达277.17%;水解温度为80℃时,4.5 h后色值增幅仅为18.22%,适当降低水解温度可减轻糖液色值增幅。
(2)精制处理后的糖液色值为5.4 IU,浊度为10.0 MAU,电导率为4.0 μS/cm,试验显示HPD 100脱色树脂、D 001 FD强酸型阳离子树脂和D 354 FD弱碱型阴离子树脂满足对糖液脱色和脱盐的作用,对最终产品指标检测符合药典版标准要求起到了决定性的作用。
(3)试验优化蔗糖水解最佳水解条件为:水解温度80℃,水解时间4.0 h,柠檬酸用量0.50%,蔗糖水解率为100%。与余小娜[11]、黄立新[3]等优化的实验结果柠檬酸用量0.9%、0.15%(w/w蔗糖),水解温度85、90℃相比,通过适当延长水解时间,降低水解温度有效减少了色素的产生,同时降低后续脱色、除盐的负荷。
(4)果糖结晶工艺条件:纯度88%以上果糖液,固形物含量87°Bx,调整糖膏中水-乙醇比例为1∶4,温度低于45℃加入糖膏量的5%果糖晶粉起晶,常温下结晶48 h后,真空抽滤、醇洗分离结晶体,65℃真空干燥得到结晶果糖,果糖单次结晶率为56.34%;葡萄糖结晶工艺条件:纯度65%以上葡萄糖液,固形物含量83°Bx,调整糖膏中水-乙醇比例为1∶2,温度低于45℃加入糖膏量的5%葡萄糖晶粉起晶,常温下结晶48 h后,真空抽滤、醇洗分离结晶体,65℃真空干燥得到结晶葡萄糖,葡萄糖单次结晶率63.27%。
实验选择在常温下钙型树脂分离高浓度的果葡糖液,可避免40~50℃条件下不断重复分离低浓度糖液易被微生物感染的状况,有效降低能源消耗,提高设备周转率;结晶实验在常温下进行,结晶起种量仅为糖膏的5%,同时,通过添加适量乙醇降低糖膏的粘度,提高了结晶速度,得到较好的结晶率;实验通过直接将纯度65%以上的葡萄糖液直接结晶的方式,在得到葡萄糖产品的同时也提高了分离母液中果糖纯度的作用,有效减轻果葡糖液分离负荷。
聂圣才[6]在自制模拟移动床技术制备结晶果糖研究中对比显示:果糖分离交换柱的单柱径高比为1∶10的分离效果不及径高比1∶20的交换柱,本实验果糖分离交换柱的单柱径高比为1∶10,实验过程中存在果葡糖分离时间差不太明显的现象(图2、图3所示);另外,树脂填装密实可提高分离效果,本实验选用大孔钙型树脂转型,存在树脂不易填充密实的问题,对果糖的分离效果有一些影响,试验后期可筛选比对不同树脂对果糖分离的效果,优化更适用于果糖分离的树脂。
实验选用白砂糖为原料制取结晶果糖,原料带入及生产过程中产生的杂质相对较少,后续工艺易于净化处理,同时,由于果糖的结晶采用添加适量乙醇结晶及适量乙醇醇洗分离的方式,得到的结晶果糖产品疏松不易结团,也避免了结晶分离过程及后续贮存过程微生物的污染。从产品检测结果可以看出,本工艺所制成的结晶果糖同时满足GB/T 26762-2011《结晶果糖、固体果葡糖》和中华人民共和国药典2015版2部《果糖》的标准要求,产品除可用于食品行业也可用于医用,医疗方面的广泛应用可大幅提升产品的附加值,成本优势更佳。
[1] 杨瑞金,潘允红,王文生,等. 化学法分离果糖和葡萄糖[J]. 冷饮与速冻食品工业,1997(3):28-31.
[2] 保国裕,蓝艳华. 高值化产品-蔗糖制结晶果糖方法探讨[J]. 甘蔗糖业,2015(2):49-52.
[3] 黄立新,余业棠. 酸水解蔗糖生产转化糖的研究[J]. 食品科学,2003,24(3):24-26.
[4] 徐珊珊. 高纯度结晶果糖制备技术的研究[D]. 重庆:西南大学,2007.
[5] TONG Y, SHI L X, LI W,. An investigation of the property of the complex carrier for separating fructose from fructose-glucose syrup [J]. Chemical Journal of Chinese Universities, 2000,21(5):825-827.
[6] 聂圣才. 顺序式模拟移动床技术制备结晶果糖研究[D]. 济南:山东轻工业学院,2012.
[7] 杨瑞金,潘允鸿,王文生. 果糖液的结晶性能研究[J]. 无锡轻工大学学报,1996,15(2):115-118.
[8] 李闯,王超,胡雪芹,等. D-果糖的酶法制备及其结晶条件的研究[J]. 安徽农业科学,2015,43(12):3-5,18.
[9] 闫序东.果糖结晶工艺研究[D]. 无锡:江南大学,2008.
[10] 胡瑞云,沈石妍,王智能,等. 甘蔗色素多酚提取工艺研究用[J]. 中国糖料,2019,41(3):36-39.
[11] 余小娜,盛淑玲. 转化糖浆制备工艺研究[J]. 许昌学院学报,2016,35(3):107-111.
[12] 黄广盛,李杨训,莫慧平. 甘蔗制糖工艺学:第2版[M]. 北京:轻工业出版社,1991.
[13] 中国轻工总会甘蔗糖业质量监督检测中心. 甘蔗制糖化学管理统一分析方法:第3版[M]. 北京:轻工业出版社,1995.
[14] 国家食品药品监督管理总局. 食品中果糖、葡萄糖、蔗糖、麦芽糖、乳糖的测定:GB 5009.8-2016[S]. 北京:中国标准出版社,2016.
[15] 国家质量监督检验检疫总局. 结晶果糖、固体果葡糖:GB/T 26762-2011[S]. 北京:中国标准出版社,2011.
[16] 国家质量监督检验检疫总局. 食用葡萄糖:GB/T 20880-2018[S]. 北京:中国标准出版社,2018.
[17] 国家药典委员会. 中华人民共和国药典,果糖[S]. 2部. 北京:中国医药科技出版社,2015.
Study on the Optimum Technology of Producing Crystalline Fructose by Hydrolysis of Sucrose
HU Rui-yun, WANG Zhi-neng, YANG Liu, YANG Ting, YING Xiong-mei, GUO Jia-wen, SHEN Shi-yan, LI Yan-fang
(Sugarcane Research Institute, Yunnan Academy of Agricultural Sciences/Key Laboratory of Sugarcane Biotechnology and Genetic Improvement of Yunnan, Kaiyuan, Yunnan 661699)
In order to improve the comprehensive benefits of sugar industry, the crystal fructose with higher added value is developed with white granulated sugar as raw material, and the optimal process for producing high purity crystalline fructose from sucrose is discussed. High concentration sucrose solution (55% w/w) is used as raw material and citric acid as sucrose hydrolysate. Fructose is separated and purified by calcium resin through sucrose hydrolysis, decolorization and Cation Anion Exchange. The optimal hydrolysis conditions of sucrose are as follows: The results show that hydrolysis temperature is 80℃, hydrolysis time is 4.0 h, citric acid dosage is 0.50%, and sucrose hydrolysis rate is 100%; The conditions of fructose crystallization are as follows: under the system of water ethanol ratio of 1∶4, the purity of fructose is more than 88%, the solid content of sugar paste is more than 87°Bx, the amount of seed crystal is 5% and the crystallization time is 48 h. The crystallization rate of fructose is 56.34%; The conditions of glucose crystallization are as follows: in the system of water ethanol ratio of 1∶2, the purity of glucose is above 65%, the solid content of sugar paste is more than 83°Bx, the amount of crystal seed is 5% and the crystallization time is 48 h. The crystallization rate of glucose reaches 63.27%. The method of high concentration sucrose hydrolysis and crystallization at room temperature can reduce energy consumption. At the same time, the purity of fructose in mother liquor is increased from 33.3% to 60.2% by direct crystallization and separation of glucose solution with purity above 65%. This method could reduce the effect of separation and purification of fructose solution and load of fructose solution.
Sucrose; Fructose; Glucose; Hydrolysis; Separation; Crystallization

1005-9695(2021)01-0074-08
2020-09-27;
2021-01-10
云南省重大科技专项-甘蔗所现代科研所建设(2019ZG012-01)资助
胡瑞云(1966-),女,工程师,主要从事制糖生产、酒精生产研究、管理工作;E-mail:huruiyun2005@163.com
沈石妍(1968-),女,高级工程师,主要从事蔗糖深加工及副产物综合利用方面研究;E-mail:okmlshshy@sina.com
胡瑞云,王智能,杨柳,等. 蔗糖水解制取结晶果糖技术研究[J]. 甘蔗糖业,2021,50(1):74-81.

