FOLFIRINOX 方案与AG 方案一线治疗晚期胰腺癌多中心观察性研究
袁贯平,江志敏,马冬,潘梓春,丁颖,谢德荣*
FOLFIRINOX 方案和AG 方案是目前晚期胰腺癌一线治疗的主流方案[1],Ⅲ期随机临床的资料显示 FOLFIRINOX 方案中位生存期 11.1 个月[2],AG 方案中位生存期 8.5 个月[3],从数值看似乎FOLFIRINOX 方案优于AG 方案,但由于研究间的基线资料不同,不能将研究间的结果直接进行比较。因此有学者采用网络Meta 分析的方法,间接对这两个方案进行了比较[4],认为FOLFIRINOX 方案疗效优于目前临床常用的所有方案,与AG 方案相比,死亡风险下降21%。但是临床实践中不可能完全按Ⅲ期临床研究的纳入标准及排除标准收治患者,剂量也会根据病人的实际情况作出各种各样的调整,这样Ⅲ期临床研究的结果不一定能在真实世界中完全重复[5]。真实世界临床研究的系统评价,认为FOLFIRINOX 方案和AG 方案疗效相等[6],但该系统评价存在一些不足。我们开展FOLFIRINOX 方案和AG 方案一线治疗晚期胰腺癌的多中心观察性研究,研究目的是总结经验指导临床实践。
1 资料与方法
1.1 临床资料
病例资料来源于广东省人民医院消化肿瘤内科、中山大学孙逸仙纪念医院肿瘤科、中山大学附属第一院肿瘤科、广东药科大学附属第一医院以及中山市人民医院肿瘤科。纳入标准:①2016 年1 月至2020 年6 月,在各中心住院治疗、病理诊断为胰腺癌;②无手术根治治疗指征;③未接受其它抗癌治疗的初治患者,年龄大于18 岁,体能状态评分(performance status,PS)小于或等于2 分,骨髓像或血像正常可耐受化疗;④预计生存期大于3 个月,使用 FOLFIRINOX 方案或 AG 方案的一线治疗;⑤有完整生存资料,签署知情同意书。合并其它肿瘤或接受放射治疗、免疫治疗、撤回知情同意书、未完成一个周期化疗的患者被排除
患者接受的化疗方案均为目前国内外公认的标准治疗方案,两个方案均为CSCO 推荐的晚期胰腺癌一线治疗方案,所有药物均未超适应证使用,是临床常规治疗的一部分,患者也签署化疗知情同意书。所有治疗均符合现行的胰腺癌诊疗常规,没有明显违反伦理规范。
1.2 治疗方法
一线化疗方案为FOLFIRINOX方案或AG方案,具体采用的化疗方案由各中心医生根据患者的实际情况与患者讨论后决定。FOLFIRINOX 方案剂量可以根据实际情况作出调整,临床调整较多的是将氟尿嘧啶400 mg/m2静脉推注取消、伊立替康由 180 mg/m2降为 160 mg/m2、奥沙利铂 85 mg/m2。
1.3 观察指标
主要观察终点指标为总生存(OS),定义为一线化疗开始至患者死亡、或末次随访时间;次要观察终点指标疾病无进展生存(PFS),定义为一线化疗开始至患者疾病进展、死亡、或末次随访时间,以最先发生事件为准。基线资料的CA199 水平。其他观察指标包括有效率、不良反应等。但该研究多数病例为回顾性观察性研究,可能存在复查时间点不统一、不良反应记录不全等情况,因此对其他观察指标未作硬性规定。

表1 治疗方案
1.4 数据录入及核查
各中心人员一同严格按制定的病例纳入标准及排除标准筛选患者,录入数据包括研究中心的名称、住院号、年龄、性别、PS 评分、原发肿瘤部位、基线资料的CA199 水平、开始化疗时间、化疗方案及剂量、化疗周期数、疾病进展时间、二线化疗方案、死亡时间或末次随访时间、有效率、不良反应等。
1.5 统计方法
PS评分、肿瘤原发部位、有效率、不良反应发生率等计数资料采用χ2检验,年龄等计量资料采用t检验,CA199 采用Z检验,生存资料检验采用K-M,有大于25%理论频数小于5 的使用fisher 检验。以P≤0.05 为有统计学意义,所有统计均通过统计软件SPSS Statistics Version 21.0 实现。
2 结 果
2.1 两组患者的基线资料
2016 年 1 月~2020 年 6 月,五个中心共纳入符合纳入标准和排除标准病例62 例,均为各中心连续病例。末次随访时间为2020 年10 月31 日。按一线化疗方案分为FOLFIRINOX 方案组和AG 方案组,因资料缺项较多,无法录入病理确诊到开始一线化疗的时间等基线资料。部分基线资料见表2。两组基线资料基本均衡,FOLFIRINOX 组年龄(54.65±7.694)岁较 AG 组(58.19±11.461)岁年轻;PS 评分 0~1 分占比较 AG 组占比高;胰体、尾部选择FOLFIRINOX 组化疗的比例(76.9%)较AG组(69.4%)高,但差别均无统计学意义,两组基线资料基本均衡。

表2 两组病例部分基线资料
2.2 疗效比较
2.2.1 总生存(OS)比较 根据一线化疗方案的不同,分为FOLFIRINOX 方案组和AG 方案组。FOLFIRINOX 方案组中位 OS 为 13 个月(95%CI:7.5~18.5),AG 方案组中位 OS 为 11 个月(95%CI:9.9~12.1),两者差别无统计学意义(P=0.202)。如图1 所示。

图1 FOLFIRINOX 方案组与AG 方案组的OS 曲线图
2.2.2 疾病无进展生存(PFS)比较 根据一线化疗方案的不同,FOLFIRINOX 方案组 PFS 为 10 个月(95%CI:9.1~10.8),AG 方案组中位为 11 个月(95%CI:7.4~14.6),两者差别无统计学意义(P=0.132)。如图2 所示。

图2 FOLFIRINOX 方案组与AG 方案组的PFS 曲线图
因该研究多数病例为回顾性研究,疗效评价时间点不统一,多数为患者出现症状或体征后才给予复查;检查方法也不一致,有CT 检查、MR 检查、B 超检查等,相当多的患者与基线资料的检查方法不一致;疗效评价全部为研究者评价,没有经过独立的第三方评价。因此有可能人为地高估了PFS 时间。因此,对两方案PFS 的比较结果的解读必须注意这种可能性。
2.2.3 序贯治疗 一线接受FOLFIRINOX 方案、二线接受AG 方案化疗的病例有5 例,反之有6 例,纳入分析总共11 例。前者中位OS 为13 个月(95%CI:6.6~19.4),后者为11 个月(95%CI:10.2~12.1)。因例数较少未作统计学分析,但两者95%CI 基本重叠,推测疗效相似。如图3。

图3 FOLFIRINOX方案组或AG方案序贯治疗OS曲线图
2.2.4 CA199水平与疗效相关性 将收集的CA199数值,提取中位数190.5 U/mL,当CA199 大于等于190.5 U/mL 时,对比 FOLFIRINOX 方案组和 AG 方案组的OS 曲线图,我们发现,FOLFIRINOX 方案组中位 OS 为 13 个月,95%CI(8.1~17.9),AG 方案组中位 OS 为 11 个月,95%CI(10.4~11.6),Log-Rank检验P 值为0.214,两者差别无统计学意义,如图 4。当 CA199 小于 190.5 U/mL 时,FOLFIRINOX方案组中位 OS 为 10 个月,95%CI(4.1~15.9),AG方案组中位 OS 为 13 个月,95%CI(10.4~15.6),Log-Rank 检验P 值为0.524,两者无统计学意义,如图5。可见,以CA199 中位数为截点,似乎无法预测疗效。
当CA199 大于或等于正常值 59 倍(CA199>=2065 U/mL)时,FOLFIRINOX 方案组共4 例,AG 方案组共 7 例,AG 组 OS 中位数为 10.2 m,FOLFIRINOX 组OS 中位数为3.5 m。当CA199 大于或等于正常值59 倍时,似乎选择AG 方案比FOLFIRINOX方案更为合适;而CA199 低于或等于35 U/mL,FOLFIRINOX 方案似乎更好。如表3。
2.2.5 客观有效率、不良反应比较 因原始记录缺项较多,放弃进行客观有效率及不良反应的分析。

图 4 CA199 大于等于 190.5 U/mL 时 FOLFIRINOX 方案组与AG 方案组的OS 曲线图
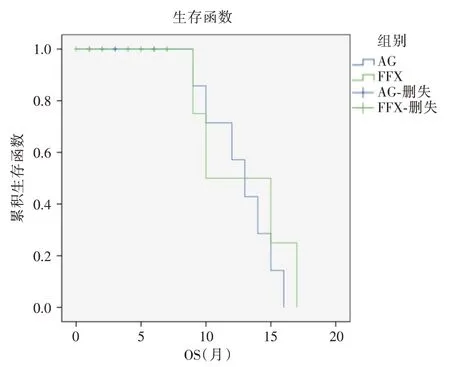
图 5 CA199 小于 190.5 U/mL 时 FOLFIRINOX 方案组与AG 方案组的 OS 曲线图

表3 CA199(U/mL)对FOLFIRINOX 方案和AG 方案疗效预测
3 讨 论
本研究为多中心真实世界的观察性研究,观察资料的缺项较多,且随访时点、疗效评价方法不统一,无法进行方案间客观有效率、不良反应的比较,疾病无进展生存资料也可能存在被高估的可能,这的确是真实的情况。研究的主要观察终点指标为总生存,死亡的时间或末次随访的时间是确切的,不会因为其他的检查时间、方法不统一而受到影响,因此分析一线不同化疗方案的OS 差异,可以部分地回答临床医生关心的问题,因此该研究还是具有一定的临床意义。
FOLFIRINOX 方案和AG 方案是目前晚期胰腺癌一线治疗主流方案[1],日本真实世界临床研究显示2013 年后,接受AG 方案的患者占所有患者的60.7%,FOLFIRINOX 方案仅占14.4%[7]。似乎更多的临床医生在选择化疗方案上倾向于AG 方案。对于我们本次研究,62 例连续病例中36 例应用AG 方案,占58%,AG 方案似乎也较为常用。
在纳入分析的62 例患者中,两组的基线资料基本均衡,但FOLFIRINOX 方案组在数值上看似乎较为年轻、更多的患者PS 评分为0/1 分,这也反映了临床医生的用药习惯,对于一般情况较好、较年轻的患者会更多考虑选择FOLFIRINOX 方案,而对于年老、一般情况稍差的患者,更多地是选择AG 方案。尽管AG 方案组似乎有较多的预后差的因素,但两组的中位OS 相似(FOLFIRINOX 组中位OS 为13 m,AG 组中位OS 为11 m),生存曲线基本重叠在一起,差别无统计学意义(P=0.151)。研究结果支持系统评价的结论[6]。可以认为真实世界研究里,FOLFIRINOX 方案和AG 方案一线治疗晚期胰腺癌,疗效相似。
总生存时间受后线治疗的影响,所以也必须关注PFS。但由于前面所讨论的原因,本研究的PFS 可能被高估,不能反映真实的疗效,这是客观事实。两组方案的中位PFS 相似(FOLFIRINOX 组中位PFS 为10 m,AG 组中位PFS 为11 m),差别无统计学意义(P=0.155),与文献报道一致[8-10]。研究结果也支持FOLFIRINOX 方案和AG 方案一线治疗晚期胰腺癌是等效的。
我们的研究结果提示FOLFIRINOX 方案和AG方案一线治疗晚期胰腺癌疗效相似,但无法回答这两个方案的用药顺序问题。有研究提示[11],一线应用FOLFIRINOX 方案、进展后二线应用AG方案,其中位OS 为13.65 个月,而相反的用药顺序,中位OS 则为13.78 个月,两组生存曲线几乎完全交织在一起,差别无统计学意义,提示用药的顺序不影响疗效。我们对其中11 例一线使用FOLFIRINOX 方案、二线应用 AG 方案(5 例)或相反(6 例)的患者进行分析,结果也提示两组生存曲线基本重叠。同样提示FOLFIRINOX 方案和AG 方案的用药顺序不影响疗,两方案应互为一、二线。
虽然FOLFIRINOX 方案和AG 方案一线治疗晚期胰腺癌疗效相似,用药顺序也不影响疗效,但临床更需要可以预测某一化疗方案的优势人群,尽可能做到精准治疗。2019 年 ASCOGI 报道[12],基底样型胰腺癌似乎对FOLFIRINOX 方案疗效较差,但绝大数医院目前无法根据组学分析对胰腺癌进行分类,因此缺乏临床实用意义。复旦大学对 2 个Ⅲ期临床研究[2,3]的数据进行深度挖掘,发现CA199 的水平与不同化疗方案的疗效存在一定的关系[13]。因此建议当CA199 的水平正常时应更多选择FOLFIRINOX 方案,而CA199 异常升高特别是高于正常值59 倍或以上,应选择AG 方案。我们的结果表明,当CA199 高于或等于正常值的59 倍,似乎选择AG 方案比FOLFIRINOX 方案更为合适(AG 组 OS 中位数为10.21 m,FOLFIRINOX 组OS 中位数为3.5 m),但是由于标本量太少,仍需扩大标本量进行探讨。
本真实世界观察性研究,因例数较少及记录缺项较多,无法得出确切的结论。初步结果提示FOLFIRINOX 方案和AG 方案一线治疗晚期胰腺癌疗效相似;用药顺序似不影响疗效;CA199 水平用于预测不同方案的疗效可能有一定帮助,值得进一步探讨。

