胰十二指肠切除术后胰瘘合并出血二次手术2例并国内文献复习
刘钧豪,罗宇荣,李海量,李晓锋,高鹏,曾宪成
胰十二指肠切除术(pancreatoduodenectomy,PD)是治疗壶腹部周围恶性肿瘤及胰腺恶性肿瘤的标准手术。胰瘘(pancreatic fistula,PF)是PD 术后最常见的并发症,大量文献报道并分析了PF 的危险因素,胰肠吻合技术、胰管直径、胰腺质地与术后胰瘘的发生密切相关[1-3]。随着手术技术及围术期综合诊治水平的提高,国内大型外科中心的PD 术后的死亡率已降至4.4%,但胰瘘的发生率仍高达22.8%[4,5]。胰肠吻合技术的改进有效地降低了胰瘘的发生率,但是并不能完全避免胰瘘的发生[6,7]。术后胰瘘的及时诊断及早期治疗是降低 PD 患者围手术期死亡率的关键[8,9]。PF 和 PD术后大出血是胰十二指肠切除手术术后最为严重的两个并发症。单中心研究发现胰瘘合并迟发性出血发生率约为63%[10]。关于胰瘘引起腹腔迟发性出血的原因目前尚不清楚明确的机制,可能是因为胰瘘所引起的消化性溃疡及动脉瘤形成所导致的出血[11,12],故 PF 被认为是 PD 术后迟发性出血的独立危险因素和始动因素[13]。关于PD 术后胰瘘合并出血的二次手术方式的临床报道及研究较少,本文报道的2 例患者胰瘘高危患者,胰腺质地软,胰管直径小<3 mm,都采用了套入式胰肠吻合方式,术后均出现了胰瘘合并迟发性腹腔出血,经保守治疗无效后进行了二次手术治疗。本文结合该2 例PD 术后胰瘘合并出血二次手术病例,对PD 术后胰瘘合并出血的二次手术方式进行文献复习,并对PD 术后胰瘘合并出血的治疗方式及手术时机进行探讨。
1 病例资料
1.1 病例1
男性患者,65岁,因“皮肤黏膜黄染20余日”入院。肝功能检查示:总胆红素(TBIL)431 μmol/L,直接胆红素(DBIL)130 μmol/L,CA19-9 20 kU/L,CEA 6 ng/mL;上腹部CT 提示“胆总管胰头段扩张”(图1A)。于2018-07-25 行腹腔镜辅助下胰十二指肠根治性切除术(Child 法),术中可见胰腺质地软,胰管直径<3 mm,遂行胰肠套入式吻合法。手术顺利。术后病理提示高级别十二指肠乳头高级别内瘤变。
术后1 周腹腔引流液淀粉酶高于正常值3 倍,考虑术后胰瘘。遂予腹腔持续负压冲洗。患者诉全腹胀痛,以右上腹为甚,行彩超检查示腹腔局部脓肿,行多次腹腔穿刺引流,穿刺后腹痛症状缓解。术后第13 天右侧腹腔引流管引流出暗红色液体150 mL,予去甲肾上腺素氯化钠溶液冲洗腹腔双套管后,出血停止,急查血红蛋白118 g/L。术后第15 天晨引流管引流出暗红色液体300 mL。遂急诊行DSA 检查,检查结果示:未见明显出血点(图1B),复查红蛋白90 g/L。考虑患者为胰瘘诱发的术后出血,复查血常规见血红蛋白较前明显降低,不排除腹腔内有活动性出血的可能。
术后第15 天当日急诊行剖腹探查术。手术经过:术中见腹腔内可见大量血凝块、少量血性液体及炎性坏死组织,主要集中于胰肠吻合口周围量,腹腔内脏器广泛充血、水肿,以右上腹尤为明显,检查胃肠吻合口、肠肠吻合口无异常,检查胆肠吻合口无胆汁渗漏,检查胰肠吻合口崩裂约1/2圈,有胆汁样液体流出,探查胰腺吻合口时后方突然有活动性出血,无法直视,压迫出血点,拆除胰肠吻合口,检查发现门静脉主干可见长约1.1 cm破口,有活动性出血,用3-0 Prolene 线缝合门静脉破口,缝合后无明显渗血。主胰管被胰液腐蚀难以辨别,横断胰腺2 次寻找主胰管,在疑似主胰管处放置6F 硅胶支撑管并缝合固定,缝扎胰腺断端出血点,重新行胰肠端侧吻合:3-0 Prolene 线全层贯穿缝合胰腺小肠浆肌层收拢悬吊,3-0 Prolene 线连续缝合小肠后壁及胰腺下缘和小肠前壁及胰腺上缘,再将悬吊Prolene 线收拢打结,胰管支撑管自小肠引出,行外引流术;右肝下、左肝下、盆腔、胰肠吻合口旁放置双套管引流。
术后予腹腔持续负压冲洗,术后引流管未见血性液体流出,术后腹腔引流液术后逐渐减少,但引流液淀粉酶仍高于正常值3 倍。复查腹部CT后未见明显腹腔积液(图1C),逐渐拔除左肝下、盆腔、右肝下、胰肠吻合口旁引流管,双侧腹腔引流管引流液腹腔引流管于术后43 日拔除。患者于再次手术后52 日康复出院。(见表1)
1.2 病例2
男性患者,59 岁,因“反复恶心呕吐1 月余”入院。上腹部MRI 提示:十二指肠大乳头处结节软组织影,考虑腺癌可能性大;肝内外胆管扩张;胰管扩张(图2A)。行十二指肠镜可见十二指肠壶腹部占位性病变(图2B),活检病理提示十二指肠乳头腺癌;肝功能检查示:TBIL 45.2 μmol/L,ALT 67 U/L,DBIL 32.5 μmol/L,CA19-9 14 kU/L,CEA 3 ng/mL。2018-07-18 行腹腔镜辅助下胰十二指肠切除术,术中可见胰腺质地软,胰管<3 mm,行胰肠套入式吻合法。

图1 患者1 影像学资料A:术前CT 箭头示十二指肠壶腹占位性病变;B:急诊DSA 未见明显出血点;C:二次手术后上腹部CT 未见明显积液
术后每日胆肠引流管可引流出淡黄色液体450 mL,其余引流管引流量未见明显异常。术后第2 天查血常规:WBC 14.45×109/L,中性粒细胞绝对值(GR)13.4×109/L,HGB 102 g/L;血肌酐(Scr)243 μmmol/L;术后第 4 天查血常规:WBC 21.01×109/L,HGB 76 g/L,Scr 253 μmmol/L;术后第5天查血常规:WBC 24.09×109/L,HGB 75 g/L,Scr 343 μmmol/L;考虑术后胰瘘引起的迟发性腹腔出血合并腹腔感染,腹腔感染诱发了肾脏功能的衰竭,遂予连续肾脏替代治疗(CRRT)对症支持治疗,并积极行抗感染、抑酶、腹腔冲洗治疗。术后第6 天复查腹部CT 示:腹腔内多发积液积血,腹腔多发渗出(图2C)。患者术后第8天出现气喘、气促,端坐呼吸等症状,查血气分析:PH7.25、pO 270 mmHg、PaCO 255 mmHg;予抗感染、抑酶、腹腔冲洗、连续肾脏替代治疗等对症支持治疗后,患者全身情况无明显改善。
术后第9 天行剖腹探查术。手术经过:腹腔内可见大量血凝块及少量血性液体量约800 mL,腹腔内脏器广泛充血、水肿,检查胆肠吻合口完整,胃肠吻合口及肠肠吻合口无异常,检查整个术区未见明显活动性出血,无胆汁渗漏,检查胰肠吻合口发现少量胆汁样液体流出,吻合口附近可见皂化斑,胰肠吻合口附近组织水肿明显,局部解剖结构不清,吻合口上方裂开1 针,于胰肠吻合口上方加固2 针,彻底清除腹腔内坏死组织、积液、积血后,并结扎出血风险较高的血管(胃十二指肠动脉、胃右动脉、胃网膜右动静脉),分别于右肝下、左肝下、盆腔、胰肠吻合口旁放置双套管引流。
术后予腹腔持续负压冲洗。患者二次术后各腹腔引流管每日引流液500 mL,未见血性液体。二次手术后第3 天复查腹部CT 见肝周积液较前明显减少(图2D)。患者行二次手术后仍需CRRT维持肾脏功能,并于二次术后29 日自动出院,返回当地继续治疗。随诊两月后患者因全身多器官功能衰竭死亡。(见表1)

表1 2018 年广东省第二人民医院普外二科2 例PD 术后胰瘘合并出血二次手术患者临床资料
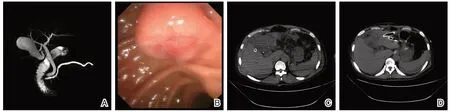
图2 患者2 临床资料 A:术前MRCP 可见胆管、胰管扩张,此为十二指肠壶腹占位性病变特有的“双管征”;B:术前十二指肠镜检查可发现十二指肠壶腹占位性病变;C:PD 手术后第6 天腹部CT 可见大量肝周积液;D:二次手术后第三天腹部CT 扫描肝周积液明显减少
2 讨论及文献复习
通过检索万方、中国知网、维普、PubMed、Medline 数据库,检索关键词:胰十二指肠切除术(pancreatoduodenectomy,PD)、胰瘘(pancreatic fistula,PF)、术后并发症、出血、诊治、二次手术。检索截止日期为2020 年9 月。
检索到临床资料相对较完整的6 篇文献[14-19],共计报道PD 术后胰瘘合并出血二次手术患者19 例,结合本组2 例,共21 例。由于大量临床资料的缺失,无法进行准确的统计分析。在21 例PD术后胰瘘合并出血二次手术患者中,死亡4 例(21.0%)。除冯健等[17]报道的3 例患者未报道二次手术方式外,采用经主胰管外引流的例数最多,为6 例(28.6%)。(表2)

表2 截至2020 年9 月中国报道的PD 术后胰瘘合并出血二次手术患者一般资料
国际胰腺外科协作组(International Study of pancreatic Group Surgery,ISGPS)在 2016 年更新了胰瘘的定义,胰瘘是指术后第3 天及以后,腹腔引流液的淀粉酶超过正常上限3 倍,同时产生了一定的临床影响,需积极行临床治疗。胰瘘按照严重程度分为生化瘘,B 级胰瘘和C 级胰瘘。C 级胰瘘往往需要外科手术的干预[20]。胰腺手术后出血按时间分为早期出血(术后24 h 以内)及迟发性出血(术后24 h 以后);按出血的部位分为腔内及腔外出血;按血红蛋白降3g/dL 分为轻型及重型出血[21]。目前,国内外对二次手术时的手术方式尚无明确定论,但在处理PD 术后胰瘘及胰瘘合并迟发性出血的流程上已经达成了共识。研究认为,前哨性出血是PD 术后迟发性大出血前一个很重要的特征性标志,当出血前哨性出现时,临床医师应该积极地处理[22]。介入治疗被认为是PD 术后出血的首选治疗[23]。在行介入治疗前行腹部的增强CT检查必要的,这有助于发现出血的责任血管,也避免了介入治疗中的盲目性。但在进行了上述积极处理后仍有部分病人需要外科手术治疗[13]。
关于二次手术的时机及手术方式并无统一的标准。笔者认为对于胰瘘合并出血的外科手术治疗重点应该集中在处理胰瘘上,并不只是单纯的止血,在处理出血的基础上必须有效地解决胰瘘的问题。
关于处理胰瘘的方式主要分为完全胰腺切除术及保留胰腺的二次手术。保留胰腺是目前较为主流的手术方式。胰管支撑外引流的方式有两种:一是经消化道的外引流;二是经皮外引流。前者适用于一般情况较好,组织水肿较轻的病例,后期窦道形成拔除胰管支撑引流管后,胰液通过窦道进入空肠,进而改善病人营养状态,提高患者生存质量;后者适用于腹腔感染较重、组织水肿明显的病例。通过对主胰管的桥接外引流技术防止胰液渗漏于腹腔从而阻止胰瘘发生,并控制因胰瘘导致的出血,这是目前治疗PD 术后胰瘘合并出血的主要手术方式。
Ribero[24]等对胰瘘二次手术中行经主胰管经肠道外引流术及全胰切除术进行了回顾性研究,研究显示相比全胰切除术,主胰管经肠道外引流明显降低了二次手术后的死亡率(43.5%versus 0,P<0.03)。Denost 等[25]对主胰管经皮外引流术进行了报道,术后的死亡率约为28.6%(8/21)。刘军桂等[8]对7 例PD 术后胰瘘合并出血的患者进行了报道,6 例采用了拆除原吻合口基础上的主胰管外引流术,其称之为“胆胰分离术”,该类手术使胆汁/肠液和胰液的完全分离,使得肠激酶无法激活胰液中的胰蛋白酶,并将胰液完全外引流,阻断了术后胰瘘的病情进展。胰腺缝扎及主胰管封闭即使用Prolene 线对胰腺断面进行连续缝合或使用生物胶水对主胰管进行封闭从而减少胰液的外渗。此种手术方法在行PD 手术中运用的较多,但在胰瘘的二次手术中的报道较少。Castro[26]对PD二次手术中主胰管封闭术及全胰切除术进行了比较,结果显示相较全胰切除术,主胰管封闭术具有更高的死亡率及术后并发症率。
胰胃吻合技术(pancreaticogastrostomy,PG)已经普遍运用于PD 术中胰消化道吻合技术中,其安全性得到了公认。Bcherlier 等[27]报告了 12 例 PD后胰肠吻合口渗漏的患者,其中8 例在术后8 天中位时间行全胰腺切除术,4 例在术后中位时间10 天接受 PG 治疗,接受 PG 治疗的 4 例患者全部存活,而接受CP 治疗的患者仅有50%存活,PG 治疗后需要进一步干预的必要性和术后糖尿病的发生率也较低。Bouras[28]等对多中心 140 例 PD 术后胰瘘并进行二次手术患者进行了回顾性研究,其建议行保守治疗失败后的患者根据患者病情采用不同手术方案。对于一般情况差且需要快速剖腹手术的患者,可采用主胰管的外引流。在条件较好的情况下,也可考虑采用其他方法,如主胰管的内引流或胰胃造口。在困难的情况下,如胰腺创面渗血或保留胰腺失败,仍然可以行全胰切除术。
通过检索国内文献,目前国内各大中心在PD术后胰瘘合并出血治疗方式选择上相对保守。腹腔冲洗可有效阻止生化胰瘘及部分B 级胰瘘的进展[29];介入治疗是PD 术后迟发性出血的首选治疗,血管栓塞及血管覆膜支架的应用在PD 术后迟发性出血治疗上均有良好的效果[13,23]。但是对于胰瘘相关性的出血,在进行内科药物治疗、腹腔冲洗及介入治疗后,胰瘘及腹腔血性引流液无减少趋势,目前仍推荐积极手术治疗[30]。
反思病例1,门静脉出血在胰瘘导致的出血较为罕见,术前DSA 未见明显出血点,由于经验缺乏,术前未行经皮的门静脉造影。二次手术时,由于术后粘连、吻合口位置以及胰瘘等多种原因,二次手术显露门静脉极为困难,二次手术的难度和风险极高。有学者提出门静脉覆膜支架置入术应该作为PD 术后门静脉出血的首选治疗方案[17],但是笔者认为胰瘘的手术处理应放在PD 术后胰瘘相关性出血治疗的核心位置,在有效控制出血后应尽快处理胰瘘。病例2 的术后出血及腹腔感染均由术后胰瘘所导致,由于腹腔感染、腹腔内压力增高及手术的创伤导致了患者术后第四天出现了肾功能衰竭。在进行了外科手术干预后,虽然出血及腹腔感染情况得到了控制,但患者术后仍需CRRT 治疗,这可能是腹腔感染对肾脏功能造成了不可逆的打击。胰瘘引起的腹腔感染往往伴随着腹腔内组织脏器的水肿,腹腔压力高,随之出现肾脏灌注不足的情况,这可能是患者2 过早出现肾功能损伤的主要原因。故当同时出现胰瘘、出血、腹腔感染时,应积极行外科手术治疗,可能有效降低PD 患者围术期死亡率及多器官功能衰竭发生率。该两例患者均为胰瘘高危患者,术中均采用了套入胰肠式吻合,但没有足够证据支持该两例患者术后的C 级胰瘘合并出血与吻合方式有关。尽管胰肠吻合的方式及技术不断更新,但吻合质量远比吻合方式更为关键。
综上所述,PD 术后胰瘘合并出血的治疗往往需要介入科、重症医学科、外科的多学科参与,但是外科治疗仍然是关键一环。当判断吻合口开裂合并出血时应积极手术干预,根据病人的个体情况及各个中心的技术水平选择不同类型的保胰手术。

