改性球形活性炭对氨气吸附性能的研究
金青青,梁晓怿,张佳楠,周晓龙
(华东理工大学化工学院,上海200237)
氨气(NH3)是一种有毒的碱性气体,对人类健康和环境均造成严重危害[1]。 NH3通常是从农业、化肥、食品饮料和橡胶工业中排放的,其对人体与环境的毒性作用与其高水溶性有关[2]。 NH3不仅可以形成盐类颗粒物引起空气污染, 而且氧化后生成一氧化氮,产生光化学烟雾,对环境造成进一步影响。 因此探究有效脱除NH3的方法是当今亟需解决的问题。
目前用于NH3的吸附材料主要有沸石分子筛、硅胶、活性炭、氧化铝、金属有机框架材料等。活性炭具有很高的比表面积和丰富的孔结构, 是一种良好且高效的吸附剂,但未改性的活性炭在脱氨中的应用受到限制。 NH3是一种直径约为0.3 nm 的小分子,在室温条件下,其只能通过吸附作用被与其直径相似的孔隙捕获,大多数活性炭的平均孔径为1~2 nm,吸附时活性炭表面只被利用了很小一部分,导致其对NH3只存在很弱的吸附作用,吸附能力较差[2]。 因此需要对活性炭进行改性处理,提高其对NH3的吸附能力。 国内外对探究改性活性炭脱除NH3的方法做了很多研究。
改性方法主要包括活性炭的表面改性[3-11],即对活性炭进行表面酸碱处理或氧化处理, 研究其表面结构的变化及对NH3吸附性能的影响。 或者以金属氧化物[12-13]、金属氯化物[2,13-14]为浸渍剂对活性炭进行改性。球形活性炭强度高,具有很高的比表面积及发达的孔隙结构, 且具有在实际应用中易于装填等优点。本研究选择沥青基球形活性炭为载体,对活性炭进行金属盐溶液浸渍改性, 用固定床吸附装置评价浸渍前后样品对NH3的吸附能力。
1 实验部分
1.1 主要试剂和仪器
球 形 活 性 炭,实 验 室 自 制;NH3(99.99%)、N2(99.99%);六水合氯化钴、二水合氯化铜、氯化镍、无水硫酸铜、硝酸铜,均为分析纯。
空 气 压 缩 机(QWWJ-2000);NH3转 子 流 量 计(FL-3006);空气转子流量计(KZ-7002-05A);恒温振荡水浴摇床(SPH-110X12)。
1.2 吸附剂的制备
以球形活性炭为载体,将活性炭置于120 ℃烘箱干燥至恒重,称取25 g 干燥后的活性炭放入100 mL锥形瓶中,配制一系列不同浓度的浸渍剂,采用等体积浸渍法将不同浓度的浸渍剂溶液分别加入活性炭中,放入水浴摇床,于25 ℃震荡浸渍48 h。抽滤浸渍后的样品,于120 ℃烘箱中干燥至恒重,得到活性炭吸附剂。
未浸渍的样品称为基炭,浸渍后的样品称为a%X, 其中a 表示浸渍剂质量与浸渍的活性炭质量之比(含结晶水的浸渍剂的质量均已换算成对应无水浸渍剂的质量),即浸渍比,X 表示浸渍剂;吸附NH3后的活性炭样品用E-a%X 表示。 如10%CoCl2表示浸渍10%CoCl2溶液的球形活性炭,E-10%CoCl2表示吸附NH3后的失活球形活性炭。
1.3 吸附实验流程
图1 为NH3吸附实验流程图。

图1 NH3 吸附实验流程图Fig.1 Flow diagram of NH3 adsorption experiment
压缩空气经装有活性炭、棉花的气体过滤装置,分成两路:一路加湿,一路为干空气。 通过调节阀门7 的开度, 调节两股空气的流量从而使混合后的湿度达到实验要求。 压缩钢瓶里的高纯NH3经防腐蚀流量计与调节好湿度的空气在混合器中混合, 进入装有吸附剂的玻璃吸附柱。 吸附柱下端出口依次串联指示剂瓶(20 mL 水加2~3 滴1%的酚酞指示剂)、吸收剂瓶(100 mL 0.1 mol/L HCl 溶液,定期更换)。每次实验结束,关闭NH3钢瓶阀门,用N2吹扫整个管路,避免管路中残余的NH3泄露。
2 表征与测试
2.1 结构表征
采用Nova Nano SEM 450 扫描电子显微镜(SEM)观察材料的外貌形态;使用JEM-2100 透射电子显微镜(TEM)观察材料的颗粒大小、分散度;采用18 KW/D/max2550VB/PC 型X 射线衍射仪(XRD)对材料进行物相表征; 利用NOVA-2000 全自动物理化学吸附仪对材料孔径分布进行表征分析, 样品先在120 ℃、真空条件下脱气12 h,然后在-196 ℃进行N2吸脱附实验;采用Chem-BET Pulsar-1 全自动程序升温化学吸附仪对失活样品进行程序升温脱附研究,取0.1 g 样品,以10 ℃/min 的速率升至600 ℃进行TPD 测试,得到NH3的出口浓度信号。
2.2 NH3 吸附性能测试
2.2.1 实验条件
空气流量:1.5 L/min;NH3流量:4.5 mL/min;实验温度:20 ℃±3 ℃;空气湿度:50%±3%;玻璃吸附柱中的装炭量:19 mL。
2.2.2 实验步骤
制备好的吸附剂少量分批装入吸附柱, 并振动均匀。 打开空气阀门,调整实验所需湿度。 打开NH3阀门,此时刻记为t1,调节好空气与NH3流量,进行NH3吸附性能的测试, 酚酞指示剂由无色变为浅粉色视为吸附柱被穿透,即为实验终点,记录此时刻为t2,t2-t1为吸附剂对NH3的防护时间, 进而计算NH3吸附量。 样品对NH3的吸附量单位为:mg/mL,即每毫升炭吸附的NH3质量。
3 结果与讨论
3.1 浸渍剂种类的影响
为考察不同浸渍剂的NH3吸附性能,分别选取浸渍比为10%、30%的CuSO4、Cu(NO3)2、CuCl2、NiCl2、CoCl2溶液进行比较,在浸渍温度为25 ℃、浸渍时间为48 h 条件下进行改性,其对NH3吸附量如图2 所示。从图2 可以看出,负载不同金属盐溶液的改性活性炭脱除NH3的效果有一定差别。 浸渍比为10%、30%时,CuSO4、Cu(NO3)2、CuCl2、NiCl2、CoCl2改性活性炭的NH3吸附量分别为7.67,19.54;5.48,14.79;10.23,30.5;12.05,33.23;12.6,35.24 mg/mL。 相同浸渍比条件下,3 种铜盐溶液中,CuCl2对NH3的脱除效果最好且3 种氯盐溶液对NH3的吸附效果明显优于CuSO4、Cu(NO3)2。可能是由于CuCl2在水中的溶解度最高, 浸渍过程中,CuCl2颗粒在活性炭内表面的分散度也更高,因此其对NH3吸附效果也最好。

图2 浸渍比为10%、30%的不同浸渍剂改性活性炭样品对NH3 的吸附量Fig.2 NH3 adsorption capacity of samples modified by different impregnant of 10%and 30%
两种浸渍比条件下,3 种氯盐溶液对氨的吸附量差别不大但明显优于CuSO4和Cu(NO3)2。 等体积浸渍过程中,氯盐溶液具有较高的溶解度,一定体积水溶液中能溶解更多的浸渍剂,对于溶解度较小的CuSO4来说,实验中最多只能做到30%的浸渍比。
为 进 一 步 比 较CuCl2、NiCl2、CoCl2对NH3的 吸附效果,又对比了浸渍比为40%时的结果(见图3)。从图3 看出, 浸渍比为40%时,CoCl2浸渍的样品吸氨效果仍优于CuCl2和NiCl2。推测原因是CoCl2在活性炭内表面能更好地分散, 与CuCl2、NiCl2相比有更高的利用率,同时这可能也与CoCl2和NH3的反应机理相关。 在所有浸渍剂中,CoCl2浸渍改性活性炭脱除NH3效果最好,因此选择CoCl2溶液为浸渍剂。

图3 浸渍比为40%的CuCl2、NiCl2、CoCl2浸渍炭对NH3 的吸附量Fig.3 NH3 adsorption capacity of samples impregnated with 40%CuCl2,NiCl2 and CoCl2
3.2 浸渍比的影响
为考察不同浸渍比的影响,分别选取浸渍比为0%(基炭)、10%、20%、30%、40%、50%、60%的CoCl2溶液,在浸渍温度为25 ℃、浸渍时间为48 h 条件下对活性炭进行浸渍改性,其脱除NH3的吸附量见图4。 由图4 可知,基炭对NH3的吸附能力很差,吸附量为1.46 mg/mL。 浸渍了CoCl2的样品对NH3的吸附量明显增高,当浸渍比从0% 增加至50%时,防护时间由8 min 增至296 min,吸附量由1.46 mg/mL增至最大54.05 mg/mL,与基炭相比提高了约37 倍。由此可见CoCl2的加入对NH3吸附有决定性的影响, 加入CoCl2能显著提高活性炭对NH3的脱除效果。
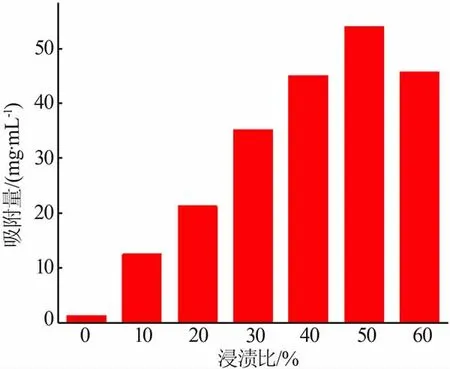
图4 不同浸渍比CoCl2 改性活性炭对NH3 的吸附量Fig.4 NH3 adsorption capacity of samples impregnated with different ratio of CoCl2
而当浸渍比继续增加至60%时,样品对NH3的吸附量反而降低,推测是因为浸渍剂含量太高,浸渍过程中在活性炭内部表面分布不均匀、有重叠、分散度变差, 造成实际吸附时CoCl2与NH3接触面积变小、吸附位点减少,CoCl2的实际利用率随之降低。当活性炭中可与NH3发生反应的CoCl2耗尽后, 吸附剂床层即被穿透,酚酞指示剂随之变色。
3.3 改性球形活性炭的性能表征分析
3.3.1 SEM、TEM、XRD 分析
基炭的SEM 图如图5 所示。 基炭表面光滑,直径约为0.7 mm,内部分布着均匀的孔隙结构。
图6a、b 分别为基炭与50%CoCl2的活性炭样品的TEM 图。 50%CoCl2活性炭与基炭的TEM 图相比并无明显差异,看不到CoCl2颗粒。
基炭及浸渍炭的XRD 谱图见图7。 所有曲线形状大致相似,在2θ 为23°和43°附近出现2 个宽峰,分别对应着炭材料的(002)和(100)特征衍射峰。 随着CoCl2浸渍量的不断增加,样品中活性炭的晶型结构可能被部分破坏,其无定型程度不断增加,XRD 中炭信号逐渐变弱,两处宽峰的强度也随之逐渐变弱。
“单层分散理论”[15-16]指出,许多氧化物和盐类可在载体表面自发形成单层或亚单层(未敷满的单层)分散,在XRD 谱图中不会出现金属盐的晶相峰。浸渍炭的XRD 谱图中除了上述两个特征峰外,没有出现明显的CoCl2的特征峰,这种现象符合“单层分散理论”。本研究所用球形活性炭具有很高的比表面积(见表1,基炭比表面积约为1 600 m2/g),其单层负载容量很大[16],活性组分CoCl2是重金属元素化合物,虽然其在载体中含量很高,但其在活性炭表面仍然以单层分散形式存在,因此在XRD 谱图中没有出现CoCl2的晶相峰,这与上文TEM 结果一致。
3.3.2 孔结构分析
对不同CoCl2浸渍比吸附NH3前后的样品进行低温N2吸脱附实验,测定其比表面积和孔容,结果见表1。 样品的比表面积通过BET 法求得,孔容和孔径分布采用密度函数理论(DFT 模型)计算求得。

图5 基炭的SEM 图Fig.5 SEM images of the unimpregnated carbons

图6 基炭(a)及50%CoCl2 样品(b)的TEM 图Fig.6 TEM images of the unmodified carbon(a)and carbon impregnated with 50%CoCl2(b)
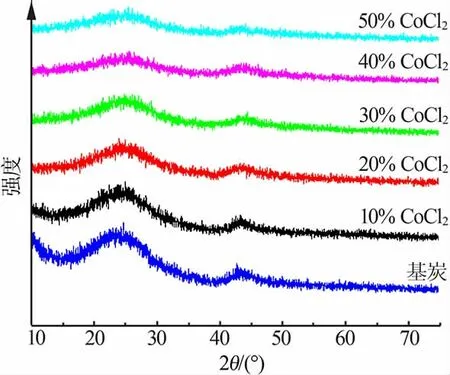
图7 基炭及浸渍炭的XRD 图Fig.7 XRD patterns of unmodified carbon and impregnated carbons
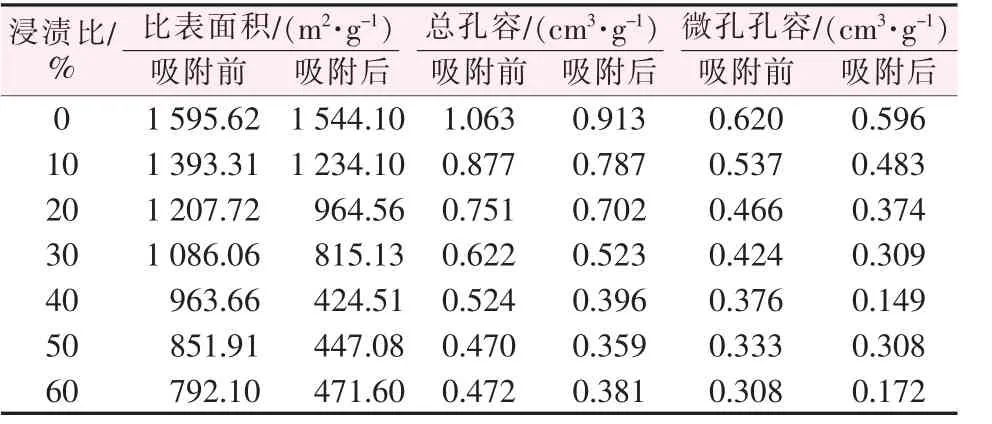
表1 基炭及浸渍炭样品吸附NH3 前后孔结构数据Table 1 Pore structure of unmodified and impregnated samples before and after adsorption of NH3
基炭吸附NH3前后比表面积和微孔孔容变化均不大, 表明基炭对NH3的吸附作用很差。 50%CoCl2的样品吸附前后比表面积分别为851.91、447.08 m2/g,降低了47.52%,微孔孔容降低了7.51%。E-60%CoCl2比表面积大于E-50%CoCl2,这是由于60%CoCl2对NH3吸附效果很差, 其吸附前后比表面积的变化小于50%CoCl2。 40%CoCl2吸附NH3前后微孔孔容的变化相比50%CoCl2更大,可能是在实际反应过程中,40% CoCl2吸附NH3的生成物更多地积聚在微孔里,而50%CoCl2吸附NH3生成物有部分沉积在中孔里,导致其微孔孔容下降不明显。
与基炭相比, 随浸渍比的增加, 样品的比表面积、总孔容及微孔孔容均逐渐降低,这是因为CoCl2进入了微孔并占用了一部分的孔道结构。 与吸附前的样品相比,吸附后的样品比表面积、总孔容及微孔孔容也呈现出明显的降低。 推测是因为NH3与CoCl2反应生成的产物沉积在活性炭内部,使得总孔容、微孔孔容均呈现明显的降低趋势。
图8 为基炭与浸渍炭的总累积孔容分布图,可以看出随CoCl2浸渍比的不断增加,微孔孔容(<2 nm)明显降低,说明在浸渍过程中CoCl2进入到微孔中,使得微孔孔容逐渐变小。 同时,中孔孔容(2~35 nm)也在减小,说明有部分浸渍剂也进入中孔中。这是因为随着浸渍比的增大,微孔被填充的越来越多,导致一些浸渍剂偏向于浸入孔容相对较大的中孔, 使得中孔孔容也逐渐降低。
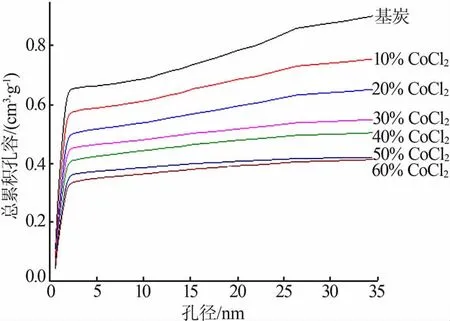
图8 基炭及浸渍炭的总累积孔容分布图Fig.8 Total cumulative pore volume distribution of unmodified carbon and impregnated carbons
为进一步比较浸渍及吸附对样品孔容的影响,又单独对比了基炭和50%CoCl2浸渍炭吸附NH3前后总累积孔容分布,如图9 所示。 基炭吸附NH3前后微孔孔容几乎没有变化, 中孔孔容存在少量的降低, 说明NH3分子只凭借简单的物理吸附存在于基炭的中孔里。 但由于基炭对NH3的吸附能力很弱,防护时间很短, 只导致了中孔孔容的略微下降。 而50%CoCl2浸渍炭吸附后的样品与吸附前的样品相比微孔孔容下降十分明显,中孔孔容变化不大,这是由于浸渍剂主要进入活性炭的微孔,与NH3吸附后生成的产物也沉积在微孔中, 导致吸附后的样品微孔孔容存在进一步明显降低。

图9 基炭及50%CoCl2 浸渍炭吸附NH3前后样品的总累积孔容分布图Fig.9 Total cumulative pore volume distribution of unmodified carbon and 50%CoCl2 impregnated carbon before and after NH3 adsorption
3.3.3 CoCl2 利用率及吸附机理分析
为进一步探究CoCl2吸附NH3过程中的实际利用率, 图10 给出了活性炭吸附的NH3与浸渍加入的CoCl2的物质的量比[n(NH3)/n(CoCl2)]的数据。 为验证低浸渍比对浸渍剂利用率的影响, 也给出了浸渍比为4%的相应数据。 等体积浸渍法使用的溶液总是略微过量的,因此实际CoCl2的浸渍量通过样品堆密度校核得到,从而计算实际浸渍的CoCl2的物质的量。
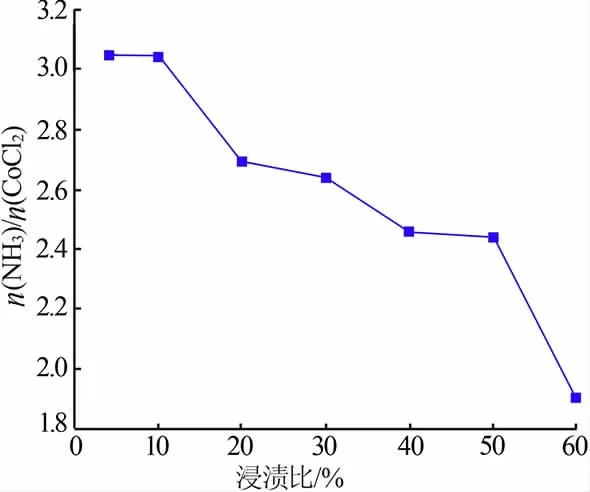
图10 浸渍炭n(NH3)/n(CoCl2)数据Fig.10 n(NH3)/n(CoCl2)data of impregnated samples

图11 50%CoCl2 浸渍炭吸附NH3 后样品过滤结晶后得到的产物Fig.11 Product filtered and crystallized by the exhausted 50%CoCl2 impregnated carbon
在浸渍比很低,为4%、10%时,n(NH3)/n(CoCl2)约为3 左右,随着浸渍比增加,该数值不断降低,直至浸渍比为60%时该数值下降到1.91。 这一结果表明CoCl2的利用率随着浸渍比增加是不断减小的。
对吸附后产物的物化性质进行分析及利用NH3-TPD 结果来说明CoCl2吸附NH3的机理。 CoCl2与NH3的 配 合 物 有3 种[17]:三 氯 化 六 氨 合 钴[Co(NH3)6]Cl3,橙 黄 色 晶 体;二 氯 化 氯 五 氨 合 钴[Co(NH3)5Cl]Cl2,紫红色晶体;三氯化五氨一水合钴[Co(NH3)5H2O]Cl3,砖红色晶体。 [Co(NH3)6]Cl3中的NH3与中心原子Co 的配位非常紧密,NH3不会在酸溶液中发生解离和质子化,使得[Co(NH3)6]Cl3可以从浓盐酸溶液中重结晶析出[17]。
根据这一性质, 将E-50%CoCl2样品加入一定量的水溶液中,静置、过滤后,得到橙黄色的溶液。再向溶液中加入浓盐酸溶液,冰水浴后有晶体析出,抽滤干燥后得到了淡黄色晶体,如图11 所示。 且对不同CoCl2浸渍比浸渍炭吸附后的样品进行同样处理,也得到了相同的结果。因此从吸附后样品结晶的颜色推测NH3与CoCl2反应生成[Co(NH3)6]Cl3。
3.3.4 NH3-TPD 分析
图12 为不同CoCl2浸渍比样品吸附NH3后的NH3-TPD 曲线。 所有曲线均有一个明显的特征峰,位于100~300 ℃,这表明NH3与CoCl2生成的产物会在高温条件下脱附释放出NH3。不难发现,随浸渍比增加,峰面积明显增大,表明对NH3的吸附量增加。 NH3与CoCl2的相互作用是弱吸附作用,生成的络合物[Co(NH3)6]Cl3在较低温度(约60~80 ℃)就会解离并逐渐释放出NH3,150~170 ℃达到高峰,直至300 ℃左右,不再有NH3析出。

图12 浸渍炭吸附NH3 后样品的NH3-TPD 图Fig.12 NH3-TPD profiles of impregnated carbons after NH3 adsorption
4 结论
1)不同金属盐溶液浸渍改性的球形活性炭对NH3的吸附效果有较大差别, 且负载同种金属不同盐溶液的活性炭吸附NH3的性能也有很大不同。 本实验选用的金属盐浸渍剂中,CoCl2浸渍改性球形活性炭脱除NH3的效果最好。 2)浸渍CoCl2对脱氨效果有很大改善,但NH3吸附量并非随浸渍比的增大而单调增加, 浸渍剂的实际利用率会随着浸渍比的增加而逐渐降低。 浸渍比增加至60%时,吸附量反而下降,最佳浸渍比为50%。 此种条件下,改性活性炭对NH3的防护时间达到296 min,穿透吸附容量达到54.05 mg/mL,是基炭的37 倍。 3)浸渍后及吸附后的样品比表面积、总孔容、微孔孔容均呈现明显的降低,且通过对吸附NH3后的失活样品进行分析表征,推测CoCl2与NH3反应生成了络合物[Co(NH3)6]Cl3。

