低温胁迫下羊蹄甲和洋紫荆家系叶片相对电导率的变化*
王 洋 魏 丹 张梅兰 冯志坚陈友光 张 耕
(1.广东省森林培育与保护利用重点实验室/广东省林业科学研究院,广东 广州 510520;2.南雄市林业科学研究所,广东韶关 512400;3.华南农业大学,广东 广州 510520;4.广东如春生态集团有限公司,广东 广州 510520)
羊蹄甲Bauhinia purpurea 和洋紫荆Bauhinia variegata 为豆科Leguminosae 苏木亚科Caesalpinioideae 羊蹄甲属Bauhinia 景观树种,是我国南方地区的乡土树种,具有地域景观代表性。两者适应性强、生长快速、花量大、花期长[1],是广东、广西、福建、海南地区优良的观花行道树和园景树,广泛应用于公园和街道绿化中[2-3]。近年来,四川、重庆、江西和湖南局部地区也有引种种植,种苗主要来自于广东珠三角地区,由于冬季低温,苗木生长不佳,即使在广东粤北地区,也存在同样的问题。
低温是限制植物自然地理分布和引种应用的主要因素,也是危害栽培生产的主要自然灾害之一[4]。生物膜结构的动态变化是研究植物抗寒能力及抗寒机理的重要依据[5-6],低温会破坏细胞的膜结构,降低膜的流动性和对物质的吸收和运输,使细胞内的溶质外渗,电导率增大[7-9]。电导率法常用于测定植物膜结构的伤害程度,进而分析其抗寒能力[10]。利用人工气温箱试验测定植物在低温胁迫下叶片电导率的变化,具有周期较短、可控性较强的优点,可弥补野外试验的不足。
本文以羊蹄甲和洋紫荆各9 个具有优良观赏性的家系为试验材料,通过人工低温胁迫试验,研究两种植物不同家系的叶片电导率的变化,并对其恢复生长情况进行调查统计,为其选育、引种驯化和推广应用提供理论参考。
1 材料与方法
1.1 试验材料
2014 年在广州、韶关、肇庆,收集具有优良观赏性、长势良好的羊蹄甲、洋紫荆单株种子,于2014 年6 月广东省林业科学研究院苗圃进行播种育苗。苗圃地位于广州市,处于亚热带季风气候区,年平均温度为21.8℃,温度最高的月份为8月,最低为1 月,平均相对湿度77%,年均降雨量1 899.8 mm,集中在4—10 月。经过在广东省林业科学研究院苗圃6 个多月的栽培,进一步筛选出羊蹄甲和洋紫荆各9 个观赏性较强的优良家系(表1、表2),每家系选择10 株于华南农业大学林学与风景园林学院楼进行人工气温箱试验。
1.2 试验设计
将苗木置于人工气温箱内,设置光照强度为1 200 lx,光照时间为12 h/d,相对湿度控制在75%~85%之间,分别设置9、6、3、0、-3℃共5种温度梯度,以3℃·d-1的速率进行降温处理。当温度降至设定温度时,保持24 h 后选择第2~6 片展开叶进行电导率测定。每个家系准备3 份叶片,去除叶脉,每份称重0.3 g,用30 mL 蒸馏水浸泡24 h 后用DDS-11AGA 型数字电导仪测定液体的电导率R1,再将测定后的各样品置于100℃的沸水水浴锅中20 min,冷却至室温后测定其电导率R2,通过计算R1、R2 之间的比值得出相对电导率,用来表示质膜相对透性[5]。低温处理结束后,将所有试验苗木放置于苗圃中,进行低温胁迫后自然条件下的恢复管理。10 d 后,对其恢复后的形态特征进行调查。
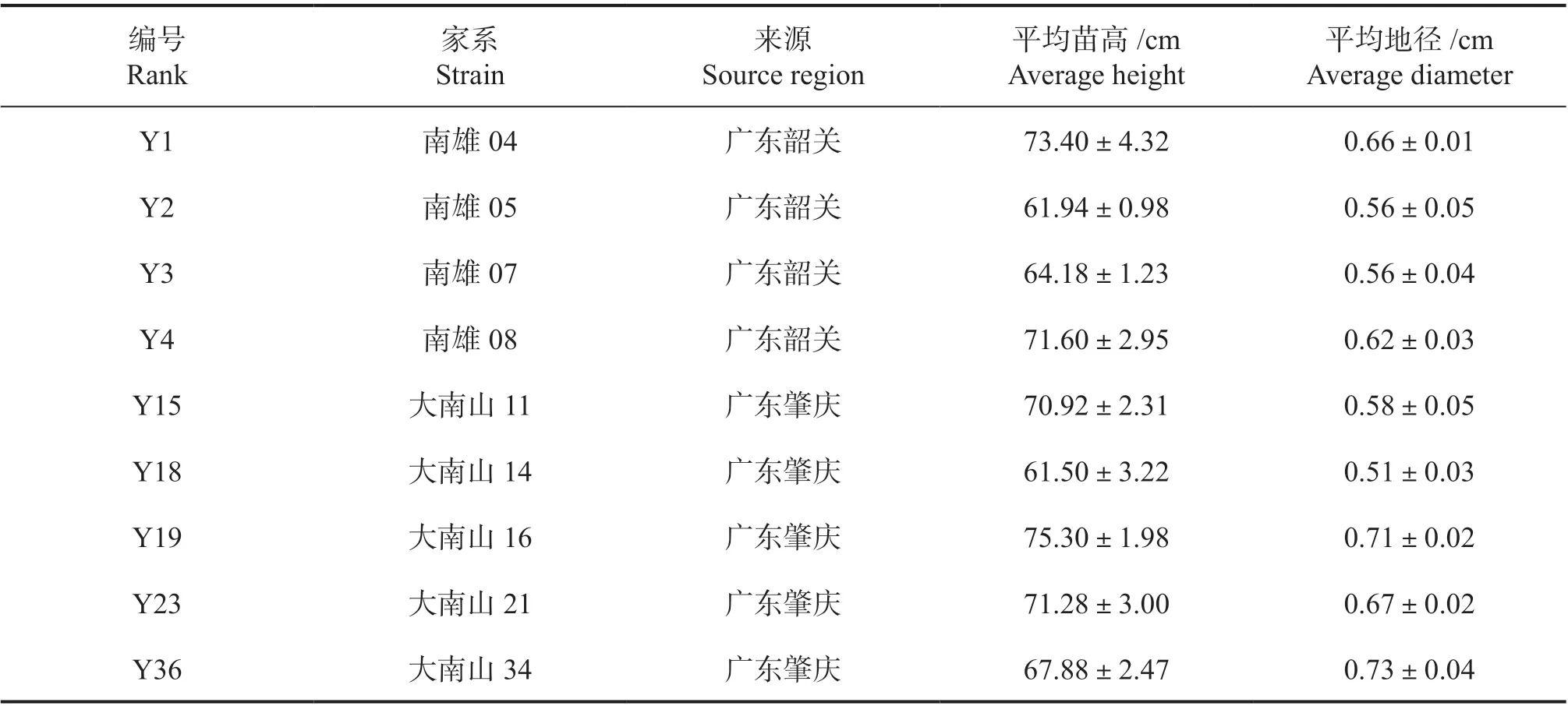
表1 羊蹄甲不同家系的概况Tab.1 Basic situation of different families of B. purpurea
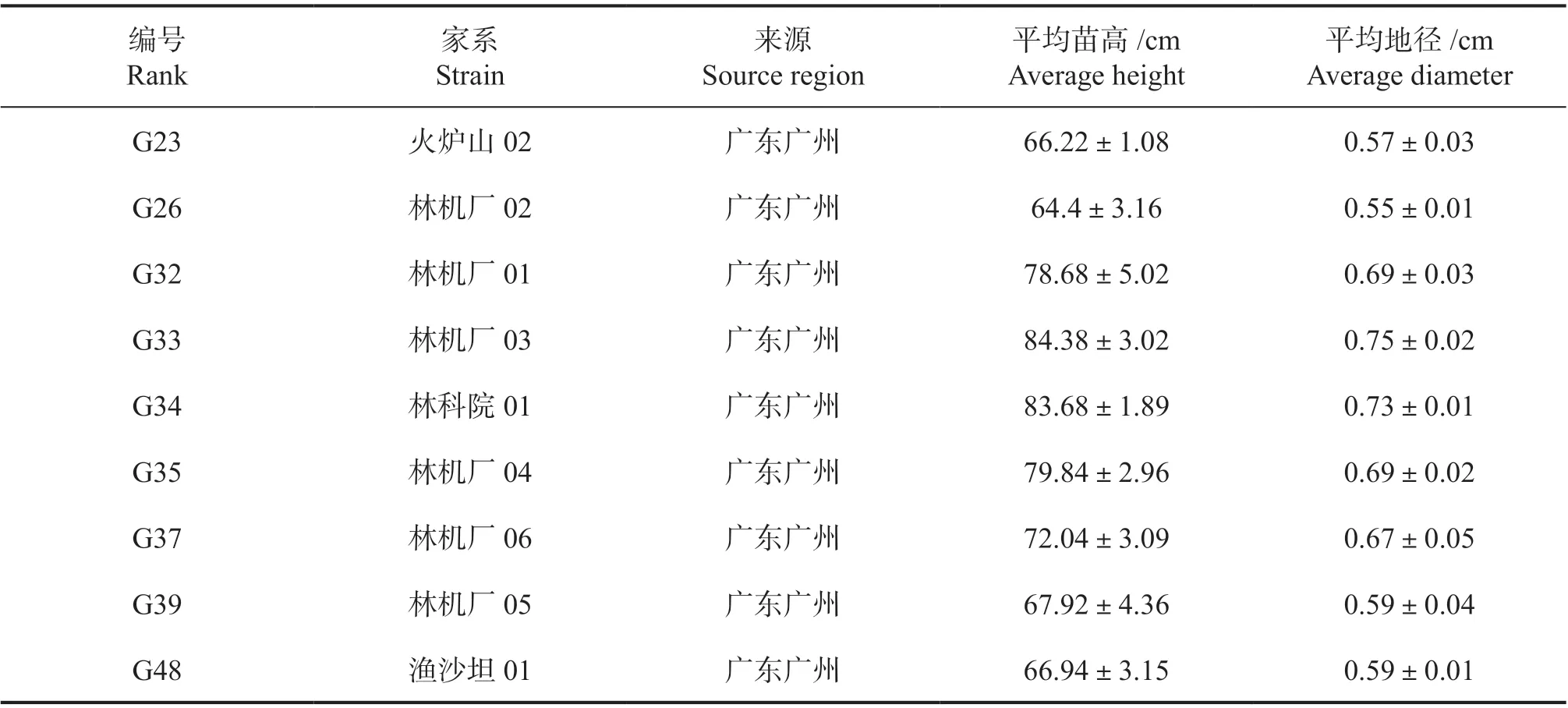
表2 洋紫荆不同家系的概况Tab.2 Basic situation of different families of B. variegata
1.3 统计方法
使用Microsoft Excel 2016 和SPSS 22 进行试验数据处理,使用Origin 2017 进行绘图。
2 结果与分析
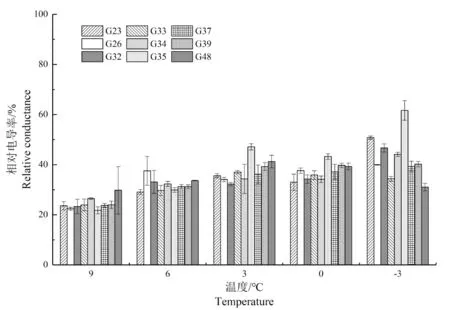
图1 低温胁迫下羊蹄甲不同家系相对电导率变化Fig.1 Relative conductance in different families of B.purpurea under cold stress
2.1 低温胁迫对羊蹄甲家系叶片质膜透性的影响
如图1 所示,整体上羊蹄甲9 个家系的叶片相对电导率随着温度的降低呈上升趋势,但不同家系和不同温度的上升趋势不同。在一定低温范围内(0~9℃),所有家系的相对电导率均随着温度的降低而增加,其中,Y19 的上升幅度最大,0℃时的叶片相对电导率比9℃时增加220.42%;Y1 在此温度区间的相对电导率上升幅度最小,仅为44.96%,其次为Y15 和Y3,分别增长了68.17%和76.80%。当温度从0℃降到-3℃时,除Y15、Y18、Y19 外,其他家系叶片相对电导率均上升。在整个胁迫期间,增长率最大的是Y2,比9℃时增长了259.02%;增长率最小的为Y15,仅增长了31.49%,其次为Y18、Y4,分别增长了75.70%和92.58%。
2.2 低温胁迫对洋紫荆家系叶片质膜透性的影响
如图2 所示,洋紫荆不同家系的叶片相对电导率随着低温胁迫的加剧整体呈上升趋势,同样分两个阶段对不同家系的相对电导率变化进行分析。在0~9℃之间,G35 相对电导率增加最大,为98.64%,其他家系的叶片相对电导率上升速率均较缓。当温度从0℃降到-3℃时,除G48 外,其他家系相对电导率均呈上升趋势。在整个胁迫期间,G35 的相对电导率增长最明显,-3℃胁迫下比9℃处理时增加了183.24%,其次为G23、G32,分别增加了115.15%、100.17%;G48 的相对电导率增长量最小,整个胁迫期间仅增加了4.28%,其次为G33,电导率增长量为43.59%。
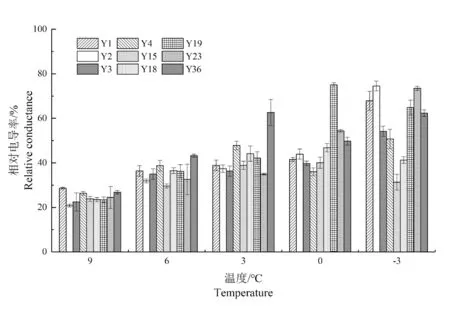
图2 低温胁迫下洋紫荆不同家系相对电导率变化Fig.2 Relative conductance in different families of B.variegata under cold stress
2.3 低温胁迫后恢复生长
对各家系低温胁迫后恢复生长的形态特征进行调查,结果表明:在羊蹄甲9 个家系中,Y15的茎、叶均表现正常,说明该家系在-3℃低温胁迫下能够较为正常地生长,抗寒性较强;其余家系的茎、叶均干枯凋落,说明这些家系无法适应-3℃低温胁迫,抗寒性较弱(表3)。
在洋紫荆家系中,G26、G34 和G48 家系的试验苗木的茎、叶均正常,说明这些家系在-3℃低温胁迫下能够较为正常地生长,抗寒性较强;G23、G35 和G37 家系部分植株茎表现正常,说明这些家系能够在一定程度上适宜低温胁迫;其余家系的10 株试验材料均为茎、叶干枯,说明这些家系无法适应-3℃低温胁迫,抗寒性较弱(表4)。
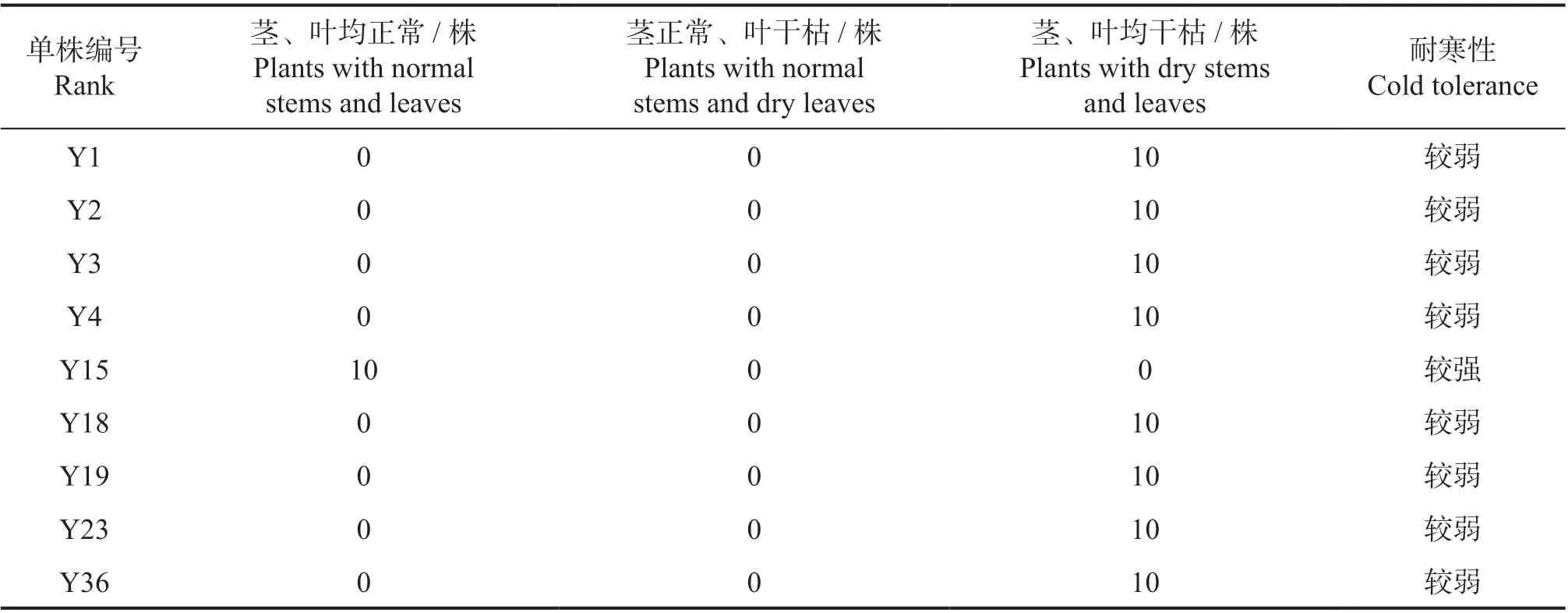
表3 羊蹄甲不同家系低温胁迫后的恢复生长Tab.3 Features of different families of B. purpurea under cold stress
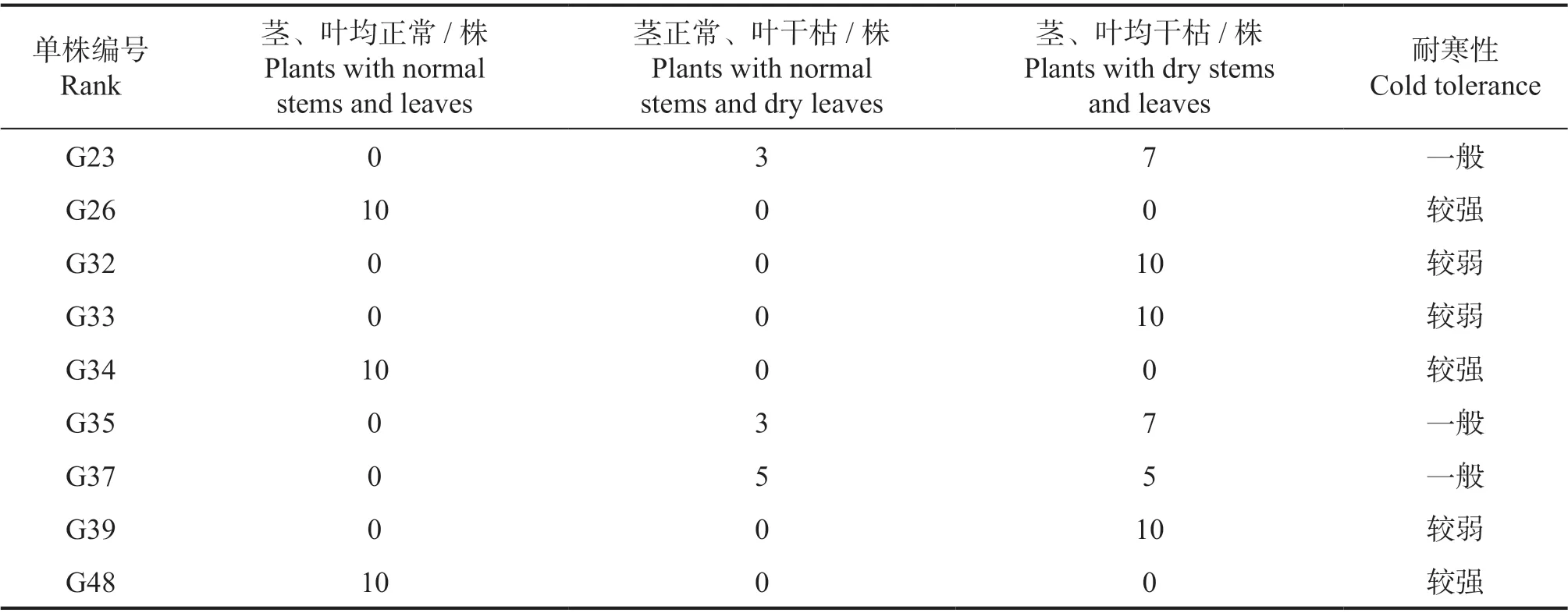
表4 洋紫荆不同家系低温胁迫后的恢复生长Tab.4 Features of different families of B. variegata under cold stress
3 结论与讨论
当受到低温胁迫时,植物的生物膜系统首先受到伤害,导致细胞膜透性增大,电解质外渗,细胞膜透性的变化可直接反应植物受低温伤害的程度[11-12]。研究表明,电导法在研究植物抗寒方面具有准确、灵敏、易操作等优点,当植物受到低温伤害时,叶片的电导率增加,并与温度呈负相关。本试验结果显示,羊蹄甲和洋紫荆家系的叶片相对电导率基本上随温度的降低而增加。但当温度为-3℃时,少数家系,如Y15、Y18、Y19、G48 的相对电导率呈下降趋势,可能是由于这些家系在降温过程中产生了低温防御反应,细胞膜得到一定程度的修复。对于羊蹄甲9 个家系来说,Y15 的电导率变化最小,表明其抗寒性较强,通过恢复生长后的形态特征调查也证实了这一点。Y15 在恢复生长后10 株苗木茎、叶均表现正常,而其他家系的茎、叶均干枯。相比于羊蹄甲,洋紫荆家系整体上电导率变化较小,表明其抗寒性强于羊蹄甲。通过相对电导率变化及恢复生长情况调查,得出9 个家系中,G48、G26、G34 的抗寒性较强。
植物抗寒机制错综复杂,不同物种、品种,甚至家系的抗寒性存在一定的差异[13-15]。本实验仅对羊蹄甲和洋紫荆不同家系的相对电导率和恢复生长情况进行了测定、调查分析,可在一定程度上反应不同家系抗寒能力,但要全面了解其抗寒生理生化机制,须对相关抗寒指标,如叶绿素含量、丙二醛、超氧化物歧化酶、脯氨酸、可溶性糖等进行全面综合的测定分析[16-17],从而建立能准确反应羊蹄甲和洋紫荆不同家系抗寒能力的综合评价体系,为其引种、选育和推广应用提供依据。

