分级微/纳结构ZnO的制备及其光催化性能
向小倩,廖小刚,李 纲,胡学步,田 甜,2
(1 重庆理工大学 化学化工学院,重庆 400054;2 中国兵器工业集团 第五二研究所,内蒙古 包头 014000)
ZnO是一种典型的直接带隙半导体材料,在室温下的禁带宽度为3.37 eV,激子结合能约为60 meV,其作为光催化剂具有价廉易得、环境友好和性能优良等优点,是光催化领域的首选材料之一[1-2]。近年来,由低维纳米单元自组装而成的分级微/纳米结构光催化材料受到极大关注,这源于该种结构既保留了纳米颗粒尺寸小、比表面积高、催化活性强等方面的优点,同时又有效克服了纳米粒子在使用后不易回收的缺点,显示出更为优异的结构整体效应。Wang等[3]以硫酸锌、尿素和柠檬酸钠为原料,经水热处理和后续低温煅烧得到了粒度为3~6 μm的分级多孔ZnO微球。该微球具有分级孔结构、大比表面积和一定浓度的氧空位等结构特征,对罗丹明B溶液表现出良好的光催化降解能力。潘超等[4]以PVC/Zn(Ac)2复合纳米纤维为模板,采用模板辅助共沉积技术制备出三维ZnO纳米纤维/纳米线分级结构。较之单一的纳米颗粒或纳米纤维,该三维结构能为乙醛分子和氧分子提供更加易于扩散和输运的通道,因而具有更为优异的光催化降解乙醛的性能。Yu等[5]以ZnCl2和葡萄糖的水溶液为原料,采用一锅煮法制得了由纳米晶组装而成的ZnO多孔空心微球。该光催化剂除具有良好的性能外,还具有易于回收的特点。在每轮光催化反应完成后,通过简单的静置处理步骤即可实现催化剂从反应液中的高效分离与回收。经过6次循环使用后,ZnO空心微球的催化活性未见明显降低。研究发现,分级微/纳结构ZnO材料的光催化性能受其形貌、比表面积、晶化程度、微结构等因素影响较大[6-7]。因此,探索具有新颖形貌和微结构的分级ZnO材料的制备新方法,并深入研究制备方法与光催化能力之间的依赖关系,以助推ZnO材料在光催化领域的实用化进程,具有十分重要的现实意义。基于此,本工作选用两种不同的合成方法,即溶剂热法和草酸盐法,制备出具有分级微/纳结构但形貌迥异的两种ZnO材料,并选择亚甲基蓝溶液作为模拟有机污染物,对其光催化性能进行对比评价。借助X射线衍射、热重、扫描电镜、N2吸附-脱附曲线等测试手段对材料进行表征,并结合自由基捕获实验,对两种样品光催化性能存在差异的原因进行分析。最后,基于实验结果提出了分级微/纳结构ZnO光催化降解亚甲基蓝溶液的可能机理。
1 实验材料与方法
1.1 实验原料
异丙醇、丙三醇、乙二醇、无水乙醇、六水合硝酸锌、二水草酸,由成都市科隆化学品有限公司提供,均为分析纯;去离子水为实验室自制。
1.2 实验方法
1.2.1 溶剂热法
称取20 mmol六水合硝酸锌,将其溶解于由260 mL异丙醇和40 mL丙三醇组成的混合溶液中。随后将该溶液转移至容积为500 mL的聚四氟乙烯反应釜中,密封后在180 ℃下水热反应24 h。反应结束后,将釜中沉淀抽滤,并用无水乙醇洗涤数次,在50 ℃下烘干。将烘干后的前驱体物质置于马弗炉中煅烧,煅烧温度为450 ℃,煅烧时间为90 min,升温速率为2 ℃/min,所得样品命名为ZnO-A。
1.2.2 草酸盐法
称取20 mmol六水合硝酸锌,将其溶解于由120 mL乙二醇和40 mL蒸馏水组成的混合溶液中,所得溶液记为A;称取20.01 mmol二水草酸,将其溶解于由120 mL乙二醇和40 mL蒸馏水组成的溶液中,所得溶液记为B;在搅拌下,将B逐滴滴加到A中,滴加完毕后继续搅拌30 min。随后将该混合液转移至容积为500 mL的水热釜中,密封后于140 ℃水热反应24 h。反应完毕后,对釜中沉淀进行抽滤,并用无水乙醇洗涤数次,在50 ℃下烘干,即得到前驱体物质。将该前驱体进行煅烧,煅烧温度为400 ℃,煅烧时间为90 min,升温速率为2 ℃/min,所得样品命名为ZnO-B。
1.3 分析表征
样品的晶相结构和相纯度测试在XRD-7000型X射线衍射仪上完成;采用Quanta 600F型扫描电镜观察样品的形貌;样品的热分解曲线在STA 2500型差热分析仪上测得,空气氛围,升温速率为3 ℃/min,温度为25~550 ℃;样品的N2吸附-脱附曲线在Micrometritics ASAP2020氮气吸附仪上完成,工作温度为-198.5 ℃;样品的氧空位测试和自由基捕获实验在JES FA200型电子顺磁共振仪(EPR)上完成,采用5,5-二甲基-1-吡咯啉-N-氧化物(DMPO)作为捕获剂;XPS测试在X射线光电子能谱仪(XPS, Thermo ESCALAB250)上完成;采用UV-2550型紫外可见分光光度计测得材料的UV-vis漫反射光谱,以BaSO4作为参照,扫描范围为200~800 nm;样品的光致发光光谱(PL)测试在FLS 980型荧光光谱仪上完成,激发波长为325 nm。
1.4 光催化降解实验
以亚甲基蓝溶液作为模拟污染物来评价不同制备方法所得ZnO的光催化性能。实验在自制的光催化反应器上完成。具体实验如下:称取0.0100 g催化剂放入200 mL浓度为10 mg/L的亚甲基蓝溶液中,随后鼓入空气,使催化剂和染料溶液在暗光条件下混合2.5 h以达到吸附平衡。然后开启光源(黑光灯,8 W,主波长365 nm),进行光催化降解反应。每隔15 min抽取5 mL亚甲基蓝溶液,测定其即时浓度。亚甲基蓝溶液的浓度根据朗伯-比尔定律计算获得(通过测定其最大吸收波长处的吸光度值)。吸收光谱测试在UV-2550分光光度计上完成,波长测试范围为200~700 nm。在测定吸光度前,需对待测液进行离心处理,以消除催化剂颗粒对测试的干扰。亚甲基蓝溶液的降解率A为:
(1)
式中:C0为达到吸附平衡后亚甲基蓝溶液的浓度值;C为亚甲基蓝溶液的实时浓度值。
2 结果与讨论
2.1 XRD分析
采用X射线衍射仪对不同合成方法制得的含锌前驱体材料及其煅烧产物的物相组成进行判定。图1为溶剂热法和草酸盐法所得锌前驱体及其煅烧产物的XRD谱图。由图1(a)可见,溶剂热法所得锌前驱体的XRD谱图与标准数据库中C3H6O3Zn的衍射数据(PDF#23-1975)完全一致,所得锌前驱体的物相组成为丙三醇锌(C3H6O3Zn)。图1(b)为草酸盐法锌前驱体的XRD谱图,其与标准数据库中现有的无水草酸锌(PDF#37-0718)或含水草酸锌(PDF#25-1029和PDF#14-0740)的衍射数据均不能吻合,但根据本实验采用的反应体系,推断该前驱体物质为含有锌元素的草酸盐。为了便于表达,将该前驱体物质表述为ZnC2O4·nH2O。
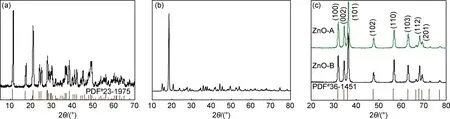
图1 溶剂热法(a)和草酸盐法(b)所得锌前驱体及其煅烧产物(c)的XRD谱图
图1(c)是将两种锌前驱体煅烧后所得产物的XRD谱图。可知,两个样品的XRD特征衍射峰均与PDF#36-1451衍射数据完全吻合,证实产物为具有六方纤锌矿结构的ZnO。此外,还能观察到样品的衍射峰峰型尖锐,表明所得ZnO结晶较好。在谱图中未观察到其他杂质峰出现,说明两种方法制得的ZnO纯度较高。
2.2 TG分析
为了解不同制备方法所得锌前驱体的热分解行为,在空气氛围中对其进行热重分析,测试温度为25~550 ℃,升温速率为3 ℃/min,相应结果示于图2。可知,在290~410 ℃内,溶剂热法所得锌前驱体发生了明显的质量损失,这归因于锌前驱体的分解和ZnO的生成。失重率为48.05%,与通过2C3H6O3Zn+7O2→2ZnO+6CO2+6H2O计算出来的理论失重率48%接近,进一步证实溶剂热法所得前驱体物质正是丙三醇锌。450 ℃后TG曲线上再无明显的质量损失现象,表明丙三醇锌已分解完全,因此将溶剂热法所得丙三醇锌前驱体转变为ZnO的煅烧温度设定为450 ℃。而对于草酸盐法所得锌前驱体而言,其热分解可分为3步:(1)在25~120 ℃出现轻微失重,这是样品表面物理吸附水的挥发所致;(2)在180~300 ℃时发生的质量损失,对应于结晶水的脱除,即发生了ZnC2O4·nH2O→ZnC2O4+nH2O反应。此步的失重率为26.80%,可以确定草酸盐法所得锌前驱体的化学组成为ZnC2O4·3H2O;(3)失重发生在300~390 ℃,归因于草酸盐的分解和ZnO的生成。该阶段失重率为34.37%,与通过2ZnC2O4+O2→2ZnO+2CO2+2CO计算出来的理论值36.6%吻合较好。400 ℃后TG曲线上再无明显的质量损失现象,表明ZnC2O4·3H2O已分解完全,因此将草酸盐法所得锌前驱体转变为ZnO的煅烧温度设定为400 ℃。
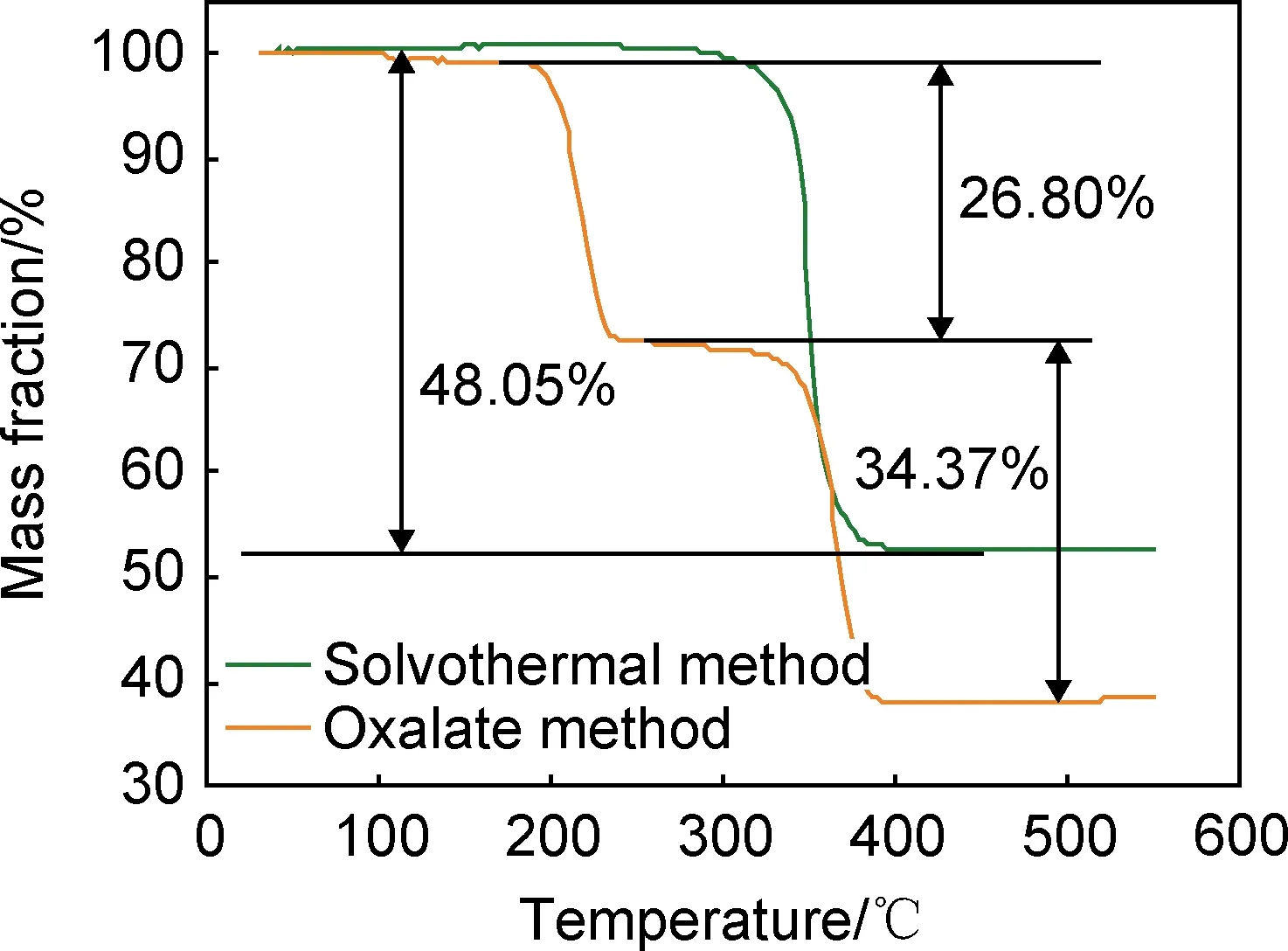
图2 不同制备方法所得锌前驱体的热重曲线
2.3 SEM分析
图3为两种不同方法得到的ZnO产物的SEM图。可知,溶剂热法制得的ZnO整体上呈现出花状微球形貌,微球直径从9~35 μm不等,分散性较好。放大图显示花状微球具有分级结构,由众多纳米片围绕着中心自组装而成,单个纳米片的厚度约为650 nm。草酸盐法所得ZnO呈现出棒状结构,直径介于1~5 μm,长度从几微米到几十微米不等,分散性较好。研究证实[8-9],由草酸盐法得到的微米棒通常是由众多纳米晶自组装而成,即本研究中草酸盐法所获ZnO亦具有分级微/纳结构。总体而言,两种制备方法得到的ZnO产物分散性都很好,其原因在于反应体系中的有机溶剂具有出色的分散性[10]。进一步观察还能发现,煅烧得到的两种ZnO产物的表面均很粗糙,且有一些裂纹出现,这应该是前驱体物质在热分解过程中CO2和H2O的脱除与释放引起的。

图3 ZnO产物的SEM图
2.4 比表面积和孔结构分析
为了获得产物的比表面积和孔结构信息,对两种ZnO样品进行N2吸附-脱附曲线测试,相应结果示于图4。从图4(a)中可以看出,两种方法所获ZnO样品的N2吸附-脱附等温曲线上均出现了明显的迟滞环,这是毛细管的凝聚作用引起的,证实两种样品均具有典型的介孔构造特征。介孔的出现源于含锌前驱体在受热分解时CO2和H2O等的释放,这与SEM观察到的现象一致。根据IUPAC分类,两个样品的迟滞环形状为H3型,表明两种方法所制ZnO的孔道为狭缝状[11-12]。图4(b)为样品的孔径分布曲线。可知,两种制备方法所得ZnO的孔径分布较窄,且主要集中在介孔区域,证实所得样品的介孔结构较好。为了便于比较,将两种ZnO样品的比表面积、孔容和孔径物理参数归纳于表1中。由表1可知,两种样品的比表面积、孔容和孔径等参数均较为接近。

表1 不同制备方法获得的ZnO的物理参数
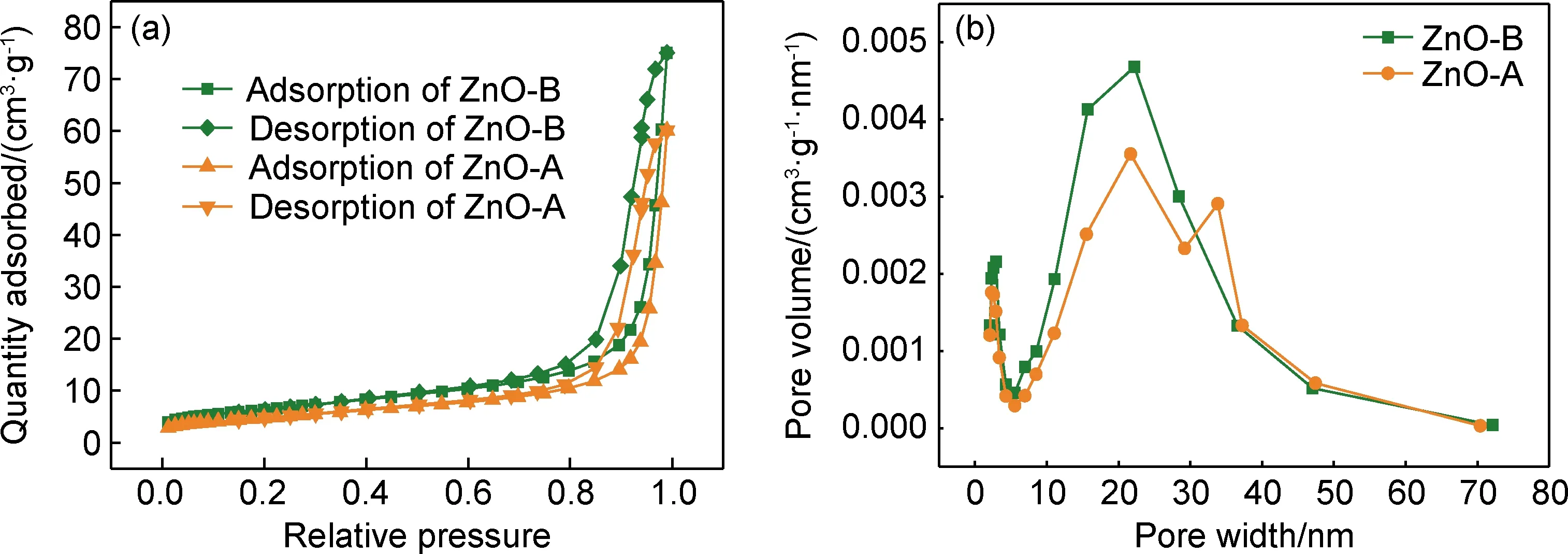
图4 不同方法所获得ZnO的N2吸附-脱附曲线(a)和相应的孔径分布曲线(b)
2.5 光催化性能评价
以亚甲基蓝溶液为模拟有机污染物,在自制的光催化反应器上对两种ZnO样品的光催化性能进行评价。图5为不同样品对亚甲基蓝溶液的降解效果,C0-C以及ln(C0/C)随紫外光照时间的关系图。由图5(a)可知,当亚甲基蓝溶液中无催化剂ZnO时,其在紫外灯下经过60 min照射后降解率仅为2.39%,表明单纯的紫外光对亚甲基蓝溶液的光解作用可以忽略。然而,向反应体系中引入少量ZnO催化剂(0.0100 g),在紫外灯下经历同样时间的辐照,亚甲基蓝溶液的降解率均有了一定程度的提高。ZnO-A样品对亚甲基蓝溶液的降解率为12.07%,而ZnO-B样品对亚甲基蓝溶液的降解率则达到77.08%。从光催化结果看出,草酸盐法制得的ZnO的光催化性能相较于溶剂热法制的ZnO更为优异。为了判断ZnO样品光催化降解亚甲基蓝溶液的反应动力学级数,图5(b),(c)分别给出了(C0-C)和lnC0/C随紫外光照射时间的关系曲线。可知,两种ZnO样品光催化降解亚甲基蓝溶液时所对应的ln(C0/C)-t曲线的线性关系都优于相应的(C0-C)-t曲线,且线性拟合相关系数R值均大于0.97,表明两种方法制得的ZnO对亚甲基蓝溶液的光催化降解均为一级反应。根据拟合曲线算得ZnO-B和ZnO-A样品光催化降解亚甲基蓝溶液的反应速率常数分别为0.02425,0.00317 min-1,即相同条件下,ZnO-B光催化降解亚甲基蓝溶液的速率是ZnO-A的7.65倍,再次证实ZnO-B具有比ZnO-A更为优异的光催化性能。
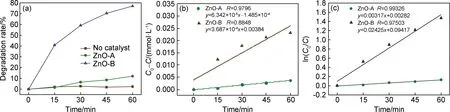
图5 不同样品对亚甲基蓝溶液的降解效果(a),C0-C(b)以及ln(C0/C)(c)随紫外光照时间的关系图
2.6 活性物种捕捉及氧空位测试

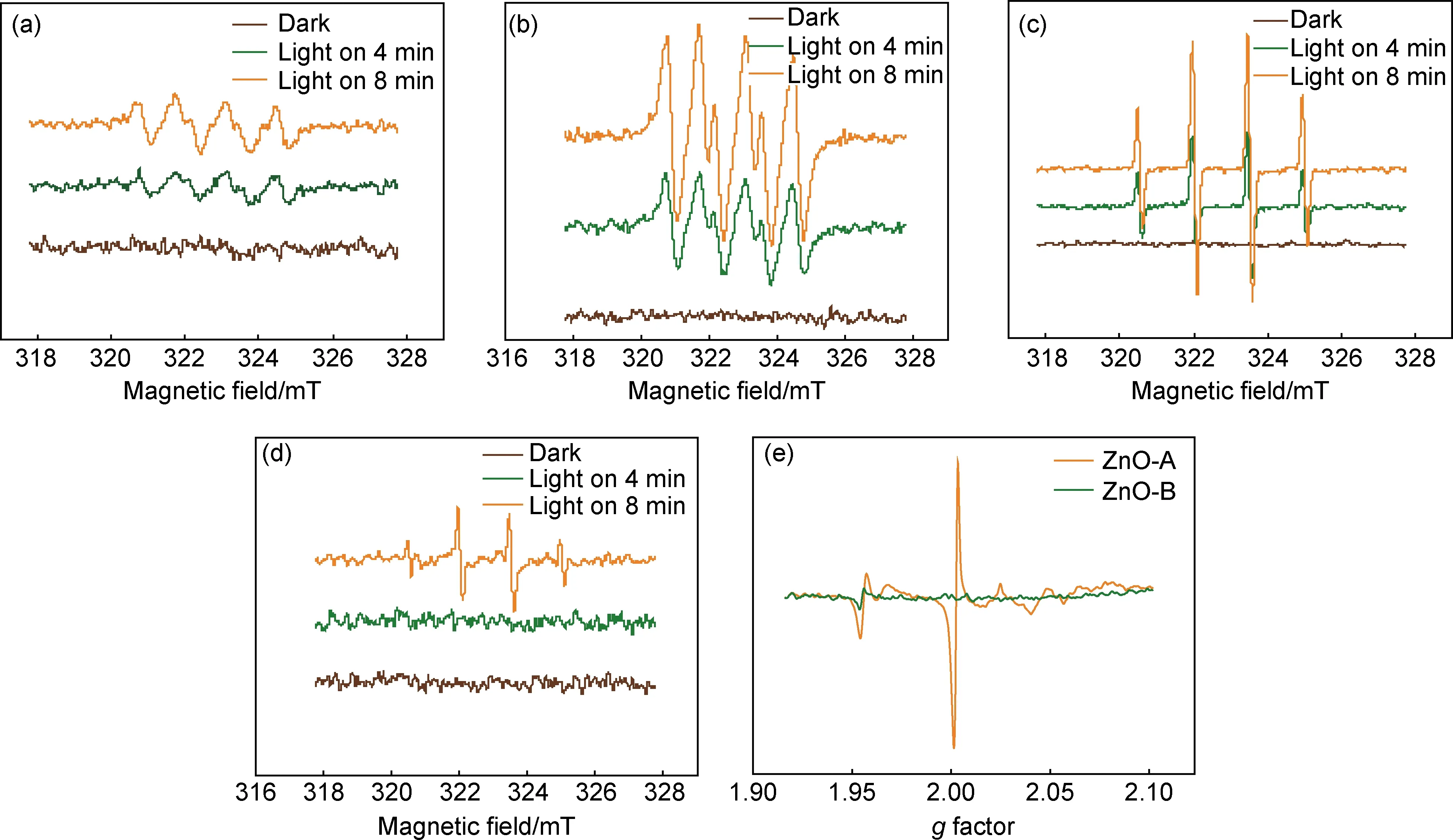
图6 样品的EPR谱图 (a)ZnO-B体系中的超氧自由基;(b)ZnO-A体系中的超氧自由基;(c)ZnO-B体系中的羟基自由基;(d)ZnO-A体系中的羟基自由基;(e)氧空位

此外,鉴于产物ZnO-A的颜色为灰白色,推测其可能含有晶体缺陷,因此对两种方法所制得的ZnO进行氧空位缺陷检测(图6(e))。可知,ZnO-A样品较之ZnO-B样品表现出更强的氧空位信号,即ZnO-A样品具有更高的氧空位含量。进一步对两种样品的O进行高分辨XPS测试,结果示于图7。可见,样品的O1s谱可以拟合为两个峰。对于ZnO-B,在530.46 eV的峰为晶格氧(Olatt),532.00 eV处的峰归因于吸附氧(Oad)[15]。与ZnO-B相比,ZnO-A的O1s光谱中Oad键合能较低(531.60 eV),且信号更强,根据峰面积计算出的Oad含量为27.74%,高于ZnO-B中的20.38%。吸附态氧的比例通常与Ov(氧空位)含量成正比[16],表明ZnO-A中含有更多的Ov,此与EPR测定的氧空位结果吻合较好。

图7 不同制备方法所得ZnO表面的O1s XPS谱图
2.7 能带结构与PL分析
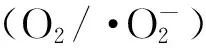
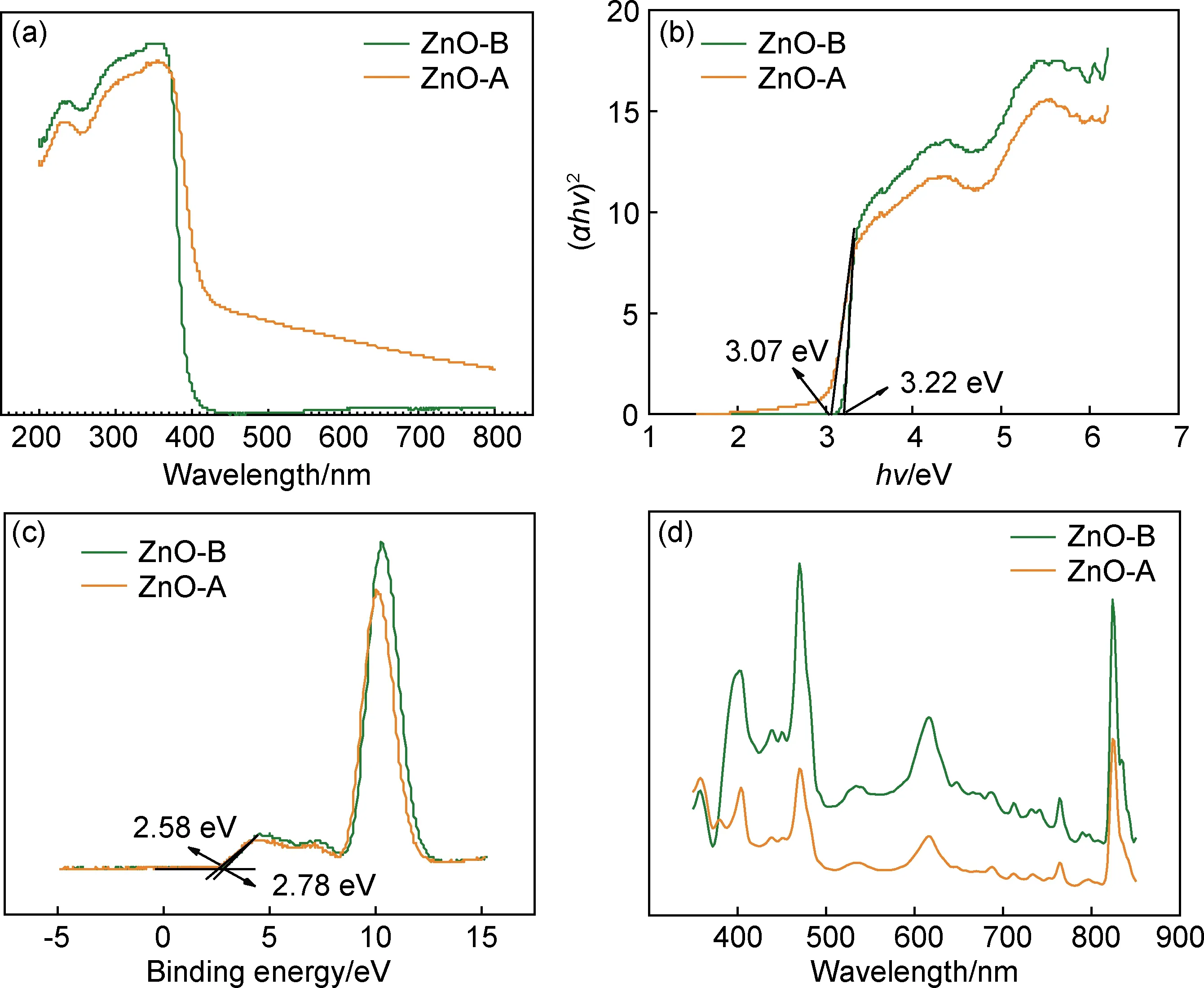
图8 不同制备方法所制得ZnO的UV-vis谱(a),(αhν)2-(hν)关系曲线(b),XPS价带谱(c)和光致发光谱(d)
2.8 光催化机理分析
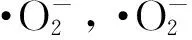
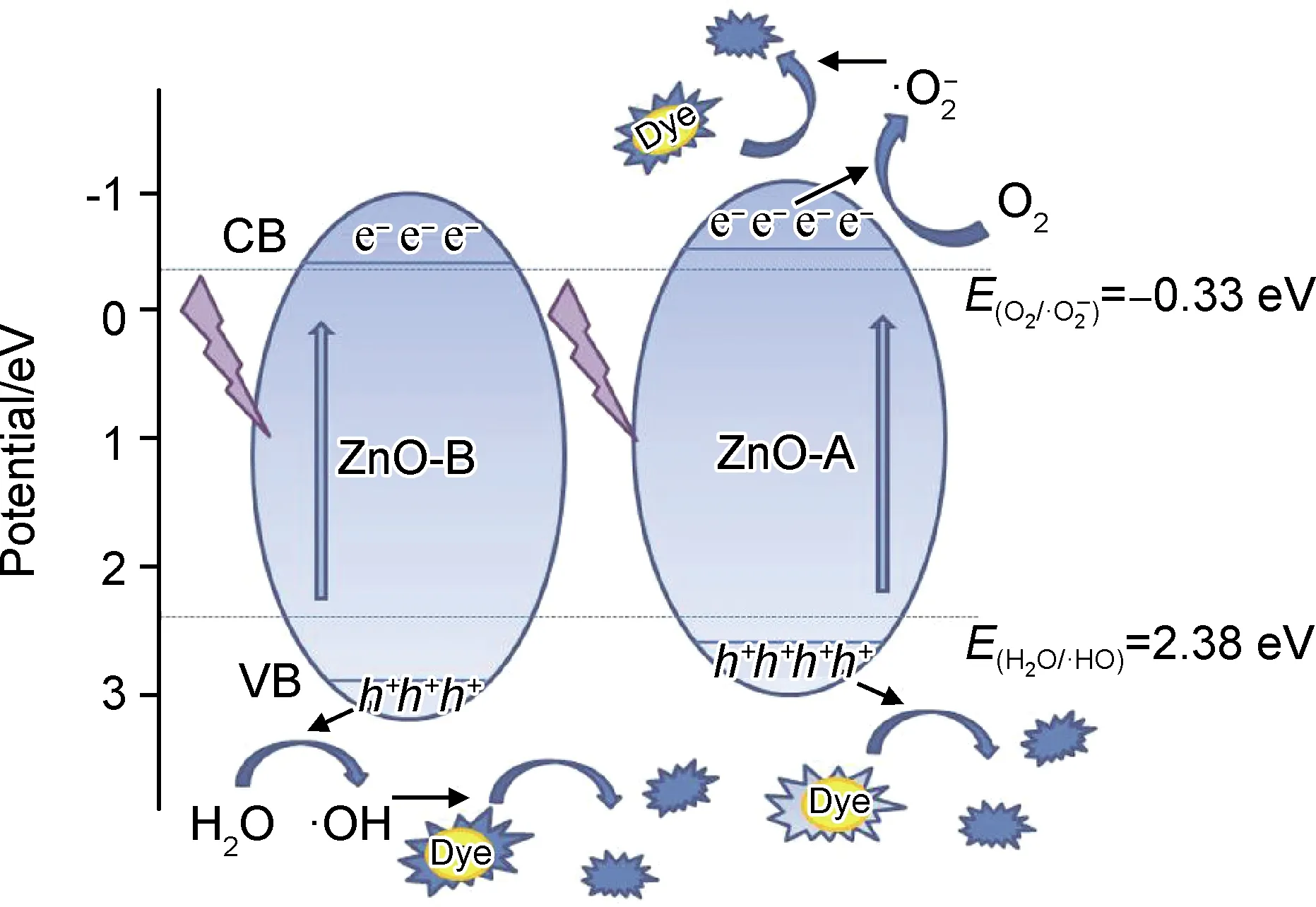
图9 光催化机理示意图
(2)
e-+h+→calories
(3)
h++ H2O →·OH+H+
(4)
(5)
(6)
2HO2·+ H2O → H2O2+O2
(7)
(8)
inorganic molecules
(9)
3 结论
(1)分别采用溶剂热法和草酸盐法制得具有分级微/纳结构但形貌迥异的两种ZnO材料。溶剂法所得ZnO呈花状微球形貌,由纳米片自组装而成;草酸盐法所得ZnO呈微米棒状形貌,由纳米颗粒为基本单元发展而成。
(2)草酸盐法所得ZnO较之溶剂热法所得ZnO具有更优异的光催化能力。在同等实验条件下,ZnO-B和ZnO-A样品对亚甲基蓝溶液的降解率分别为77.08%和12.07%,且前者降解亚甲基蓝溶液的反应速率常数是后者的7.65倍。

