金属离子对玫瑰花色苷水提液稳定性的影响
王贵一,于雅静,何贵萍,3,张佳琪,3,余佳熹,吕远平,*
(1.四川大学 轻工科学与工程学院,成都 610065;2.四川大学 健康食品科学评价体系研究中心, 成都 610065;3.四川大学 食品科学与技术四川省高校重点实验室,成都 610065)
玫瑰(RosarugosaThunb.)为蔷薇科(Rosaceae)蔷薇属(Rosa)多年生常绿或落叶灌木[1]。玫瑰花中含有丰富的多酚类、多糖类和小分子活性物质。玫瑰花色鲜艳,富含类黄酮类化合物,主要为花色素(anthocyanidins)和黄酮醇类物质[2]。花色素作为天然色素,其含有丰富的营养物质及对人体有益的功能性活性成分,具有消炎、抗氧化等作用[3],天然色素着色均匀,色泽鲜艳,亮度好,常作为安全的着色剂被用于食品、药品、化妆品等行业[4-5]。
花色苷(anthocyanin)是由一分子花青素(anthocyanidin)配基与一个或多个糖基通过糖苷键结合形成的配糖体,属于类黄酮化合物,具有基本的C6-C3-C6碳骨架结构[6-7]。通常在低pH范围内(pH<3),花色苷以明亮红色的黄烊盐阳离子形式存在,随着pH升高至4~6,水解成无色的半缩醛形式,或者去质子化变成蓝色的醌型碱,pH在接近7时,C环开始打开出现黄色的查尔酮形式[8]。花色苷具有抗氧化、抗炎、抗肿瘤等生物活性和保健功能,具有较高的社会和经济价值[9]。
花色苷分子中含有大量酚羟基和甲氧基等取代基,化学性质活泼,在加工过程中稳定性较差,花色苷的颜色和生物活性易受金属离子等因素的影响[10]。通常,将体系pH值调到3及以下,这样的酸性环境有利于花色苷向黄烊盐阳离子形式转变,赋予更好的稳定性[11]。本研究采用CIELAB色空间及花色苷保存率为评价指标,研究金属离子对玫瑰花色苷水提液稳定性的影响,为玫瑰花色苷的开发利用提供了依据。
1 材料与方法
1.1 材料
玫瑰花瓣(中华1号):四川千领农业科技有限公司;氯化钠、氯化镁、氯化钾、乙酸铅、氯化钙、氯化锌、氯化锰、氯化铝、氯化铜、氯化铁:均为分析纯,成都科龙化工试剂厂。
1.2 主要仪器与设备
CM-5型分光测色计 柯尼卡美能达株式会社;UV-2000型紫外可见分光光度计 尤尼柯(上海)仪器有限公司;ESJ210-4A型电子天平 沈阳龙腾电子有限公司;ST2100型实验室pH计 奥豪斯仪器有限公司;XK96-A型快速混匀器 江苏新康医疗有限公司;Milli-Q Direct型水纯化系统 默克密理博公司;HWS-26型电热恒温水浴锅 上海齐欣科学仪器有限公司。
1.3 实验方法
1.3.1 玫瑰花色苷提取工艺流程
玫瑰花粉末(过60目标准筛)→超声辅助溶剂浸提(55 ℃,2 h)→抽滤→玫瑰花色苷水提液。
1.3.2 单因素实验
称取2.0 g玫瑰花粉末,加入100 mL pH值为3.0的超纯水,在55 ℃水浴锅中浸提2 h,抽滤得到玫瑰花色苷超纯水提液,备用。根据GB 5749-2006《生活饮用水卫生标准》[12]对水中常见金属离子限量的不同,分别配制不同浓度梯度的NaCl、MgCl2、CaCl2、KCl、ZnCl2、CuCl2、MnCl2、AlCl3、FeCl3、(CH3COO)2Pb溶液,分别加入超纯水配制的玫瑰花色苷水提液中,模拟生活用水,进行单因素实验[13]。各金属离子的最大浓度分别为NaCl、MgCl2、CaCl2、KCl(100 mmol/L)、ZnCl2、CuCl2(20 mmol/L)、MnCl2(2 mmol/L)、AlCl3、FeCl3(10 mmol/L)、(CH3COO)2Pb (0.05 mmol/L)。加入金属离子的玫瑰花色苷水提液在室温下避光保存,测定颜色的动态变化并计算花色苷的保存率,分析各金属离子对玫瑰花色苷水提液稳定性的影响。
1.3.3 CIELAB色空间及测定方法
CIELAB色空间,即L*、a*、b*色空间,是目前常用的表征物体颜色的方法之一,其组成见图1。
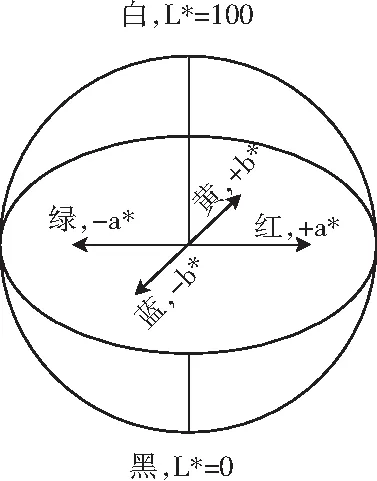
图1 CIELAB均匀颜色空间Fig.1 CIELAB uniform color space
其中,L*值、a*值和b*值分别表示亮度和色度坐标;a*值和b*值分别表示红绿轴和蓝黄轴上颜色的饱和度;色差△E*表示颜色变化的程度,由以下公式计算确定:
△E*值越大,越容易被肉眼识别,规定△E*>3.5时,肉眼能观察到色泽的变化[14]。
1.3.4 玫瑰花色苷颜色变化的测定
选择CM-5分光测色计的液体测量模式,将待测花色苷样液注入厚2 mm的石英比色皿(CM-A97)至刻度线以上,采用标准光源D65,以超纯水为空白校准,在25 ℃恒温下测定各项指标,每个样品平行测定3次[15]。将水提液的pH值调至3.0,在室温下避光保存,以提取液制备0 h的初始L*、a*、b*值为标准颜色,150 h内测定各样品溶液L*、a*、b*值的动态变化,计算△E*值,分析其颜色变化。
1.3.5 玫瑰花色苷保存率的计算
玫瑰色素中主要的呈色物质为花色苷,其存在高度分子共轭体系,具有酸性和碱性基团,玫瑰花色苷溶液在200~400 nm之间有较多吸收峰,在可见光区有518 nm一个较大吸收峰,选取518 nm作为检测波长[16]。分别在518 nm下测定初始花色苷水提液的吸光度A0及存放150 h后水提液的吸光度A1,以超纯水为空白对照组。按照以下公式计算花色苷保存率:
2 结果与分析
2.1 玫瑰花色苷超纯水提液的稳定性
在518 nm检测波长下,测得超纯水提取的花色苷水提液A0为0.6491 nm,经150 h存放后,其水提液吸光度A1为0.4855 nm,根据计算可得,超纯水提取液的保存率为74.8%。
2.2 Na+、Mg2+、K+、Pb2+对玫瑰花色苷稳定性的影响
Na+、Mg2+、K+、Pb2+对玫瑰花色苷水提液放置过程中颜色稳定性的影响见图2,放置150 h后的保存率见表1。
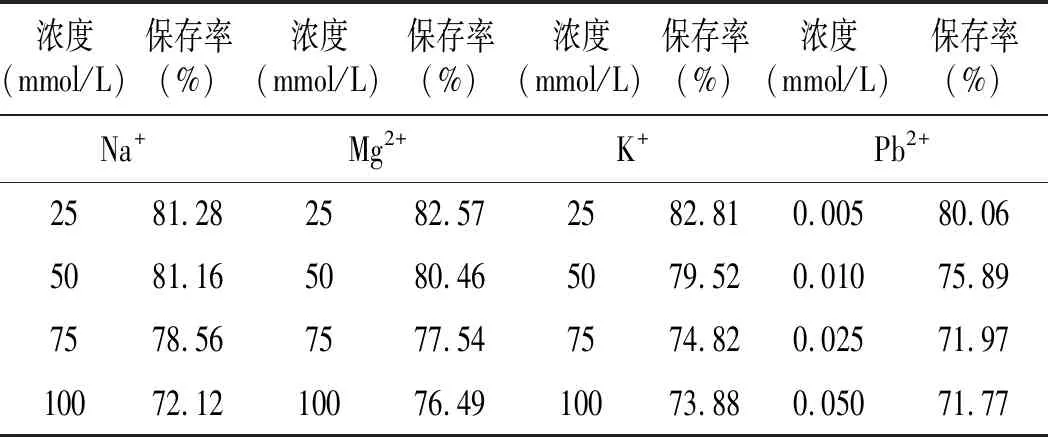
表1 Na+、Mg2+、K+、Pb2+对玫瑰花色苷保存率的影响Table 1 Effect of Na+,Mg2+,K+,Pb2+ on the retention rates of rose anthocyanins
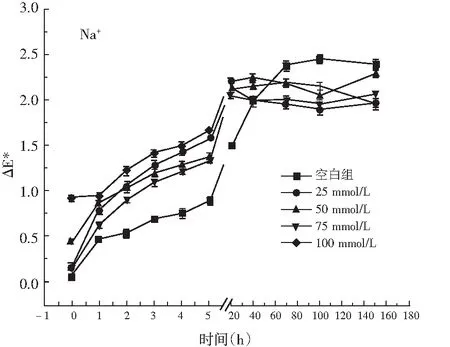
图2 Na+、Mg2+、K+、Pb2+对玫瑰花色苷水提液颜色稳定性的影响Fig.2 Effect of Na+,Mg2+,K+,Pb2+ on color stability of aqueous solution of rose anthocyanins
生活饮用水中Na+、Mg2+、K+的浓度低于100 mmol/L,Pb2+的浓度低于0.05 mmol/L。由图2可知,4种不同浓度的金属离子的△E*值随着放置时间的延长而缓慢增大,但最终都趋于较稳定。150 h后,△E*数值均小于3.5,表明无肉眼可见的颜色变化。
由表1可知,同一种金属离子,随着浓度的增加,其保存率均下降。加入Na+、Mg2+、K+、Pb2+4种金属离子的花色苷水提液在常温下放置150 h后,其花色苷均有所损耗,但150 h后,最终花色苷保存率与超纯水提取液的保存率相近。说明自来水中含有的Na+、Mg2+、K+、Pb2+对玫瑰花色苷的稳定性几乎无影响。
2.3 Ca2+、Zn2+、Mn2+、Al3+对玫瑰花色苷稳定性的影响
Ca2+、Zn2+、Mn2+、Al3+4种金属离子对玫瑰花色苷水提液放置过程中颜色稳定性的影响见图3,放置150 h后的保存率见表2。

表2 Ca2+、Zn2+、Mn2+、Al3+对玫瑰花色苷保存率的影响Table 2 Effect of Ca2+,Zn2+,Mn2+,Al3+ on the retention rates of rose anthocyanins

图3 Ca2+、Zn2+、Mn2+、Al3+对玫瑰花色苷水提液颜色稳定性的影响Fig.3 Effect of Ca2+,Zn2+,Mn2+,Al3+ on color stability of aqueous solution of rose anthocyanins
由图3可知,在20 h内,各浓度的Ca2+、Zn2+、Mn2+、Al3+的玫瑰花色苷水提液的△E*值随放置时间延长而增大。20 h后,Ca2+、Zn2+、Mn2+、Al3+的玫瑰花色苷水提液的△E*值都出现不同程度的波动,但值均小于3.5,即肉眼不能察觉到颜色变化。
由表2可知,在常温下放置150 h后,这4种金属离子均能提高花色苷水提液的花色苷保存率。对于同一种金属离子,保存率随离子浓度增大而增大。一般来说,花色苷分子中羟基数目多则稳定性较弱,发生甲基化、糖基化和酰基化反应可以提高稳定性。可能是这几种金属离子与花色苷分子中相邻的酚羟基螯合形成稳定的络合物,对花色苷结构起到一定的保护作用[17-18]。说明自来水中含有少量的Ca2+、Zn2+、Mn2+、Al3+对玫瑰花色苷的颜色稳定性无明显影响,离子浓度达到一定值时能提高花色苷的保存率。
2.4 Cu2+对玫瑰花色苷稳定性的影响
Cu2+对玫瑰花色苷水提液放置过程中颜色稳定性的影响见图4,添加Cu2+的水提液放置150 h后的花色苷保存率见表3。
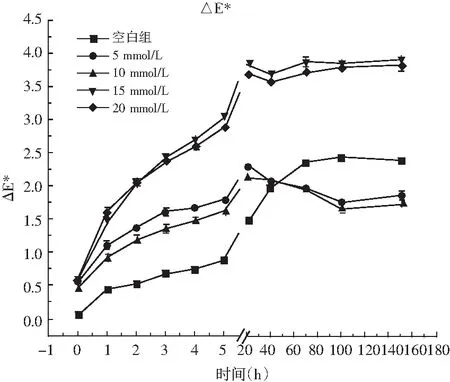
图4 Cu2+对玫瑰花色苷水提液颜色稳定性的影响Fig.4 Effect of Cu2+ on color stability of aqueous solution of rose anthocyanins

表3 Cu2+对玫瑰花色苷保存率的影响Table 3 Effect of Cu2+on the retention rates of rose anthocyanins
由图4可知,水中Cu2+浓度在10 mmol/L以内时,玫瑰花色苷水提液的△E*值均不会超过3.5,即水提液的颜色不会发生肉眼可见的变化,但a*值和b*值都有小幅度减小;当水中Cu2+浓度在10~20 mmol/L时,放置20 h后△E*值超过3.5,此后在3.5~4.0范围内波动并逐渐趋于稳定,a*值和b*值减小的幅度比低浓度时大,表现为红色减小和蓝色增加;Cu2+浓度在5~20 mmol/L范围内,随着Cu2+浓度的增大,玫瑰花色苷保存率有所降低,但仍高于不含金属离子的超纯水对照组。Cu2+浓度在5 mmol/L时,其保存率高达90.93%,即水提液中Cu2+浓度越大,保存率越低。由于本实验中加入的Cu2+溶液浓度很低,生活饮用水卫生标准规定Cu2+限量为1.0 mg/L,因此认为Cu2+本身的颜色不会对水提液的颜色产生影响。
玫瑰花色苷水提液中含有的Cu2+浓度大于10 mmol/L时,产生褪色现象,色泽随放置时间的延长逐渐变化。对放置150 h的添加20 mmol/L Cu2+的玫瑰花色苷水提液进行光谱扫描,其最大吸收波长从518 nm红移至524 nm处,说明Cu2+与花色苷发生了一定的反应。其中一种原因可能是花色苷分子上的酚羟基、甲氧基等取代基具有孤对电子,而Cu2+作为过渡元素阳离子,能够提供空轨道,与花色苷络合形成蓝色的铜-花色苷络合物[19],表现为水提液红色减小和蓝色增加,特征吸收峰改变,另一种原因可能是Cu2+具有催化作用,能够催化花色苷分子上的酚羟基氧化,从而改变了花色苷水提液的颜色,此分析与周兆祥等对栀子花黄色素与金属离子效应的研究结果一致[20]。由于花色苷结构中酚羟基越多越不稳定,Cu2+催化氧化能一定程度上提高其结构的稳定性[21],造成水提液褪色和花色苷保存率比空白组高的现象。
综上所述,玫瑰花色苷作为食品原料加工时,应尽量避免与铜质器具接触,加工用水中的Cu2+浓度应低于10 mmol/L,此时玫瑰花色苷的稳定性较好。
2.5 Fe3+对玫瑰花色苷稳定性的影响
Fe3+对玫瑰花色苷水提液放置过程中颜色稳定性的影响见图5,添加Fe3+的水提液放置150 h后的花色苷保存率见表4。

表4 Fe3+对玫瑰花色苷保存率的影响Table 4 Effect of Fe3+on the preservation rates of rose anthocyanins

图5 Fe3+对玫瑰花色苷水提液颜色稳定性的影响Fig.5 Effect of Fe3+on color stability of aqueous solution of rose anthocyanins
由图5可知,水中Fe3+浓度在2.5~10 mmol/L时,a*、b*、△E*值随着Fe3+添加量的增加而迅速发生改变,△E*值随着放置时间的增加逐渐升高,20 h后逐渐趋于稳定。10 mmol/L的Fe3+可使花色苷水提液的△E*值达到10以上,肉眼可观察到明显的褪色现象。水提液的△E*值变化主要是a*值和b*值共同决定的,a*值减小(红色减退),b*值增大(蓝色减退),两者的变化趋势都与△E*值相同。
由表4可知,玫瑰花色苷水提液中加入Fe3+并放置150 h后,玫瑰花色苷的保存率下降,并随着Fe3+浓度的增大,保存率降低。即使Fe3+浓度仅为2.5 mmol/L,花色苷保存率也仅有53.59%。根据生活饮用水卫生标准,Fe3+限量为0.3 mg/L。
玫瑰花色苷水提液中含有的Fe3+浓度高于2.5 mmol/L时,会产生明显的褪色现象,并且花色苷的保存率显著降低,说明高浓度的Fe3+可削弱花色苷的稳定性。对放置150 h的添加2.5 mmol/L Fe3+的玫瑰花色苷水提液进行光谱扫描,其原本的最大吸收波长(518 nm)已经完全消失,波峰移动至紫外区,说明花色苷的分子结构已经被Fe3+完全破坏或已经生成其他物质。造成这一现象的原因可能是Fe3+具有较强的氧化作用,能迅速氧化破坏花色苷分子中的酚羟基;也可能是因为花色苷的邻位羟基结构不稳定,容易与Fe3+等金属离子配合形成络合物,这种络合物的稳定性强于花色苷,因此生成后不可逆转[22-23]。李颖畅等研究发现Fe3+使蓝莓花色苷溶液产生沉淀,颜色由红色变为黄褐色,花色苷保留率降低;马越[24]试验证明向紫玉米花色苷的溶液中加入Fe3+,溶液迅速变成黄褐色,并产生黑褐色沉淀,可能是因为多酚类色素与Fe3+反应生成复杂络合物。
Fe3+对花青素具有破坏作用,使花青素的稳定性下降[25],在此实验中,较低浓度的Fe3+即可破坏玫瑰花色苷,降低其保存率,使颜色发生明显改变。食品生产中应注意避免铁质用具与玫瑰花色苷接触,加工用水中也应尽量除去Fe3+。
3 结论
根据《生活饮用水卫生标准》对常见金属离子限量的不同,在pH值为3.0的溶液中,Na+、Mg2+、K+、Pb2+对玫瑰花色苷的颜色稳定性无明显影响;Ca2+、Zn2+、Mn2+、Al3+4种离子不会使花色苷水提液颜色发生明显改变,花色苷保存率有所提高,可能是由于花色苷分子中相邻酚羟基与这4种金属离子螯合,形成稳定络合物,从而对花色苷结构起到一定的保护作用。Cu2+可能通过催化花色苷分子上的酚羟基氧化等,导致水提液颜色产生肉眼可见的变化;较低浓度的Fe3+即可使花色苷水提液明显褪色,花色苷保存率也大幅降低,可能是Fe3+的强氧化作用破坏花色苷分子中的酚羟基,从而使玫瑰花色苷的颜色和结构都发生改变。所以玫瑰花色苷作为天然色素使用时,应避免与铜、铁质器具接触。本研究对玫瑰天然色素的开发应用具有一定的实用意义。
花色苷类天然色素在食品中的稳定性应用研究仍然是今后花色苷研究的重点方向,使用花色苷作为着色剂时,应考虑到花色苷产品本身的纯度、结构等的不同,还需考虑与其密切相关的应用环境条件。

