水合盐基中低温热化学储热材料性能测试及数值研究
李威,王秋旺,曾敏
(西安交通大学能源与动力工程学院,热流科学与工程教育部重点实验室,陕西西安710049)
引 言
随着传统化石能源枯竭和环境恶化等问题的日益严重,大力发展新能源和可再生能源以缓解全球能源危机和资源短缺是必经之路[1-3]。据国际能源署(IEA)报道,到2040年太阳能、风能等一次能源占比将达40%以上[4]。然而,由于可再生能的间歇性以及与需求侧之间的不匹配性,导致可再生能源的高效利用受到限制[5-6]。为解决能源供给与需求的不匹配性,储能技术应运而生。
与显热储热和相变潜热蓄热相比,热化学储热(TCES)能量密度更大(1~2 GJ/m3,即270~540 kW·h/m3),几乎无热损失,最重要的是,其可实现跨季节性长期热储存[7-8]。目前化学蓄热系统还处于实验室规模研究阶段,尚未投入工程应用,仍有待进一步研究和发展[9-10]。其中,基于水合盐的中低温(≤200℃)热化学储热系统凭借其安全可靠、运行要求简单等优势逐渐受到研究人员的重视[11-15]。无机盐/水蒸气工质对的气-固反应方程如下:
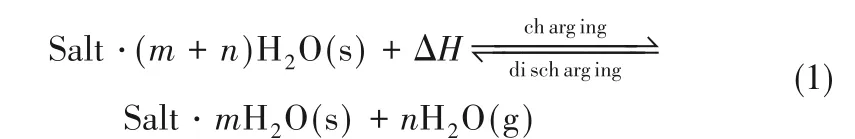
充热(脱附)阶段,水合盐在太阳热能或工业余热等低品位热源驱动下,解吸出水蒸气形成无水盐或少水盐直至反应结束。当用户需要用热时(包括空间加热和生活热水生产),将水蒸气或湿空气通入反应床中诱发水合反应,释放的热量可被提取利用。热化学储热工作原理如图1所示。
储热材料作为热化学储热系统的关键部分,对整个系统的性能有着重要影响。由于纯水合盐存在水合特性差[16]、热导率低、稳定性差、易过度吸水潮解、结块或膨胀等问题[17],将水合盐浸渍于多孔基体内是目前常用的改善上述问题的有效方法。Zhang等[18]制备了活性氧化铝/LiCl复合吸附剂用以实现低温(≤120℃)条件热存储。通过控制吸湿盐LiCl含量在阈值之下以防止溶液渗漏,最终获得的储热密度为318 kW·h/m3。Xu等[19]合成了沸石/MgCl2复合吸附剂并提出多形式吸附方式,即包括多孔基质的物理吸附、水合盐的化学吸附以及盐溶液的吸收效应,结果在200℃充热条件下实现1368 kJ/kg的高储热密度。介孔炭/CaCl2复合材料在1000 W/m2辐照条件下蓄热密度可达254 kW·h/m3,伴随的最高蒸汽吸附量为0.81 g/g[20],具有中低温条件下化学储热的应用前景。Nonnen等[21]分别将NaCl、CaCl2、MgCl2和MgSO4包覆于沸石微孔内,并比较了这些复合吸附剂的吸附能力和储热密度,结果表明沸石/MgCl2样品具有最高的储热密度,为275 kW·h/m3,比纯沸石高53%。类似的,介孔硅质页岩/LiCl[22]、聚硅氧烷泡沫/MgSO4[23]、硅胶/Al2(SO4)3[24]等复合热化学材料均被制备用以改善蓄热性能。然而,复合吸附剂仍有一些不足需要改进,例如沸石解吸温度较高、蛭石热导率低、聚硅氧烷泡沫机械强度差等。
本文开发了K2CO3@EG复合吸附剂,并对其进行了热化学性能研究。膨胀石墨具有丰富的微观结构和高比表面积,可使内嵌的水合盐与水蒸气充分反应,提升传质性能。此外,由于石墨具有很高的热导率,因此该复合吸附剂可提高传热效果。K2CO3·1.5H2O可在较低的温度下(约100℃)实现很大程度的脱附,更符合中低温化学蓄热要求。热化学性能测试结果和所选用的储热单元模拟结果初步验证了该复合吸附剂在中低温TCES系统的可行性。
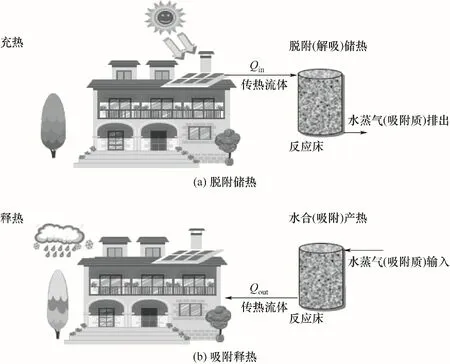
图1 水合盐基化学蓄热系统运行示意图Fig.1 Schematic diagram of hydrated salt-based chemical heat storage system
1 材料与实验方法
1.1 复合吸附剂的制备
半水碳酸钾K2CO3·1.5H2O购自于中国国药试剂有限公司,纯度为分析纯级别(>98%);膨胀石墨由江苏先丰纳米有限公司提供(纯度>99%,商家提供的孔径参考值为100~200μm)。首先,将碳酸钾水合物与膨胀石墨置于烘箱中加热至150℃并维持2 h以上,使水分完全脱附。之后称取0.750 g干燥后的膨胀石墨[15%(质量)]和4.25 g K2CO3[85%(质量)],加入去离子水将其溶解形成悬浊液,并置于超声波分散条件下持续6 h,使膨胀石墨粉末均匀分散于盐溶液,盐分充分浸渍于膨胀石墨的孔内。然后再将该悬浊液置于马沸炉中以2℃/min的升温速率加热至200℃并维持2 h,最后在封闭条件下将其自然冷却至室温,最终获得含膨胀石墨质量分数15%的复合吸附剂(CS15)。此外,将完全脱附后的纯盐K2CO3作为对照组与复合储热材料进行对比研究。
1.2 测试与分析
扫描电镜(GeminiSEM 500)用以探测样品微观形貌,利用X射线衍射仪检测复合吸附剂样品是否制备成功。复合吸附剂和纯水合盐的比热容、脱附反应热(储热密度)等热物性用同步热分析仪(STA449F3,耐驰,德国)测量分析,测试是在氮气条件下,升温速率为5℃/min。同步热重分析仪可配备水蒸气发生器以进行蒸汽的脱附-吸附循环实验。利用动态蒸汽吸附仪对样品的吸附性能进行测试。
2 表征与测试结果
2.1 微观形貌
图2为膨胀石墨、K2CO3纯盐以及K2CO3@EG复合吸附剂的SEM图。从图2(a)中可以看出膨胀石墨具有层状孔结构,这些丰富的孔可以充分包覆水合盐进而促进传热传质效果。K2CO3纯盐呈粉末状,粒度为微米级[图2(b)]。由图2(c)可以看出对于复合吸附剂,水合盐均匀分布于膨胀石墨内(红圈内所示)。这不仅可以防止水合盐过度吸附潮解而渗漏,同时载体材料和水合盐形成换热网络,增强了热质传递能力。

图2 膨胀石墨(a),纯水合盐(b)以及K2CO3@EG复合吸附剂(c)的SEM图Fig.2 SEM images of expanded graphite(a),pure salt(b),and composite sorbent of K2CO3@EG(c)
2.2 吸附特性
吸附式储热材料的吸附动力学性能对储热系统的释热功率有着直接的影响。图3显示了纯水合盐与复合吸附剂CS15对水蒸气的吸附动力特性。在进行吸附测试前,样品均被加热以使吸附剂成为无水的干燥状态。
图3(a)为纯水合盐和复合吸附剂在30℃、相对湿度(RH)为29%,即水蒸气压力约为1230 Pa条件下的吸附情况。该蒸气压对应的饱和温度为10℃,符合冬季环境温度。可以看出复合吸附剂CS15吸附速率更快,说明掺杂EG后,吸附剂的吸附动力学性能得到提升。其在250 min左右达到吸附平衡状态,吸附量约为0.166 g/g。而对于纯盐达到吸附平衡所需时间约为360 min,且平衡吸附量略小于理论值0.1956 g/g。这可能是纯盐水合过程中较差的传质效果导致的反应不充分造成的。此阶段发生的反应为:
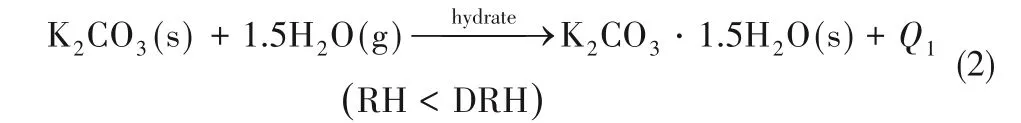
为进一步掌握吸附剂在不同工况下的吸附效果,还选择了相对湿度为40%(1710 Pa)和55%(2335 Pa)进行吸附特性研究,二者对应的饱和温度分别为15和20℃,结果如图3(b)所示。可以看出对于固定的相对湿度即水蒸气分压条件下,复合吸附剂CS15的吸附动力性能优于纯盐。值的注意的是,对于55%RH的情况,纯盐在达到吸附平衡一段时间后,蒸汽吸附量再次增加,这是因为水合盐在较高的蒸汽分压下过度吸附液解进而形成溶液,浓盐溶液进一步吸收水分稀释,此阶段发生的反应为:
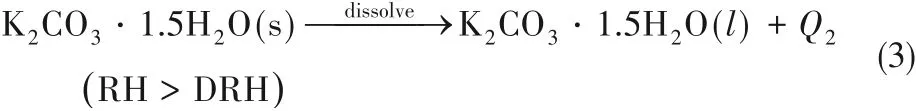
这说明纯盐K2CO3不适用于热化学储热系统。而对于CS15样品,在较高蒸汽分压条件下,吸附量达到理论平衡值后虽然有所提升但并未观察到液解和渗漏现象,这反而有助于储热密度的提升[19]。实际上,无论是开式或闭式系统,在吸附剂吸附蒸汽进行水合释热过程中,水蒸气压力一般不高于2000 Pa,这也证明了该复合吸附剂用于储热系统的安全性。两类吸附剂详细的吸附平衡时间和吸附量见表1。
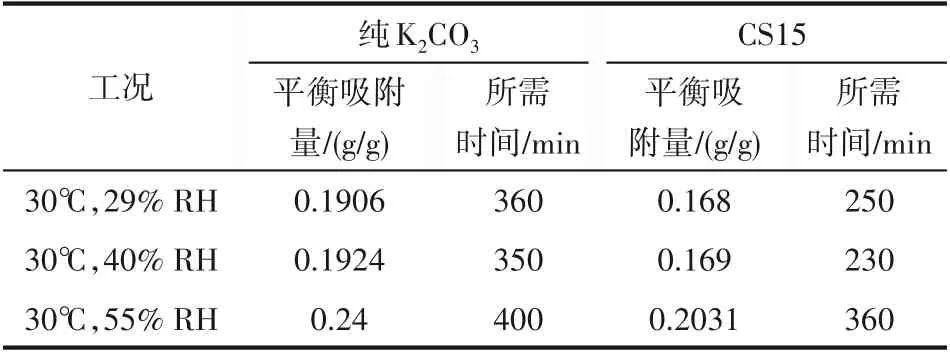
表1 两种吸附剂不同工况下平衡吸附量及所需时间Table 1 Equilibrium adsorption capacities and corresponding times of sorbents
2.3 储热密度
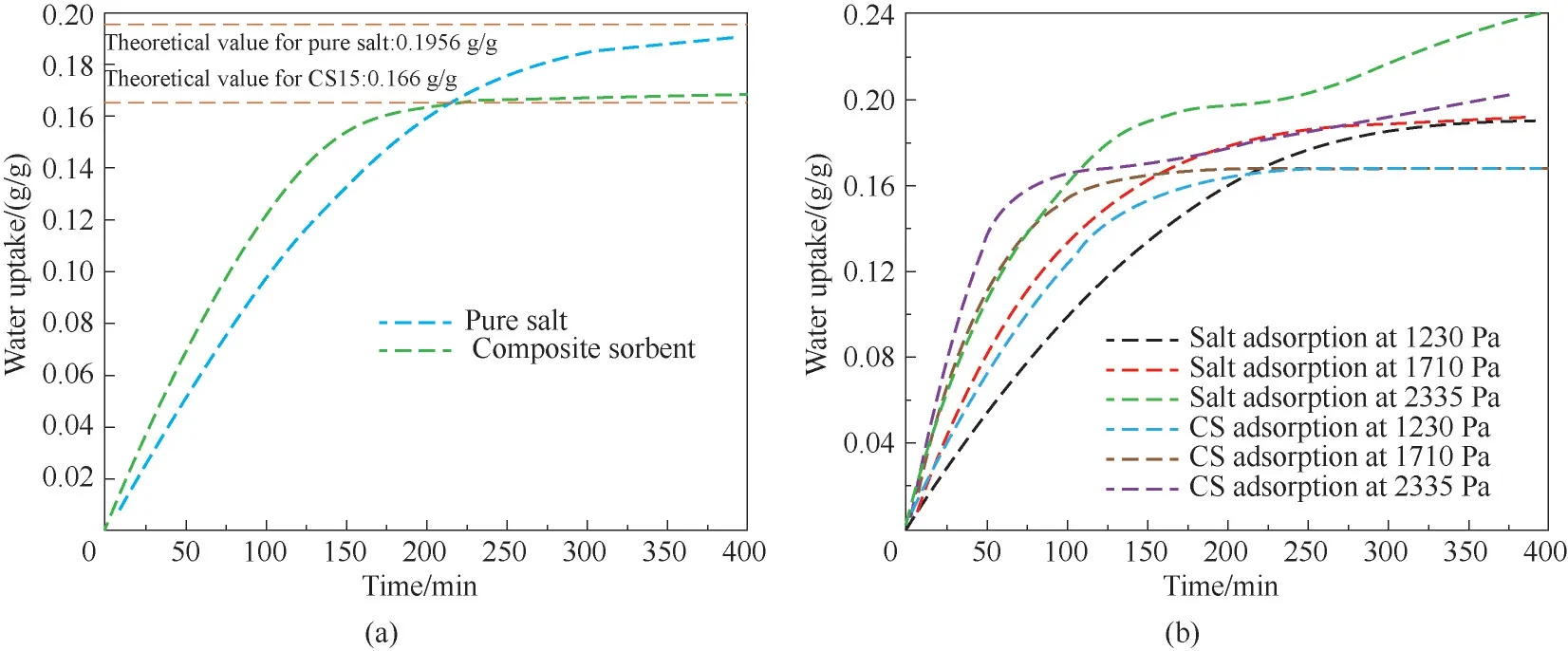
图3 纯盐与复合吸附剂在30℃,(a)29%RH和(b)不同相对湿度条件下的吸附情况Fig.3 Adsorption of pure salt and composite sorbent at 30℃with(a)29%RH and(b)various vapor pressures
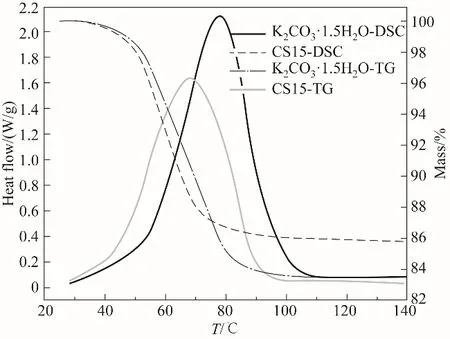
图4 纯盐与复合吸附剂的TG-DSC测量结果Fig.4 TG-DSCresults of the pure salt hydrate and the composite sorbent
对于热化学储热材料,一般将其脱附反应焓视为理论储热密度。在对复合吸附剂CS15进行同步热分析(TG-DSC)前,将样品置于30℃、29%RH恒温恒湿条件下使其完成水合过程。TG-DSC结果如图4所示。K2CO3·1.5H2O的理论储热密度(ESD)为580 kJ/kg,在105℃左右可基本完成脱附。而对于CS15吸附剂,由于膨胀石墨的添加导致储热密度有所降低,为505 kJ/kg,且脱附基本完成所需的温度不超过100℃。该现象产生的原因是石墨的添加导致脱附反应活化能的降低[25-26]。其机理解释为:一方面,膨胀石墨基质作为LiOH水合盐的结晶位点,附着在其表面的水合盐晶体颗粒是微纳尺度级别的,这已由SEM等表征结果揭示。由于该微纳尺寸效应,处于不饱和以及不稳定状态的表面原子可以放大表面晶格振动幅度并具有高表面能,这导致了水合盐基复合储热材料的脱附温度降低。另一方面,石墨基体中的水合盐的结晶度低于纯水合盐,较低的结晶度也会导致晶体转变温度的降低[27-28]。可见,该复合吸附剂充热温度相比于纯盐有了明显降低,这使得储热过程更易进行。
2.4 循环稳定性
循环稳定性作为储热材料的重要指标之一,关系到储热系统的可行性和经济效益。以5℃/min的升温速率将样品从室温加热至105℃,并保持该状态15 min。之后,将样品冷却至30℃,随后在30℃、29%RH(1230 Pa)条件下进行吸附水合作用。将此脱附-吸附操作连续进行15次。
图5显示了纯盐和CS15样品连续15次脱附/吸附循环测试结果。可以看出,纯K2CO3的脱附-吸附量随循环次数的增加显著降低,因此储热密度也明显下降,由最初的580 kJ/kg降为420 kJ/kg,下降幅度约为27.6%。而K2CO3@EG复合吸附剂循环效果则较好,虽然储热密度也略有降低,但并不明显,由最初的505 kJ/kg减为450 kJ/kg,下降幅度约为10.9%。经历连续13次脱附-吸附循环后,从第14次循环开始,复合吸附剂的储热密度已然超过纯盐的相应值。可见,虽然复合吸附剂因为多孔基体的添加而使理论储热密度有所降低,但随着循环次数的进行,其储热密度将大于纯水合盐。同时该循环结果也进一步验证了所制备复合材料用于中低温热化学储热的可行性。
为更全面地研究水合盐基热化学储热系统,数值模拟研究是十分必要的。仿真结果可为后续实验工作提供一定的指导和借鉴作用,而储热材料的性能测试如反应热(储热密度)、热导率等参数可直接用于仿真研究。另外,模拟所需的关于化学反应的重要参数如反应活化能等需基于材料的性能测试结果进一步进行推导。相关研究在文献[25]中已有详细介绍,本文不做重复赘述。
3 数值研究
3.1 物理模型
本文所研究的水合盐基热化学蓄热模型采用本课题组前期工作提出的整体式储热管道结构[25],以其中一个储热单元为研究对象,如图6所示。对储热单元的吸附释热过程进行模拟研究。

图5 (a)纯K2CO3和(b)CS15复合吸附剂在循环过程中含水量和储热密度的变化Fig.5 Water uptakes and energy storage densitiesof pure K2CO3 and CS15 sorbent in cyclability testing
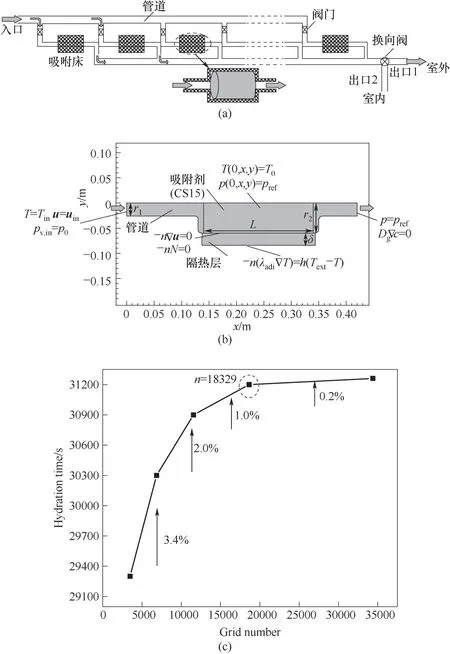
图6 整体式储热管道(a)和储热单元对称结构一半及边界条件示意图(b),网格独立性验证(c)Fig.6 Schematic of the integral heat storage pipe(a)and a half of the symmetrical structure and boundary conditions(b),grid independence verification(c)
3.2 理论模型
3.2.1 控制方程及条件 为建立并解决控制方程,需对模型做一些合理假设。具体的假设在先前的工作中[29]已有详细介绍。主要控制方程及相关介绍已列于表2,边界条件和初始条件见图6(b)所示:入口气体的蒸汽浓度、温度及速度已知,压力出口,储热单元外围由隔热层包覆,其与周围存在对流换热。
3.2.2 模型对照及网格无关系验证 本研究中的控制方程以及初始、边界条件由有限元软件COMSOL Multiphysics解决。网格无关性验证结果如图6(c)所示,最终选取网格数为18329的条件进行数值模拟。有关模型正确性在文献[25,30]中已有详细介绍,此处不再赘述。
4 数值结果分析与讨论
4.1 温度场及吸附转化率
湿空气(pv=1230 Pa)入口速度为0.3 m/s。由图7可知,在吸附释热阶段,由于水蒸气与吸附剂的水合放热反应,吸附剂反应床温度在短时间内骤升,由初始时刻的20℃提升到将近50℃,随后温度稍有降低,持续一段时间后,反应床降温速率增大直到水合反应结束。出口空气温度变化趋势与吸附床相似,只是略低于吸附剂温度,这是因为吸附剂与空气之间存在传热温差。约经历520 min后,吸附床完成较大程度的转化(α>95%)。图8定性显示了不同时刻吸附转化率分布场。可以看出,转化过程逐渐由靠近入口的一端向靠近出口的一端迁移,在400 min后储热单元整体水合转化程度超过50%。

表2 控制方程及描述Table 2 Governing equations and descriptions
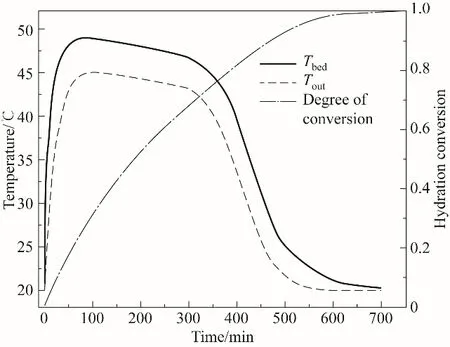
图7 释热过程中反应床及出口空气温度及吸附转化率变化Fig.7 Temperature evolutionsof reaction bed and outlet air and conversion degree duringdischarging
4.2 不同相对湿度的影响
由于相对湿度或水蒸气分压对水合盐基储热系统有着重要的影响,本节讨论具有不同相对湿度的湿空气对吸附水合过程的影响。由图9可知,随着水蒸气分压力的提升,反应床所能达到的最高温度也随之增大。对于入口初始温度为20℃的湿空气,当相对湿度RH=52%、72%和86%时,吸附床所能达到的最高温度分别约为49、56和61℃。可以推断,较高的相对湿度可以提高输出热功率。另一方面,虽然最高温度随着蒸汽分压力的增大而上升,但释热时间却相反。尤其对于供热而言,稳定的释热条件尤为重要。三种工况下所能实现的较为稳定的热生产持续时间分别约为80、150和250 min。因此,在进行释热过程时,需兼顾所需温度、输出热功率以及稳定产热的时间等因素,根据实际需求选择合适的操作条件。
4.3 储热单元热性能
对于热化学储热系统而言,热功率和热效率是两个非常重要的参数指标。热功率的基本定义可表述为:


图8 吸附床在不同时刻吸附转化程度Fig.8 Distributions of conversion degrees of sorption bed at different times

图9 不同相对湿度对吸附床温度的影响Fig.9 Effectsof different relative humidity on adsorption bed temperature
数值计算结果表明,对于参考条件而言,当释热阶段基本完成时(α=95%),储热单元的释热功率和释热阶段的热效率分别为97 W和81.2%。该水平的释热功率和热效率适用于长期储热-供热系统,同时说明该复合吸附材料搭载所设计的整体式储热系统具有很好的应用前景。
5结 论
本文以K2CO3水合盐和膨胀石墨(EG)分别作为化学蓄热材料和多孔基质,研制了用于中低温条件下热化学储热的复合吸附剂K2CO3@EG,并对其进行了储热性能测试和相关储热单元的数值研究。主要结论如下。
(1)相比于K2CO3纯盐,添加15%质量分数膨胀石墨的复合吸附剂K2CO3@EG具有更高的吸附动力性能。在较低的蒸汽压力下(1230 Pa)也能达到理论吸附平衡值,当蒸汽压力过高时,亦可有效避免过度吸附而造成的水合盐潮解渗漏等问题。
(2)复合吸附剂在105℃左右可基本完成脱附,相比于纯盐,脱附温度明显降低。其储热密度为505 kJ/kg。虽然比纯K2CO3水合盐的理论储热密度小,但其循环稳定性好,经过13次循环之后,其储热密度已超过纯盐的相应值,经历连续15次脱附-吸附循环测试后,储热密度降低幅度约为
10.9%。
(3)对于填充复合吸附剂的储热单元,在参考条件下,传热流体(空气)在较短时间内可实现25℃的温度提升,维持相对稳定一段时间后温度明显逐渐下降直至水合释热过程结束。
(4)增大入口流体的相对湿度或蒸汽分压可提高吸附床和流体的最高温度,但释热时间和较为稳定的产热时间段却明显降低。现实情况下可根据实际需求选择适当的释热条件,该数值研究可为工程应用或相关实验研究提供一定的借鉴或参考作用。另外,在基准条件下,该储热单元在释热阶段的热功率和热效率分别为97 W和81.2%。

