索拉菲尼治疗原发性肝癌的效果及对患者血清HSP90α、VEGF水平的影响
刘人杰


【摘要】 目的:探討索拉菲尼治疗原发性肝癌(PLC)的效果及对患者血清热休克蛋白90α(HSP90α)、血管内皮生长因子(VEGF)水平的影响。方法:选取2018年1-12月本院收治的不可手术切除的PLC患者63例为观察对象。按照治疗方式分为对照组(n=31)和观察组(n=32)。对照组采用肝动脉化疗栓塞术(TACE)治疗,观察组在TACE基础上口服索拉菲尼治疗。比较两组疗效、瘤体体积、血清HSP90α、VEGF、安全性、生存情况、总生存期。结果:两组ORR比较,差异无统计学意义(P>0.05);观察组DCR为81.25%,高于对照组的58.06%,差异有统计学意义(P<0.05)。随着治疗时间延长,两组瘤体体积均减小,差异均有统计学意义(P<0.05)。治疗4、12周后,观察组瘤体体积均小于对照组,差异均有统计学意义(P<0.05)。治疗12周后,两组血清HSP90α、VEGF水平均下降,且观察组均低于对照组,差异均有统计学意义(P<0.05)。两组胃肠道反应、骨髓抑制发生率比较,差异均无统计学意义(P>0.05);观察组高血压、皮肤黏膜反应发生率均高于对照组,差异均有统计学意义(P<0.05)。观察组1、2年生存率均高于对照组,总生存期较对照组延长,差异均有统计学意义(P<0.05)。结论:索拉菲尼治疗原发性肝癌能提高疾病控制效果,降低血清HSP90α、VEGF水平,减小病灶,减轻肿瘤负荷,提高生存率,延长生存期,但会增加高血压、皮肤黏膜反应,应密切观察,及时控制,确保治疗顺利进行。
【关键词】 索拉菲尼 原发性肝癌 HSP90α VEGF 安全性 生存期
Effect of Sorafenib in the Treatment of Primary Liver Cancer and Its Influence on Serum HSP90α and VEGF Levels/LIU Renjie. //Medical Innovation of China, 2021, 18(14): 0-019
[Abstract] Objective: To investigate the effect of Sorafenib in the treatment of primary liver cancer (PLC) and its influence on the serum levels of heat shock protein 90α (HSP90α) and vascular endothelial growth factor (VEGF). Method: A total of 63 unresectable PLC patients admitted to our hospital from January to December 2018 were selected as the observation objects. According to the treatment methods, they were divided into control group (n=31) and observation group (n=32). The control group was treated with hepatic arterial chemoembolization (TACE), and the observation group was treated with oral Sorafenib on the basis of TACE. The curative effect, tumor volume, serum HSP90α, VEGF, safety, survival, median survival and overall survival were compared between the two groups. Result: There was no significant difference in ORR between the two groups (P>0.05). The DCR of the observation group was 81.25%, higher than 58.06% of the control group, the difference was statistically significant (P<0.05). With the prolongation of treatment time, the tumor volume of both groups decreased, the differences were statistically significant (P<0.05). After 4 and 12 weeks of treatment, the tumor volume in the observation group were smaller than those in the control group, the differences were statistically significant (P<0.05). After 12 weeks of treatment, serum levels of HSP90α and VEGF were decreased in both groups, and the observation group were lower than those in the control group, the differences were statistically significant (P<0.05). There were no significant differences in the incidence of gastrointestinal reactions and bone marrow suppression between the two groups (P>0.05). The incidence of hypertension and skin mucosal reaction in the observation group was higher than that in the control group, the differences were statistically significant (P<0.05). 1 year and 2 years survival rates of the observation group were higher than those of the control group, overall survival time of the observation group was longer than that of the control group, the differences were statistically significant (P<0.05). Conclusion: Sorafenib treatment of primary liver cancer can improve the disease control effect, reduce serum HSP90α and VEGF levels, reduce the focus, reduce the tumor load, improve the survival rate, prolong the survival period, but will increase hypertension, skin mucosal reaction, should be closely observed, timely control, to ensure the smooth treatment.
[Key words] Sorafenib Primary liver cancer HSP90α VEGF Safety Survival time
First-authors address: Jiamusi Tuberculosis Hospital, Jiamusi 154007, China
doi:10.3969/j.issn.1674-4985.2021.14.004
原发性肝癌(PLC)为我国常见的恶性肿瘤之一,据报道2018年我国肝癌发病率(9.20%)、死亡率(12.90%)分别居恶性肿瘤的第4位、第3位[1]。由于PLC起病隐匿,不易发现,多数患者确诊时已发展为中晚期,错失了最佳手术治疗机会,手术切除效果差,难以达到根治的效果[2-3]。目前对不可手术的PLC患者,标准治疗方法是肝动脉化疗栓塞术(TACE),其通过使用栓塞剂封闭肿瘤的主要供血血管,抑制肿瘤生长,促进肿瘤坏死,达到治疗目的[4-5]。但经TACE治疗后的PLC患者预后仍欠佳,其中重要原因是TACE难以完全阻断肿瘤供血血管,而且栓塞后肿瘤局部发生缺血缺氧会刺激大量血管内皮生长因子(VEGF)产生,促进新生血管形成,继续向肿瘤供血,最终导致PLC患者的病情恶化[6-7]。索拉菲尼是一种肿瘤靶向治疗药物,本研究观察了索拉菲尼治疗PLC的效果及对患者血清热休克蛋白90α(HSP90α)、VEGF水平的影响,现报道如下。
1 资料与方法
1.1 一般资料 选取2018年1-12月本院收治的不可手术切除的PLC患者63例为观察对象。纳入标准:(1)符合《原发性肝癌诊疗规范(2017年版)》相关诊断标准[8],且经CT、MRI、临床病理确诊,经外科医师确认无法手术;(2)巴塞罗那分期B、C期;(3)Child-Pugh分级A、B级;(4)初诊患者,无相关治疗史;(5)至少存在一个可测量病灶;
(6)预计生存期>3个月。排除标准:(1)合并黄疸、难治性腹水、肝肾综合征者;(2)存在出血倾向、凝血功能障碍;(3)合并其他恶性肿瘤;(4)TACE治疗禁忌证;(5)门静脉主干完全栓塞、肿瘤远处转移;(6)孕期、哺乳期患者;(7)年龄>70岁。按照治疗方式分为对照组31例和观察组32例。患者均签署同意书,本研究已通过医学伦理委员会同意。
1.2 方法 (1)对照组采用TACE治疗:患者取仰卧位,常规行Seldinger技术穿刺股动脉,用肝管及微导管超选至肿瘤靶血管,造影确认导管位于靶血管。将50 mg洛铂(生产厂家:海南长安国际制药有限公司,批准文号:国药准字H20080359,规格:10 mg)+10~20 mL超液化碘化油制成混悬液,注入靶血管,注射量根据肿瘤大小调整。10 min后造影观察栓塞情况,若肿瘤仍有显影,注入明胶海绵颗粒补充栓塞直至靶血管完全闭塞。退出微导管,连接高压注射器造影,若肿瘤血管完全闭塞,退出导管及血管鞘。压迫止血15 min,加压包扎,下肢制动24 h。TACE治疗每4周1次,治疗12周。
(2)观察组在TACE基础上口服索拉菲尼治疗,TACE方法同对照组,TACE治疗第5天,给予甲苯磺酸索拉非尼片(生产厂家:江西山香药业有限公司,批准文号:国药准字H20203397,规格:0.2 g)0.4 g/次,2次/d,口服,治疗12周。
1.3 观察指标及判定标准
1.3.1 疗效评价 治疗12周后进行评价,完全缓解(CR):目标病灶完全消失;部分缓解(PR):目标病灶縮小≥30%,无新发病灶;疾病稳定(SD):目标病灶缩小<30%或扩大<20%,无新发病灶;疾病进展(PD):新病灶出现和/或原病灶扩大≥20%。客观有效率(ORR)=(CR例数+PR例数)/总例数×100%;疾病控制率(DCR)=(CR例数+PR例数+SD例数)/总例数×100%。
1.3.2 瘤体体积测定 治疗前及治疗4、12周后,分别使用CT增强扫描进行3D重建,测定瘤体体积,瘤体体积=(π×长径×短径×高/6)cm3。
1.3.3 血清学检测 治疗前及治疗4、12周后,采集外周静脉血5 mL,3 000 r/min离心10 min,取上清液待测。采用酶联免疫吸附法检测血清HSP90α、VEGF水平,HSP90α试剂盒购自上海博耀生物科技有限公司,VEGF试剂盒购自上海康朗生物科技有限公司。
1.3.4 安全性评价 观察两组胃肠道反应、骨髓抑制、高血压、皮肤黏膜反应发生情况。
1.3.5 随访情况 随访2年,观察患者1、2年生存率和总生存期。
1.4 统计学处理 采用SPSS 25.0软件对所得数据进行统计分析,计量资料用(x±s)表示,比较采用t检验,组内比较采用配对t检验,多组数据比较采用方差分析;计数资料以率(%)表示,两组间比较采用独立样本字2检验。以P<0.05为差异有统计学意义。
2 结果
2.1 两组基线资料比较 对照组男21例,女10例;年龄35~69岁,平均(57.98±5.63)岁;巴塞罗那分期:B期7例,C期24例;Child-Pugh分级:A级23例,B级8例。观察组男23例,女9例;年龄36~68岁,平均(57.12±5.19)岁;巴塞罗那分期:B期9例,C期23例;Child-Pugh分级:A级25例,B级7例。两组基线资料比较,差异均无统计学意义(P>0.05),具有可比性。
2.2 两组疗效比较 两组ORR比较,差异无统计学意义(字2=1.556,P=0.212);观察组DCR为81.25%,高于对照组的58.06%,差异有统计学意义(字2=4.019,P=0.045)。见表1。
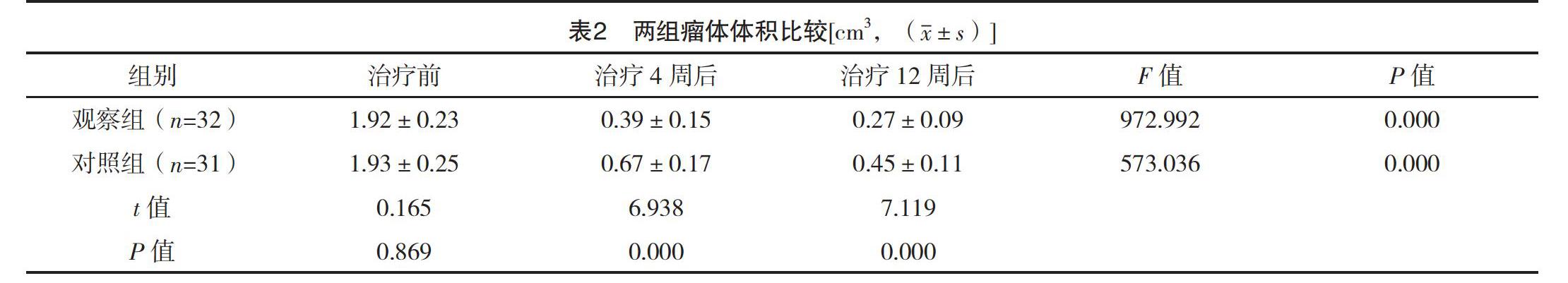
2.3 两组瘤体体积比较 随着治疗时间延长,两组瘤体体积均减小,差异均有统计学意义(P<0.05);治疗4、12周后,观察组瘤体体积均小于对照组,差异均有统计学意义(P<0.05)。见表2。
2.4 两组血清HSP90α、VEGF水平比较 治疗前,两组HSP90α、VEGF水平比较,差异均无统计学意义(P>0.05);治疗12周后,两组血清HSP90α、VEGF水平均下降,且观察组均低于对照组,差异均有统计学意义(P<0.05)。见表3。
2.5 两组安全性比较 两组胃肠道反应、骨髓抑制发生率比较,差异均无统计学意义(P>0.05);观察组高血压、皮肤黏膜反应发生率均高于对照组,差异均有统计学意义(P<0.05)。见表4。
2.6 两组随访情况比较 观察组1、2年生存率均高于对照组,总生存期较对照组延长,差异均有统计学意义(P<0.05),见表5。
3 讨论
PLC是一种高度血管依赖的恶性肿瘤,其生长、转移与血管生成密切相关。PLC瘤体内血管富集,易导致其在肝内扩散及血行转移[9]。肝癌瘤体的95%血液来源于肝叶动脉,采用TACE能够阻断肝动脉对肿瘤供血,使肿瘤组织发生变性坏死;输注化疗药物,并长时间维持肿瘤组织附近化疗药物呈高浓度,杀灭肿瘤细胞,进一步消除肿瘤病灶[10-11]。由于TACE栓塞不完全、需多次治疗、新生血管形成,增加PLC复发、转移的风险[12-13]。
索拉菲尼是一种针对VEGF及其受体的多激酶抑制剂,其可作用于受体酪氨酸激酶、丝氨酸/苏氨酸激酶,阻断该信号通路激活,抑制肿瘤细胞生长并促使其凋亡;还可抑制多种血管生成因子的释放,减少肿瘤新生血管形成,抑制肿瘤复发、转移[14-15]。本研究结果显示,治疗后近期疗效观察中,观察组疾病控制率(DCR)、瘤体体积均优于对照组,远期疗效观察中,观察组生存率及总生存期均优于对照组,差异均有统计学意义(P<0.05)。提示,索拉菲尼治疗PLC能进一步消减病灶,提高疾病控制效果,提高远期疗效,延长患者的生存期。这是由于索拉菲尼发挥抑制肿瘤细胞增殖、抑制肿瘤新生血管形成等作用,提高肿瘤病灶清除效果,进一步减小瘤体体积,提高疗效,延长患者的生存时间,改善预后。
HSP90α是一种高度保守的二聚体分子伴侣,几乎参与肿瘤所有进程,已成为肿瘤治疗一个新的靶点[16]。在肿瘤细胞内,HSP90α可使过度激活或突变的信号传导蛋白保持活性,加速肿瘤细胞的恶性转变;HSP90α被释放到细胞外后,能诱导基质金属蛋白酶成熟,促进肿瘤侵袭、转移[17]。相关研究显示,PLC患者的血清HSP90α水平较肝硬化患者、慢性肝炎患者明显升高[18],与肝癌侵袭转移潜能呈正相关。VEGF是一种血管生成诱导因子,其可激活一系列的信号通路,加速血管内皮、淋巴管内皮细胞的增殖,促进新生血管生成[19]。本研究结果显示,治疗12周后,两组血清HSP90α、VEGF水平均下降,且观察组均低于对照组,差异均有统计学意义(P<0.05)。表明索拉菲尼治疗能抑制PLC患者血清HSP90α、VEGF的表达水平。原因可能为索拉菲尼本身属于VEGF靶向药物,可阻断VEGF靶点相关信号通路,抑制肿瘤新生血管形成,从而抑制肿瘤组织生长,减少由肿瘤组织细胞对HSP90α的释放,降低血清HSP90α、VEGF水平,而这些物质的减少也利于延缓肿瘤的发展。本研究结果还显示,索拉菲尼治疗可引起高血压、皮肤黏膜反应,可能与索拉菲尼抑制VEGF、血小板衍生生长因子(PDGF)等有关[20]。这些不良反应经及时处理后均可控制,未影响后续治疗。
綜上所述,索拉菲尼治疗原发性肝癌能提高疾病控制效果,降低血清HSP90α、VEGF水平,减小病灶,减轻肿瘤负荷,提高生存率,延长生存期,但会增加高血压、皮肤黏膜反应,应密切观察,及时控制,确保治疗顺利进行。本研究存在样本量小、选择偏倚等不足,仍需大本量、多中心数据支持。
参考文献
[1]王宁,刘硕,杨雷,等.2018全球癌症统计报告解读[J/OL].肿瘤综合治疗电子杂志,2019,5(1):87-97.
[2]应倩,汪媛.肝癌流行现况和趋势分析[J].中国肿瘤,2020,29(3):185-191.
[3]张鹭,江建宁.原发性肝癌发病机制和治疗的最新进展[J].肝脏,2020,25(5):12-15.
[4]孙玉,张洪海,生守鹏,等.经肝动脉化疗栓塞术联合射频消融治疗巴塞罗那B期原发性肝癌的效果及预后影响因素分析[J].临床肝胆病杂志,2019,35(4):818-824.
[5]刘磊,韩文豪,陈涛,等.晚期肝癌患者血清转化生长因子β1在肝动脉化疗栓塞术前后变化及对预后的意义[J].中国普通外科杂志,2018,27(1):94-100.
[6] Melincovici C S,Boca A B,Uman S,et al.Vascular endothelial growth factor (VEGF) - key factor in normal and pathological angiogenesis[J].Rom J Morphol Embryol,2018,59(2):455-467.
[7]陈秀峰.经皮肝动脉化疗栓塞术后联合阿帕替尼或索拉非尼对原发性肝癌患者甲胎蛋白的影响[J].医学临床研究,2020,37(4):551-553,556.
[8]中华人民共和国卫生和计划生育委员会医政医管局.原发性肝癌诊疗规范(2017年版)[J].中华肝脏病杂志,2017,25(12):886-895.
[9]丛文铭,吴孟超.努力提高我国肝癌微血管侵犯的精细化诊断和个体化治疗水平[J].中华肝胆外科杂志,2019,25(10):721-724.
[10]金泓宇,袁驰,廖明恒,等.载药微球在肝细胞肝癌动脉化疗栓塞治疗中的研究进展[J].中国普外基础与临床杂志,2020,27(2):232-238.
[11]沈迪,张莉,金恩浩,等.甲胎蛋白对原发性肝癌患者TACE治疗效果及预后的评估价值[J].实用癌症杂志,2019,34(4):640-643.
[12]邓林,孙文杰,高知玲,等.中晚期原发性肝癌患者TACE术后早期复发危险因素[J].中国介入影像与治疗学,2020,17(2):65-69.
[13]张春宁,林华明,麦大海,等.肝動脉化疗栓塞术治疗中晚期原发性肝癌及预后相关因素分析[J].肝脏,2018,23(3):43-45.
[14]王健,李荣军,徐春霞,等.索拉菲尼联合TACE治疗中晚期原发性肝癌的疗效观察及对患者血清AFP、VEGF水平的影响[J].标记免疫分析与临床,2019,26(4):641-644,670.
[15] Wang C,Vegna S,Jin H,et al.Inducing and exploiting vulnerabilities for the treatment of liver cancer[J].Nature,2019,574(7777):268-272.
[16]汪梦楠,刘利霞,邓耀棠,等.热休克蛋白90对人肝癌细胞自噬相关转录因子EB的调控机制[J].生理学报,2020,72(2):157-166.
[17]龙婧,李倩,郑琪,等.热休克蛋白90α在肿瘤中的研究进展[J].中国临床研究,2019,32(3):421-423.
[18]任玲君,余国庆,方丽娟.热休克蛋白90α甲胎蛋白和磷脂酰肌醇蛋白聚糖3联合检测在原发性肝癌诊断中的应用[J].浙江临床医学,2020,22(6):874-876.
[19]杨锦锋,曾荣耀.血管内皮生长因子和缺氧诱导因子-1α的表达与原发性肝癌患者临床病理特征及预后的关系[J].中国慢性病预防与控制,2020,28(12):48-51.
[20]陈雪雯,严军华,张希琳,等.索拉菲尼致手足皮肤毒性反应1例[J].临床皮肤科杂志,2019,48(12):47-48.
(收稿日期:2021-03-18) (本文编辑:姬思雨)

