小于2 cm单发性肾结石3种手术方法比较
朱瑞龙 蔡超 吴荣海 徐炜 邓硕 陈伟文
江门市中心医院泌尿外科,广东 529000
相关指南推荐,对小于2 cm的单发性肾结石,体外冲击波碎石(extracorporeal shockwave lithotripsy,ESWL)和输尿管软镜碎石术(retrograde intrarenal surgery,RIRS)为首选治疗方法。然而,ESWL治疗效果因结石大小、硬度、位置和肾盂肾盏解剖结构等因素影响而异[1-2];RIRS一期手术成功率受输尿管软条件影响,对肾下盏结石效果较差,且其器械成本较高,学习曲线较长,不易推广[3]。近年来,超微通道经皮肾镜和4.8F可视穿刺经皮肾镜的出现[4-6],使小于2 cm的单发性肾结石的治疗有了更多的选择。本研究回顾性分析本院自2018年1月至2019年12月收治的123例1~2 cm单发性肾结石患者资料,分组分别行超微通道经皮肾镜碎石术、输尿管软镜碎石术和4.8F可视穿刺经皮肾镜碎石术,治疗效果满意,现总结如下。
1 资料与方法
1.1 一般资料 回顾性分析2018年1月至2019年12月于本院就诊的1~2 cm的单发性肾结石患者的临床资料。纳入标准:年龄在18~85岁,男女均可;经CT检查确定为单发性肾结石,最大直径为1~2 cm;患者明白并自愿参与研究过程;排除手术禁忌证。共选取符合上述纳入标准的患者123例,分为超微通道经皮肾镜组、输尿管软镜组和4.8F可视肾镜组。超微通道经皮肾镜组40例,男24例,女16例,年龄(53.7±9.8)岁,结石直径(1.7±0.2)cm,CT值(1 099.8±297.8)Hu;输尿管软镜组42例,男24例,女18例,年龄(53.3±11.7)岁,结石直径(1.6±0.3)cm,CT值(999.2±388.4)Hu;可视肾镜组41例,男20例,女21例,年龄(55.8±11.3)岁,结石直径(1.6±0.4)cm,CT值(1 001.7±345.3)Hu。3组患者术前临床资料差异均无统计学意义(均P>0.05)(表1)。所有患者术前行血常规、尿常规、肝肾功能、电解质、凝血功能、中段尿培养等检验,计算机体层摄影尿路造影明确结石位置及大小、CT值、肾积水情况。术前应用敏感或广谱抗生素治疗至少1 d。

表1 3组单发性肾结石患者的一般临床资料比较
1.2 手术方法 超微通道经皮肾镜组:患者取截石位,患侧输尿管镜下逆行留置F5输尿管导管,留置尿管。改俯卧位,B超引导下穿刺目标肾盏,置入斑马导丝,用筋膜扩张器将通道扩张至F12或F14,置入“卜”形鞘并连接负压吸引,置入小儿输尿管镜(F4.5/6.5),以钬激光碎石,将结石碎片化,经“卜”形鞘吸引至结石收集瓶,选择性留置双J管(不确定结石碎片已完全清除或有明显出血者),不留置肾造瘘管。输尿管软镜组:患者取截石位,输尿管硬镜(F8/9.8)进入患侧输尿管,置入超滑导丝,沿导丝置入F12/14软镜外鞘至肾盂,沿外鞘直视下置入一体化电子输尿管软镜,采用人工注水方法保持视野清晰,以钬激光碎石,将结石粉末化,术后留置双J管及尿管。4.8F可视肾镜组:患者取截石位,患侧输尿管留置F5输尿管导管,留置尿管。改俯卧位,以结石所在的肾盏穹窿部为穿刺目标,超声引导,用4.8F可视穿刺针进行全程直视下穿刺进入目标肾盏,见到结石后,连接可视肾镜系统,以钬激光将结石粉末化并未冲至肾盂,不留置双J管及肾造瘘管。所有手术主刀为副主任医师以上并具有多年相关手术临床经验的医师执行。
1.3 观察指标 统计手术时间(超微通道经皮肾镜组从穿刺到缝合皮肤的时间,输尿管软镜组从输尿管硬镜进入至成功留置尿管的时间,可视肾镜组从穿刺到拔出穿刺针的时间)、术中出血量(术后2 h查血常规对比术前Hb的下降值)、术后住院时间、术后2 d复查CT,术后1个月复查KUB,参照≤4 mm定义为无临床意义的残余结石,判断近期和远期结石清除率,观察术后24 h生命体征,术后2 h复查血白细胞计数、降钙素原等炎性指标,出现以下任意两项认为出现全身炎症反应综合征(systemic inflammatory response syndrome,SIRS):(1)体温>38℃或<36℃;(2)脉搏>90次/min;(3)呼吸>20次/min或动脉血二氧化碳分压(PaCO2)<32 mmHg(4.3 kPa,1 mmHg=0.133 kPa);(4)白细胞计数(WBC)>12×109/L或WBC<3×109/L或未成熟白细胞≥10%。
1.4 统计学方法 所有数据均采用SPSS19.0软件进行统计学分析。符合正态分布的计量资料以(±s)表示,比较采用单方向方差分析;偏态分布计量资料以M(P25,P75)表示,采用秩和检验(Mann-WhitneyU检验);计数资料用率表示,比较采用χ2检验。P<0.05为差异有统计学意义。
2 结 果
所有患者手术顺利完成,均无输血,未发生石街、迟发出血、脏器损伤、尿源性脓毒血症等严重并发症。3组间术中术后效果、术后结石清除率与炎性指标发生率比较见表2~3。手术时间输尿管软镜组最长,超微通道经皮肾镜组与可视肾镜组差异无统计学意义;术后Hb下降值超微通道经皮肾镜组最大,输尿管软镜组与可视肾镜组差异无统计学意义;术后住院时间输尿管软镜组最长,超微通道经皮肾镜组与4.8F可视肾镜组差异无统计学意义;术后第2天结石清除率超微通道经皮肾镜组最高,输尿管软镜组与可视肾镜组差异无统计学意义;术后1个月结石清除率超微通道经皮肾镜组和可视肾镜组最高,组间差异无统计学意义,输尿管软镜组最低;术后高热、WBC与PCT等炎性指标异常的发生率均以超微通道经皮肾镜组最低。
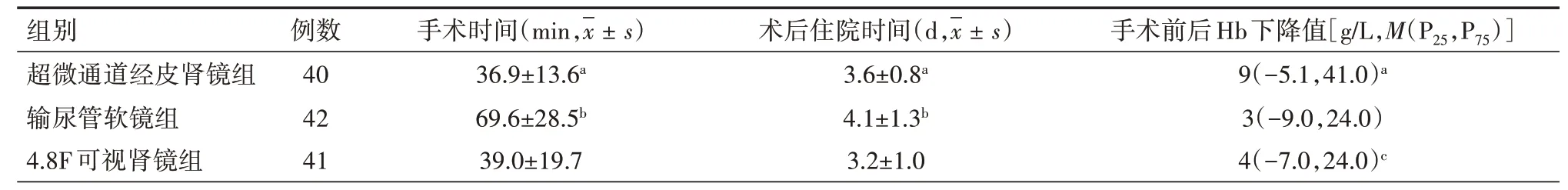
表2 3组单发性肾结石患者术中、术后效果比较
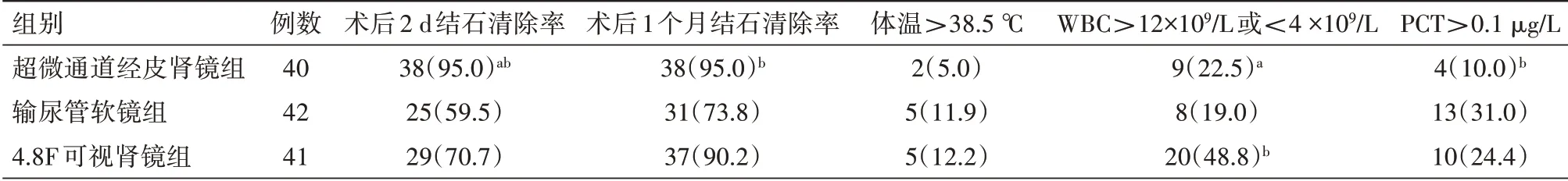
表3 3组单发性肾结石患者术后结石清除率与炎性指标发生率比较[例(%)]
3 讨 论
美国泌尿外科学会(AUA)和欧洲泌尿外科学会(EAU)指南推荐,对于小于2 cm的单发性肾结石,ESWL和输尿管软镜为首选治疗方法,经皮肾镜碎石取石术(percutaneous nephrolithotomy,PCNL)虽然结石清除率高,但并发症发生率相对较高,仅作为小于2 cm肾结石的二线治疗方法。然而最近10年,人们的微创观念日益增强,各种新型微创技术的诞生,使小于2 cm单发性肾结石的治疗有了新的选择。如何以更小的创伤,更低的并发症发生率,取得更高的结石清除率成为了学者们不断进取的方向。本院应用超微通道经皮肾镜碎石术、输尿管软镜碎石术和4.8F可视穿刺经皮肾镜碎石术分别治疗小于2 cm的单发性肾结石,治疗效果满意,均能达到微创目的,远期结石清除率分别达到95.0%、73.8%和90.2%,无输血病例,未发生石街、迟发出血、脏器损伤、尿源性脓毒血症等严重并发症。
超微通道经皮肾镜碎石术最早由我国曾国华等[4]在2013年提出,以10~12F带吸引功能的“卜”型鞘作为通道,利用外径为7F的超细肾镜碎石,并借助负压吸引器将碎石屑吸出。该术式最大的特点在于其通道仅为12~14F,相较于传统PCNL,减少通道横截面,能有效降低术中及术后出血的发生率[7];同时,“卜”型鞘连接负压吸引,主动清除结石碎片,维持术中肾盂内低压,保持术野清晰,缩短手术时间,提高结石清除率,降低尿源性脓毒血症的发生率。此外,该术式可实现完全“无管化”,即不留置双“J”管和肾造瘘管,缩短术后住院时间,减轻管道对患者带来的不适与经济负担。术中确认无结石残留、灌注水比较清亮、仔细检查肾盏肾盂无撕裂、穿刺通道无动脉性喷血、术前感染指标无明显升高、无合并UPJ狭窄或输尿管中下段梗阻的患者,可实施“无管化”。本组患者近期和远期结石清除率均最高,所有病例均未输血,未出现迟发性出血病例,发热、WBC升高以及PCT等炎性指标异常的发生率均为最低。然而,10~12F的通道虽小,但毕竟存在体表伤口,虽未出现大出血病例,但相对另外两种术式仍有较多的出血,成为了此术式的美中不足,分析原因可能与相对较大的通道对肾脏形成的创伤和实施无管化时肾脏伤口失去压迫止血有关。
输尿管软镜碎石术经自然通道入路,微创与低出血风险是其最大的优点,尤其是在一些孤立肾、肥胖、凝血功能障碍等特殊患者治疗方面有一定的优势[8-9]。然而,输尿管软镜的成功率以及结石清除率受肾脏解剖结构影响,漏斗角度陡峭(<45°)、漏斗宽度较小(<5 mm)、IW漏斗长度较长(>10 mm)的患者,会明显增加输尿管软镜的难度[10]。虽然软镜裸镜状态下可以进入大部分肾盏,但置入钬激光之后,其末端的弯曲度会变小,导致手术视野不完全,影响了碎石效率与结石清除率。此外,术后感染也是输尿管软镜容易发生的并发症,术前存在明显的尿路感染、手术时间过长、术中冲洗液流量过多和压力过大,均为术后感染的危险因素[11]。本组患者术中出血量最低,创伤最小,但近期和远期结石清除率均不及超微通道经皮肾镜碎石术组,且体温、WBC、PCT等炎性指标异常发生率为最高,虽未发生严重的尿源性脓毒血症,但相比于超微通道PCNL,输尿管软镜仍然存在较高的术后感染风险。
4.8F可视穿刺经皮肾镜碎石术最早由美国Desai等[6]在2011年提出,在全程可视化穿刺后,不行通道扩张,仅使用F4.85外鞘完成碎石,由于操作通道仅有F4.85,体表伤口和对肾实质的损伤微乎其微,使其在微创性方面可以与输尿管软镜相媲美。该系统主要优势在于穿刺全程可视,可避免损伤血管及周围重要脏器,防止穿刺过深;穿刺无死角,不受漏斗角度、漏斗宽度、IW漏斗长度以及输尿管条件影响,对于不适合ESWL与输尿管软镜治疗的患者仍能提供治疗方法[12],也能为传统PCNL无法处理的平行盏展提供辅助治疗[13]。然而,受制于通道大小,该系统不能自主清除结石,也不能保持良好的灌注水循环,容易导致肾盂内压力过高容易增加尿源性脓毒血症的风险。本组患者术中出血量最低,与输尿管软镜组比较差异无统计学意义,近期结石清除率不及超微通道经皮肾镜碎石术组,但得益于术中主动把结石粉末冲至肾盂,并且不留置双J管,增加了术后排石的机会,使得其远期结石清除率与超微通道经皮肾镜碎石术组相当。然而,本组体温、WBC、PCT等炎性指标异常发生率为最高,虽未发生严重的尿源性脓毒血症,但仍然存在较高的术后感染风险。
综上所述,超微通道经皮肾镜有更高的结石清除率和更低的感染风险;输尿管软镜和4.8F可视穿刺经皮肾镜则有更少的出血和更低的创伤;4.8F可视穿刺经皮肾镜在穿刺过程中有优势,不受肾脏与输尿管条件影响,3种方法均疗效良好、安全,值得临床推广。
——可重复性或一次性输尿管软镜孰优孰劣?

