人参二醇对APP-SH-SY5Y细胞中Tau蛋白磷酸化及Fyn/GluN2B信号通路的影响
梁喜才 蔺莹 肖洪贺 孔亮 杨静娴


摘要目的:研究人參二醇(PD)对转染APP基因的人神经母细胞瘤细胞SH-SY5Y(APP-SH-SY5Y)中Tau 蛋白磷酸化的影响及其作用机制。方法:采用分子对接技术验证PD 与非受体酪氨酸激酶Fyn 的靶向性。在体外培养SH-SY5Y 细胞,构建APP-SH-SY5Y细胞模型和绿色荧光蛋白(GFP)-SH-SY5Y细胞模型(对照细胞),通过检测细胞中β淀粉样蛋白(Aβ1-42)的表达来验证APP-SH-SY5Y细胞模型是否构建成功。以GFP-SH-SY5Y细胞为对照,采用CCK-8 法检测5、10、20、30、40 μmol/L 的PD 和125、250、500、1 000、2 000 nmol/L 的PP2(Fyn 抑制剂,阳性对照)作用24 h 对APP-SH-SY5Y细胞存活率的影响,以确定最佳给药浓度。以APP-SH-SY5Y细胞为对象,分别检测最佳浓度PD、PP2 作用24 后细胞中Ca2+浓度及磷酸化Tau 蛋白(p-Tau)/Tau、磷酸化非受体酪氨酸激酶Src(p-Src)/Fyn、磷酸化谷氨酸受体2B(p-GluN2B)/GluN2B比值。结果:分子模拟对接结果显示,PD可靶向结合Fyn 蛋白。与GFP-SH-SY5Y细胞比较,APP-SH-SY5Y细胞中Aβ1-42蛋白表达水平显著升高(P<0.01)。PD和PP2 的最佳作用浓度分别为20 μmol/L和500 nmol/L。20 μmol/L PD、500 nmol/L PP2 均可显著升高细胞的存活率,显著降低细胞中Ca2+浓度以及p-Tau/Tau、p-Src/Fyn、p-GluN2B/GluN2B比值。结论:PD可通过抑制Fyn/GluN2B信号通路来降低APP-SH-SY5Y细胞中Ca2+浓度及Tau蛋白的磷酸化水平。
关键词人参二醇;转染APP基因的人神经母细胞瘤细胞SH-SY5Y;Tau 蛋白;磷酸化;非受体酪氨酸激酶Fyn/谷氨酸受体2B信号通路
ABSTRACT OBJECTIVE:To study the effects and mechanism of panaxadiol(PD) on Tau protein phosphorylation in theSH-SY5Y cells transfected with APP gene(APP-SH-SY5Y). METHODS:The target of PD and non-receptor tyrosine kinases Fynwas verified by molecular docking. SH-SY5Y cells were cultured in vitro,and the APP-SH-SY5Y cell models and green fluorescent(GFP)-SH-SY5Y cell model(control cell)was constructed. The expression of Aβ 1-42 was detected so as to verify the success ofAPP-SH-SY5Y cell model. Taking GFP-SH-SY5Y cells as control,the effects of 5,10,20,30,40 μmol/L PD and 125,250,500,1 000,2 000 nmol/L PP2(Fyn inhibitor,positive control)on the survival rate of APP-SH-SY5Y cells were detected byCCK-8 assay after treated for 24 h, so as to confirm the optimal concentration. The concentration of Ca2 + , the ratiofophosphorylated Tau protein(p-Tau)/Tau,phosphorylatedn Src(p-Src)/Fyn and phosphorylated glutamate receptor2B(p-GluN2B)/GluN2B were detected in APP-SH-SY5Y cells after trated with the optimal concentration of PD and PP2 for 24 h. RESULTS:Theresults of molecular simulation docking showed that PD could target Fyn protein. Compared with GFP-SH-SY5Y cells,the proteinexpression of Aβ1-42 in APP-SH-SY5Y cell were increased significantly(P<0.01). The optimal concentration of PD and PP2 were20 μmol/L and 500 nmol/L. The 20 μmol/L PD and 500 nmol/L PP2 could increase the survival rate of the cells and reduced theconcentration of Ca2 + ,the ratio of p-Tau/Tau,p-Src/Fyn,and p-GluN2B/GluN2B. CONCLUSIONS:PD can reduce the thephosphorylation of Tau protein through inhibiting Fyn/GluN2B signaling pathway.
KEYWORDS Panaxadiol;APP-SH-SY5Y cells;Tau protein;Phosphorylation;Fyn/GluN2B signaling pathway
阿尔茨海默病(Alzheimers disease,AD)是一种进行性的神经退行性疾病,患者通常会出现以记忆力衰退、学习能力减弱为主的症状,并伴有情绪调节障碍以及运动能力丧失[1]。目前主流观点认为,AD的病因与β淀粉样蛋白(β-amyloid protein,Aβ)和Tau 蛋白过度磷酸化造成的神经元大量死亡而导致的认知缺陷有关[2]。其中,Tau 蛋白的过度磷酸化是由Aβ神经毒性引起的病理生理级联反应,而磷酸化的Tau 蛋白同样影响着Aβ的沉积,进一步协同产生神经毒性,形成恶性循环,最终导致神经系统衰竭、神经变性和认知能力下降[3-4]。已有研究证实,Aβ可通过激活非受体酪氨酸激酶Fyn 并开放谷氨酸受体2B(GluN2B)通道,引起Ca2+大量内流,进一步诱导Tau 蛋白的过度磷酸化[5-8]。可见,Fyn/GluN2B信号通路可通过调控Tau 蛋白的磷酸化而影响AD的发生与发展。
人参二醇(panaxadiol,PD)是从人参Panax ginsengC. A. Mey.中提取得到的一种三萜皂苷类单体化合物,是人参的三大苷元之一,在人参总皂苷水解物中的含量高达8.75%[9]。PD 具有多种药理作用,包括抗癌、抗缺氧损伤、抗自由基等[10-13]。同时,PD对Aβ损伤的神经元具有保护作用[14-15]。APP基因是较早被发现的AD患者脑内的突变基因之一,表达APP基因的细胞系能够分泌高水平的Aβ,该细胞系已被广泛用于AD的研究[16]。本课题组前期成功构建了APP 基因转染的人神經母细胞瘤细胞SH-SY5Y(APP-SH-SY5Y 细胞)来模拟Aβ沉积致AD发病的细胞模型,并发现PD对该细胞具有神经保护作用,但其保护机制尚不明确。鉴于此,本研究拟考察PD 对APP-SH-SY5Y 细胞中Tau 蛋白磷酸化及Fyn/GLuN2B信号通路的影响,以期为PD防治AD提供新的理论依据。
1 材料
1.1 主要仪器
Ti-S 型荧光显微镜购自日本Nikon 公司;TGL-20M型台式高速冷冻离心机购自湖南湘仪实验室仪器公司;NU-4750E型CO2培养箱购自美国Nuaire 公司;MR-96A型酶标仪购自美国Molecular Devices 公司;UV-5600 型紫外-可见光分光光度计购自上海元析仪器有限公司;Tanon-5200 型自动化学发光图像分析仪购自上海天能科技有限公司。
1.2 主要药品与试剂
PD 对照品(批号19666-76-3,纯度98.36%)购自成都普菲德生物技术有限公司;Fyn 抑制剂PP2 对照品(阳性对照,批号172889-27-99,纯度>98%)购自美国MedchemExpress 公司;DMEM 高糖培养基、胎牛血清(FBS)、胰蛋白酶消化液和青霉素/链霉素(P/S)双抗均购自美国Gibco 公司;绿色荧光蛋白(GFP)-APP 质粒、GFP质粒以及pLP1 质粒、pLP2 质粒、pLP/VSV-G质粒均由本课题组前期自行构建;脂质体-2000 转染试剂、聚凝胺转染增强剂均购自美国Invitrogen 公司;全蛋白提取试剂盒(批号KGP250)、BCA 法蛋白定量检测试剂盒(批号KGP902)、CCK-8 法细胞增殖检测试剂盒(批号KGA317)均购自江苏凯基生物技术股份有限公司;CalbryteTM520 AM试剂盒(批号21131)购自美国AAT Bioquest公司;兔抗鼠、Fyn 多克隆抗体购自沈阳万类生物科技有限公司;兔抗鼠磷酸化Src(p-Src)多克隆抗体购自美国RD 公司;兔抗鼠A β 1-42 GluN2B、磷酸化(p-GluN2B)、Tau、磷酸化Tau(p-Tau)多克隆抗体均购自北京博奥森生物技术有限公司;兔抗鼠β-肌动蛋白(β-actin)多克隆抗体购自美国Abcam 公司;辣根过氧化物酶(HRP)标记的羊抗兔免疫球蛋白G(IgG)二抗购自武汉ABclonal 公司;荧光素Cy3 标记的驴抗兔IgG 二抗购自美国Jackson 公司;其余试剂均为分析纯或实验室常用规格,水为去离子水。
1.3 细胞
人神经母细胞瘤细胞SH-SY5Y、人源胚胎肾细胞293T(human emborynic kidney 293T,HEK 293T)均由首都医科大学提供。
2 方法
2.1 PD与Fyn蛋白的分子模拟对接
以“panaxadiol”为关键词,在中药系统药理学分析平台数据库(TCMSP,https://tcmspw.com)中检索得到PD 的二维结构,保存为“mol2”格式文件;以“Fyn”为关键词,通过PDB数据库(https://www.rcsb.org/)检索并下载Fyn 的蛋白结构,保存为“mol2”格式文件。将两者的“mol2”格式文件分别导入AutoDockTools-1.5.6 软件中,调整X、Y、Z 坐标轴并用Autodock vina 1.1.2 软件进行模拟对接。对接完成后,用Discovery Studio 2017 软件显示对接后的作用力,并以对接评分来评估结合亲和力。若评分<-4.0,则认为化合物与靶点蛋白具有较强的亲和力[17]。以Fyn 抑制剂PP2 为阳性对照,同法进行PP2与Fyn蛋白的分子模拟对接。
2.2 APP-SH-SY5Y细胞模型的构建
将GFP(或GFP-APP)质粒15 μg、pLP1 质粒6.5 μg、pLP2 质粒2.5 μg、pLP/VSV-G 质粒3.5 μg 与DMEM 高糖培养基250 μL 混合均匀,在室温下孵育5 min。用脂质体-2000 介导转染HEK 293T 包装细胞,分别于转染24、48、72 h 时收集上述HEK 293T 细胞培养液的上清液。将上述上清液混合后,以3 000 r/min 离心20 min 去除细胞碎片,然后以0.22 μm滤膜过滤,滤液用100 kDa超滤管以5 000 r/min 离心1 h,得到浓缩液。再将SH-SY5Y细胞以1×106个/孔接种于6 孔板中,待细胞生长至密度为70%时,弃去培养液;加入0.5 mL上述浓缩液、0.5 mL不完全培养基(不含P/S 和FBS 的DMEM高糖培养基)和聚凝胺转染增强剂(10 μg/mL)适量后,置于37 ℃、5%CO2培养箱(下同)中常规培养12 h,然后换成完全培养基(含P/S 和FBS 的DMEM高糖培养基)继续培养;培养至第3 天时,将培养基换为含有嘌呤霉素(4 μg/mL)的完全培养基继续培养,每2 天换液1 次,培养1周后用于实验。
2.3 APP-SH-SY5Y细胞模型构建情况的验证
采用Western blot 法进行检测。取第2 代APP-SHSY5Y细胞和GFP-SH-SY5Y细胞,分别以1×106个/孔接种至6 孔板中,分别作为APP组和GFP组(对照组)。常规培养12 h 后,根据全蛋白提取试剂盒说明书方法提取细胞中总蛋白,采用BCA法对蛋白进行定量后,在沸水浴中煮沸5 min 进行变性。取变性后蛋白(20 μg)进行10%十二烷基硫酸钠-聚丙烯酰胺凝胶电泳(恒压80 V,电泳时间2.5 h),然后转移到聚偏二氟乙烯膜上(电压80 V 转印0.5 h)。用5%脱脂奶粉封膜1 h,加入Aβ1-42(稀释比例为1 ∶ 400)、β-actin(稀释比例为1 ∶ 2 000)一抗,4 ℃孵育过夜;TBST 缓冲液洗膜5 min×4 次,加入HRP 标记的IgG 二抗(稀释比例为1 ∶800),室温孵育1h。ECL显色后,用全自动化学发光图像分析仪拍照,保存。以β-actin 为内参,采用Image J 1.51 软件检测条带灰度值,以目标蛋白与内参蛋白条带灰度值的比值表示目标蛋白的相对表达水平。实验重复3 次。
2.4 PD和PP2 给药浓度的考察
采用CCK-8 法检测细胞存活率,以确定PD 和PP2的最佳给药浓度。将APP-SH-SY5Y细胞以1×104个/孔接种到96 孔板中(含完全培养基,下同),然后将其分为不同浓度的PD(5、10、20、30、40 μmol/L,浓度依据前期预实验结果设置)组(记为“APP+PD组”)和不同浓度的Fyn 抑制剂PP2(125、250、500、1 000、2 000 nmol/L,浓度依据前期预实验结果设置)组(记为“APP+PP2 组”),每组均设置3 个复孔;同时,另设加入GFP-SH-SY5Y细胞的对照组(记为“GFP 组”)和空白组。经相应培养基培养24 h 后,向每孔中加入CCK-8 溶液10 μL,常规孵育2h。然后,使用酶标仪在450 nm波长下检测各孔的吸光度(A),并计算细胞存活率:细胞存活率(%)=(A实验孔-A空白孔)/(A对照孔-A空白孔)×100%。实验重复3次。
2.5 细胞中Ca2+浓度的检测
采用CalbryteTM 520 AM 探针法进行检测。将APP-SH-SY5Y 细胞分别以1×104 个/孔接种到96 孔板中,然后将其分为GFP 组、APP 组、APP+PD组(PD浓度为20 μmol/L)和APP +PP2 组(PP2 浓度为500 nmol/L),每组设置3 个复孔。分别处理24 h 后,根据CalbryteTM520 AM 试剂盒说明书方法操作,使用荧光显微镜在610~640 nm波长范围内扫描各孔的荧光情况并检测其荧光强度,以此反映Ca2+浓度[18]。实验重复3次。
2.6 细胞中Fyn、GluN2B、Tau蛋白磷酸化水平的检测
采用免疫细胞化学法进行检测。将APP-SH-SY5Y细胞分别以1×104个/孔接种到96 孔板中,按“2.5”项下方法进行分组、处理24 h 后,向各孔中分别加入4%多聚甲醛溶液50 μL,在4 ℃条件下固定30 min。细胞用磷酸盐缓冲液(PBS)洗涤3 次,然后用0.1%Triton X-100 试剂在室温下透化5 min;再用PBS 洗涤3 次,然后分别加入相应一抗(Fyn 稀释比例为1 ∶ 500,p-Src 稀释比例为1 ∶800,GluN2B、p-GluN2B 稀釋比例均为1 ∶1 000,Tau、p-Tau 稀释比例均为1 ∶400)50 μL,4 ℃孵育过夜;吸弃培养液,用PBS 洗涤细胞3 次,再加入荧光素Cy3 标记的IgG 二抗(稀释比例为1 ∶200,室温下孵育1 h;加入4′,6-二脒基-2-苯基吲哚(DAPI)试剂,室温避光孵育15 min,用PBS 洗涤3 次。使用荧光显微镜拍摄照片,然后用Image J 1.51 软件测定细胞的荧光强度,以磷酸化蛋白和总蛋白荧光强度的比值表示该蛋白的磷酸化水平。实验重复3 次。
2.7 统计学方法
使用GraphPad Prism 5 软件对数据进行统计分析。实验结果以x±s 表示,两组间比较采用t 检验;多组间比较采用单因素方差分析,组间两两比较采用LSD检验。P<0.05 表示差异具有统计学意义。
3 结果
3.1 PD与Fyn蛋白的分子模拟对接结果子对接结果显示,PD、PP2 与Fyn 蛋白的氨基酸残基均可以形成较强的氢键(PD 的对接评分=-9.5;PP2 的对接评分=-9.1),两者具有很好的空间及电性互补特征,易于形成稳定的结合构象。该结果表明,PD与Fyn 蛋白具有强相互作用,脱靶可能性较小,可为后续实验验证提供理论依据。PD、PP2 与Fyn 蛋白的分子对接2D图见图1。
3.2 APP-SH-SY5Y细胞模型的建立情况分析结果与GFP组(0.21±0.11)比较,APP组细胞中Aβ1-42蛋白的表达水平(0.82±0.08)显著升高(P<0.01),表明APP-SH-SY5Y细胞模型构建成功。GFP组和APP组细胞的荧光显微图见图2(图中,白光表示白光镜下图,荧光表示GFP荧光图,合并表示两者的合并图),Aβ1-42蛋白表达的电泳图见图3。
3.3 PD和PP2 给药浓度的筛选结果与GFP组比较,APP组细胞的存活率显著降低(P<0.01)。与APP 组比较,各给药组细胞的存活率均显著升高(P<0.05 或P<0.01);且组间比较发现,当PD浓度达到20 μmol/L、PP2 浓度达到500 nmol/L 时,再增加药物浓度后细胞的存活率均无显著变化(P>0.05),因此以20 μmol/L PD和500 nmol/L PP2 进行后续实验。各组细胞存活率的检测结果见表1。
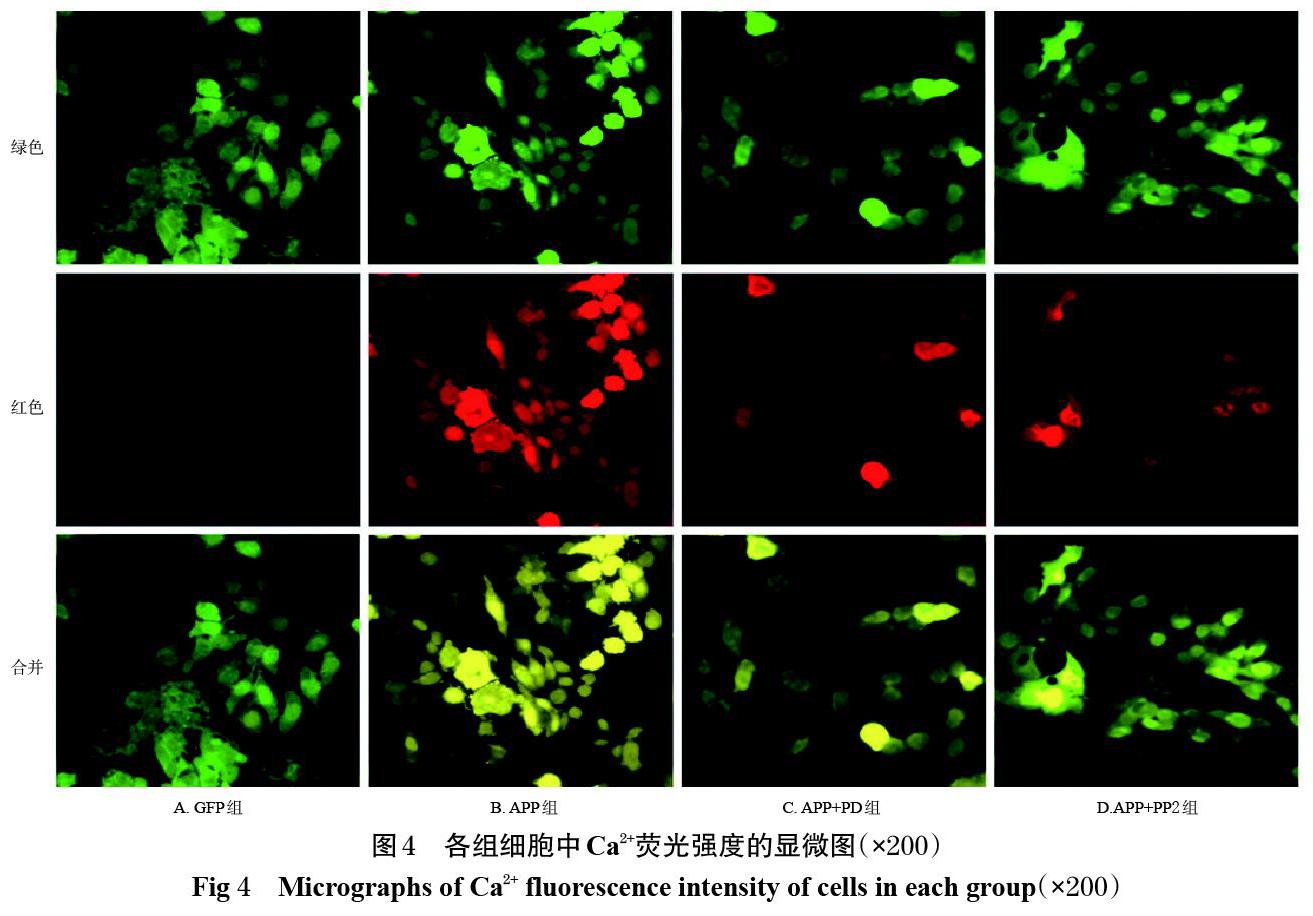
3.4 各组细胞中Ca2+浓度的检测结果与GFP组比较,APP组细胞中Ca2+的浓度显著增强(P<0.01);与APP组比较,APP+PD、APP+PP2 组细胞中Ca2+的浓度均显著减弱(P<0.01)。各组细胞中Ca2+浓度的检测结果见表2、其显微图见图4(图中,绿色表示GFP荧光;红色表示CalbryteTM 520荧光;合并为两者合成图)。
3.5 各组细胞中Tau蛋白磷酸化水平的检测结果与GFP 组比较,APP 组细胞中p-Tau/Tau 比值显著升高(P<0.01);与APP组比较,APP+PD、APP+PP2 组细胞中p-Tau/Tau 比值均显著降低(P<0.05)。各组细胞中Tau 蛋白磷酸化水平的检测结果见表3,其荧光显微图见图5。
3.6 各组细胞中Fyn/GluN2B 信号通路相关蛋白磷酸化水平的检测结果与GFP组比较,APP组细胞中p-Src/Fyn、p-GluN2B/GluN2B 比值均显著升高(P<0.01);与APP 组比较,APP+PD、APP+PP2 组细胞中上述指标比值均显著降低(P<0.05)。各组细胞中Fyn/GluN2B 信号通路相关蛋白磷酸化水平的检测结果见表3,其荧光显微图见图6。
4 讨论
据2019 年的一项研究指出,我国约有1 450 万AD患者,随着人口老龄化的加剧,AD的患病率也将不断上升,预计到2050 年,我国AD患者将超过3 000 万[19]。AD病因复杂,学术界至今仍未完全阐明其发病的具体机制。有研究认为,Tau 蛋白的过度磷酸化是AD病机之一,p-Tau 蛋白的积累会造成神经元的死亡并导致记忆丧失[2]。然而,Tau 病理学的发展是一个复杂的多因素过程,减少AD患者脑中Tau 蛋白磷酸化的机制仍有待进一步深入研究。有研究表明,Tau 蛋白的磷酸化与Fyn活性有关,Fyn 的激活可促进APP 转基因小鼠脑中Tau蛋白的磷酸化,而抑制Fyn 活性则可减少其Tau 蛋白的磷酸化[20]。这提示,抑制Fyn 活性可缓解AD 的病理进展。
本研究先通过分子模拟对接发现,PD与Fyn 蛋白具有强烈的亲和力,提示PD 可靶向抑制Fyn 蛋白活性。接着,本研究构建了APP-SH-SY5Y细胞模型来验证PD能否通过抑制Fyn 活性从而发挥对AD的改善作用。该细胞模型可以模拟AD患者脑内Aβ对神经系统的损害,包括降低细胞存活率、促进乳酸脱氢酶释放、诱导细胞凋亡等[21-22]。本研究结果表明,经PD干预后,APP-SHSY5Y细胞的存活率显著升高;同时,笔者还观察到APP-SH-SY5Y细胞中Ca2+浓度显著增加,这可进一步引起Tau 蛋白的磷酸化[5-8],而PD和Fyn抑制剂PP2 均可降低APP-SH-SY5Y细胞中Ca2+浓度及Tau 蛋白的磷酸化水平。
为了阐明PD抑制Tau 蛋白磷酸化的潜在机制,笔者进一步验证了Fyn/GluN2B 信号通路相关蛋白在APP-SH-SY5Y 细胞中的表达情况。结果显示,在APP-SH-SY5Y细胞中,Aβ引起了Fyn/GluN2B信号通路的激活;而PD和PP2 干预24 h 后,APP-SH-SY5Y细胞中p-Tau/Tau、p-Src/Fyn(Fyn是Scr 家族中的一员,p-Src/Fyn比值可反映Fyn 蛋白的磷酸化水平)、p-GluN2B/GluN2B比值均显著降低。这提示,PD可通过抑制Fyn/GluN2B信号通路阻断Aβ引起的神经毒性,从而降低Tau 蛋白的磷酸化水平。
综上所述,PD可通過抑制Fyn/GluN2B信号通路抑制APP-SH-SY5Y细胞中Tau 蛋白的磷酸化,为PD治疗AD提供了科学依据。但本研究仅从激活Fyn 的角度阐述了PD 的可能作用机制,未在其沉默条件下进行验证。在后续实验中,笔者将采用APP/PS1 双转基因小鼠为AD动物模型,在体内深入探讨PD对该模型小鼠脑内Tau蛋白磷酸化的影响。
参考文献
[ 1 ] 冯晓宾,陈浙丽.多学科协作团队在阿尔茨海默病患者早期康复中的应用效果[J].中国医药导报,2019,16(18):150-153,170.
[ 2 ] HYMAN B T,PHELPS C H,BEACH T G,et al. Nationalinstitute on aging-Alzheimers association guidelines forthe neuropathologic assessment of Alzheimers disease[J].Alzheimers Dement,2012,8(1):1-13.
[ 3 ] MILA A M,SALVADO G,GISPERT J D,et al. Amyloidbeta,Tau,synaptic,neurodegeneration,and glial biomarkersin the preclinical stage of the Alzheimers continuum[J]. Alzheimers Dement,2020,16(10):1358-1371.
[ 4 ] CONGDON E E,SIGURDSSON E M. Tau-targeting therapiesfor Alzheimer disease[J]. Nat Rev Neurol,2018,14(7):399-415.
[ 5 ] KNOX R,ZHAO C,MIGUEL-PEREZ D,et al. EnhancedNMDA receptor tyrosine phosphorylation and increasedbrain injury following neonatal hypoxia-ischemia in micewith neuronal Fyn overexpression[J]. Neurobiol Dis,2013,51:113-119.
[ 6 ] MIYAMOTO T,STEIN L,THOMAS R,et al. Phosphorylationof tau at Y18,but not Tau-Fyn binding,is requiredfor tau to modulate NMDA receptor-dependent excitotoxicityin primary neuronal culture[J]. Mol Neurodegener,2017,12(1):41.
[ 7 ] LI K,JIA H,SHE X,et al. Role of NMDA receptors innoise-induced tau hyperphosphorylation in rat hippocampusand prefrontal cortex[J]. J Neurol Sci,2014,340(1/2):191-197.
[ 8 ] YADIKAR H,TORRES I,AIELLO G,et al. Screening oftau protein kinase inhibitors in a tauopathy-relevantcell-based model of tau hyperphosphorylation and oligomerization[J]. PLoS One,2020,15(7):e0224952.
[ 9 ] 张春红,李向高,张连学,等.薄层扫描法测定人参总皂苷酸水解物中人参二醇的含量[J]. 特产研究,2006,6(2):71-73.
[10] 郭冬阳,洪秀芳,沈灵芝,等.基于RNA测序研究人参二醇对大鼠心血管内皮细胞基因表达的影响[J].心电与循环,2020,39(1):26-30.
[11] 周金娜,董成梅,邹澄,等.酸酐酯化法制备原人参二醇衍生物及其抗肿瘤活性[J].昆明医科大学学报,2019,40(11):21-25.
[12] 王雨辰. AngⅡ诱导非小细胞肺癌A549 细胞上皮间质转化的机制研究及20(S)-原人参二醇的干预作用[D].长春:吉林大学,2019.
[13] 刘林增.人参二醇的现代药学与生物活性研究进展[J].山东医学高等专科学校学报,2019,41(4):267-268.
[14] 郑丽华. Aβ1-40对原代培养胎鼠皮质神经元的神经毒性作用及人参二醇保护作用的实验研究[D].杭州:浙江大学,2007.
[15] 于振波.新人参二醇对老年大鼠痴呆的作用研究[D].长春:吉林大学,2012.
[16] 宋喜君,周鹤妍,常平,等. APPswe基因慢病毒表达质粒的构建及对其SH-SY5Y细胞生长和凋亡的影响[J].基因组学与应用生物学,2021,6(1):1-14.
[17] 陈佳,李伟,刘征,等.基于GEO数据库的DPN相关靶点挖掘及与芍药苷分子对接研究[J].广东药科大学学报,2020,36(4):514-518.
[18] QIAN H,CHEN Q,ZHANG S,et al. The claudin familyprotein Fig A mediates Ca2+ homeostasis in response to extracellularstimuli in aspergillus nidulans and aspergillusfumigatus[J]. Front Microbiol,2018,5(9):977.
[19] 王英全,梁景宏,贾瑞霞,等. 2020-2050 年中国阿尔茨海默病患病情况预测研究[J].阿尔茨海默病及相关病杂志,2019,2(1):289-298.
[20] DANIELA M F,JOANA M S,CARIAN S C,et al. Allostericmodulation of AMPA receptors counteracts Tau-relatedexcitotoxic synaptic signaling and memory deficitsin stress and Aβ-evoked hippocampal pathology[J]. MolPsychiatry,2020,5(28):10.
[21] 闫宇辉,张二飞,李红艳,等.楮实子水提物对APP 转染的SH-SY5Y 细胞的影响[J].中成药,2020,42(1):187-192.
[22] 王晶.表没食子儿茶素没食子酸酯对稳定表达淀粉样前体蛋白的SH-SY5Y细胞抗炎抗凋亡作用研究[J].成都醫学院学报,2017,12(3):254-259.
(收稿日期:2020-12-01 修回日期:2021-04-08)
(编辑:林静)

