黄连温胆汤含药血清干预IR-3T3-L1细胞的最佳浓度与时间筛选
韩宇博,田苗,刘紫君,娄宏君,王瑞楠,张丹丹,郭东浩,刘莉*
(1.黑龙江中医药大学,黑龙江 哈尔滨 150040;2.黑龙江中医药大学附属第一医院,黑龙江 哈尔滨 150040)
胰岛素抵抗(insulin resistance,IR)是指机体对胰岛素调节作用/葡萄糖利用敏感度反应下降,代偿性增加胰岛素分泌水平,以保持内环境及血糖稳态[1-2]。中医药在改善IR从而防治代谢性疾病及糖尿病方面具有鲜明特点,笔者前期研究[3-6]发现:黄连温胆汤可降低饮食诱导代谢综合征大鼠血压、血糖、体质量、血脂水平,降低炎性细胞因子及脂联素水平,可上调胰岛素受体底物、葡萄糖转运体等基因的mRNA和蛋白表达,改善IR。基于体外细胞培养体系研究黄连温胆汤含药血清的作用机制具有重要意义。体外研究中,如何制定含药血清与细胞培养体系的比例,能够产生最佳干预效果,是亟须解决的问题。因此本研究探讨黄连温胆汤含药血清干预IR-3T3-L1细胞的最佳浓度与时间,为后续进一步的机制研究提供确切的实验依据。
1 材料
1.1 实验细胞株及动物
3T3-L1小鼠胚胎成纤维细胞购买于中国科学院细胞库。30只SPF级雄性SD大鼠购自黑龙江中医药大学实验动物中心,体质量(200±20)g,动物许可证号:SCXK(黑)2 015 006。饲养环境温度22~24 ℃,相对湿度40%~50%;饲养密度为5只/笼,自由饮食水,隔日更换垫料,适应性饲养1周后用于实验研究,研究过程符合动物伦理学要求。
1.2 实验药品
黄连温胆汤:黄连10 g,清半夏10 g,竹茹15 g,枳实10 g,陈皮15 g,茯苓10 g,生姜5 g,炙甘草10 g,所有饮片购自黑龙江中医药大学附属第一医院草药局,经黑龙江中医药大学药学院生药学教研室鉴定,符合2015版《中华人民共和国药典》一部要求。盐酸二甲双胍标准品购自天津阿尔法生物科技有限公司。
1.3 实验试剂
OriCellTMSD大鼠骨髓间质干细胞成脂诱导分化培养基试剂盒(赛业生物科技有限公司),DMEM高糖培养基(Gibco),胎牛血清(Fetal bovine serum,FBS)(HyClone),胰蛋白酶(Gibco),PBS(HyClone),地塞米松(Sigma),DMSO(Sigma),戊巴比妥钠(Sigma),葡萄糖测定试剂盒(中生北控生物科技公司),葡萄糖氧化酶(Glucose oxidas,GOD)Elisa试剂盒(Mobio),CCK-8试剂盒(索莱宝)。
1.4 实验仪器
BSC-1300IIAz生物安全柜(江苏苏净集团),CKX41 FS倒置相差显微镜(OLYMPUS),MCO-18AC二氧化碳培养箱(Panasonic),MULTISKAN FC酶标仪(Thermo),SORVALL ST8/8R低温离心机(Thermo)等。
2 方法
2.1 黄连温胆汤含药血清的制备
将黄连温胆汤各饮片混合,加入14倍量的蒸馏水,煎煮3次,每次煎煮1 h,纱布过滤,3次药液合并,减压浓缩至稠膏状,并用冻干机做成冻干粉。30只SD大鼠用随机数字法分为黄连温胆汤组15只,空白组15只,黄连温胆汤组每日灌服黄连温胆汤冻干粉稀释液(2.1 g生药/mL,每100 g体质量给予2 mL药液),空白组每日灌服与中药组等体积蒸馏水,每日早、晚各灌胃1次,连续灌胃5次,于末次灌胃1 h后将大鼠用1%戊巴比妥钠麻醉,无菌条件下腹主动脉采血并分离血清,0.22 μm微孔滤膜过滤,56 ℃,30 min灭活,分装并区分标注为空白血清和含药血清,-80 ℃保存备用[7]。
2.2 诱导3T3-L1细胞成脂分化
参照OriCellTMSD大鼠骨髓间质干细胞成脂诱导分化培养基试剂盒说明书,在超净工作台中配制诱导培养基A液和B液,确保混合均匀之后即可使用。其中A液包括基础培养基175 mL,FBS 20 mL,双抗2 mL,谷氨酰胺2 mL,地塞米松200 μL,胰岛素400 μL,3-异丁基-1-甲基黄嘌呤200 μL,罗格列酮200 μL;B液包括基础培养基175 mL,FBS 20 mL,双抗2 mL,谷氨酰胺2 mL,胰岛素400 μL。5%CO2,37 ℃培养条件下的3T3-L1细胞,每隔3 d换增殖培养基1次,直到细胞融合达到100%或者过融合;移除细胞增殖培养基,向60 mm培养皿中加入3 mL诱导培养基A液维持3 d,更换培养液为2 mL B液维持24 h,再换回A液,如此反复3个循环,用B液维持培养4~7 d直到脂滴变得足够大、圆。油红染色并在倒置显微镜下拍照。
2.3 胰岛素抵抗3T3-L1细胞模型构建及分组
在96孔板上培养3T3-L1成纤维细胞,成脂分化后加入含有1 μmol/L地塞米松的增殖培养基,培养96 h即可构建IR-3T3-L1脂肪细胞模型,且36 h内模型稳定[8-9]。将IR-3T3-L1脂肪细胞随机分为模型组(8%空白血清)、中药高剂量组(8%含药血清)、中药中剂量组(4%含药血清+4%空白血清)、中药低剂量组(2%含药血清+6%空白血清)和二甲双胍组(8%空白血清+1 mmol/L盐酸二甲双胍溶液),另外选用分化成熟的3T3-L1细胞作为正常组(8%空白血清),共6组,每组3个复孔,分别在加药后12 h、24 h和36 h收取培养板各孔剩余培养液,用于指标测定。
2.4 检测指标测定方法
CCK-8测定细胞活力:向培养板的每孔加入10 μL CCK-8溶液孵育1 h;用酶标仪测定在450 nm处的吸光度,计算细胞活力;参照葡萄糖测定试剂盒说明书完成培养液葡萄糖含量检测,葡萄糖消耗量=未接种细胞的培养液葡萄糖含量-样本培养液葡萄糖含量;应用ELISA法检测培养液中GOD含量。
2.5 统计方法
应用SPSS 24.0软件进行统计分析,符合正态分布的计量资料用“均数±标准差”表示,多组间样本比较采用单因素方差分析,非正态分布样本多组间样本比较采用非参数检验;认为P<0.05时差异具有统计学意义。
3 结果
3.1 诱导3T3-L1细胞成脂分化情况
如图1所示,3T3-L1小鼠成纤维细胞复苏后贴壁良好,细胞呈梭形,细胞内无脂滴;3T3-L1达到融合状态后,加入诱导培养基A液作用3 d,再更换为诱导培养基B液作用1 d,如此反复3个循环,细胞回缩变圆,细胞内逐渐出现脂滴;继续应用诱导培养基B液作用4~7 d,细胞内充满脂滴,呈典型的“戒环状”;油红染色成功,脂滴被染为红色,可见3T3-L1细胞诱导分化率达80%以上。
3.2 细胞活力水平比较
如表1所示,干预12 h和36 h时,各组OD450nm较正常组下降,但差异无统计学意义(P>0.05);干预24 h时,模型组和二甲双胍组OD450nm较正常组下降,差异具有统计学意义(P<0.05)。

注:A:3T3-L1小鼠成纤维细胞复苏后状态;B:3T3-L1细胞第3次换入诱导培养基B液;C:3T3-L1细胞继续用诱导培养基B液培养4天;D:3T3-L1脂肪细胞油红O染色。图1 诱导3T3-L1细胞成脂分化情况(100×)

表1 各组CCK-8孵育后吸光度水平比较
如图2所示,干预12 h、24 h和36 h的各组间细胞活力差异无统计学意义(P>0.05),干预12 h、24 h时,中药高、中、低剂量组细胞活力相当,干预36 h时,中药高、低剂量组细胞活力较中药中剂量组有下降趋势。

图2 12 h、24 h及36 h各组细胞活力水平
3.3 葡萄糖消耗量水平
如表2所示,药后干预12 h、24 h及36 h,正常组葡萄糖消耗量均高于其余5组;各组给药干预12 h,模型组葡萄糖消耗量明显低于其余5组,差异具有统计学意义(P<0.01);各组给药干预24 h后,各组葡萄糖消耗量较12 h增高,但中药低剂量组与模型组比较,差异无统计学意义(P>0.05),其余各组葡萄糖消耗量仍高于模型组(P<0.05);各组给药干预36 h后,中药高剂量组和中药低剂量组葡萄糖消耗量与模型组比较,差异无统计学意义(P>0.05),仅中药中剂量组和二甲双胍组葡萄糖消耗量较模型组升高,差异具有统计学意义(P<0.05)。随着取样时间点的推迟,各组葡萄糖消耗量增加,模型组与各用药组间差值增大。
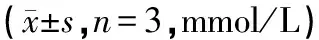
表2 各组12 h、24 h、36 h取样点葡萄糖消耗量水平 的比较
3.4 ELISA测得葡萄糖氧化酶水平
标准曲线回归方程:Y=0.035 02+0.019 92X,R2=0.999 71;所有数据处理均去除本底,即去除孔板本身的OD值。将各组检测所得OD值代入回归方程,得到各组葡萄糖氧化酶浓度(GOD),见表3。干预12 h和24 h时,各组培养基中GOD浓度水平相当,差异无统计学意义(P>0.05);干预36 h时,模型组培养基中GOD浓度低于中药中剂量组,差异具有统计学意义(P<0.05)。

表3 各组间葡萄糖氧化酶水平的比较
4 讨论
血清药理学是由日本学者田代真一首次提出的,它是一种研究非单体药物的药理学方法,通过实验对象经口给药一段时间后采集血液,制备含药血清,从而模拟药物从体内经吸收代谢后出现的新成分和产物。由于这种方法提取的含药血清比较接近药物在体内的代谢情况,所以更适合药物种类繁多、成分复杂、含量不确定的中药复方研究。本实验属中药血清药理学范畴,其意义在于模拟体内药理活动过程,是中药药理学研究的重要方法,自发明以来被广泛使用[10]。
目前诱导3T3-L1脂肪细胞的方法很多,最常用的是传统“鸡尾酒”法[11],但“鸡尾酒”法存在诸多影响因素,例如FBS的质量、诱导剂的配制、诱导剂作用时间、细胞融合程度等,因此涌现出大量学者研究诱导配方的改进,尚无统一造模方法可供参考。考虑使用已经商品化的OriCellTMSD大鼠骨髓间质干细胞成脂诱导分化培养基试剂盒进行实验,减少影响因素。虽然该试剂盒主要应用于骨髓间质干细胞成脂分化,但其具有增强趋向脂肪细胞分化的能力,同时诱导培养基A组成较传统“鸡尾酒”法多了罗格列酮溶液,罗格列酮是噻唑烷二酮类胰岛素增敏剂,可激活特异性过氧化物酶体增殖因子γ型受体,Vishwanath D[12]等研究与其相似,在传统“鸡尾酒”法加入曲格列酮溶液(同属噻唑烷二酮类胰岛素增敏剂)后明显提高3T3-L1细胞诱导分化率。在本实验中,诱导时间持续16~19 d,相比于传统方法诱导时间较长,但实验重复性较好,经油红O染色鉴定,认为成脂分化率可稳定维持在80%以上。
目前,IR-3T3-L1脂肪细胞模型的建立方法主要有:①炎症因子刺激,例如肿瘤坏死因子α[13]、白介素6[14]等;②棕榈酸或游离脂肪酸刺激[15];③高浓度胰岛素刺激[16];④糖皮质激素刺激,例如地塞米松[17]。本实验应用含1 μmol/L地塞米松的增殖培养基培养分化成熟的3T3-L1脂肪细胞,建立IR-3T3-L1脂肪细胞模型。进一步用于黄连温胆汤含药血清干预IR-3T3-L1脂肪细胞最佳浓度和时间的筛选。
黄连温胆汤含药血清所产生的量效关系与动物的给药量及体外培养体系中血清的浓度共同决定,前期研究中,依据含药血清色谱峰强度及数量分析实验,已经确定了大鼠的给药量,因此,本实验中将相对固定的黄连温胆汤含药血清以不同比例加入到培养体系,以期明确体外培养体系中黄连温胆汤含药血清的最佳配比关系。本实验设定整个培养体系中总血清浓度所占比为13%,其中FBS浓度占5%,因为从3T3-L1成纤维细胞诱导分化为脂肪细胞,再到建立胰岛素抵抗模型,培养体系中均含有FBS,全部换为大鼠含药血清或正常血清易引起3T3-L1脂肪细胞“不适”,对生长环境感到陌生,维持5%FBS浓度的目的就是为了保证3T3-L1脂肪细胞以较好状态存活,排除细胞自身的影响。笔者将黄连温胆汤含药血清分为3个不同比例,分别是8%、4%和2%,将其命名为中药高、中、低剂量组,余下血清用正常大鼠血清补充,以保证各组间相对一致,具有可比性。IR-3T3-L1脂肪细胞模型在36 h内较为稳定[8],因此本研究在36 h内设定了3个取样点,分别为12 h、24 h和36 h,通过观察不同浓度黄连温胆汤含药血清对IR-3T3-L1脂肪细胞葡萄糖消耗量、葡萄糖氧化酶含量和细胞活力的影响,筛选含药血清干预IR-3T3-L1的最佳浓度和最佳时间。
CCK-8法是目前常用于测定细胞活力的方法之一[18-19]。本实验结果表明,黄连温胆汤含药血清及二甲双胍溶液对IR-3T3-L1脂肪细胞活性无明显影响,该浓度的范围的黄连温胆汤含药血清及二甲双胍溶液的细胞毒性可忽略不计。各组干预24 h的实验结果中,模型组和二甲双胍组OD450nm较正常组下降,但经细胞活力公式计算后二者无差异,说明培养板、培养基及CCK-8溶液本身可能存在对吸光度的影响,在排除它们的干扰后,本实验结果较为准确,认为黄连温胆汤含药血清不同浓度及不同作用时间对IR-3T3-L1脂肪细胞活力无明显影响,对于最佳药物浓度及干预时间的筛选,可忽略细胞活力的影响。
本实验进一步检测各组培养基中葡萄糖消耗情况,实验结果表明:黄连温胆汤各剂量组和二甲双胍能够改善3T3-L1脂肪细胞的IR程度,随着取样时间点的推迟,各组葡萄糖消耗量逐渐增加,模型组与各用药组间差值增大。在干预36 h时,模型组与其他用药组葡萄糖消耗量差值最大,可见干预时间达到36 h时,用药组发挥了最大改善胰岛素抵抗的作用,但仅有中药中剂量组、二甲双胍组与模型组差异具有统计学意义,说明随着干预时间的推移,中药高、低剂量两组提高葡萄糖消耗量的作用逐渐减弱,只用中药中剂量组和二甲双胍组能够一直保持提高葡萄糖消耗量的作用,因此推测中剂量的黄连温胆汤含药血清(4%)干预IR-3T3-L1脂肪细胞36 h,可明显改善其胰岛素抵抗水平,增加葡萄糖消耗量及葡萄糖的利用度。
本实验亦应用ELISA法测定各组培养基中GOD含量,首先是想明确3T3-L1脂肪细胞培养基中是否含有GOD,目前的结果显示培养基中含有GOD,而且在干预36 h中药中剂量组明显出现提高葡萄糖消耗量的同时,中剂量组GOD含量与模型组比较差异明显,说明在药物的干预作用下,可调节IR-3T3-L1脂肪细胞培养基中的GOD含量,而且GOD来源于细胞,通过某种机制将胞内的GOD释放到培养基中,但应考虑样本量的限制,由于是进行最佳药物剂量和最佳干预时间的筛选,所以本实验每组设计3个复孔,若想明确GOD含量变化情况,可在后续实验中扩大样本量,同时提高实验的重复性。本实验中检测的是培养基中的GDO含量,可能存在细胞外影响机制,后续实验考虑弃掉培养基,通过裂解细胞,检测细胞内GOD含量,以明确问题所在。
综上所述,黄连温胆汤含药血清及二甲双胍溶液无细胞毒性,对IR-3T3-L1脂肪细胞的活力无影响,在最佳药物浓度及干预时间的筛选时可忽略细胞活力的因素,仅考虑葡萄糖消耗量的变化即可。最终确定中剂量的黄连温胆汤含药血清(4%)干预IR-3T3-L1脂肪细胞36 h是最佳给药方案,可用于后续机制探讨的实验研究。

