铜电极电解不同浓度食盐水的实验探究
于 宁
(辽宁省大连经济技术开发区第二中学 116600)
国内现行教材大都采用石墨电极作为阳极进行电解饱和食盐水实验.苏教版选修教材《实验化学》专题5的拓展实验采用了铜电极(用铜丝作为阴阳两极)电解饱和食盐水.受此启发,将此实验装置“放大”,并将饱和食盐水更换为不同浓度的食盐水进行实验,得到更多有趣的现象.
一、实验装置
教材中拓展实验装置如图1所示.将此装置“放大”——试管放大为烧杯,铜丝放大为铜棒,如图2所示.
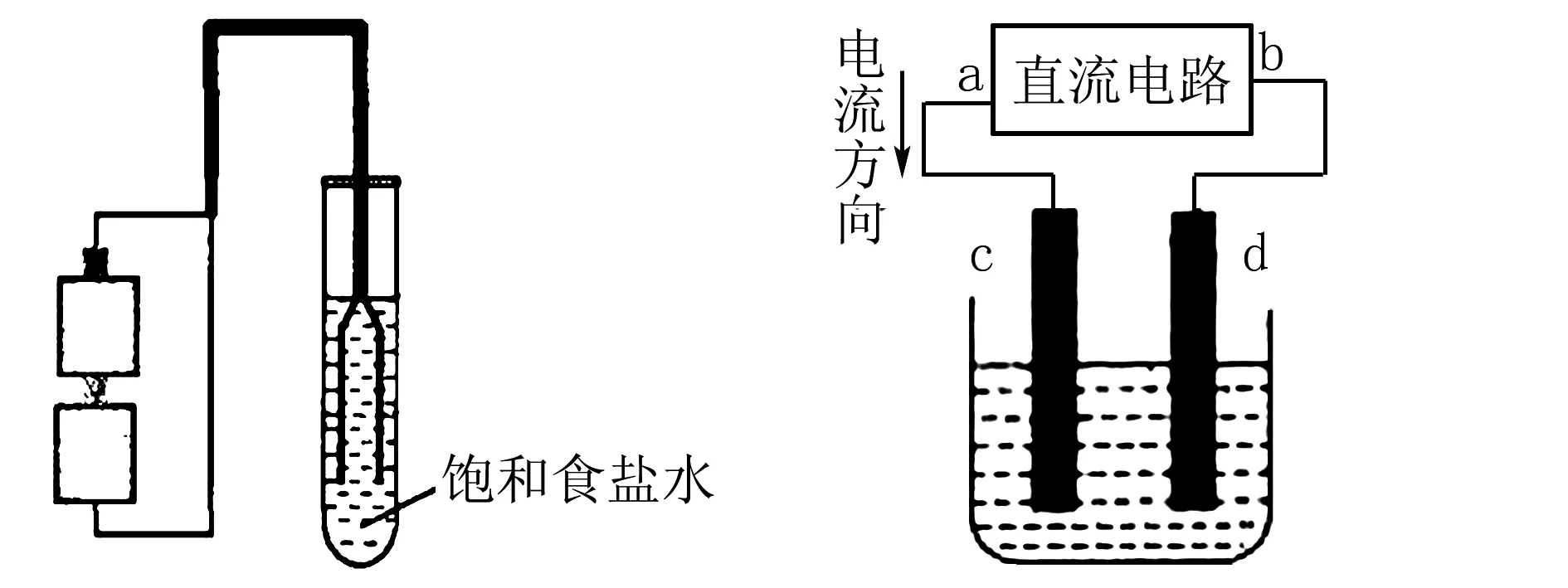
图1 图2
二、实验操作、现象及解释
向大烧杯中分别注入饱和食盐水、体积比V(饱和食盐水)∶V(蒸馏水)=5∶1、5∶2、5∶3的溶液、蒸馏水,调节电压为1.5V.记录刚出现白色沉淀的时间,观察两极沉淀物的颜色及生成的先后顺序.
1.两电极的实验现象及解释
铜电极电解不同浓度食盐水的两电极的实验现象是相同的,即:
(1)电解发生后,阴极立即有无色气体放出,且源源不断.
(2)阳极铜丝逐渐“溶解”,由粗变细;结束电解时取出观察其紫红色光泽不变.
对现象的解释如下:
(1)阴极总反应:2H2O+2e-→2OH-+H2↑(还原反应)
(2)铜电极露出的部分被“溶解”后仍为铜,故仍有金属光泽.
2.溶液中的实验现象及解释[阳极铜“溶解”后的最终存在形式(+1价、+2价)的探究]
阳极金属放电都易生成相对稳定的离子.正如Fe-2e-→Fe2+(如果生成Fe3+则被Fe还原为Fe2+)一样,铜放电的初产物为:Cu-2e-→Cu2+.那么阳极生成的Cu2+最终会以怎样的形式存在呢?实验表明,铜放电的初产物Cu2+最终的存在形式与Cl-浓度密切相关.将其反应过程分为3个阶段,如图3所示.
图3
(1)电解饱和食盐水
理论上发生A、B、C,由于动力学因素,只发生A,故溶液未出现白色沉淀,直接由澄清变为黄色沉淀.
阳极反应:Cu-2e-→Cu2+
Cu2++Cu+4Cl-→2[CuCl2]-
阳极总反应:Cu-e-+2Cl-→[CuCl2]-
因Cl-浓度很大,使Cu2+全部生成无色的[CuCl2]-,故始终(约15分钟)没有观察到白色沉淀.当阴极产生的OH-移动到阳极附近时,有:[CuCl2]-+OH-→CuOH↓(黄色)+2Cl-;2CuOH(黄色)→Cu2O(砖红色)+H2O.橙色沉淀是CuOH、Cu2O的混合物.因此约15分钟时,在阳极铜周围看到黄色沉淀,继而迅速转变为橙色和砖红色.
(2)电解高浓度不饱和食盐水
理论上发生A、B、C,由于动力学因素,只发生A、B,故溶液需等待较长时间才能出现白色沉淀,继而变黄.
阳极反应:Cu-2e-→Cu2+
Cu2++Cu+4Cl-→2[CuCl2]-
Cu2++Cu+2Cl-→2CuCl↓
阳极总反应:2Cu-2e-+3Cl-→[CuCl2]-+CuCl↓
因Cl-浓度大,使Cu2+先生成无色的[CuCl2]-,再生成CuCl↓,故需等待较长时间(170秒)才能观察到白色沉淀.逐渐增多的白色沉淀CuCl与阴极生成的OH-相遇时,生成更难溶的黄色沉淀CuOH(CuCl、CuOH的溶度积分别为1.2×10-6和1.0×10-14),即:CuCl+OH-→CuOH+Cl-,且2CuOH(黄色)→Cu2O(砖红色)+H2O.因此白色沉淀片刻后变为黄色、橙色、砖红色.
(3)电解中等浓度不饱和食盐水
实际上发生A、B、C,故溶液需等待一会儿便可出现白色沉淀,再有蓝色沉淀(少量)生成,白色沉淀继而变黄.
阳极反应:Cu-2e-→Cu2+
Cu2++Cu+4Cl-→2[CuCl2]-
Cu2++Cu+2Cl-→2CuCl↓
阳极总反应:
5Cu-6e-+6Cl-→Cu2++2[CuCl2]-+2CuCl↓
因Cl-浓度较大,使Cu2+先生成无色的[CuCl2]-,再生成CuCl↓,故需等待一会儿(48秒)才能观察到白色沉淀且白色沉淀量逐渐增多.Cl-消耗完后,Cu2+“显露”出来,与阴极OH-生成蓝色絮状沉淀Cu(OH)2,且Cu2+移动至阴极的速度比OH-移动至阳极的速度快,因此蓝色沉淀产生在阴极附近.由于“显露”出的Cu2+量很少,故产生的蓝色沉淀量很少.量较多的白色沉淀逐渐变为黄色、橙色、砖红色.
(4)电解低浓度不饱和食盐水
实际上发生B、C,故溶液很快就出现白色沉淀,再有蓝色沉淀(大量)生成,少量的白色沉淀继而变黄.
阳极反应:Cu-2e-→Cu2+
Cu2++Cu+2Cl-→2CuCl↓
阳极总反应:3Cu-4e-+2Cl-→Cu2++2CuCl↓
因Cl-浓度小,使Cu2+直接生成CuCl↓,故很快(21秒)就能观察到白色沉淀.由于“显露”出的Cu2+量很多,故产生的蓝色沉淀量很多.量较少的白色沉淀逐渐变为黄色、橙色、砖红色.
(5)电解纯净的蒸馏水
实际上发生C,故溶液有大量的蓝色沉淀生成,由于动力学因素,反应很缓慢,需等待很长时间.
三、实验结论
由上述现象可推出以下三个结论:
1.电解饱和食盐水和蒸馏水的过程中始终不会出现白色沉淀;而电解高、中、低浓度的不饱和食盐水的过程中均会产生白色沉淀,且白色沉淀生成的速度逐渐加快,等待时间越来越短(实验测得从电解开始到产生白色沉淀的时间分别为170秒、48秒、21秒),最终生成的砖红色沉淀量越来越少.
2.电解饱和食盐水和高浓度不饱和食盐水最终都只产生砖红色沉淀(大量);电解中等浓度不饱和食盐水、低浓度不饱和食盐水和纯净的蒸馏水最终都有蓝色沉淀生成,且蓝色沉淀的量越来越多.刚出现蓝色沉淀(极少量)对应的不饱和食盐水中Cl-的浓度便是临界浓度.
3.对临界Cl-浓度从理论上无法计算出(因不知Cu2+的浓度),故从实验现象推测临界浓度的范围:体积比V(饱和食盐水)∶V(蒸馏水)为5∶1的溶液电解结束后只有砖红色沉淀生成,而体积比V(饱和食盐水)∶V(蒸馏水)=5∶2的溶液电解结束后除有大量的砖红色沉淀生成之外,还有少量蓝色沉淀出现.因此推测临界Cl-浓度必定在V(饱和食盐水)∶V(蒸馏水)为5∶1到5∶2之间,且接近于5∶2(也就是说,推测临界Cl-浓度必定对应的是中等浓度的不饱和食盐水).若想进一步更深入地了解精确的临界Cl-浓度,可配制体积比V(饱和食盐水)∶V(蒸馏水)=5∶1到5∶2之间的不同浓度的不饱和食盐水进行再次探究.

