利用低品位红土镍矿制备纳米二氧化硅粉体
常龙娇 曹诗圆 罗绍华
(1.渤海大学 化学与材料工程学院,辽宁 锦州 121013;2.辽宁硅材料工程技术研究中心,辽宁 锦州 121013;3.东北大学秦皇岛分校 资源与材料学院,河北 秦皇岛 006004)
红土镍矿为硫化镍矿经过风化后淋滤再沉积所形成的氧化镍矿,其镍储存量约占世界陆地镍资源储存量的60%,是全球镍产量的主要来源之一[1-2]。目前针对红土镍矿的研究大多是提取其中含量较少的镍,其主要处理方法包括火法和湿法[3]两大工艺。火法工艺包括还原硫化熔炼镍锍法和还原熔炼镍铁法等,湿法工艺主要有常压酸浸法[4]、高压酸浸法[5]和还原焙烧—氨浸法[6]等,这些工艺在处理红土镍矿的过程中具有能耗大、成本高、废料多等缺点,不利于资源节约和环境保护。
红土镍矿中的硅含量较高,但到目前为止,相关研究及利用鲜见报道,因此在红土镍矿的加工过程中,如何合理开发利用矿物中所富含的硅元素,从而避免资源浪费以及环境污染具有重要的研究价值[7-9]。本文前期以红土镍矿为原料,碱溶液为反应助剂,经水热反应使红土镍矿的结构得以破坏,经水浸过滤,矿物中的硅以硅酸钠的形式进入滤液,铁、镁、镍等有价元素形成金属富集渣。硅酸钠滤液后续用于制备纳米二氧化硅,为二氧化硅材料的开发提供了有力支持;金属富集渣可用于提取制备氧化镍,同时也为铁、镁的提取创造了有利条件。整个水热反应过程在较低的温度下进行,无废弃物排放,节能环保。
在纳米二氧化硅粉体的制备过程中,利用低品位红土镍矿碱式水热反应所产生的硅酸钠滤液为原料,选择硫酸作为沉淀剂、硫酸钠作为分散剂、聚乙二醇(PEG 200~800)作为表面活性剂,选用反应条件较温和的化学沉淀法,最终醇洗制备出纳米二氧化硅[10],所得二氧化硅粉体后续作为正极材料的原料用于锂离子电池[11]的制备,扩大了锂离子电池正极材料的选择范围,可提高以二氧化硅为原料产业的原料供应量,满足国家发展资源节约型的循环经济要求。因此在实验室小型实验的基础上对制备二氧化硅的工艺进行中试,为其工业化的实现提供了的理论依据和技术支撑。
1 实验
1.1 原料
原料红土镍矿产自印尼,其主要化学成分详见表1,矿物相组成和微观形貌如图1所示。由表1可知,红土镍矿中的二氧化硅、氧化铁等含量较高,且二氧化硅含量高于50%,若只提取矿物中的镍,将产生大量废料,不仅浪费资源而且污染环境。从图1可看出,实验用红土镍矿的主要物相为游离态的石英、利蛇纹石和赤铁矿,颗粒不均匀,呈不规则状。

图1 红土镍矿的XRD图谱和SEM照片

表1 红土镍矿的主要化学组成
实验用氢氧化钠、硫酸、硫酸钠、氯化钡、PEG 200~800、无水乙醇均为分析纯试剂。
1.2 实验设备
采用日本理学公司Ultima IV型X射线衍射仪(工作电压为35 kV,Cu靶Kα射线,扫描速度为0.04 °/s,波长λ=1.544426 Å,2θ衍射角扫描范围为10°~90°)分析红土镍矿和所制备粉体的物相组成;红土镍矿和所制备粉体的微观形貌采用日本岛津公司JEM-ARM200F型扫描电子显微镜进行分析(工作电压为15 kV,工作距离为17 mm,加速电流为15 mA);采用英国马尔文公司Nano-ZS90型激光粒度仪(测试介质为水)对制备的纳米二氧化硅粉体的粒度分布进行测试。
1.3 实验流程
利用低品位红土镍矿制备纳米二氧化硅粉体的工艺流程详见图2。采用碱式水热法,在反应过程中通过向体系添加助剂氢氧化钠,使红土镍矿的结构在较温和的条件下得以破坏。水热反应后得到的熟料采用去离子水浸出,过滤分离,最终铁、镁和镍等金属元素在渣中富集,所得滤液为硅酸钠溶液。向所得硅酸钠溶液中加入适量的分散剂(10%硫酸钠溶液)和表面活性剂(PEG 200~800),混合均匀后放入集热式磁力搅拌器中水浴加热升温至50 ℃,开启机械搅拌,搅拌速度控制在300~700 r/min。向体系中滴加6%~14%的稀硫酸溶液,并用pH试纸测定酸度值,当溶液的pH值约为3时,停止滴加稀硫酸溶液,将反应体系再次升温至一定温度,保温熟化,得到悬浮液,将所得悬浮液经离心机(2 000 r/min,5 min)液固分离,获得的沉淀用去离子水反复洗涤至检不出硫酸根离子,再用无水乙醇洗3次以上,放入烘箱80 ℃干燥12 h,把烘干的产物放入马弗炉于400 ℃焙烧。最后,将焙烧后制得的样品密封保存,后续进行理化性能检测。考察硫酸浓度、熟化温度、熟化时间、搅拌速度和表面活性剂种类等因素对产物粒径的影响。
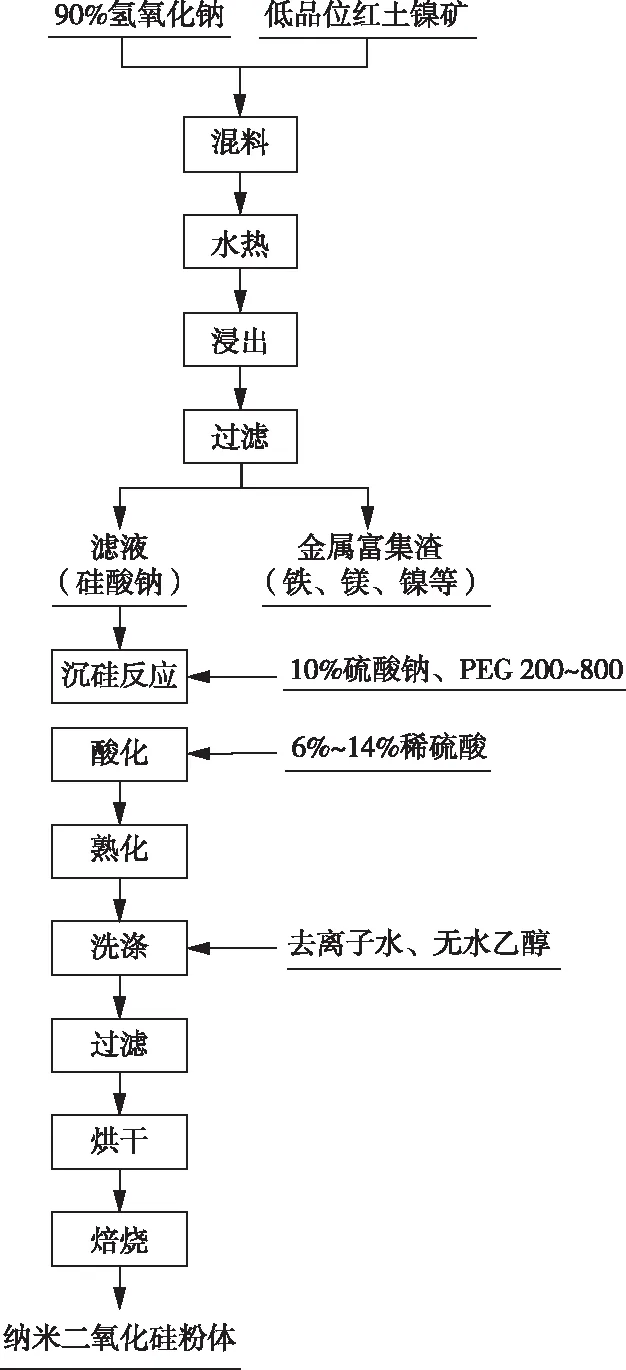
图2 红土镍矿制备纳米二氧化硅粉体工艺流程
2 结果与讨论
不同工艺参数条件下所得二氧化硅粒径分布结果如图3所示。
2.1 硫酸浓度对二氧化硅粉体粒径分布的影响
加入硫酸的作用主要是使硅酸钠中的硅酸根离子转变为二氧化硅沉淀,其次是为了中和矿物在水热反应过程中加入的过量氢氧化钠。由于实验选用的分散剂为硫酸钠,因此在这里选用硫酸作为沉淀剂可很好地避免了再引入其他杂相。将硫酸加入到混有分散剂与表面活性剂的溶液中,滴定终点pH值为3左右,保证了体系能够顺利沉出纳米二氧化硅。
理论上讲,酸度越高,对二氧化硅的沉淀效果越好,但通过实验结果发现,当硫酸浓度过高时,生成的沉淀粒径相对较大,并且体系中过量的硫酸根离子残留会导致洗涤时用水量大大增加,严重浪费水资源。实验还发现,当选择的硫酸浓度过小时,滴加过程不好控制,导致产品粒径分布不均匀,既影响了产品的粒度,又影响其均匀度。硫酸浓度对二氧化硅的粒径分布影响如图3a所示。从图3a可知,当硫酸浓度为10%时,粒度分布最均匀,此时平均粒径约为230 nm,当硫酸浓度为其他值时,所得产品的粒径较大或均匀度不理想,因此最佳硫酸浓度选择为10%。
2.2 熟化温度和熟化时间对二氧化硅粉体粒径分布的影响
熟化作用会使反应体系中的大晶粒继续均匀生长,变得更加粗壮、完整,小晶粒被溶解,并且使原本吸附在沉淀上的杂质重新进入溶液,从而提高产物二氧化硅的纯度。
温度对反应体系中硅酸根离子的聚合速率有显著影响,二氧化硅粉体的生长速度随着温度的升高而增加。温度越高,粒子间发生碰撞几率越大,颗粒间团聚效果越明显;温度过低,反应速率低,分子的扩散作用减弱,颗粒间易形成较大的团聚。不同熟化温度下二氧化硅粉体的粒径分布如图3b所示。60 ℃时,部分颗粒出现了严重的团聚现象,其粒度范围主要在400 nm左右;70 ℃时,颗粒分布范围较窄,说明分布最均匀,其平均粒径最小,约为200 nm;80 ℃和90 ℃时,高温导致了颗粒团聚严重,平均粒径较大,分别为250 nm和350 nm。因此最佳的熟化温度为70 ℃,该条件得到的二氧化硅粉体均匀度最好,粒度相对最小。

(a)不同硫酸浓度;(b)不同熟化温度;(c)不同熟化时间;(d)不同搅拌速度;(e)不同PEG种类;(f)不同硅酸钠浓度
如果熟化时间太短,产品虽具有良好的均匀度和流动性,但其粒径却较大,但熟化时间太长,会造成颗粒一直生长,增加了颗粒间的碰撞几率,发生团聚,不利于超细粉体的形成,因而对超细粉体的结构形成来说,熟化时间的选择尤为重要。不同熟化时间下制得的二氧化硅的粒径分布如图3c所示,可见,当熟化时间为1 h时,产品平均粒径最小,约为250 nm,此时颗粒均匀度也最好,因此实验的最佳熟化时间选择为1 h。
2.3 搅拌速度对二氧化硅粉体粒径分布的影响
搅拌在化学反应体系中常常用来加快反应速率,其主要是增加了反应物粒子之间的有效碰撞,进而对整个化学反应进程起加速作用。在沉硅反应过程中,搅拌所起的作用不仅仅是增大硅酸根离子之间的碰撞几率,大大缩短体系的反应时间,在硫酸的滴定过程中,搅拌还能使硫酸迅速与硅酸钠溶液混合,有效地防止体系局部浓度不均匀,避免胶体过早地出现所造成的颗粒团聚。
实验研究了搅拌速度为400、500、600、700 r/min时产品的粒径分布状况。3d为不同搅拌速度下所得二氧化硅粉体的粒径分布图。根据实验结果可知,当转速为400 r/min时所得产品粒径较小,主要分布在100 nm左右,但在400 nm附近也出现了少量颗粒分布,说明其均匀度不好;当搅拌速度在400 r/min以上时,转速越高,所得二氧化硅粉体的平均粒度越小。实验过程中,当转速选为700 r/min时,由于搅拌强度过高,液滴严重飞溅,导致二氧化硅产品的回收率较低。因此,为了使二氧化硅产品产量得到保证,实验最终选用的最佳搅拌速度为600 r/min。
2.4 PEG种类对二氧化硅粉体粒径分布的影响
在沉硅过程中分别加入非离子型表面活性剂PEG 200、PEG 400、PEG 600、PEG 800,考察非离子型表面活性剂PEG种类对二氧化硅产品粒径的影响,各表面活性剂的加入量均为10%。试验所得不同PEG种类对纳米二氧化硅粒径的分布影响如图3e所示。加入PEG 800时,由于发生严重团聚现象,因此所得二氧化硅产品的粒径最大,分布于400 nm左右;与之相比加入表面活性剂PEG 200和PEG 600时,二氧化硅产品的粒径相对较小,约为350 nm,说明团聚现象减弱;从图3e可以看出,加入非离子型表面活性剂PEG 400时,所得二氧化硅粉体粒径呈正态分布,分布范围较窄,平均粒径最小,约为250 nm,说明PEG4 00对二氧化硅粉体的分散效果最好。因此,后续试验选择最为适宜的表面活性剂是PEG 400。
2.5 硅酸钠稀释浓度对二氧化硅粉体粒径分布的影响
低品位红土镍矿碱式水热过程中产生的硅酸钠溶液经数据处理后计算得出其浓度约为18%,为了进一步探究硅酸钠浓度对制得二氧化硅粉体粒径的影响,将硅酸钠溶液的浓度分别稀释至6%、10%与14%,在其它最佳反应条件下,进行四组不同浓度(6%、10%、14%、18%)的实验探究,结果如图3f所示。从图3f可以看出,硅酸钠浓度对所得二氧化硅粉体的粒径有明显影响,硅酸钠溶液浓度越大,二氧化硅粉体粒径越大。这是因为,低浓度时,硅酸根离子较少,晶粒生长速度缓慢,所以产物粒径较小,同时又存在部分晶粒的生长过程不均匀,最终导致了当硅酸钠溶液浓度过低时产品均匀度不佳的问题尤为显著;与之相反,硅酸钠浓度较高时,有大量硅酸根离子参与晶粒生长,由于二氧化硅生长过程的稳定性,又同时伴随着团聚现象的发生,最终导致了粒径分布较大。因此,将硅酸钠溶液适当地稀释至一定浓度范围内,有利于二氧化硅粉体粒径的减小和均匀分布。
2.6 纳米二氧化硅粉体表征
在最佳工艺条件下制得的二氧化硅粉体的XRD和SEM分析结果如图4所示。从图4可以看出,制得的二氧化硅粉体具有与晶体二氧化硅(曲线2)完全不同的XRD图谱,且衍射峰的强度相对较弱,仅在2θ为25°附近出现了一个强度较小的非晶衍射峰,随后在2θ为33°附近出现了两个强度更小的小尖峰后趋于平滑,表明制得的二氧化硅粉体为无定型非晶态结构。由图4的扫描电镜照片可知,所得二氧化硅粉体颗粒粒径约为200 nm,大小分布均匀,颗粒的分散性与球形度较好。

图4 二氧化硅的XRD图谱和SEM照片
3 结论
1)以稀硫酸为沉淀剂,硫酸钠为分散剂,聚乙二醇为表面活性剂,采用化学沉淀法可以将低品位红土镍矿碱式水热过程中所产生的硅酸钠溶液进行二次利用制备出二氧化硅粉体。
2)最佳制备工艺参数条件为:硫酸浓度10%、熟化温度70 ℃、熟化时间1 h、搅拌速度600 r/min、表面活性剂为PEG 400。
3)硅酸钠溶液浓度对纳米二氧化硅粉体粒径具有影响,将所得硅酸钠滤液稀释至一定浓度范围内有利于二氧化硅粒度的减小和均匀分布。最佳反应条件下制得的纳米二氧化硅粉体的微观形貌呈球形、颗粒尺寸分布均匀(200 nm左右),分散性好。

