先心病患者在介入诊疗中辐射剂量控制分析
刘伟宾, 马晓海, 吴文辉, 王霄芳, 凌 雁, 黄连军
先天性心脏病(congenital heart disease,CHD)是先天畸形中最常见疾病,严重影响我国出生人口质量和生存状态[1]。随着介入诊疗技术飞速发展,利用DSA设备开展CHD介入手术种类日趋广泛[2],单纯动脉导管未闭(patent ductus arteriosus,PDA)、房间隔缺损(atrial septal defect,ASD)、卵圆孔未闭(patent foramen ovale,PFO)、室间隔缺损(ventricular septal defect,VSD)、肺动脉狭窄(pulmonary stenosis,PS)等数量大[3],但未成年人对X射线辐射更加敏感,合并或复杂CHD多,可能会对患者造成高辐射剂量和潜在辐射损伤,如何保证在临床需求下对患者辐射剂量进行合理控制是当前亟需解决问题。本研究通过采集CHD患者介入诊疗辐射剂量监测数据进行统计,结合辐射实践情况评估放射生物效应危害及发生概率,探讨如何控制辐射剂量。
1 材料与方法
1.1 临床资料
2017年11月至2018年3月,连续观察北京安贞医院使用SIEMENS AXIOM artis zee biplane DSA设备介入诊疗CHD患者237例,男78例(32.9%),女159例(67.1%);年龄0.3~65岁,婴儿(<1岁)22例(9.3%),幼儿(1~4岁)79例(33.3%),儿童(5~11岁)41例(17.3%),少年(12~18岁)18例(7.6%),青年(19~35岁)35例(14.8%),中年(36~59岁)37例(15.6%)、老年(>60岁)5例(2.1%);PDA 76例(32.1%),ASD 65例(27.4%),PS18例(7.6%),VSD18例(7.6%),PFO 8例(3.4%),其他(合并或复杂)(OTHER)52例(21.9%)。DSA设备检查程序及曝光参数选择均满足临床诊疗需求。
1.2 方法
1.2.1 数据统计 按年龄(婴儿、幼儿、儿童、少年、青年、中年、老年)、疾病(PDA、ASD、PS、VSD、PFO、OTHER)分组统计DSA设备实时监测总辐射时间(total radiation time,T,min)、介入参考点累积剂量(cumulative dose,CD,mGy)、剂 量 面 积 乘 积(dose area product,DAP,Gy·cm2),估 算 峰 值 皮 肤 剂 量(peak skin dose,PSD,mGy)、 有 效 剂 量(effetive dose,ED,mSv)数据(表1,2);由CD估算患者PSD,(PSD=1/2或4/5CD[4]);由DAP估算ED,ED=DAP×0.17mSv/(Gy·cm2)(心血管介入诊疗平均转换因子)[5];CD及PSD按(0~,100~,150~,500~,1 000~,2 000~)分段进行频数统计(表3)。

表1 237例CHD患者介入诊疗年龄分组监测及估算辐射剂量统计情况
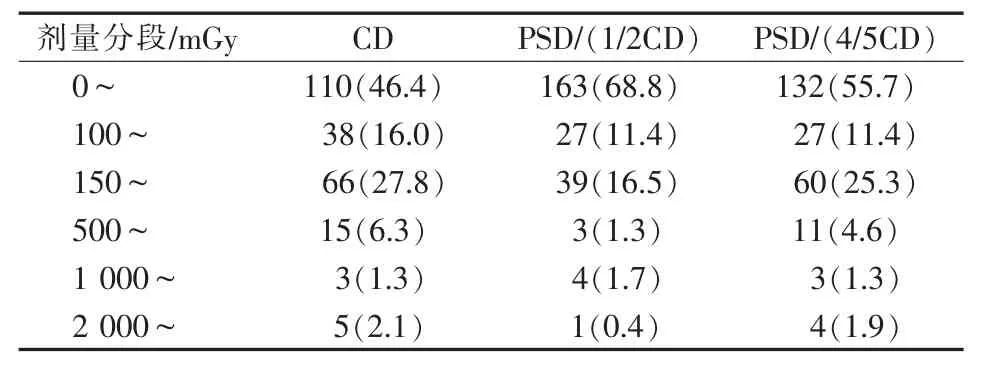
表3 CHD患者介入诊疗辐射剂量分段频数统计n(%)
T为总辐射时间,是透视时间与摄影采集时间之和,为影响辐射剂量重要因素;CD为各体位介入参考点(interventional reference point,IRP)辐射剂量累积,IRP为X射线基准轴上等中心点偏向焦点一方15cm处,代表焦皮距近似值;DAP为X线束横截面积与平均空气比释动能乘积,反映患者在介入诊疗中受到X射线辐总授予能,本质上与焦点距离无关,表征X射线辐射长期风险;PSD为皮肤各入射区域或点剂量累积;ED(mSv)为在非均匀照射下反映身体所有器官或组织当量剂量所致效应合并危害,表征人体全身对低剂量辐射所致随机效应的加权风险,用于评估随机效应发生概率。
1.2.2 分析方法 描述性分析患者实时监测数据T、CD、DAP及估算数据PSD、ED;依据ICRP建议由分段统计CD、PSD(1/2CD)、PSD(4/5CD)数据评估组织效应风险,由ED评估随机效应发生概率,结合介入诊疗辐射实践情况进行分析,探讨辐射剂量控制方法。
1.3 数据处理
采用Microsoft Excel整理归纳、SPSS17.0统计软件分析,计数资料以例数和百分数表示,记量资料以中位数M(最小值,最大值)表示,组间比较用中位数。
2 结果
2.1 监测估算数据
CHD患者介入诊疗以未成年为主分布于各年龄段、各病种,辐射剂量参数总体T(min)为3.05(0.15,48.98),CD(mGy)为113(1.3,4048),PSD(1/2CD,mGy)为56.5(0.65,2024),PSD(4/5CD,mGy)为90.4(1.04,3238),DAP(Gy·cm2)为11.62(0.28,387.4),ED(mSv)为1.98(0.05,65.87),各参数个体之间差异较大;年龄分组中各参数均以少年组相对较大,病种分组中各参数均以VSD和OTHER组相对较大。

表2 237例CHD患者介入诊疗疾病分组监测及估算辐射剂量统计情况
2.2 组织反应评估风险
高辐射剂量会对患者产生潜在伤害,尤其是敏感人群及敏感区域。ICRP103号[6]指出:单次急性或每年反复持续小剂量X线照射吸收剂量小于0.1 Gy时,组织或器官不会出现临床功能损伤,不存在确定性效应风险;对于胎儿诱发畸形(人类主要器官形成期受孕后3~7 W)存在约0.1 Gy真实预剂量;单次照射对于性腺0.15 Gy即可见精子数量减少、2~5 Gy可暂时不育、5~6 Gy或以上可永久不育,对于卵巢2.5~6.0 Gy可致不育;ICRP118号[7]建议:急性照射对于晶体、造血系统、心血管系统剂量阈值为0.5 Gy,诱导心脏病发生单次照射阈值约为1 Gy,皮肤吸收剂量约2 Gy时可出现暂时性红斑、达到6 Gy可出现主红斑、超过6 Gy可有局部烧灼、疼痛、瘙痒、皮温升高及水肿、超过10 Gy可出现迁延红斑、约12 Gy为晚期皮肤坏死阈剂量。
术前对介入诊疗辐射实践正当性判定不充分、术中未对非照射部位及敏感部位合理防护或剂量控制,辐射剂量超过组织或器官确定性阈值则会产生组织效应。本研究中辐射剂量分段统计以<100 mGy为主,>500 mGy较少,如以CD、PSD(1/2)、PSD(4/5)评估,仅有46.4%、68.8%和55.7%CHD患者不会产生组织反应;如辐射集中于胎儿、性腺、晶体、造血系统、心血管系统及固定皮肤区域等会对患者产生伤害。
2.3 随机反应风险概率
ICRP103号建议:诱发癌症和遗传效应标称危险系数修改为5.5%/Sv和0.2%/Sv。则本研究诱发癌症和遗传效应风险为0.109‰(0.003‰,0.362‰)、0.004‰(0.000 1‰,0.13‰)。
3 讨论
CHD是胚胎发育期心脏及大血管形成障碍或发育异常,或出生后本应自动关闭的通道未闭合,遗传因素仅占约8%,而92%是由宫内环境因素引起,射线辐射是其原因之一。CHD仅有少数类型可自然恢复,部分患者症状轻或无症状至成年后才被发现,大多数需及时经外科手术或介入手术矫治,除病情复杂外大部分能治愈。利用DSA设备开展介入诊疗具有微创、高效、无瘢痕、恢复快等特点,对患者能有效纠正先天心血管结构畸形、改善血流动力学缺陷、提高早中期生存质量。但X射线辐射会对CHD患者产生影响,尤其是未成年人生长发育快,细胞分裂活跃,对X射线敏感度较成人高,即使受小剂量辐射,诱发肿瘤和遗传性疾病等随机效应发生率远超过成年人,且年龄越小机率越大[8]。胎儿、婴幼儿、儿童及青少年随机性效应敏感度超过平均水平2~3倍,60岁以上降至预期剩余寿命平均水平1/5[9]。据国外研究[10]发展中国家平均CHD出现率为8‰,我国2018年启动新生儿先天性心脏病筛查,健康中国行动推进委员会办公室2019年7月25日新闻发布会显示国内CHD仍居出生缺陷首位,CHD介入诊疗种类广、需求量大,本研究中以未成年为主分布于各年龄段,VSD、合并或复杂CHD辐射剂量较高,CD有8例(3.4%)超过1 Gy,甚至有达到4 Gy,存在较高辐射组织效应风险及随机效应发生概率。由此,CHD介入诊疗中辐射剂量控制应引起高度重视。
CHD患者在介入诊疗中影响辐射剂量因素多与患者个体差异及病情复杂程度、术者诊治水平及辐射剂量控制、放射技师配合默契程度均有关联。我国2008年才开始实施介入医师及单位准入制、培训基地评审,指导CHD介入诊疗规范开展,但介入医师少、培养缓慢,介入治疗已进入平台期[10],术中辐射防护意识及技能未免参差不齐,而DSA设备厂家参数设置并不一致,放射技师对曝光参数调节又缺乏统一标准,同年龄段、同病种、同术式辐射剂量难免存在差异。本研究为同DSA设备连续5个月开展介入诊疗监测数据,包括婴儿、幼儿、儿童、少年、中年、老年不同患者群体,涵盖PDA、ASD、PS、VSD、PFO及其他合并或复杂先天心脏畸形,涉及不同介入医师团队和DSA设备放射技师,在满足诊疗需求下总体及各分组的不同辐射剂量参数个体之间差异较大。长期以来,国内CHD介入诊疗多注重手术技巧、疗效及并发症,辐射剂量控制意识相对薄弱,不除外个别医院或术者使用成年人曝光参数对未成年人实施。国内介入诊疗并未制定辐射剂量参照水平,而国外依据辐射剂量参照值促进介入诊疗辐射剂量控制,美国2017版辐射剂量参照值比2014版已有所下降[11]。
CHD介入诊疗应在保证临床需求下通过各种措施避免或减少患者不必要的照射、最大限度降低辐射剂量,减轻患者潜在辐射伤害。①强化放射防护、辐射安全与防护、DSA设备性能及操作、CHD介入诊疗技能培训,依据具体从事放射专业细化培训具体内容,线上实名认证、人脸识别、实时监控,促使介入放射全员资质控制。②高度重视设备验收、状态及稳定性检测,尽可能选用高量子探测效率探测器,保证安装皮肤间隔器安防止焦皮距过近,及时准直矫正X线球管,控制漏射线及散射线,配备可靠防护设备或设施,尤其是为未成年人及育龄群体提供专用防护用品,确保X线质量、性能、防护安全。③术前应对患者病情充分论证、权衡辐射实践正当性,非全麻手术应与患者耐心沟通注意配合事项,依据患者具体情况制定个性化诊疗方案,检查程序与曝光参数选择应严格遵循低辐射剂量原则(as low as reasonably achievable,ALARA)。④术中严格控制照射野,对特定兴趣区使用准直等措施,为非照射区及敏感区屏蔽保护,对≤1岁婴儿诊疗时如视野(field of view,FOV)<20 cm应去除防散射光栅。利用CAREmonitor功能输入患者身高及体重,同步调整检查程序参数,及时处理图像并记录分析辐射剂量数据防止皮肤或其他组织累积剂量过大。⑤术中及时升高诊疗床使患者与X射线球管尽可能远、尽量降低数字平板探测器贴近患者使之与皮肤保持在5 cm以内。减少或避免采用穿透患者密度过大的体位,尽可能多角度分散照射避免同区域长时间剂量累积。选择暴露区域小、限束的最大FOV,待虚拟限束稳定后才行透视或摄影采集。用上序列末帧图像提供静态图像作参考,保持无辐射时才对患者进行重新定位。采用透视存储功能减少高剂量率摄影采集[12],如ASD以透视为主。利用影像自动回放、影像冻结、路图等功能帮助定位导管减少采集次数,最大限度减少透视及摄影采集,非必要时不要开启曝光开关,诊疗完成及时关闭射线。
强化儿童心脏及介入培训基地建设,规范培养CHD诊疗后备人才,借助非辐射手段避免或减少不必要的辐射实践。①重视CHD临床及介入医师培养,熟知各种CHD血流动力改变、诊疗方法及远期预后,切实提高诊治水平和治疗经验。②利用经胸超声(transthoracic echocardiography,TTE)在介入诊疗术前评估、术中监测封堵、定位[13];或直接引导下经皮开展简单CHD介入治疗,必要时合并DSA设备引导下完成;或全程引导下非体外循环外科微创封堵。③严格把握手术指征,紧密结合传统外科技术与经皮心导管技术,全程在经食管超 声(transesophageal echocardiography,TEE)监 测下微创完成手术。④采用心内超声(intracardiac echocardiography,ICE)[14]是将超声探头经外周静脉入径送至心腔内指导CHD介入封堵;⑤利用人工智能(artificial intelligence,AI)[15]在CHD预测、智能诊断、医学图像分割和识别以及临床决策支持等方面为心脏儿科医师减少诊断和治疗偏差,以选择最佳个性化治疗方案、术者决策和修复时机。
CHD介入诊疗应参照国外依据多介入中心建立辐射剂量参考值;为介入医师和放射技师术中辐射剂量控制进行效果评估和改进。①利用互联网大数据、云计算、区块链等智慧信息数据处理技术,将介入辐射剂量结构性数据融入临床信息系统和影像信息数据系统构建介入影像数据库。②统一各类型DSA设备剂量参数设置,依据患者年龄、体质指数、疾病种类及复杂程度分类,开发辐射剂量统计评估软件,自动同步实时监测辐射剂量数据至辐射剂量数据系统,通过单中心介入影像数据库制定本中心参照值。③克服各中心数据独立、信息封闭孤岛,整合各中心介入影像数据库,实现各中心数据互联互通、信息共享、交换融合,制定国内辐射剂量参照水平,与国外介入辐射剂量参照值对比,及时改进辐射剂量控制中的短板与不足。④系统梳理数据库资源,强化数据安全、隐私泄露、伦理规避等问题,推动医疗数据库建设健康发展,为CHD患者介入诊疗辐射剂量控制提供保障。
总之,CHD介入诊疗应高度重视辐射剂量控制问题,提高术者及介入放射技师辐射剂量控制意识,采用多种手段减少或避免辐射暴露,通过数据库建立辐射剂量参照值,最大限度降低曝光时间,避免或减少不必要的辐射实践,防止组织效应发生,降低随机效应发生概率,促进CHD诊疗效益最大化,确保介入诊疗创造医学和社会价值获得最佳效益。

