超声乳化联合房角分离术治疗原发性闭角型青光眼合并白内障的临床疗效观察△
平丽 田秀红 姚帮桃
(1.天津市蓟州区人民医院眼科 天津 301900;2.南京市溧水区人民医院眼科 南京211200)
原发性闭角型青光眼(primary angle closure glaucoma,PACG)是一种眼科常见病和多发病,它是由于眼内前房角关闭导致了房水引流途径受阻,从而引起眼压升高并伴随着眼部组织病理性改变的眼科疾病[1]。该病的病因尚未被明确阐述,可能与瞳孔阻滞、高褶虹膜或与晶状体较厚或位置靠前等因素有关[2]。大多数患者常合并年龄相关性白内障,倘若治疗不及时,将会对患者视功能造成不可逆转的损伤,甚至导致失明,严重影响生活质量和信心。传统观点上,针对PACG合并白内障患者主要先采用单纯小梁切除术建立新的外引流途径缓解眼压,待病情平稳后再择期行白内障手术以提高患者视力。但随着眼科显微手术日新月异的进步,越来越多的眼科手术者采用一期青光眼白内障联合手术方式并取得了良好的疗效。本研究中,我们采用超声乳化人工晶状体植入联合房角镜辅助下房角分离术(phacoemulsification with intraocular lens implantation and gonioscopy assisted goniosynechialysis,Phaco-IOL-GSL)的三联疗法治疗合并有白内障的PACG患者,并对其术后眼压、最佳矫正视力(best corrected visual acuity, BCVA)、中央前房深度及并发症等资料进行详细分析,现总结如下。
1 资料与方法
1.1 资料 收集2016年2月~2019年6月期间在天津市蓟州区人民医院眼科就诊的房角粘连均≥180o的PACG合并白内障患者52例(59眼),其中男性21例(23眼)、女性31例(36眼),年龄54~76岁,平均年龄(62.8±5.8)岁。所有患者随机分为观察组28例(32眼)、对照组24例(27眼),观察组应用Phaco-IOL-GSL,对照组应用超声乳化人工晶状体植入联合小梁切除术(phacoemulsification with intraocular lens implantation and trabeculectomy,Phaco-IOL-Trab)。患者术前年龄、性别、眼压、BCVA及中央前房深度比较,差异无统计学意义(P>0.05)。
入选标准:①符合原发性青光眼的诊断标准,且前房角镜下证实房角前粘连关闭(peripheral anterior synechiae,PAS)≥180o;②白内障核硬度分级为Ⅱ~Ⅳ级;BCVA≤0.5;③有意愿行手术治疗者;④无全身严重基础疾病;⑤临床随诊资料完整。
排除标准:①合并有眼内手术禁忌证患者;②既往有严重眼部外伤或眼部手术的患者;③合并有心、肝、肺、肾脏等严重全身基础疾病的患者;④依从性差不能配合治疗和随诊的患者;⑤有严重精神疾病的患者;⑥随诊资料不全者。
1.2 方法
1.2.1 手术方法 手术均由同一名经验丰富的眼科医师在同一台手术显微镜下完成。观察组应用Phaco-IOL-GSL,对照组应用Phaco-IOL-Trab。观察组:常规消毒铺巾后,开睑器开睑,聚维酮碘稀释后冲洗结膜囊,乳化专用刀分别于11:00方位做透明角膜切口,2:00方位做侧切口,前房内充满透明质酸钠,连续环形撕囊,超声乳化吸除晶状体核,I/A彻底吸除皮质,植入IOL于囊袋内;然后虹膜根部360o注入透明质酸钠以撑开前房角,前房角镜下应用虹膜恢复器将广泛粘连的房角组织仔细分离开,直至暴露出睫状体带,吸净透明质酸钠,水密封角膜内切口。对照组:术前准备同观察组,同样行聚维酮碘冲洗结膜囊后,做以上穹隆为基底部的结膜瓣,巩膜隧道刀于11:00方位做约1/2巩膜层厚的巩膜隧道切口,制作4.0 mm×4.0 mm巩膜瓣,穿刺刀平行于虹膜平面进入前房,3:00方位做侧切口,前房内充满透明质酸钠,连续环形撕囊,超声乳化吸除晶状体核,I/A彻底吸除皮质,植入IOL于囊袋内,切除3.0 mm×1.5左右的小梁组织,并行虹膜周边切除,整复上方结膜瓣。术毕涂典必殊眼膏后单眼包扎。
1.2.2 检测指标 所有患者术前、术后均行全面仔细的眼科检查,使用日本拓普康光学相干层析扫描仪检测眼前节中央前房深度,重复测量3次,取平均值。术后1个月、3个月随诊复查,随诊资料包括眼压、BCVA、中央前房深度,并详细评估手术成功率及有无严重并发症的发生,比较2组间手术前后数据资料,观察有无统计学差异。统计时BCVA需换算成logMAR BCVA。
1.2.3 手术成功判定 手术成功:无需任何处理,眼压可控制至21.0 mmHg或以下。手术失败:至少3次测量眼压≥22.0 mmHg,或术后有较大范围的PAS复发(PAS≥180o)。
1.3 统计学处理 采用SPSS19.0统计软件进行统计学分析。对计量资料进行正态性检验和方差齐性分析,若满足正态分布且方差齐,组间比较采用独立样本t检验;若满足正态分布但方差不齐,采用校正t检验。采用配对样本t检验对术前与术后不同时间点的参数进行比较,对计数资料的组间比较行χ2检验或Fisher确切概率法。P<0.05为差异有统计学意义。
2 结果
2.1 术前一般资料比较 术前观察组和对照组之间在年龄、性别、眼压、BCVA及中央前房深度方面比较,差异无统计学意义(P>0.05),见表1。
2.2 手术前后眼压、BCVA和中央前房深度的比较 术后1个月,2组的眼压、BCVA及中央前房深度均优于术前(P<0.05),差异有统计学意义(P<0.05),术后2组的眼压均较术前明显降低,BCVA明显提高,中央前房深度明显加深,见表1。
2.3 术后眼压、BCVA和中央前房深度的比较 术后1个月、3个月,观察组的眼压、BCVA与对照组比较差异无统计学意义(P>0.05),而观察组术后中央前房深度优于对照组(P<0.05),见表1。
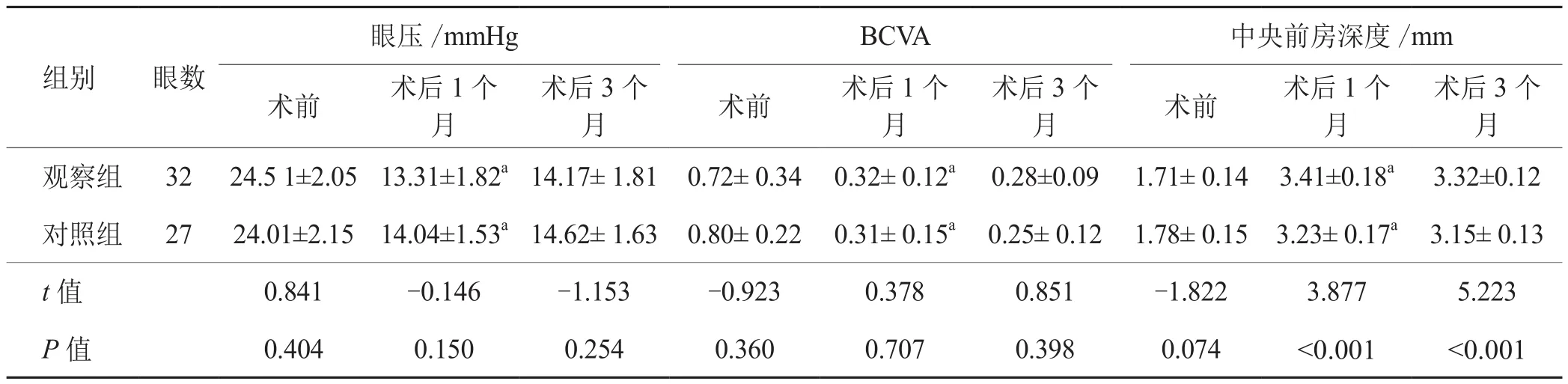
表1 2组患者术前、术后眼压、BCVA、中央前房深度比较
2.4 术后3个月手术成功率和术后并发症的比较 术后3个月,观察组的手术成功率和对照组比较差异无统计学意义(P>0.05),2组术后并发症比较差异有统计学意义(P<0.05),见表2。2组术后随访期间均未见明显严重并发症,如后囊膜破裂、脉络膜脱离、恶性青光眼。

表2 术后3个月2组间成功率和各类并发症比较
3 讨论
PACG是一种由于眼内前房角关闭导致了房水引流途径受阻,从而引起眼压升高并伴随着眼部组织病理性改变的眼科疾病,好发于老年女性[1],其发病机制尚不明确。PACG在亚洲比较流行,中国人群中有近40%比例的PACG患者单眼或双眼致盲[3]。大多数患者常合并年龄相关性白内障,且随着患者年龄的增长和白内障的进展,PACG患者的前房角则更加狭窄,房水外引流途径愈加受阻,治疗若不及时,将会对患者视神经造成不可逆转的损害。
临床上,PAS是PACG患者眼部特征性病理改变之一,急性期PACG患者PAS的主要原因可能是瞳孔阻滞,而慢性期的PACG患者,PAS则可能受多重因素的影响[4]。当PAS范围比较局限时,单纯行激光周边虹膜切除术或联合激光虹膜成形术可作为治疗PACG的首选手段[5]。然而,目前针对PAS广泛粘连的PACG伴有白内障患者,则在治疗原则尚有争议,既往观点倾向于先施行小梁切除术,再择期行白内障手术[6]。小梁切除术可建立新的房水外引流途径,从而达到降低眼压的效果。随着眼科显微技术的发展,应用Phaco-IOL-Trab治疗合并有白内障的PACG患者,可取得不错的疗效,但也可发生一些并发症,包括术中前房出血,术后浅前房、滤过泡渗漏、滤过泡瘢痕化等[7]。
尽管有报道[8]单纯Phaco-IOL治疗PACG不仅可解除瞳孔阻滞,减轻睫状突位置的前移,可有效降低一些青光眼的眼压水平,而且可明显提高患者的术后视力。但是这种治疗方式并不适用于临床上所有的PACG患者,特别是对于眼压不易控制的复杂性青光眼或者前房角关闭超过180o的青光眼患者,其对于虹膜高褶型青光眼的眼压控制效果也不佳,且在一些慢性PACG患者中,行Phaco-IOL术后周边房角前粘连状态仍会持续存在。此外,术后的炎症反应可能会进一步加重前房角粘连[9]。
Phaco-IOL-GSL则有如下优势:①Phaco-IOL-GSL可松解广泛粘连的房角,使得房角重新开放,加深前房深度,恢复小梁网功能,从而达到降低眼压的作用;②Phaco-IOLGSL将厚度为5.5 mm左右的晶状体置换为不到1.0 mm的IOL,解除患者的瞳孔阻滞状态,显著增加房角空间,解除了前房的拥挤[7];③Phaco-IOL-GSL置换了混浊的晶状体,可明显提高患者视力;④Phaco-IOL-GSL术中手柄灌注可能会促进前房角的重新开放,通过冲洗再次通畅小梁网及前房角组织,超声波可能激活小梁网滤过功能或睫状体的分泌功能[10];⑤Phaco-IOL-GSL采用的是透明角膜切口,Phaco-IOL-Trab采用的是巩膜隧道切口,Phaco-IOL-GSL切口相对较小,研究证实其术后角膜散光更小、泪膜稳定性更佳[11]。Tian等[12]应用Phaco-IOL-GSL治疗PACG患者,研究中将患者分为急性期组和慢性期组,发现术后2组均眼压控制良好,极少数患者术后出现PAS复发,慢性组炎症反应较轻,但PAS的概率高于急性组,时间节点基本上发生于术后1个月之内。
本研究中,采用Phaco-IOL-GSL治疗PACG患者28例(32眼),术后1个月随访,发现2组术后的中央前房深度较术前明显加深,而观察组术后中央前房深度明显优于对照组(P<0.05)。Phaco-IOL-GSL不仅摘除了混浊膨胀的晶状体,导致晶状体虹膜隔后移,增加了前房空间,而且解除了PAS,开放了拥堵粘连的前房角,重建了虹膜生理解剖,且不干扰房水的分泌,这些多重协同因素能够使患者术后中央前房深度在一定程度上获得更加持续满意的加深[7,10]。术后1个月、3个月,2组患者眼压术后差异无统计学意义(P>0.05),眼压预后可能与术后PAS再复发范围大小或前房角小梁网功能是否恢复等因素有关。但目前国内外学者意见尚存在分歧,且此研究并未区分急性和慢性闭角型青光眼,考虑到观察组和对照组的前房角数据缺乏一定的可比性,故仅仅着重关注了术后眼压变化和中央前房深度。虽然有一部分患者术后用房角镜观察了前房角的情况,但并未对其进行详细数据统计。在手术并发症方面上,观察组术中前房出血1眼,术后前房反应3眼,术后浅前房0眼;对照组前房出血7眼,术后前房反应10眼,术后浅前房5眼,2组间差异有统计学意义(P<0.05),表明Phaco-IOL-GSL治疗合并有白内障的PACG患者比Phaco-IOL-Trab安全性更高。本研究中所有PACG患者均是在眼压控制平稳并维持一段时间后进行手术的,避免了高眼压下手术的很多术后并发症。另外,房角分离手术是在前房角镜的辅助下完成的,操作动作轻柔,可减少无前房角镜非直视盲目分离前房角,避免了房角撕裂,减少前房出血和术后炎症反应等诸多并发症的发生[13]。且有研究[12]证明,应用Phaco-IOL-GSL分离非急性的PAS术后前房炎症相对较轻;反之,小梁切除术直接损伤了虹膜组织,可能会导致前房内前列腺素和白三烯等炎症介质的大量释放,从而加重炎症。这些原因可能解释了为何观察组术后炎症反应较之对照组炎症更轻。
本研究存在一定局限性。首先,患者样本量相对较少,随诊时间较短,需要大样本多中心的长期研究进一步证实;其次,未将患者分为急性组和慢性组,未详细区分病情严重程度,亦未关注前房角的变化情况,故缺乏急、慢性组间相关数据资料的对比分析;再次,对照组术中、术后均未使用抗代谢药物,可能会影响滤过通道及眼压控制情况,从而影响手术远期效果;最后,所有受试人群均为中国人,故结论不适用于外国人群。
综上所述,本研究结果显示观察组和对照组在随访期间术后眼压、BCVA和中央前房深度较术前差异均有统计学意义,中央前房深度及术后并发症上2组间比较差异有统计学意义,表明Phaco-IOL-GSL治疗合并有白内障的PACG患者可解除瞳孔阻滞,分离粘连的前房角,恢复小梁网功能,有效控制眼压,并显著提高视力,较Phaco-IOL-Trab疗效更确切,安全性更高,值得在眼科诊疗工作中进一步推广。

