不饱和聚酯树脂促进剂乙酰丙酮的合成研究
王坤
(新沂市星辰新材料科技有限公司, 江苏 新沂 718100)
乙酰丙酮(AA)是典型的1,3-二羰基化合物,作为一种中间体,在医药化工领域中有着广泛的应用范围。在医药工业中,我国主要用于合成磺胺二甲嘧啶,抗病毒剂WIN51711的中间体3,5-二甲基异噁唑,糖尿病药物AD-58的中间体,3,5-二甲基吡唑以及用于Combes合成法合成喹啉衍生物等[1~3]。在欧美兽药和饲料添加剂行业中,主要用于合成具有抗菌作用的痢菌净和抗鸡球虫的尼卡巴嗪的原料4,6-二甲基-2-嘧啶醇[4~6]。在日本主要用在开发催化剂和助催化剂相关领域,如用于环辛四烯、醌、醌氢醌羰基化反应,不饱和酮等低分子化合物的合成,氧化促进剂,石油裂解、催化加氢和异构化催化剂,以及低级烯烃的聚合、1,3-二烯烃的共聚等高分子化合物的合成[7~11]。以乙酰丙酮为试剂,通过利用分光光度法测定水、空气等体系中甲醛与乙酰丙酮生成的黄色化合物以此来确定体系中甲醛的含量。此外在树脂和膜的相关行业,其与金属离子生成的乙酰丙酮盐也有广泛的应用如:催化剂,树脂交联剂,树脂硬化促进剂,橡胶添加剂,超传导薄膜、热线反射玻璃膜以及透明导电膜的形成剂;用作汽油、润滑油、胶粘剂的添加剂,油漆、涂料和印花油墨的干燥剂,醋酸纤维溶剂[11~15],镀金属的原料等;乙酰丙酮是二齿配体螯合剂,可作为分析试剂检测大多数的金属离子,用作萃取剂萃取稀有的贵金属,如:合成乙酰丙酮三苯基膦羰基铑用于氢甲酰化,加氢,羰基合成等反应;乙酰丙酮稀土金属配合物在新型发光材料,萃取化学,位移试剂等方面具有广泛应用前景[16];乙酰丙酮铁作为一种塑料光降解高效光敏剂备受关注,在工业生产和环境化学方面有重要意义。以及用于处理无机材料,除去多孔性固体的金属氧化物,以增加颗粒表面积及吸附能,由于用无机酸处理时,颗粒本身也容易被破坏,而通过乙酰丙酮处理则不会出现如此问题。因为金属氧化物很容易与乙酰丙酮形成螫合物而溶解,避免破坏颗粒本身的结构。
因为乙酰丙酮下游产品种类多样、走势良好,需求量很大,市场前景优良。但目前国内乙酰丙酮总的生产能力约为11 kt/a,且使用工艺技术落后,难以满足国内消费量的不断增长,存在较大的乙酰丙酮的需求缺口,所以不得不需要从日本、德国、美国、瑞士等国家大量进口,以此来满足与乙酰丙酮相关行业的发展需要。并且根据科学发展的绿色化学理念,发展高选择性、高效的催化剂,简化反应步骤,减少污染排放,开发新的洁净生产技术,实现高效的化学反应,实现“零排放”的生产工艺迫在眉睫,以此使企业发展创造出良好的经济效益和社会效益,在绿色化学领域有着重要的应用意义。
合成乙酰丙酮的方法比较多,目前用于生产乙酰丙酮的主要合成线路有:丙酮—乙酸乙酯法、丙酮—醋酐法、乙酰乙酸乙酯—醋酐法、乙烯酮—丙酮法、丙炔—醋酸法。
丙酮线路收率最低,且工艺复杂、能耗高,不满足绿色化学的理念以及当今低碳环保的经济要求,不予考虑。丙酮—醋酐、丙酮—醋酸乙酯路线要用到危险化学品,存在安全隐患,且还存在一定的工艺优化问题,本文不予考虑。丙炔—醋酸线路需用到大量丙炔,需要依托大型炼油厂产生丙炔作为反应原料,因此也不便于推广建设。
余下的两条线路,收率相差无几,但乙酰乙酸乙酯—乙烯酮法工艺复杂、投资大,乙酰乙酸乙酯—醋酐法工艺简单、设备要求低、投资小、在实验室容易进行理论研究,也适合中小型企业将其发展推广。因此研究乙酰乙酸乙酯—醋酐法更具有更好的实际意义。
本文希望根据前人研究成果,通过进一步研究,了解乙酰乙酸乙酯—醋酐法的反应历程,突破关键技术难点,需找合适的反应条件,进一步对反应工艺进行优化,以提高原料转化率、减少副反应的发生,为扩大生产提供数据及经验,使乙酰乙酸乙酯—醋酐法投产工业化成为可能。促进乙酰丙酮相关行业的蓬勃发展,创造更多的经济效益与社会效益。
1 实验部分
1.1 实验主要仪器
SXCL-3型数显加热磁力搅拌器,郑州市博科仪器设备有限公司;DF-101Z集热式恒温加热磁力搅拌器,上海亚荣生化仪器厂;旋转蒸发器RE-52C,巩义市予华仪器有限责任公司;SHZ-D循环水式真空泵,上海精宏实验设备有限公司;ZF-I型三用紫外分析仪,上海精宏实验设备有限公司;DHG-90114型电子天平,上海亚荣生化仪器厂;KQ超声波清洗器,常熟市天量仪器有限责任公司。
1.2 实验药品
乙酰乙酸乙酯,分析纯,成都科龙化工试剂厂;乙酸酐,分析纯,重庆西南化学试剂有限公司;轻质氧化镁,分析纯,湖南湘中化学试剂有限公司;乙酸乙酯,分析纯,成都科龙化工试剂厂;乙酰丙酮,分析纯,中国医药集团上海化学试剂公司。
1.3 实验原理
1.3.1 合成原理
乙酰乙酸乙酯—醋酐法合成乙酰丙酮采用乙酰乙酸乙酯与醋酐混合在催化剂作用下加热生成乙酰丙酮,乙酸乙酯,二氧化碳。反应过程中需要将生成的乙酸乙酯不断蒸出,促进反应的发生生成乙酰丙酮粗品。合成线路如下:
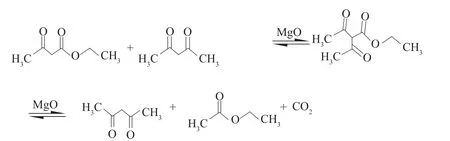
在确定合成路线后,就必须搜集整个路线中涉及到物质的物性参数,为开发工艺过程奠定基础,对相关安全、检测分析、设备、运输做出一定的思考。
1.3.2 提纯原理
(1) 蒸馏与分馏原理
蒸馏:
液态化合物的蒸汽压随温度升高而增大。当液体的蒸汽压增大至与外界压力相等时,即有气泡从液体内部溢出,这种现象成为气化。液体内部不断气化及为沸腾,这时的温度成为该液态化合物在当时大气压下的沸点,通常以101.325 kPa(1arm)作为外压的标准。
将液体加热至沸点,该液体开始沸腾而逐渐变为蒸气,使蒸气通过冷凝装置进行冷却,便凝结并再度获得这一液体,这种操作成为蒸馏。因此,蒸馏包括两个过程,即从液体变为气体的气化过程及由气体变为液体的冷凝过程。若有两种互溶的液体混合在一起,由于其蒸汽压不同,所以蒸气中两个成分的比例与液体混合物中两个成分的比例不同。蒸汽压大(即沸点低)的成分在气相中占的比例较大,若将这部分蒸气冷凝下来,那么所得的冷凝液中低沸点的成分就比原混合物的增多。重复把这部分冷凝液进行蒸馏,便有可能将液体混合物中具有不同沸点的成分逐渐分开。
分馏:
分离效率高于蒸馏(被分离组分的沸点差达150 ℃才能用蒸馏法充分分离)。实际是沸腾气化的混合物蒸气通过分馏柱并进行一系列的热交换结果。当蒸气进入分馏柱时,由于柱受外面空气的冷却,蒸气中沸点较高的物质先被冷凝,结果冷凝液中含有较多高沸点的物质,蒸气中低沸点成分就相对地增多。冷凝液向下流动时又与上升的蒸气接触(在填料表面进行),两者之间进行热交换,上升的蒸气中高沸点的物质又被冷凝下来,低沸点物质蒸气继续上升;冷凝液中低沸点的物质被气化,而高沸点者仍呈液态。经过多次的液相与气相的热交换之后,低沸点的物质不断上升,最终被蒸馏出来,而高沸点的物质则不断流回热容器中,结果使不同沸点的物质得到分离。
(2)蒸馏操作的应用
凡加热到沸点而不分解的化合物,都可以进行蒸馏。主要用于:
a.分离液体化合物,但只能当混合物各成分的沸点间有较大差异(如30 ℃以上)时才能有效地进行分离;
b.测定化合物的沸点;
c.提纯液体及低熔点固体,以除去不挥发的杂质;
d.回收溶剂,或浓缩溶液。
因乙酰乙酸乙酯与乙酰丙酮沸点相差不是特别大,所以要实现乙酰乙酸乙酯与乙酰丙酮的充分分离最好选择分馏操作。
1.3.3 实验装置
合成装置如图1。150 mL的三口瓶被固定在铁架台上,烧瓶的有口插上0~200 ℃的水银温度计,用于检测控制反应液温度,左口用塞子塞住,中口插蒸馏头,组装成蒸馏装置。由于乙酸乙酯沸点77 ℃,易气化,所以反应生成的乙酸乙酯容易蒸出。以此用来促进反应的正向进行。反应完全之后经过抽滤,将滤液装入精馏装置,精馏收集相应馏分。
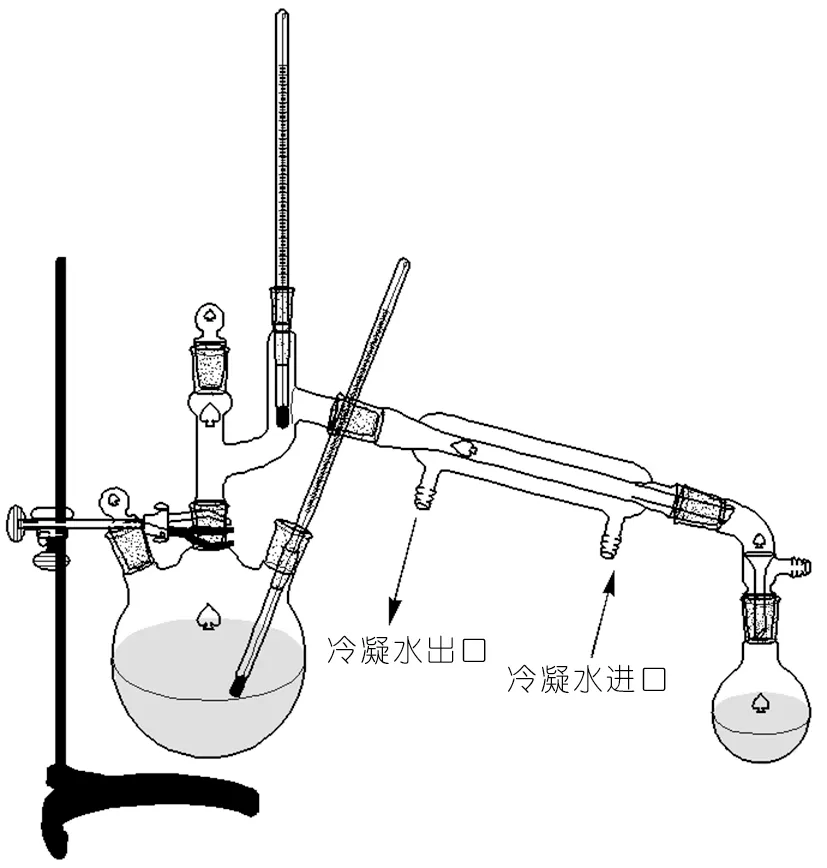
图1 合成装置示意图
2 实验结果与讨论
有文献表明,乙酰乙酸乙酯—醋酐法制乙酰丙酮路线中可以用Al2O3,MgO两性氧化物或碱土金属氧化物做为反应的催化剂,因此考虑用ZnO,CaO作为代替物以探究其是否也有相关的催化作用并验证这些氧化物的催化效果,以确定最好的催化剂。
2.1 Al2O3作为催化剂
操作:取1.3 g乙酰乙酸乙酯和1.2 g醋酸酐,加入0.015 g Al2O3在125 ℃反应。
现象:约反应40 min后,反应液呈淡黄色。随着时间的进行逐渐加深。130 min后点板分析,结果如图2。
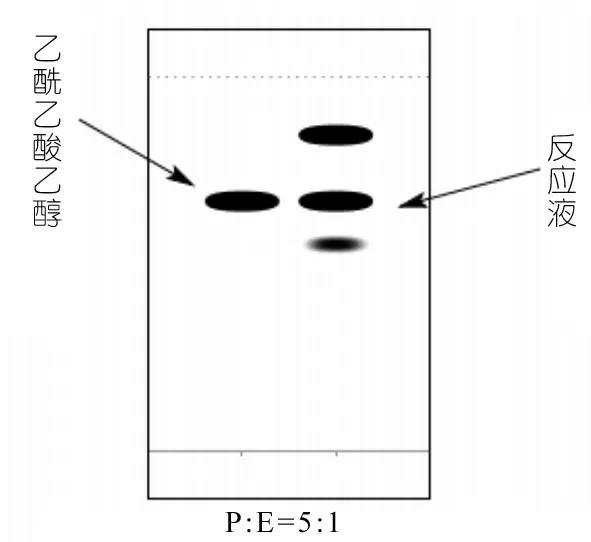
图2 Al2O3作为催化剂制备乙酰乙酸乙酯示意图
2.2 ZnO作为催化剂
操作:取1.3 g乙酰乙酸乙酯和1.2 g醋酸酐,加入0.015 g ZnO在135 ℃反应。
现象:约反应40 min后,反应液呈淡黄色。随着时间的进行逐渐加深。90 min后点板分析,结果如图3。
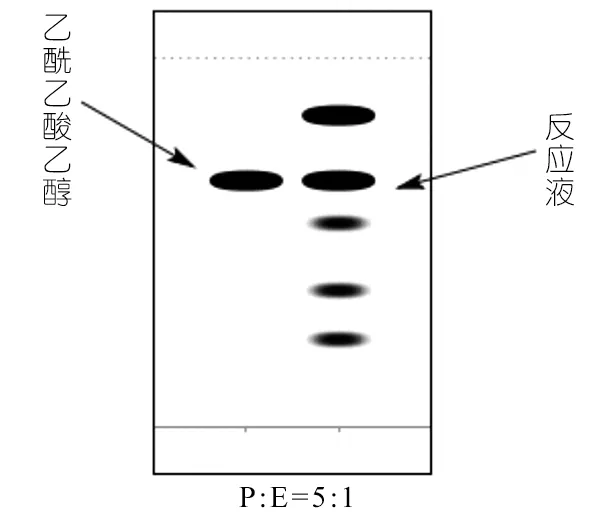
图3 ZnO作为催化剂制备乙酰乙酸乙酯示意图
2.3 CaO作为催化剂
操作:取0.66 g乙酰乙酸乙酯和0.6 g醋酸酐,加入0.015 g CaO在135 ℃反应。
现象:约反应40 min后,反应液呈淡黄色。随着时间的进行逐渐加深。2.5 h后点板分析,结果如图4。
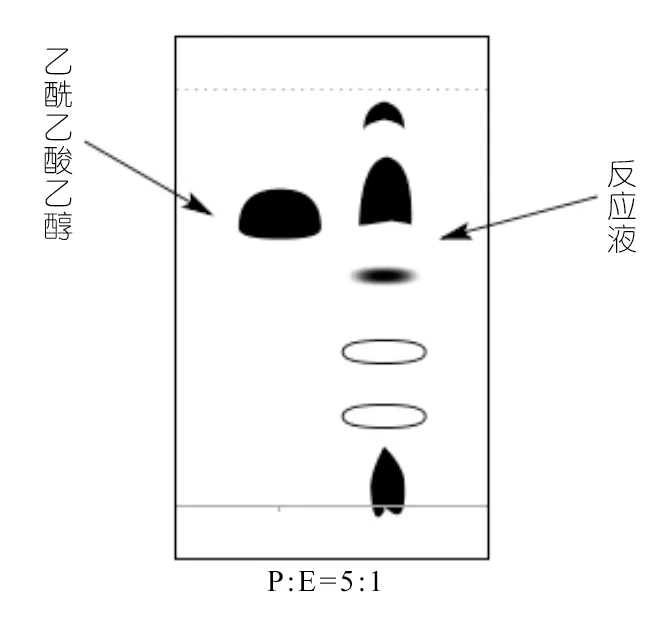
图4 CaO作为催化剂制备乙酰乙酸乙酯示意图
2.4 MgO作为催化剂
操作:取39 g乙酰乙酸乙酯和33 g醋酸酐,加入1.75 g MgO在135℃反应。
现象:在逐渐升温过程中,当温度高于100 ℃,反应液开始变澄清,溶液淡黄色逐渐加深。随着时间的进行逐渐加深。6.5 h后点板分析,结果如图5。

图5 MgO作为催化剂作为催化剂制备乙酰乙酸乙酯示意图
根据板上的情况可以得知,反应是属于一个平衡反应,反应在相当长的一段时间里都还有原料存在,不能够完全反应。所以就要求在催化剂作用下,原料能在长时间加热条件下,不产生副反应,要求反应单一。从上述结果来看,Al2O3、ZnO、CaO都不适合用于催化乙酰乙酸乙酯生成乙酰丙酮,所以MgO便是最为适合作为催化剂。
2.5 TLC上点的分析
根据乙酰乙酸乙酯—醋酐法的反应历程,得知反应会产生中间产物二乙酰乙酸乙酯,所以反应过程中板上至少会出现三个点--乙酰乙酸乙酯、二乙酰乙酸乙酯、乙酰丙酮。那么这三个物质在TLC中对应的位置应该在什么地方呢?对此做了如下实验:将乙酰乙酸乙酯钠盐与醋酸酐混合加热搅拌。
反应结果在TLC上的表现如图6。
并且将钠盐反应液加入盐酸水解发现图6中第一个点消失了,第四个点依旧存在。以及在跟踪MgO作催化剂的实验中发现反应到最后,第一个点会消失转化为其他物质。由此可以推测第一个点为二乙酰乙酸乙酯。
以MgO作催化剂的实验中,反应液蒸馏得到馏分温度为132~138 ℃无色透明液体物质。TLC检查,与标准品对照,显示为图6第二点的位置,因此初步可以断定第二个点为产物点。
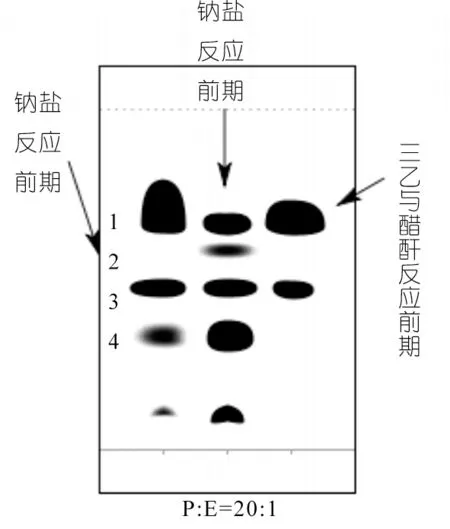
图6 三种产物在TLC中对应位置
2.6 实验中出现的问题与解决办法
2.6.1 加热器的选择问题
根据文献所述重复实验,发现催化剂MgO会与反应液产生大量的白色沉淀。使得反应液黏度增大,无法搅动。因为乙酰丙酮是一个非常常见的二齿配体,能与大多数金属离子形成配合物,如:Fe,Co,Ni,Cu,Zn,Al,Ca,Mg,Mo,Ru,Re,U,Th,Ce,Na,K,Rb,Cs,V,Cr,Mn等[9]。
白色固体一般是先出现在烧瓶壁上。因而最初做实验时,并不了解反应现象,用的是电热套型的加热器,因而在烧瓶的气液交界处特别容易形成固体。并且附着在瓶壁上越来越多。而且此反应所需反应时间比较长,往往要十几个小时,由于这也固体的形成以及长时间的加热,这些固体会变黑产生分解现象。
因此在以后的实验中,一律采用的是电热板加热器,使反应瓶接触热源的位置只在反应液面以下。
2.6.2 催化剂MgO的加入量问题
按照文献所述,加入相应的MgO,反应液几乎全部变成了固体,所以到底要加多少MgO作为催化剂,还需要进行实验来予以说明[11]。
2.6.3 缩短反应时间问题
由于反应时间比较长,也就是说能源与成本就相对较大,生产周期较长,相同时间产量就小。因此想办法缩短反应时间也是获得利润的有力途径。希望通过增加催化剂的量来加快反应的速率。但如前文所说增加催化剂的量会产生大量固体不利于反应。因此试图向反应体系中加入有机溶剂溶解和分散反应中的固体物质。由于根据反复实验表明,氧化镁做催化剂脱乙酸乙酯步温度应当高于120 ℃。因此想到用DMF或DMSO做溶剂进行尝试。
取1.3 g乙酰乙酸乙酯和1.02 g醋酸酐混合于50 mL单口瓶中,加入0.5 g DMF或DMSO及10%(醋酐量)的MgO进行反应。TLC检查结果如图7。
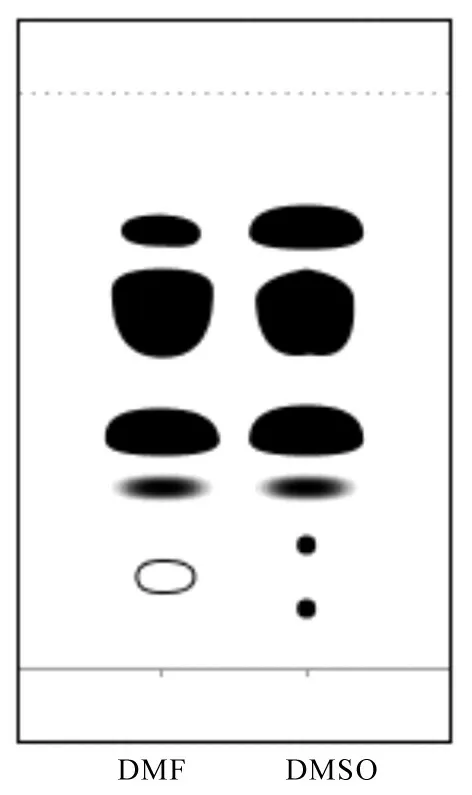
图7 TLC检查结果
反应过程中出现了更多的杂质并且随着时间的延长反应更加复杂,杂质更多。因此想通过加入溶剂以增加催化剂的量来缩短反应时间的这一想法行不通。
2.6.4 蒸馏提纯中的问题
在通过用蒸馏的方式提纯过程中,随着乙酰丙酮的蒸出,逐渐减少,使得蒸馏瓶里面蒸汽压减小,而始终在反应残夜中存在着一定量的乙酰丙酮,因此残留液应当收集在一起进一步进行蒸馏。并且在反应液的滤液中可能存在着少量的镁离子,在蒸馏过程中会形成固态物质,而且这些物质往往是先附在蒸馏的沸石表面,而使蒸馏液中的气化中心消失,产生暴沸现象。所以在蒸馏过程中往往需要用到搅拌器进行搅拌来消除暴沸现象。
2.7 最佳实验条件的选择
选定了反应路线与催化剂,就要确定反应的物料配比,反应温度,催化剂用量,反应时间,加热方式,加料方式,以得到合成乙酰丙酮最好的结果。
2.7.1 物料配比
从原料的价格上来讲乙酰乙酸乙酯与醋酸酐比较,乙酰乙酸乙酯的价格远高于醋酸酐的价格;从反应的结果上来说,醋酸酐的沸点为138.6 ℃,乙酰丙酮的沸点为140.6 ℃,而最后反应处理是依靠精馏得到产品,很难将醋酸酐与乙酰丙酮分离开,再结合化学平衡的因素,所以乙酰乙酸乙酯与醋酸酐的物料配比本实验确定为1:(1.05~1.10)之间。
2.7.2 反应温度
根据反应的现象,表明温度低于120 ℃,脱乙酸乙酯步进行缓慢。所以反应温度控制在125~145 ℃范围。
2.7.3 催化剂用量
催化剂提供反应活性中心,其数量多少对反应速度至关重要。但催化剂过多,易引起副反应生成更多副产物。例如本实验用MgO做催化剂,一般会生成相当于MgO质量3~5倍的固体。根据文献提供的资料,用相当于醋酐量3%的MgO重复实验得到大量固体,并且乙酰丙酮收率不高。选择了醋酐质量0.1%%~2.5%作为其用量的探索范围。催化剂用量—收率关系图为图8。
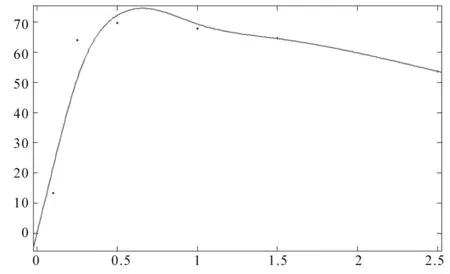
图8 催化剂用量—收率关系图
由图8可知催化剂用量为醋酐的0.65%左右对应的收率最大。
2.7.4 反应时间
根据反应实验现象,在TLC检测下发现,在MgO的催化下反应时间14 h以上乙酰乙酸乙酯才能够被作用完全。
2.7.5 加料方式
(1)反应跟踪
将26.0 g乙酰乙酸乙酯与21.42 g醋酸酐混合于150 mL三口烧瓶中加入0.021 g MgO在温度130~145 ℃下反应。30 min开始蒸出乙酸乙酯,分别在反应1 h、2 h、6 h、8 h、12 h时刻进行TLC检测,结果如图9。

图9 不同时间下反应液的变化
经过反复实验,发现每次反应都不可避免的要产生第4的一个点,且此点比乙酰丙酮的点先出现。此物质不溶于酸碱,并且使用常压蒸馏很难将其蒸出。试图通过改变加料顺序消除其产生。
(2)滴加乙酰乙酸乙酯
将0.107 g氧化镁与21.42 g醋酸酐混合于150 mL三口烧瓶中,用DF-101Z集热式恒温加热磁力搅拌器加热到120 ℃,然后开始以20 s/滴的速率滴加26.0 g乙酰乙酸乙酯。9 h后点板副反应依旧发生。经过16 h反应后,抽滤得到0.35 g固体。将滤液蒸馏,得120~130 ℃馏分4.90 g,130~140 ℃馏分9.17 g。经与标准品对照证明是同一物质,收率为70.35%。由此可知与表2.4对应的收率相差不大,所以滴加乙酰乙酸乙酯对收率没有太大影响。
(3)滴加醋酸酐
将0.107 g氧化镁与26.0 g乙酰乙酸乙酯混合于150 mL三口烧瓶中,DF-101Z集热式恒温加热磁力搅拌器加热到120 ℃,然后经过3 h将21.42 g醋酸酐滴加进反应瓶中。经过15 h反应,结果与2)相同。
最后,由于最初实验装置都是在白天进行组装,进行反应,长时间反应后反应液会变成红褐色液体。根据前文所述乙酰丙酮光照后会发生自聚反应,变为褐色液体。所以防止乙酰丙酮自聚,反应装置应该在避免光照条件下进行。
2.8 产品的精制
将20%的乙酰丙酮粗品溶于80%苯中,然后与等体积的蒸馏水振荡3h,易溶于水的乙酸分配到水相中,而乙酰丙酮则溶于苯中,再蒸去苯得到乙酰丙酮。
3 结论与展望
本文探索了以乙酰乙酸乙酯和醋酸酐为原料合成乙酰丙酮的工艺路线。确定了其最佳的原料配比,反应温度,反应时间,加热方式,催化剂种类及其用量,以及在确定反应历程的过程中对在反应中出现的问题提出了解决方案和合理的猜想,并将其做了实验验证,虽然结果并不一定是自己推测的那样,但也就证明了这样的思路行不通,以此说明在以后的工作中需要需找另外的方向来解决这些问题。该工艺为:
26.0 g乙酰乙酸乙酯与21.42 g醋酸酐在相当于醋酸酐质量0.5%的氧化镁(0.107 g)的催化剂,装入三口瓶中,控制温度在130 ℃,反应12 h,反应后期可升高温度进一步反应。总共反应15 h反应完全。其中同时蒸出反应产生的乙酸乙酯以促进反应的进行。并且应当尽量避免光照,因为乙酰丙酮在光照条件下易发生自聚现象生成棕红色物质。反应完成后将反应液抽滤,用乙酸乙酯洗涤,将滤液蒸馏,收集132 ~138 ℃馏分。收率能够达到70%。
由此工艺路线可知,该路线投资少,操作方便,设备要求简单,反应条件比较灵活,生产环保无污染。
目前生产乙酰丙酮广泛采用丙酮法,因为其原料成本低,但此法收率低,能源消耗高,设备投入大等诸多的缺点。而通过乙酰乙酸乙酯—醋酸酐法的研究得知采用乙酰乙酸乙酯—醋酸酐法优点诸多,反应比较温和,利于自动化操作,能源消耗较低,几乎不会产生“三废”问题,能够满足环保要求,但原料成本偏高。因此,一方面需要需找合适的方法,反应条件提高反应收率,另一方面想办法降低原料成本,才能带来更好的经济效益,以推动乙酰丙酮相关产业的发展。
本文在合成乙酰丙酮过程中,收率只有70%。由于时间和能力等原因,在提高其收率的工作还需要在日后进一步研究。此反应过程中产生的第四个点的副反应生成的什么物质,需要再作研究。并且有理由猜测真正促进乙酰乙酸乙酯生成乙酰丙酮的物质是第四个点的物质,因为根据实验反应跟踪的情况发现,只有当此物质生成后才会生成相应的乙酰丙酮。这一推测有待以后去证明。
以及反应生成的固体物质应该是乙酰丙酮镁,因为此固体用1:1盐酸溶解后用乙酸乙酯萃取得到了乙酰丙酮,因此它的相关处理也有待研究。

