2-羰基丙酸-2-吡啶酰腙功能化MCM-41吸附镍离子性能*
陈凤英,李海英,段玉荣,闫 宇,王 鑫
(商洛学院化学工程与现代材料学院,陕西省尾矿资源综合利用重点实验室,陕西商洛726000)
工业金属冶炼产生的废水如果未经恰当处理即向外排放,会使水体重金属离子含量急剧升高,会对人体造成不可估计的伤害[1]。重金属离子通过直接饮用水、食用被污水浇灌过的蔬菜等途径,很容易进入人体内,进而导致人体细胞发生癌变、畸形或突变等[2]。目前,处理含有重金属离子废水的方法主要有化学法、吸附法、离子交换法和生物法[3-11]等。吸附法是利用吸附剂将水体中的重金属离子富集到吸附剂上,实现水的净化。吸附法的成本相对低廉,操作简单,被广泛应用于净化含有重金属离子的废水。有序介孔分子筛MCM-41具有比表面积高、孔径分布窄、孔道规整、易于引入功能化基团等特点,作为吸附剂使用引起了人们高度的关注[12]。介孔分子筛对重金属的吸附主要是依靠表面的官能团与水体中重金属离子之间发生螯合作用,形成配位化合物,故经改性后的介孔分子筛材料通常会表现出吸附效果的显著变化[13]。镍是人体所必须的微量元素,但是人体在工作或生活环境中长期接触镍会引发皮肤炎症,增大患癌的风险[14]。因此,本文设计合成了2-羰基丙酸-2-吡啶酰腙化合物,并将其用于对MCM-41介孔分子筛的功能化,采用红外光谱法、热重和XRD对功能化后的分子筛(H2L/MCM-41)进行表征,测试了其对镍离子的吸附性能。
1 实验部分
1.1 试剂与仪器
材料:2-羰基丙酸-2-吡啶酰腙和MCM-41介孔分子筛为实验室自制,其余试剂均来自国药集团,分析纯,使用前未做进一步纯化处理。
仪器设备:5700 型红外光谱仪(美国Nicolet),UV757CRT 紫外分光光度计(上海精密仪器有限公司),NETZACH STA449C 同步热分析仪(德国耐驰),JSM-6700F场发射扫描电子显微镜(日本电子株式会社),X’Pert PRO型X射线衍射分析仪(荷兰帕纳科)。
1.2 2-羰基丙酸-2-吡啶酰腙化合物(H2L)的合成
按照1:1.1的物质的量比准确称取一定量的2-吡啶苯甲酰肼和2-羰基丙酸置于三颈瓶内,以无水乙醇为溶剂,70℃水浴加热回流反应6h,冷却、过滤、干燥得到淡黄色粗产品。将粗产物用无水乙醇重结晶,得淡黄色针状晶粒。
1.3 MCM-41分子筛的制备
实验所用钒尾矿其主要成分见表1,硅源的制备参考文献[15]。称取10g钒尾矿和22g NaOH置于烧瓶中,加入150mL蒸馏水,100℃反应6h,冷却、过滤得到硅源。

表1 实验用钒尾矿的主要成分Table 1 Main components of vanadium tailings for experiment
将一定量的CTAB溶解在2mol/L的氢氧化钠溶液中,加入硅源室温搅拌1h后,将反应物转移到反应釜中,100℃晶化3d。产物经过滤、洗涤、干燥,最后将产物在550℃活化焙烧6h,即得MCM-41介孔分子筛。
1.4 MCM-41分子筛的功能化
称取0.25g的H2L用N,N-二甲基甲酰胺配制成25 mL溶液,称取1.0g的MCM-41分子筛加入酰腙溶液中,室温下搅拌24h,使分子筛与H2L充分作用,过滤,用少量N,N-二甲基甲酰胺溶剂洗涤,空气氛中干燥得到酰腙功能化分子筛H2L/MCM-41。
1.5 吸附试验
向盛有一定体积的含镍离子模拟废水的锥形瓶中加入适量H2L/MCM-41,磁力搅拌吸附一段时间后,取上层清液离心、过滤、显色,用紫外可见分光光度计检测吸附前后溶液的吸光度,计算得到吸附剂的吸附容量(Q)与镍离子的去除率(E):
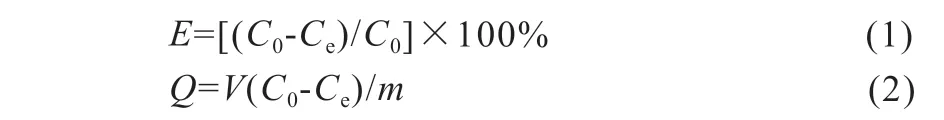
式中:C0为起始的镍离子浓度(mg/L);Ce为吸附后镍离子的剩余浓度(mg/L);V为含镍离子溶液的试验体积(L);m为吸附剂用量(g);Q为吸附容量(mg/g)。
2 结果与讨论
2.1 吸附剂的表征
图1为吸附剂MCM-41和H2L/MCM-41的XRD图谱。MCM-41的图谱在2θ=2.4°处出现了强而尖的(100)面衍射峰,与文献[12]吻合。H2L/MCM-41的XRD图谱与MCM-41相比,(100)面的衍射峰强度减小,这是由于功能化后的MCM-41的表面部分被2-羰基丙酸-2-吡啶酰腙所占据造成的。图2是吸附剂MCM-41和H2L/MCM-41的红外光谱。H2L的νC=N和νC=O分别出现在1600cm-1和1530cm-1,在H2L/MCM-41中两个峰叠加到一起,蓝移到1650cm-1处。图3是MCM-41和H2L/MCM-41在氮气气氛中,升温速率为10℃/min的热重曲线。从图3中可以看出:MCM-41失重达到平衡时,质量减少约为2.0%,这对应MCM-41表面和孔道内水的离去。H2L/MCM-41的TG曲线显示,失重达到平衡时,失重率约为16.6 %,因此H2L在MCM-41上的负载量约为14.6%。图4 为吸附剂MCM-41和H2L/MCM-41的SEM。MCM-41和H2L/MCM-41的微观形貌均为球形,MCM-41的直径约为50nm,由于H2L的负载,使得H2L/MCM-41的直径略大。
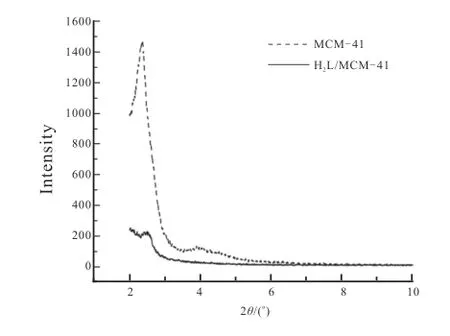
图1 吸附剂的XRD图谱 Fig.1 XRD pattern of adsorbent
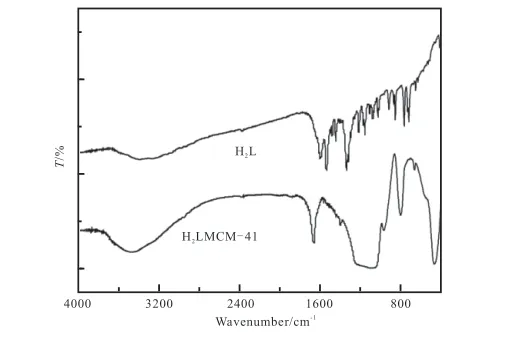
图2 吸附剂的红外光谱Fig.2 Infrared spectrum ofadsorbent
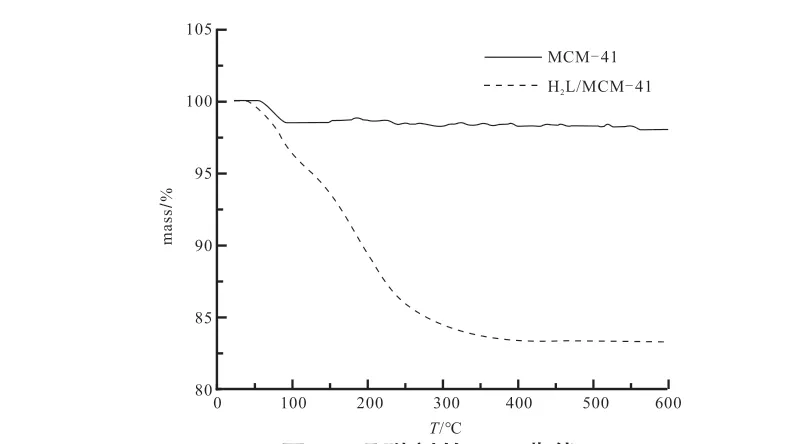
图3 吸附剂的TG曲线Fig.3 TG curve of adsorbent

图4 吸附剂MCM-41(左)和H2L/MCM-41(右)的SEMFig.4 SEM of adsorbents MCM-41 (left) and H2L/MCM-41 (right)
2.2 标准工作曲线的绘制
用分析纯硫酸镍作为镍源,配制成镍离子浓度分别为70、60 、50、40、30、20、10 mg/L的标准溶液。分别取2.5mL不同浓度的镍离子标准溶液于25mL的容量瓶中,依次滴加5mL 5% NaOH溶液,5mL 20%酒石酸钠溶液,2.5mL 4%过硫酸铵溶液和3mL 0.5%丁二酮肟溶液,用超纯水稀释至刻度,摇匀,显色25min,另外做一份空白对照溶液(不加入丁二酮肟,其他相同),用10mm的石英比色皿,在470nm波长处,测试溶液的吸光度,绘制镍离子浓度与吸光度的标准工作曲线(图5)。
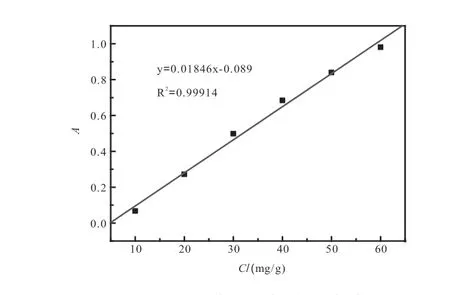
图5 镍离子的标准工作曲线 Fig.5 Standard working curves of nickel ion
2.3 吸附时间对去除率的影响
向6个各含有50mL 60 mg/L镍离子溶液的锥形瓶中分别加入0.03g H2L/MCM-41,在室温下设置集热式恒温加热磁力搅拌器的转速为600r/min,分别反应20、40、60、80、100、120 min后,取样离心、过滤后,取清液显色25min后,在470nm波长处检测显色后溶液吸光度,计算去除率,结果如图6所示。随着吸附时间的延长去除率增大,到80min基本达到平衡,这是由于H2L/MCM-41表面的孔隙逐渐被Ni离子占据并与镍离子发生配位发应,80min后吸附基本可以达到平衡,溶液中镍离子的去除率没有发生明显改变。因此,用H2L/MCM-41处理溶液中镍离子时,吸附时间选择在80min。
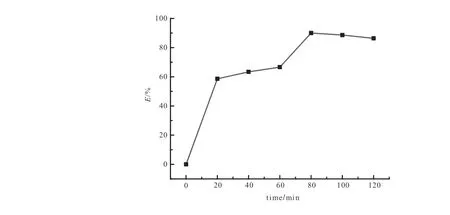
图6 吸附时间对镍离子去除率的影响Fig.6 Effect of adsorption time on removal rate of nickel ion
2.4 镍离子初始浓度对吸附性能的影响
向6个锥形瓶中分别加入25mL镍离子初始浓度为50 、60、70、80、90、100 mg/L的溶液和0.03g H2L/MCM-41,设置集热式恒温加热磁力搅拌器的转速为600r/min,在室温磁力搅拌吸附80min后,取样离心、过滤、显色,检测溶液的吸光度,计算H2L/MCM-41对镍离子的吸附容量(图7)。由图7看出,当镍离子初始浓度在50~70 mg/L范围时,吸附容量随浓度的增大而增大,当浓度超过70mg/L后,吸附量基本保持不变。这是由于当溶液体积一定时,镍离子含量随浓度的增大而增大,H2L/MCM-41对镍离子的吸附能力一定,故当吸附达到平衡后,吸附容量基本保持不变。
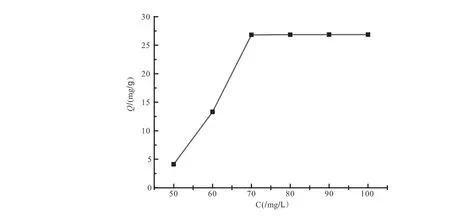
图7 镍离子初始浓度与吸附容量的关系Fig.7 Relationship between initial concentration of nickel ion and adsorption capacity
2.5 吸附剂用量对去除率的影响
分 别 称 取0.01、0.02、0.03、0.04、0.05、0.06 g H2L/MCM-41置于6个不同的锥形瓶中,加入25mL浓度为70mg/L的镍离子溶液,在室温下热磁力搅拌吸附80min后,取样离心、过滤、显色,测定溶液的吸光度,计算去除率E,实验结果如图8所示。由图8可知,在镍离子浓度为70mg/L的溶液中,吸附剂用量在0.01~0.04 g范围内,吸附剂用量与去除率呈正相关,当吸附剂超过0.04g后,虽然去除率有一定的增大,但是增大的幅度很小,考虑到实验成本因素,吸附剂用量选择0.04g。
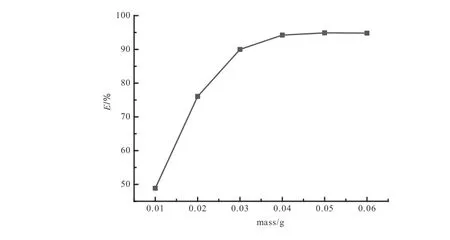
图8 H2L/MCM-41用量对去除率的影响Fig.8 Effect of H2L/MCM-41 dosage on removal rate
2.6 温度对吸附效果的影响
向5个锥形瓶中分别加入25 mL镍离子浓度为70 mg/L的模拟废水和0.04 g H2L/MCM-41,在30、40、50、60、70 ℃下磁力搅拌80min后,取样离心、过滤、显色,测定溶液的吸光度,计算吸附量,实验结果如图9所示。由图9可知,在70mg/L的镍离子溶液中,吸附剂用量是0.04g,随着温度的增加,30~60 ℃,吸附容量会随温度升高而增大;温度大于60℃后吸附容量略有下降。这可能是因为当温度升高时,分子运动速度加快,吸附反应和解附反应都加快,解附反应速率大于吸附反应速率,解附反应占据了主导地位,使得吸附量降低。
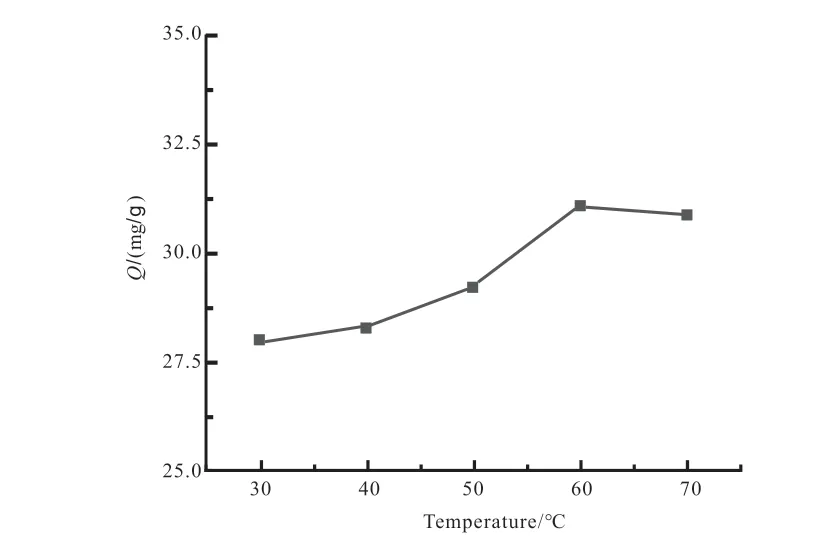
图9 温度对吸附量的影响Fig.9 Effect of temperature on adsorption capacity
2.7 吸附热力学分析
Langmuir吸附等温方程式:
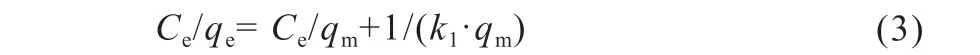
Freundlich吸附等温方程式:
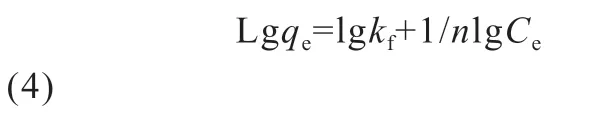
式中:qe为平衡吸附量(mg/g);qm为饱和吸附量(mg/g);k1为吸附平衡常数;Ce为吸附平衡后镍离子的浓度(mg/L);kf为Freundlich 吸附系数;n为常数,1/n用来表示吸附的难易程度。
分别用朗格缪尔(Langmuir)和弗莱特利希(Freundlich)两种等温式对H2L/MCM-41吸附热力学数据进行拟合,得到图10、图11、表2、表3。经过分析可知,H2L/MCM-41对镍离子的吸附较好地符合 Langmuir吸附等温线,相关系数为0.9860,结合试验数据通过吸附Langmuir等温线参数的进一步确定,H2L/MCM-41吸附镍离子是一个以化学吸附占主导地位的反应过程。
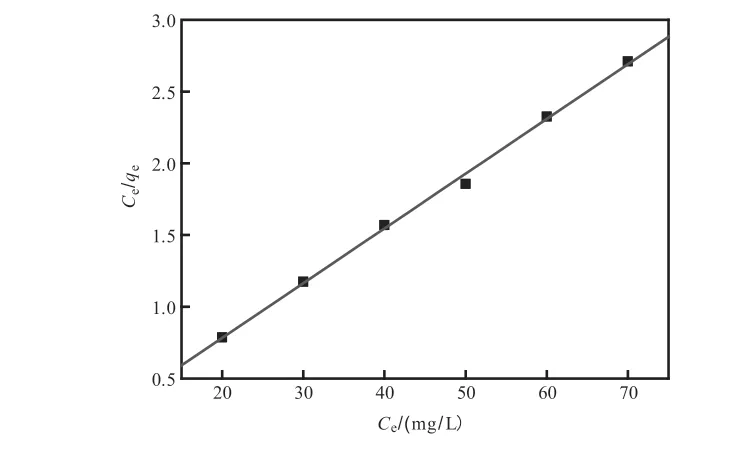
图10 H2L/MCM-41对镍离子吸附的Langmuir吸附等温线Fig. 10 Langmuir isotherm of nickel ion adsorption on H2L/MCM-41

表2 Langmuir吸附等温线参数Table 2 Langmuir adsorption isotherm parameters

图11 H2L/MCM-41对镍离子吸附的Freundlich吸附等温线Fig.11 Freundlich adsorption isotherm of nickel ion on H2L/MCM-41

表3 Freundlich吸附等温线参数Table 3 Freundlich adsorption isotherm parameters
3 结论
以钒尾矿为硅源制备出了MCM-41,对其进行功能化,测试了其对镍离子的吸附性能,得到了最佳吸附条件为:吸附时间80min,镍离子的初始浓度为70mg /L,吸附剂加入量0.04g,吸附实验温度60℃。通过对吸附过程进行热力学分析,发现H2L/MCM-41吸附镍离子过程更加符合Langmuir吸附等温线,推测吸附过程是一个以化学吸附占主导地位的反应过程。

