化学链中Cu、Fe基复合氧载体各组分间相互作用的研究进展
王敬泉,郑 敏,李 康,范宝山
(昆明理工大学 冶金与能源工程学院,云南 昆明 650093)
0 引言
CO2是主要的温室气体之一。21世纪以来,全球变暖和温室效应愈发严重,减少CO2的排放是解决此问题的重要措施。作为CO2排放的主要途径,化石能源的燃烧引起了人们广泛的关注[1]。因此,化学链燃烧技术顺应时代被提出。德国科学家Richter和Knoche在1983年首次提出化学链燃烧(Chemical-Looping Combustion,CLC) 概念[2]。CLC作为一个新型的CO2捕集工艺,在氧载体的作用下,几乎完全避免了燃料与空气的直接接触,进而避免产生NOx,并实现了CO2的内分离[3]。其原理如图1所示。
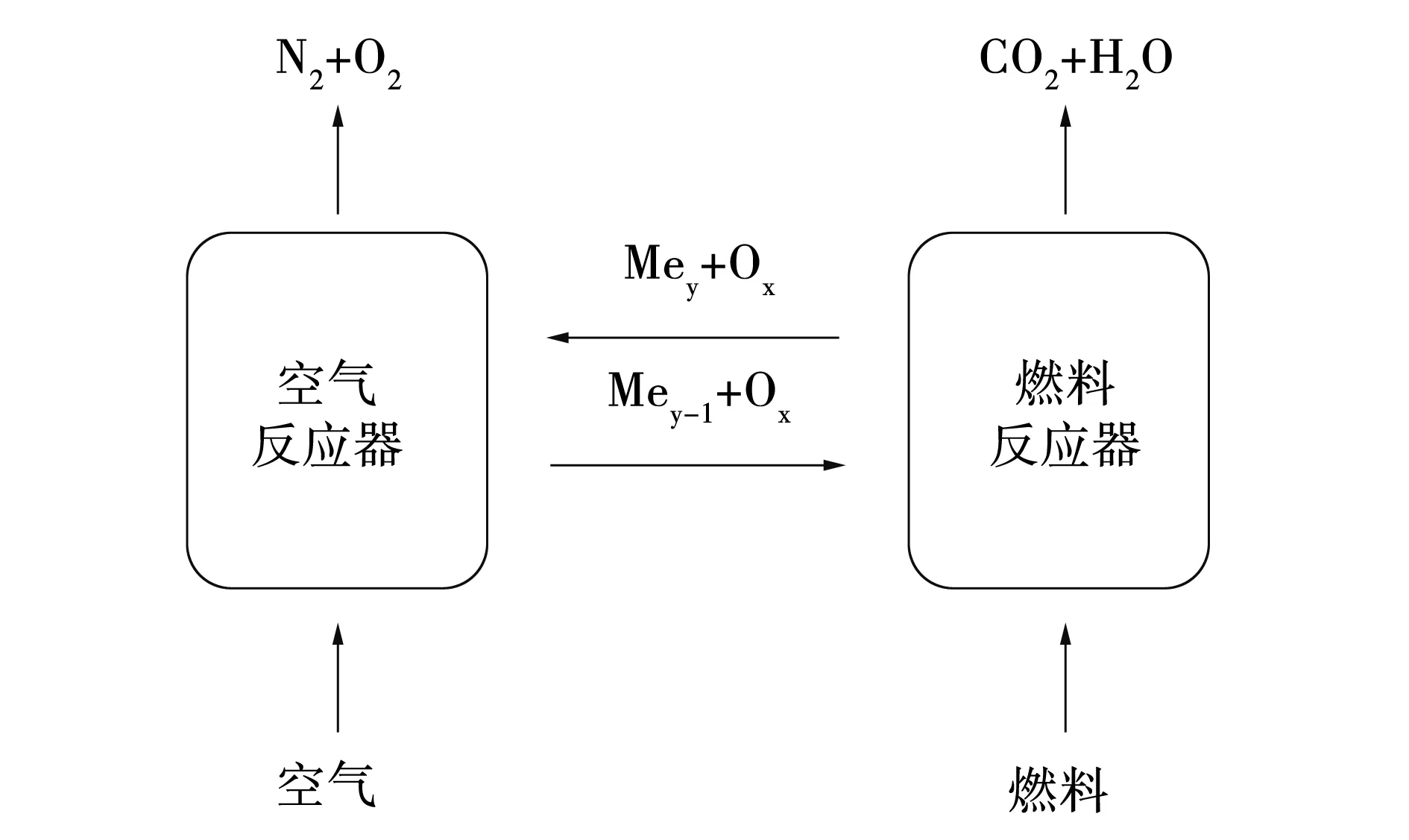
图1 化学链技术原理示意图
具体反应如下:
燃料反应器中的还原反应式
(2n+m)MexOy+CnH2m→(2n+m)MexOy-1+
nCO2+mH2O
(1)
空气反应器中的氧化反应式
(2n+m)MexOy-1+(n+m/2)O2→(2n+m)MexOy
(2)
两反应式相加,即与传统的火焰燃烧反应式完全相同
CnH2m+(n+m/2)O2→nCO2+mH2O
(3)
总反应过程与传统的燃烧方式相同,但化学链燃烧过程把传统的燃烧过程分为氧化反应和还原反应两个独立的部分,进而实现了能量的梯级利用[4]。
氧载体作为空气反应器和燃料反应器的桥梁,不仅是氧的载体,也同时传递能量,对化学链技术至关重要。主要的氧载体包括金属氧载体,NiO、CuO、Fe2O3和CoO等以及非金属氧载体CaSO4、BaSO4和SrSO4等硫酸盐,还有天然矿石,赤铁矿、钛铁矿等。
根据众多研究显示:Ni基氧载体和Co基氧载体反应活性较高、载氧量大并且有催化作用,但其价格昂贵且对环境有害[5-7];Cu基氧载体活性较高、载氧能力强、不容易与惰性载体发生反应,但其熔点较低,高温下容易发生烧结和团聚,大大降低了稳定性和反应活性[8-9];Fe基氧载体热稳定性好、价格低、环境友好,但反应活性和载氧量相对较低[10-11]。综合来看,Cu基和Fe基氧载体用于化学链燃烧最为合适。单一金属氧载体热稳定性和反应活性等性能都比较差,所以,在制备金属氧化物氧载体时,通常使用惰性载体作为负载,常见的惰性载体包括Al2O3、SiO2、TiO2、ZrO2、MgO和MgAl2O4等;也可以在氧载体的基础上,添加其他活性组分,制备多金属复合氧载体来对氧载体进行优化[12]。本文就近年来国内外有关Cu基和Fe基复合氧载体的研究现状进行了总结和分析,并在此基础上针对活性组分和惰性组分以及活性组分与活性组分之间的相互作用两个方面进行了综述和展望,进而为化学链技术中氧载体的选择和性能优化提供参考。
1 Cu、Fe基氧载体活性组分与惰性载体间的相互作用
载体一般不参与化学反应,所以又被称之为惰性载体。常见的惰性载体包括Al2O3、MgAl2O4、TiO2、SiO2、YSZ、海泡石及膨润土等。但也有部分惰性载体在特定条件下会和氧载体中其他组分或者燃料产生反应[13]。以惰性载体作为负载可以提高金属氧载体的破碎强度、反应活性、孔隙率和比表面积等性能,但同时,若活性组分和惰性载体反应生成尖晶石等物质,则会大大降低氧载体的反应活性、载氧性能或者使氧载体烧结。本章综述了Cu、Fe基氧载体活性组分与惰性载体间的相互作用。活性组分与惰性载体的相互作用主要为活性组分负载惰性载体,增强了氧载体的反应活性及热稳定性和机械稳定性等;也有部分惰性载体与活性组分反应生成稳定尖晶石,大大影响了氧载体的反应性能。目前有关活性组分与惰性载体间的作用机理的报道较少,研究两组分间的作用机理,针对不同的活性组分优选出最合适的惰性载体将会是未来研究的主要方向。
1.1 CuO与惰性载体的相互作用
用于制备铜基氧载体的惰性载体可分为两类:一类是可与CuO发生反应,生成高熔点的第三相,而生成的第三相作为铜基载氧体的惰性载体,这一类惰性载体主要包括:Al2O3和Fe2O3;另一类惰性载体包括:SiO2、ZrO2、TiO2、MgAl2O4等,首先SiO2、ZrO2、TiO2、MgAl2O4均具有高的熔点,其次不与CuO发生反应,且自身化学性质稳定。采用第一类惰性载体,会加大活性成分CuO的用量,增大氧载体的制备成本;且生成的第三相容易包裹在活性成分CuO的表面,阻碍其释氧和吸氧,降低反应速率。因此,采用第二类惰性载体制备铜基载氧体更加合适[14]。
对于第一类惰性载体,文圆圆[15]等人制备了CuO/Al2O3氧载体,发现锻烧后的氧载体中只有CuO和CuAl2O4两种物质, 载体中的Al2O3已经全部与CuO化合生成CuAl2O4,所以系统中真正的载体的是CuAl2O4,CuAl2O4在950 ℃下可以轻微释氧,但释氧速率很慢。同样,CuO和Fe2O3体系中,稳定的第三相CuFeO2起到惰性载体的作用
CuO+Al2O3=CuAl2O4
(4)
CuO+Fe2O3=CuFe2O4
(5)
4CuAl2O4=4CuAlO2+2Al2O3+O2
(6)
4CuFe2O4=4CuFeO2+2Fe2O3+O2(g)
(7)
Mei[16]等人对CuO/CuAl2O4进行了表征,研究了其氧解偶机理。发现CuAl2O4分解到CuAlO2的速度很慢,后续的再生无法完成,Al2O3的加入降低了氧载体的释氧速率。王坤[17]等人制备了CuO/CuAl2O4氧载体,与铜矿石在释氧性等方面做了对比。因为CuO/CuAl2O4只由CuO和CuAl2O4两种成分,而铜矿石除了CuO和CuFe2O4之外,还有CaSO4、SiO2等多种少量组分。所以,此复合氧载体的释氧速率和释氧率都比铜矿石要高。孙小青[18]等人发现温度超过800℃时,CuO可快速分解释放出O2(4CuO→2Cu2O+O2↑)。CuAl2O4稳定性较高,分解反应较难发生。华佳亮[19]等人研究了Al2O3,Fe2O3,ZrO2,TiO2,SiO2五种惰性载体的铜基氧载体,认为Al2O3和Fe2O3会与CuO反应生成惰性尖晶石,不适合作为CuO的惰性载体。
对于第二类惰性载体,罗明[20]等人使用CuO/SiO2氧载体对煤CLOU过程进行了研究,结果表明,多次循环反应后,氧载体的组分没有发生变化,说明活性组分与惰性载体没有发生反应。桂进发[21]发现在TiO2、ZrO2和SiO2负载下,铜基复合氧载体的熔点分别达到了1 850 ℃、2 680 ℃和1 650 ℃,具有良好的热稳定性以及机械稳定性,与王坤[22]等人结果一致,三种不同负载的氧载体释氧性能Cu/Zr>Cu/Ti>Cu/Si,吸氧性能没有较大差距。桂进发[23]等人还基于密度泛函理论计算了CuO在TiO2、ZrO2、CuAl2O4和MgAl2O4负载上的吸附能,TiO2的吸附能最低,负载于CuAl2O4的CuO释氧能量势垒最低,以此证明它反应活性最高。董亮[24]以MgAl2O4、SiO2、ZrO2为惰性载体制备了不同惰性载体添加比例的铜基氧载体,研究了温度、惰性载体的种类和添加比例对铜基载氧体释氧反应和吸氧反应的影响,结果显示,氧载体中活性组分均没有与惰性载体发生反应,释氧速率测量显示:CuO/MgAl2O4>CuO/ZrO2>CuO/SiO2,吸氧反应速率相差不大。
综上所述,Al2O3为惰性组分时,真正的惰性载体是CuAl2O4,虽然CuAl2O4在高温下可以释氧,但释氧速率很慢,主要起负载作用;在CuO和Fe2O3体系中,生成的CuFe2O4是活性组分,熔点较低可能会使氧载体烧结,活性组分释氧分解产生的CuFeO2是实际的惰性载体,熔点为1470K。CuO与惰性载体反应式如表1所示。为了保护环境免受温室效应的影响,迫切需要减少化石燃料特别是煤燃烧的二氧化碳排放。煤的化学链燃烧因其在没有巨大成本损失的情况下固有的分离CO2的优势而受到极大关注。由于CuO不易与煤和灰分中的SiO2、TiO2等杂质反应,铜基氧载体应用于煤的化学链燃烧前景广阔。CuO氧载体最大的缺点就是易烧结,上述众多研究表明SiO2、ZrO2、TiO2和CuAl2O4惰性载体都可以很大程度上解决此问题。惰性载体对CuO热稳定性及释氧性能的影响是研究铜基复合氧载体的关键,惰性组分对CuO反应性能的作用机理目前还不明确,有待进一步研究。
1.2 Fe2O3与惰性载体的相互作用
在铁基复合氧载体中,活性组分会与TiO2、SiO2、MgO和Al2O3等惰性组分反应生成尖晶石,生成物熔点较高且不易还原,降低了氧载体的反应活性。但通常是Fe2O3深度还原的FeO与惰性载体发生反应,Fe2O3不与惰性载体直接反应,因此可以通过控制反应温度等方法,尽量避免Fe2O3被深度还原为FeO,进而减少惰性尖晶石的生成。本节对近年来有关Fe2O3与惰性载体相互作用的研究进展进行了综述。

表1 CuO与惰性载体反应式
1.2.1 化学链燃烧中Fe2O3与惰性载体的相互作用
程伟良[25]等人分别在700℃、800℃和900℃下研究了Fe2O3/TiO2和Fe2O3/ZrO2复合氧载体的反应特性,Fe2O3和TiO2在负载过程中生成了Fe2TiO5,由于其熔点较低,载体表面出现明显烧结现象。而Fe2O3/ZrO2氧载体的XRD衍射峰主要对应Fe2O3和ZrO2,无其它物质生成。Zafar[26]等人分别以MgAl2O4和SiO2做载体制备铁基复合氧载体,用于甲烷化学链燃烧,结果表明,由于惰性FeSiO3的生成而产生严重烧结,故可以认为Fe2O3/SiO2不适宜作为氧载体,而Fe2O3/MgAl2O4具有较高的反应活性。雍其润[27]探究了不同条件下灰分对Fe2O3的影响。在碳不充足的情况下,Fe2O3会与灰中不同组分发生反应,生成多种复合铁化合物,如MgFe2O4、Fe2SiO4、CaFe2O4和Ca2Fe2O5等,这些复合铁化合物的生成会阻碍Fe2O3的还原反应过程。MgFe2O4是一种尖晶石结构的复合铁氧化物,具有较高的熔点(1713℃)和较好的热稳定性,难以被还原。灰中SiO2会与Fe2O3反应生成难以被还原的Fe2SiO4,减少了活性组分Fe2O3的量,降低了氧载体的反应活性
MgO+Fe2O3=MgFe2O4
(8)
2FeO+SiO2=Fe2SiO4
(9)
1.2.2 化学链重整、制氢中Fe2O3与惰性载体的相互作用
Chen[28]等人,制备了Fe2O3/Al2O3和Fe2O3/TiO2用于化学链制氢(CLHG)工艺,研究发现负载在Al2O3上的氧载体反应活性高于负载在TiO2上的氧载体,因为TiO2与Fe2O3在高温下相互作用生成FeTiO3,导致了氧载体较低的反应活性,而在多次循环后未发现FeAl2O4的生成。Ma[29]等人研究了MgAl2O4、SiO2载体在CLHG中对氧载体反应性的影响,由于FeO和载体SiO2之间的反应,形成了部分稳定的硅酸铁相FeSiO3,减少了活性组分Fe2O3的量,进而降低了H2的产率,而Fe2O3/MgAl2O4反应活性较好,没有铝酸盐生成。朱珉[30]等人研究发现900℃、CO2/CH4比为1时,还原后的氧载体以FeAl2O4为主,CH4重整反应后,铁铝尖晶石全部消失,氧化反应后,铁基氧载体活性组分为Fe2O3,说明氧载体循环性能较好。胡月[31]等人用溶胶凝胶法制备了Fe2O3/Al2O3、Fe2O3/ZrO2和Fe2O3/MgAl2O4氧载体,在1000 ℃下煅烧后,负载Al2O3、MgAl2O4和ZrO2的氧载体没有其他物相出现,说明氧载体中活性组分Fe2O3没有与惰性载体发生反应。
1.2.3 密度泛函理论研究Fe2O3与惰性载体的相互作用
Tan[32]等人基于密度泛函理论计算和分子动力学模拟,从微观层面分析了ZrO2和Fe2O3的协同作用,研究发现,ZrO2促进了CO在铁基氧载体表面的吸附。Fe2O3/ZrO2的界面电子相互作用使Fe2O3易于接受CO中的电子,从而促进了CO的化学吸附。梁志永[33]对Fe2O3/ Al2O3氧载体的转化率、反应活性等方面进行了研究,实验发现Fe2O3/ Al2O3在800℃和900℃时具有较高的反应活性,但是在还原产物中发现有FeAl2O4成分的存在,多次循环后,依然检测到了FeAl2O4,说明Fe2O3和Al2O3之间的反应是不可逆,氧载体中活性组分与惰性组分间的反应是导致其反应活性降低的原因之一。这也和薛宝达[34]等人在研究MgO烧结机制时发现,MgO和Fe2O3在550℃以上形成MgFe2O4、和Al2O3在800~1 000℃时形成MgAl2O4。
综上所述,TiO2和SiO2会与Fe2O3形成尖晶石,尖晶石热稳定性强、无释氧性能、不易被还原,消耗了活性组分,降低了氧载体的反应性,不适合负载Fe2O3。Fe2O3与惰性载体反应式如表2所示。天然矿石来源广泛且成本较低,以天然赤铁矿和钛铁矿做氧载体,如何减少其中固有的TiO2和SiO2等组分对Fe2O3组分的负面影响或许是一个值得研究的方向;Al2O3做惰性载体,氧载体比表面积较大,热稳定性高,反应活性和循环稳定性也较好,通过使用不同的制备方法以及控制反应温度等方法,避免Fe2O3被深度还原为FeO,进而避免惰性尖晶石的生成是研究Fe2O3/Al2O3氧载体的重点之一;氢被认为是未来最有前途的能源载体之一,化学链制氢可以生产高纯度的氢气。铁基氧载体在CLHG中循环,将燃料转化为氢气。氢气可以被广泛应用于炼油厂、氨和甲醇生产部门、金属和玻璃铸造厂、食品工业等方面;煤等固体化石燃料是CLC技术中使用最多的燃料,煤和灰分的组成非常复杂,煤化学链燃烧中氧载体和煤以及灰分中各组分间的相互反应机理尚不明确,有待进一步研究。

表2 Fe2O3与惰性载体反应式
2 Cu、Fe基氧载体活性组分与活性组分间的相互作用
通常情况下,单一活性组分的氧载体反应活性和循环稳定性较差。可以利用金属氧化物之间的协同作用,制备多活性组分复合氧载体,来提高氧载体的载氧能力和反应活性,进而对整个CLC过程进行优化。但两种活性组分之间的反应可能会影响氧载体的性能,活性组分间的协同作用机理也是很多学者的研究方向。本章总结了近年来Cu、Fe基氧载体中CuO和Fe2O3与其他活性组分间相互作用的研究进展。
2.1 Cu-Fe复合氧载体的相互作用
杨伟进[35]等人在Fe2O3/Al2O3氧载体的基础上加入了质量分数10%的CuO进行修饰,研究发现,CuO与Fe2O3和Al2O3作用生成了CuFe2O4和CuAl2O4。崔东旭[36]等人用CO作为还原气体探究Cu-Fe-Al-O复合载氧体的性能,发现复合氧载体的CO2产率相当于Fe2O3的四倍,其原因是复合氧载体产生了一种溶出效应,使氧载体更抗烧结。张将[37]等人用燃烧合成法制备了氧载体CuFe2O4,发现CuFe2O4在1179.7 ℃时发生了分解反应,产生了大量的CuFeO2和O2,其过程如下
CuFe2O4→CuFeO2+1/3Fe3O4+1/3O2
(10)
在煤化学链气化反应体系中,被还原后的氧载体主要成分是Fe3O4和FeCu4
CuFe2O4→1/4FeCu4+7/12Fe3O4+5/3O
(11)
Siriwardane[38]等人发现CuO-Fe2O3双金属在促进氧释放方面具有协同效应。由60Cu20Fe20Al和40Cu40Fe20Al组成的负载型氧载体具有最高的反应速率和燃烧转化率, CuO-Fe2O3的协同效应可能是由于Fe2O3和CuO物种在CuFe2O4中高度分散所致。袁妮妮[39]等人通过模拟在铁基氧载体中添加低浓度的Cu,发现Cu的加入降低了氧载体表面的反应能垒,因此使氧载体的反应活性大幅提高。王伟[40]发现在高温条件下,Cu-Fe复合氧载体各组分间可能会发生一些反应。具体如下式
FeO+Al2O3=FeAl2O4
(12)
CuO+Al2O3=CuAl2O4
(13)
CuO+Fe2O3=CuFe2O4
(14)
但最后氧载体中没有生成FeAl2O4,说明Fe2O3没有发生深度还原生成FeO。CuO与Fe2O3在高温条件发生反应生成CuFe2O4,对提升载氧体氧传输速率有着积极意义。但CuO的存在造成了载氧体表面一定程度的烧结,降低了载氧体的反应活性。
2.2 CuO与其他活性组分的相互作用
张彬[41]采用溶胶凝胶法制备了以CuO为释氧组分的Cu-Fe、Cu-Ni、Cu-Co、Cu-Mn4种复合氧载体。对于Cu-Fe体系,最优比例为40%;70Cu30Ni氧载体具有最快的释氧速度; Co3O4本身能够释放气态氧,Cu-Co复合氧载体中具有最佳释氧性能的氧载体为60Cu40Co;Cu-Mn体系的复合氧载体,只需加入相对少量的Mn2O3(20%)即可使Cu-Mn载氧体的释氧性能达到最佳。赵方渊[42]用浸渍法制得CuO/MgO和CuO/NiO两个系列,以Al2O3,SiO2,TiO2作为惰性载体的复合铜基氧载体。分析表明,惰性载体的存在能一定程度地改善纯CuO的抗烧结性和循环反应性能。在制备Cu6Mg1Ti3氧载体过程中高温煅烧时,CuO和TiO2分别与MgO反应生成了MgCu2O3和MgTi2O5;在Cu6Mg1Zr3制备中,ZrO2并没有与MgO反应;Cu6Ni1Ti3复合铜基氧载体在制备氧载体中高温煅烧时,NiO和TiO2在高温下反应合成了NiTiO3。Sulata K[43]等人在Cu基氧载体中加入MnO和Fe2O3,会形成CuFe2O4、CuMn2O4以及Fe3O4-CuFe2O4, Mn3O4-CuMn2O4尖晶石固溶体,使氧载体的反应活性降低。王坤[44]等人用ZrO2负载,Cu/Mn为双金属活性组分做研究。发现释氧阶段供氧量越少,Cu/Mn氧载体释氧速率越快;吸氧阶段供氧量越多,Cu/Mn氧载体吸氧速率越快。
2.3 Fe2O3与其他活性组分的相互作用
付甜甜[45]等人在铁基氧载体的基础上添加了活性组分NiO,生成了高反应活性的NiFeAlO4,显著提高了铁基氧载体与CH4的反应活性
2NiO+Al2O3+Fe2O3→2NiFeAl2O4
(15)
CH4-TPSR实验表明,氧载体的还原反应分为两步:第一步为游离态的Fe2O3被还原为 Fe3O4;第二步为Fe3O4与NiFeAl2O4被还原为单质Fe和(Fe,Ni)合金。NiO添加量为10%时,载氧体的还原反应活性最高。Huang[46]等人将复合镍铁双金属氧化物作为CLG的氧载体,制备过程中Ni和Fe生成NiFe2O4,NiFe2O4的反应性在20个循环内呈下降趋势。Wei[47]等人在Fe2O3/Al2O3基础上加入了质量分数不高于2%的NiO,结果表明,Ni的加入提高了氧载体的氧化还原活性和抗烧结性,因为NiO与Fe2O3/Al2O3之间存在协同作用,形成NiFe2O4和NiAl2O4尖晶石相。Ni改性Fe2O3/Al2O3氧载体同时也具有良好的再生性能
NiO+Fe2O3→NiFe2O4
(16)
NiFe2O4+H2→Ni+Fe2O3+H2O
(17)
NiAl2O4+H2→Ni+Al2O3+H2O
(18)
彭松[48]等人使用燃烧法制备了CoFeAl2O4氧载体。研究发现,温度的增加对该氧载体还原反应有促进作用,可以提高其速率,可是温度过高会造成氧载体活性组分与惰性载体生成CoFe2O4和CoAl2O4,使得氧载体抗烧结性能和循环稳定性迅速下降。覃吴[49]等人制备了Co-Fe2O3/Al2O3复合氧载体用于与褐煤化学链燃烧,新鲜Co-Fe2O3/Al2O3(10%)氧载体XRD衍射峰可以看到Fe2O3、Al2O3、CoFe2O4成分,说明在煅烧阶段,Co和Fe发生反应生成CoFe2O4;与褐煤反应后XRD显示,衍射峰主要对应Co、Fe3O4、CoFe2O4,主要组分未发生变化,说明Co-Fe复合氧载体循环稳定性较好。Sun[50]等人向Fe2O3/Al2O3氧载体中加入MnO2或CoO后,氧载体中形成了尖晶石结构,尖晶石的形成,更容易形成晶格缺陷,提高了氧载体反应过程中晶格氧的传递速率,从而提高了反应速度,MnFe2O4和CoFe2O4氧载体同样具有较高的氧化反应性能,但是Mn和Co元素容易与煤中硫分反应生成金属硫化物,导致载氧体失活。梁皓[51]等人在Fe2O3/Al2O3基础上加入CeO2作为助剂,发现CeO2没有与Fe2O3生成固溶体,还原过程中可以观察到CeO2表面氧和晶格氧的还原峰。牛鹏杰[52]用浸渍法制备了不同配比的CaO/Fe2O3复合氧载体,结果发现CaO与Fe2O3反应形成了CaFe2O4和Ca2Fe2O5,CaO的加入增大了氧载体比表面积,优化了孔隙结构,但降低了氧载体的机械强度。
综上所述,在Cu、Fe基氧载体中添加活性组分会与CuO或Fe2O3发生反应,添加活性组分的种类和掺杂比例是影响氧载体性能的主要因素,添加合适的活性组分和选择最优掺杂比例,进而优选出性能最好的氧载体用于化学链技术中,是今后研究的重点之一;通过掺杂不同活性组分和不同制备方法,调整复合氧载体结构(如AB2O4和ABO3型等)进而提高氧载体性能的研究也有待进一步深入;目前关于多活性组分之间的协同作用机理报道较少,有待进一步研究;由于铁基氧载体的高耐硫性,用于硫磺的化学链燃烧生成高浓度SO2应用于硫酸生产工业前景十分广阔。在化学链中,在氧载体的基础上添加惰性载体和掺杂活性组分,进而对氧载体进行优选和优化,对达成我国“力争2030年前二氧化碳排放达到峰值,努力争取2060年前实现碳中和”的目标具有十分重要的意义。
3 结论
本文总结了近年来国内外有关Cu基和Fe基复合氧载体中,活性组分和惰性组分以及活性组分与活性组分之间的相互作用两个方面的研究进展,进而为化学链技术中氧载体的选择和性能优化提供参考,主要结论如下:
(1)铜基氧载体通常不易与SiO2、TiO2、ZrO2和MgAl2O4发生反应,与Al2O3反应生成CuAl2O4,虽然CuAl2O4高温下可以释氧,但释氧速率非常慢,主要起到惰性负载的作用。CuO氧载体最大的缺点就是易烧结, SiO2、ZrO2、TiO2和CuAl2O4惰性载体都可以很大程度上解决此问题。惰性载体对CuO热稳定性及释氧性能的影响是研究铜基复合氧载体的关键,惰性组分对CuO反应性能的作用机理目前还不明确,有待进一步研究;
(2)铁基氧载体在以SiO2、TiO2为惰性载体时,容易生成尖晶石结构,进而降低了氧载体的反应活性,不适合负载Fe2O3。相比之下Al2O3、MgAl2O4更适合作为铁基氧载体的惰性载体;天然矿石来源广泛且成本较低,以天然赤铁矿和钛铁矿做氧载体可以降低化学链燃烧的成本,如何减少其中固有的TiO2和SiO2等组分对Fe2O3组分的负面影响或许是一个值得研究的方向;
(3)Al2O3是目前研究最广泛的惰性载体,以Al2O3为负载的铁基复合氧载体的比表面积、载氧能力和循环稳定性都比较好。通过使用不同的制备方法以及控制反应温度等方法,避免Fe2O3被深度还原为FeO,进而避免惰性尖晶石的生成是研究Fe2O3/Al2O3氧载体的重点之一;
(4)在多活性组分复合氧载体中,添加活性组分(NiO、CoO、MnO2)可以使氧载体释氧速率和循环反应性增强,但也可能会和Fe2O3或者CuO反应产生复杂物相(如CuMn2O4、NiFe2O4、CoFe2O4等),使氧载体反应活性下降或者烧结;
(5)添加合适的活性组分和选择最优掺杂比例,进而优选出性能最好的氧载体用于化学链技术中,是今后研究的主要方向。目前关于多活性组分之间的协同作用机理报道较少,也有待进一步研究。

