复方丹参滴丸国际申报项目自制对照品的制备研究
罗学军,田介峰,李 冉,3,李瑞明*
(1.天士力控股集团有限公司天士力研究院,天津 300410;2.天士力医药集团股份有限公司创新中药关键技术国家重点实验室,天津 300410;3.天津中医药大学,天津 301617)
复方丹参滴丸(Dantonic®,美国研发代号:T89)在美国FDA法规条件下的研发经历了将近10年的周期,其中引入了许多重大的科技创新,并获得一些关键问题的突破性进展,这是全球首个由中国自主研发的产品完成美国FDAⅢ期临床试验,也是首个获得美国FDAⅢ期临床试验阳性结果的复方中药,为一个新的治疗药物品种——复方植物药用于全球临床开拓了一条重要的、全新的道路[1]。复方丹参滴丸由丹参(Salviae Miltiorrhizae radix et rhizoma)、三 七(Notoginseng Radix et rhizoma)、冰 片(Borneolum syntheticum)3味中药组成,药效成分主要有酚酸类成分(丹参素、原儿茶醛、丹酚酸U、丹酚酸T、丹酚酸D、迷迭香酸、丹酚酸B、丹酚酸A,即《中国药典》复方丹参滴丸对照指纹图谱1~8峰)、皂苷类成分(三七皂苷R1、人参皂苷R b1、人参皂苷R g1、和人参皂苷R e等)以及冰片[2]。中药国际申报CMC研究中,缺少对照品成为其不可避免的瓶颈问题,如果对照品是从非监管当局(如FDA、EMA)认可的来源获得,比如企业自制的对照品,则需要进行充分的研究,包括制备、结构鉴定、标化、包装、稳定性等[3-5]。为满足T89质量标准研究、工艺过程控制、临床样品的检测放行、药效学及药代学等各项研究,笔者项目团队分别对从丹参和三七中自制得到其质量要求中所有的对照品共计10种,解决了该产品国际申报中质量研究用对照品稀缺及质量低下这样一个瓶颈问题。本文以其中三七皂苷R1、人参皂苷Rg1和人参皂苷Re3种对照品为例,介绍其制备研究过程。
1 仪器与试药
R220 BUCHI旋转蒸发仪(瑞士BICHI公司);玻璃色谱柱(天津市玻璃仪器厂);LC80-600动态轴向加压色谱仪(法国诺华赛公司);VT6130真空干燥箱;Agilent 1260高效相色谱仪[安捷伦科技(中国)有限公司];Advance DRX 500 Bruker型核磁共振仪(美国bruker公司);METTLER XP205电子天平(梅特勒-托利多中国)。三七药材(批号201505006,云南天士力三七种植有限公司);D101型大孔吸附树脂(天津海光);D941型大孔吸附树脂;柱层析硅胶(100~200目、200~300目,青岛海洋化工);色谱纯乙腈(Dikma);色谱纯甲醇(Sigma);水为自制超纯水;其余试剂均为市售分析纯。
2 方法与结果
2.1 3个对照品的纯化制备 取三七饮片6 kg,加入6倍量70%乙醇提取两次(2.5和2 h);提取液经65℃减压浓缩至含醇量低于5%后用低速大容量多管离心机(4 200 r/min,20 min)离心,得上清液加入填装好的D101型大孔树脂色谱柱中,水除杂,用30%乙醇洗脱并收集洗脱液,洗脱液经65℃减压浓缩至含醇量低于5%,加入填装好的D941型大孔吸附树脂色谱柱中,水洗并收集洗脱液,65℃减压浓缩至干,即得三醇组总皂苷。用硅胶(200~300目)柱层析色谱法分离,得到人参皂苷Rg1粗品(22.3 g)及三七皂苷R1和人参皂苷Re的混合粗品(32.1 g),粗品分别经动态轴向加压色谱进行精制纯化,制备得高纯度的人参皂苷Rg1(5.3 g)、三七皂苷R1(5.78 g)和人参皂苷Re(5.8 g),作为3个对照品候选物。
2.2 均一化处理及均一性检测 3个对照品候选物分别用无水乙醇溶解(质量-体积比1∶20),混合均匀,在旋转蒸发仪上60℃减压回收溶剂,浓缩至干后持续减压干燥2~4 h。将干燥的对照品候选物分别转移至研钵,研细混匀即可。分别平铺于细胞培养皿中,如图1所示,将表面划分成16个区块,选取其中15个点取样,每份10 mg,精密称定,制成供试品溶液。HPLC检测,以峰面积/称样量计算15个样品的RSD,结果人参皂苷Rg1、三七皂苷R1和人参皂苷Re 15个点RSD分别为0.9%、1.2%和1.42%,表明所有候选物均一性良好。
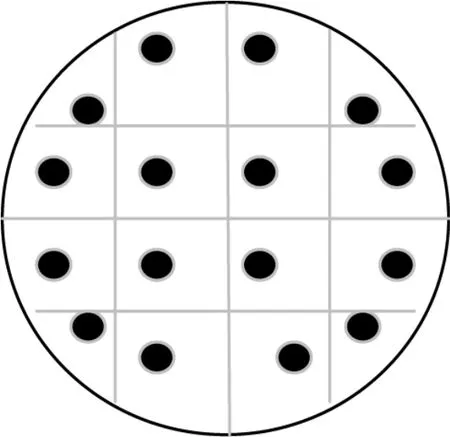
图1 对照品均一化检测取样示意图
2.3 对照品的结构鉴定
2.3.1 人参皂苷Rg1结构鉴定 化合物质谱图谱显示质荷比为801的[M+H]+峰,以及质荷比为823的[M+Na]+峰,提示试样分子量为800。另外高分辨质谱给出了801.507 1的[M+H]+峰(理论值为801.499 5),提示化合物的分子式为C42H72O14,紫外-可见光光谱显示化合物在203 nm处有最大吸收提示化合物中无共轭体系。红外图谱显示3 400 cm-1附近的羟基的特征吸收峰,提示化合物中含有羟基。化合物核磁共振数据如表1所示,与文献报道的人参皂苷Rg1核磁共振数据一致[6],综上所述将化合物鉴定为人参皂苷Rg1。结构图见图2。

图2 人参皂苷Rg1结构

表1 人参皂苷Rg1核磁共振数据(δ,ppm,Pyr-d5)
2.3.2 三七皂苷R1结构鉴定 化合物的高分辨质谱给出了931.526 8[M-H]-(理论值为931.527 2)峰,以及相关离子峰977.531 9[M+HCOO]-峰,提示该化合物的分子式为C47H80O18。紫外-可见光光谱显示化合物在203 nm处有最大吸收提示化合物中无共轭体系。红外图谱显示3 400 cm-1附近的羟基的特征吸收峰,提示化合物中含有羟基。化合物13C核磁共振数据如表2所示,与文献报道的三七皂苷R1核磁共振数据一致[6],综上所述将化合物鉴定为三七皂苷R1。结构图见图3。
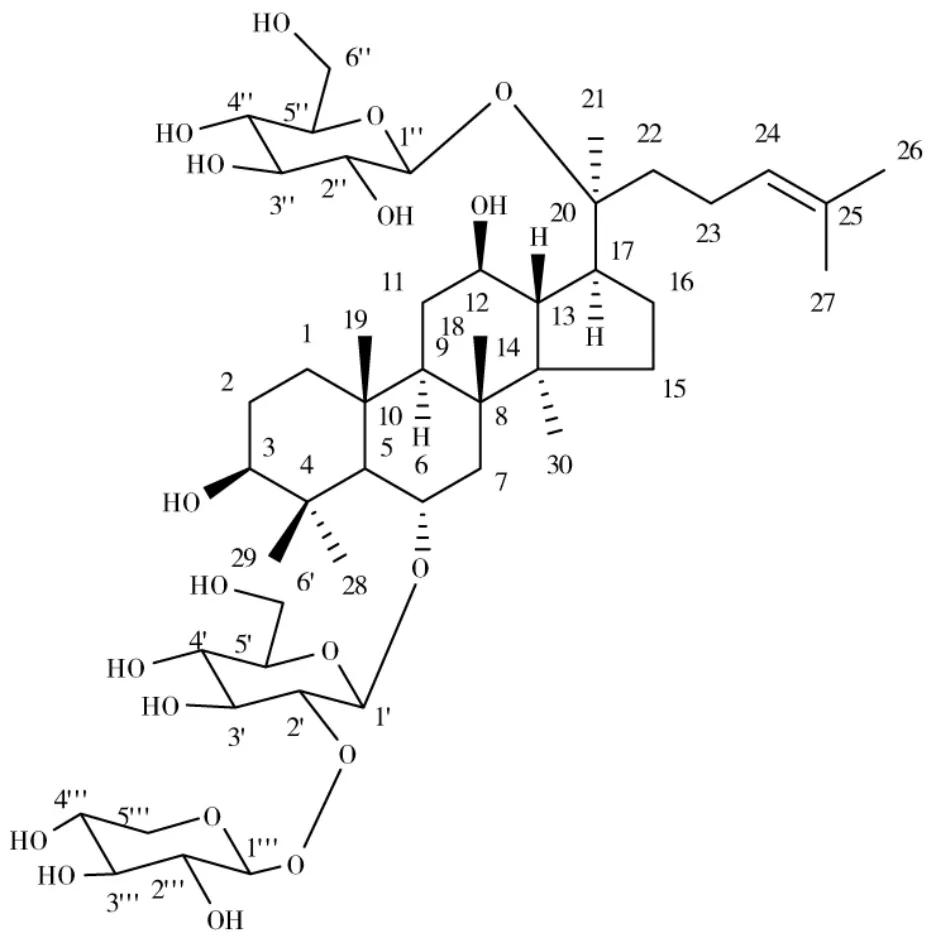
图3 三七皂苷R1结构

表2 三七皂苷R113C核磁共振数据(δ,ppm,CD3OD)
2.3.3 人参皂苷Re结构鉴定 化合物质谱图谱显示质荷比为947的[M+H]+峰,以及质荷比为969的[M+Na]+峰,提示试样分子量应为946。另外高分辨质谱给出了947.559 0的[M+H]+峰(理论值为947.557 4),提示化合物的分子式为C48H82O18,紫外-可见光光谱显示化合物在203 nm处有最大吸收,提示化合物中无共轭体系。红外图谱显示3 400 cm-1附近的羟基的特征吸收峰,提示化合物中含有羟基。化合物核磁共振数据如表3所示,与文献报道的人参皂苷Re核磁共振数据一致[6],综上所述将化合物鉴定为人参皂苷Re。结构图见图4。

图4 人参皂苷Re结构

表3 人参皂苷Re核磁共振数据(δ,ppm,Pyr-d5)
2.4 对照品的纯度定值
2.4.1 色谱纯度的测定(高效液相法)
2.4.1.1 色谱条件 色谱柱为Agilent ZORBAX Eclipse XDB C18(250 mm×4.6 mm,5μm);流动相:水(A)-乙腈(B),洗脱梯度:0~12 min,81%A,19%B;12~60 min,81%A→64%A,19%B→36%B;60~61 min,64%A→81%A,36%B→19%B;61~70 min,81%A,19%B;流速:1 ml/min;检测波长:203 nm;柱温:30℃。
2.4.1.2 供试品溶液的制备 分别取三七皂苷R1、人参皂苷Rg1和人参皂苷Re自制对照品候选物,每份约4 mg,精密称定,用甲醇分别溶解得到浓度分别为0.42、0.40和0.41 mg/ml的溶液。
2.4.1.3 专属性试验 ①取甲醇及3个供试品溶液分别进样10μl,空白溶液色谱图中,未出现和对照品待测成分色谱峰保留时间一致的色谱峰;②延长分析时间,分别取供试品溶液进样10μl,当流动相B相比例达到最高(36%)时保持60 min,均未出现新的峰面积大于主峰面积0.1%的杂质峰;③全波长扫描,分别取供试品溶液进样10μl,使用二极管阵列检测器(PDA)全波长扫描,在其他波长下未见203 nm下观察不到的新杂质峰出现。表明方法专属性良好。
2.4.1.4 准确性试验 分别称取人参皂苷Rg1、人参皂苷Re和三七皂苷R1对照品候选物适量,用色谱甲醇完全溶解并配制成15.99、16.01和16.01 mg/ml的母液,分别用甲醇稀释5个不同的浓度(约为0.1、0.2、0.4、4.0和8.0 mg/ml),分别进样10μl进行测试,3个对照品不同浓度下的色谱纯度RSD均小于1.0%,表明方法准确性良好,见表4。

表4 不同浓度下3个对照品色谱纯度数据 %
2.4.1.5 精密度试验 ①重复性:每一个对照品分别制备(0.4 mg/g)6份,所得色谱纯度的RSD均分别为0.0%、0.0%和0.0%,均小于1%;②重现性:2个不同试验室检测所得色谱纯度的RAD均为0.0%,表明方法精密度良好。
2.4.1.6 稳定性试验 取“2.4.1.2”项下供试品溶液分别在0、6、12、24、48和72 h分别进行测试分析,所有对照品所得色谱纯度与0时比RAD均为0.0%,即均小于1%,表明各供试品溶液在72 h内稳定。
2.4.1.7 色谱纯度的检测 精密量取“2.4.1.2”项下供试品溶液10μl。从色谱图测定结果看,在203 nm下,除主峰外,无可见杂质峰,按峰面积归一化法计算,三七皂苷R1、人参皂苷Rg1和人参皂苷Re自制对照品色谱纯度分别为100.00%、100.00%和100.00%。
2.4.2 水分 以上3种自制对照品按照USP37-NF29<921>Ia所规定的Karl-Fischer方法进行水分测定,结果见表5。
2.4.3 残留溶剂 按照USP37-NF32<467>所规定方法对各对照品进行溶剂残留分析,结果见表5。
2.4.4 灰分 按照USP37-NF29<281>所规定方测定各对照品中的灰分,结果见表5。
2.4.5 质量守衡法计算结果 相对纯度=色谱纯度×(1-水分含量-残留溶剂含量-灰分含量)×100%,计算各自制对照品相对纯度,结果见表5。
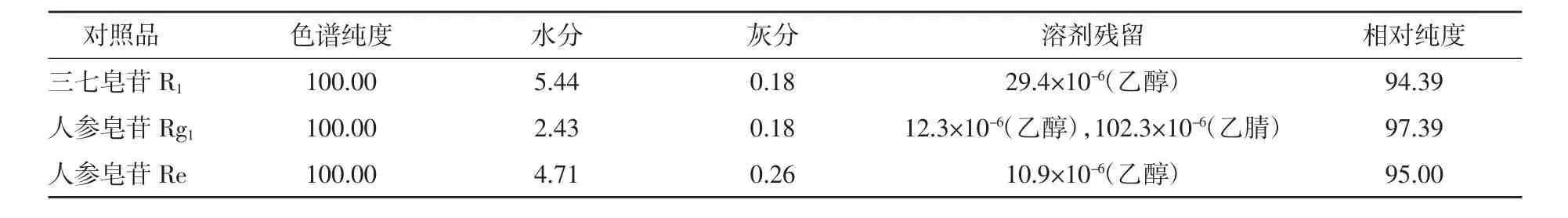
表5 3种自制对照品相对纯度检测数据 %
2.5 对照品的分装及稳定性研究 将3种对照品分别用3 ml棕色西林瓶分装,压盖密封,每支20 mg,于2~8℃下避光保存。分别于1、6、12和24个月取样,测定3个对照品的色谱纯度,结果见表6。结果显示,3种对照品24个月色谱纯度均无下降趋势,均未见降解产物,暂定3个对照品的有效期为24个月,将持续考查其稳定性。
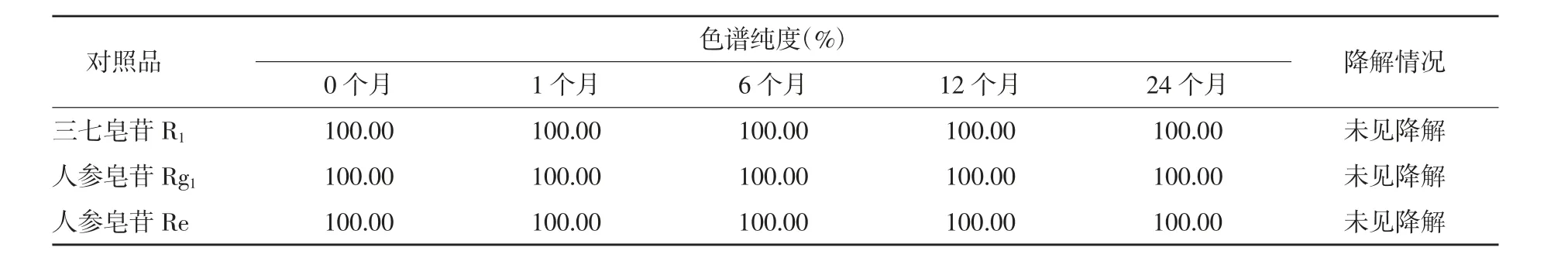
表6 3种自制对照品稳定性数据
3 讨论
三七饮片通过提取、粗分离,得到不同的中间体,中间体进一步纯化可以同时得到3个皂苷类对照品候选物,工艺较为经济,步骤少,纯度高。但是该工艺中人参皂苷Rg1与人参皂苷Re在反相制备色谱中分离度较差,人参皂苷Re需要经过2次反相制备色谱分离后色谱纯度才能达到99%以上。由于西洋参中人参皂苷Re高于三七,而Rg1含量相对较低,因此今后可以考虑从西洋参中提取制备其对照品候选物,可以降低人参皂苷Re的分离难度。
对照品的均一性是由其特殊使命决定的,是对照品必须具备的性质。自制对照品往往存在亚批混批或者同批次不均匀的现象,为了保证对照品的均一性要求根据各对照品的性质对制备得到的对照品进行均一化处理,常用的均一化手段有:共溶重结晶法、共溶冻干法和共溶浓缩干燥混匀法。
自治对照品纯度检测方法的方法学验证不同于通常的含量测定方法学验证,其验证项目需要依据风险评估结果确定。对照品色谱纯度检测需全面显示杂质情况,因此本研究采用空白溶剂、延长分析时间和全波长扫描3种方式来验证方法的专属性。浓度增加会使低于检测限的杂质得以呈现,为了验证方法的准确性,本研究中最大浓度增加至检测浓度的40倍,结果表明该方法准确性良好。

