1例免疫检查点抑制剂相关肾上腺皮质功能减退肺鳞癌患者的用药分析
吴君 李妍 王媛媛 朱熙
中图分类号 R969.3 文献标志码 A 文章编号 1001-0408(2021)22-2785-05
DOI 10.6039/j.issn.1001-0408.2021.22.17
摘 要 目的:探讨临床药师在免疫检查点抑制剂相关肾上腺皮质功能减退诊治中的作用,为类似病例的诊治提供参考。方法:1例长期静脉滴注帕博利珠单抗注射液的肿瘤免疫治疗肺鳞癌患者,因“乏力、纳差10余天”入院。临床药师查阅文献资料并结合患者查体结果(入院第2天上午8时的血浆皮质醇16.41 nmol/L,促肾上腺皮质激素8.39 pg/mL,血清电解质钠126.00 mmol/L、氯88.00 mmol/L等)和用药史(接受免疫检查点抑制剂治疗)进行不良反应关联性评价,协助医师确诊其为肾上腺皮质功能减退症,与帕博利珠单抗的关联性为“很有可能”;在医嘱停用帕博利珠单抗的基础上,临床药师建议口服氢化可的松片(上午8时20 mg,下午4时10 mg)进行糖皮质激素生理剂量替代治疗,并于治疗前对患者及其家属进行用药宣教,于用药过程中实施药学监护对糖皮质激素剂量及效果进行评估,于出院时进行用药教育。结果:医师采纳临床药师的建议。患者于给药后第5天腎上腺皮质功能减退症状显著改善,带药出院。结论:临床药师在该患者的治疗过程中,发挥了其药学特长,协助医师制定了适宜的用药方案,对患者及其家属进行了用药教育,保障了患者用药的有效性和安全性。建议在进行免疫检查点抑制剂治疗前,应完善患者基线检查,包括体格检查、上午8时血浆皮质醇水平;用药期间增加监测上午8时血浆皮质醇水平和血清电解质水平的频次;撤药后至少随访1年,以尽量对免疫检查点抑制剂相关肾上腺皮质功能减退做到早发现、早治疗。
关键词 帕博利珠单抗;肾上腺皮质功能减退;免疫相关不良反应;药学监护;临床药师
Analysis of Drug Use in a Lung Squamous Carcinoma Patient with Immune Checkpoint Inhibitors Associated Adrenocortical Insufficiency
WU Jun1,2,LI Yan2,WANG Yuanyuan1,ZHU Xi1(1. Dept. of Pharmacy,the Second Affiliated Hospital of Anhui Medical University, Hefei 230601, China; 2. Dept. of Pharmacy,the First Affiliated Hospital of Shandong First Medical University/Shandong Provincial Qianfoshan Hospital, Jinan 250014, China)
ABSTRACT OBJECTIVE: To explore the role of clinical pharmacists in the diagnosis and treatment of immune checkpoint inhibitor related adrenocortical insufficiency, so as to provide reference for the diagnosis and treatment of similar cases. METHODS: A lung squamous carcinoma patient with tumor immunotherapy, who received long-term intravenous infusion of Pembrolizumab injection, was hospitalized for more than 10 days due to fatigue and poor appetite. The clinical pharmacists consulted the literature and evaluated the correlation of ADR on the basis of patients physical examination results (plasma cortisol 16.41 nmol/L at 8:00 in the morning on the second day of admission, adrenocorticotropic hormone 8.39 pg/mL, serum electrolyte sodium 126.00 mmol/L, chlorine 88.00 mmol/L, etc.) and medication history (receiving the treatment with immune checkpoint inhibitors). The clinical pharmacists assisted the doctor to confirm that the patient was adrenocortical insufficiency, and the correlation with pembrolizumab was “very likely”. On the basis of discontinuation of pembrolizumab, it was recommended to take Hydrocortisone tablets orally (20 mg at 8:00 in the morning and 10 mg at 4:00 in the afternoon) for glucocorticoid physiological dose substitution therapy. Before treatment, the patient and his families should be educated on the use of drugs, pharmaceutical care should be implemented to evaluate the glucocorticoid dose and efficacy during treatment, and medication education was carried out at discharge. RESULTS: The doctor adopted the suggestions of the clinical pharmacist. On the 5th day after administration, the symptoms of adrenocortical insufficiency were significantly improved, and the patient was discharged with medicine. CONCLUSIONS: During the treatment of the patient, the clinical pharmacist gave full play to his pharmaceutical expertise, assisted the doctor to formulate an appropriate medication plan, and carried out medication education for the patient and his family members, so as to ensure the effectiveness and safety of the patients medication. It is suggested that the baseline examination of patients should be improved before immune checkpoint inhibitor treatment, including physical examination and plasma cortisol level at 8:00 in the morning; the frequency of monitoring plasma cortisol level and serum electrolyte level at 8:00 in the morning. should be increased during medication; the patients should be followed up for at least 1 year after withdrawal, so as to early detect and treat immune checkpoint inhibitor related adrenocortical dysfunction.
KEYWORDS Pembrolizumab;Adrenocortical insufficiency;Immune-related adverse events;Pharmaceutical care;Clinical pharmacist
免疫检查点抑制剂(immune checkpoint inhibitors,ICIs)是一类新型的抗肿瘤药物,主要通过阻断免疫抑制分子,重新激活效应T淋巴细胞的特异性杀伤肿瘤细胞的功能,发挥抗肿瘤作用[1]。ICIs具有疗效显著、总体耐受性良好、较常规化疗药毒性小等优点,在肿瘤治疗中的地位日益突出,近年来在临床上的应用亦日渐广泛[1]。ICIs主要包括细胞毒性T淋巴细胞相关抗原4抑制剂、程序性死亡蛋白1(programmed death-1,PD-1)受体抑制剂及其配体抑制剂等。该类药物在调控免疫应答以杀伤肿瘤细胞的同时,其所致过度活化的免疫细胞也可能造成机体自身免疫损伤,即诱发免疫相关不良反应(immune-related adverse events,irAEs)[2]。irAEs可累及垂体、甲状腺、胰腺、肾上腺等,引起相应的内分泌功能紊乱,其中ICIs所致肾上腺皮质功能减退较为罕见,严重者可引发肾上腺危象[1]。帕博利珠单抗是能与PD-1受体结合的单克隆抗体,可阻断PD-1受体与其配体(PD-L1、PD-L2)结合,抑制T淋巴细胞的增殖和细胞因子的生成,从而解除PD-1通路介导的免疫应答抑制。帕博利珠单抗于2018年7月20日在我国获批上市,其适应证逐步扩展到晚期非小细胞肺癌等多种恶性肿瘤,临床应用愈加普遍[3]。本文通过介绍1例帕博利珠单抗诱发肾上腺皮质功能减退肺鳞癌患者的用药情况,分析临床药师如何识别及处理ICIs相关肾上腺皮质功能减退,并探讨其在类似病例治疗中的作用,为相关临床诊治提供参考。
1 临床病例
1.1 病例资料
患者,男性,66岁,身高165 cm,体质量60 kg,因“乏力、纳差10余天”于2021年5月19日入住山东第一医科大学第一附属医院内分泌科。该患者于2020年7月因咳血至山东省胸科医院就诊,行胸部增强计算机断层扫描术(CT)示左肺门占位、左肺炎症、支气管炎、肺气肿;行支气管镜检查示左肺上叶及下叶分嵴处可见新生物,新生物致下叶支气管阻塞;病理检查示鳞状细胞癌(左下支气管开口);免疫组化检查示甲状腺转录因子1(TTF-1)(-),肺腺癌诊断标志物napsin A(-)、细胞角蛋白5/6(CK5/6)(+)、p40(+),诊断为肺鳞癌(T3N2M0ⅢA期)。该患者因肺气肿而未行手术治疗,于2020年8月3日接受多西他赛+卡铂化疗1个周期,行PD-L1检测示组织多肽特异性抗原(TPS)≥90%(高表达)。由于化疗效果不理想且PD-L1呈高表达,该患者于2020年9月起接受帕博利珠单抗注射液200 mg(静脉滴注,每21天给药1次)进行抗肿瘤免疫治疗。入院前,该患者自述自觉乏力、纳差已有10余天,时有恶心、腹胀,无腹痛、腹泻,无发热、寒战。该患者有高血压病史3年余,血压最高150/100 mmHg(1 mmHg=0.133 kPa),目前规律口服琥珀酸美托洛尔缓释片47.5 mg(每天1次),血压维持在130/80 mmHg左右;否认其他慢性病病史,否认食物药物过敏史,其余病史无特殊。
1.2 入院查体与诊断
该患者入院查体无明显异常,体温36.6 ℃,心率97次/min,呼吸16次/min,血压107/81 mmHg。入院第2天上午8时,实验室检查示患者血浆皮质醇16.41 nmol/L↓(正常范围为172.00~497.00 nmol/L,“↓”表示低于参照范围下限,下同),促肾上腺皮质激素(ACTH)8.39 pg/mL(正常范围为5.00~60.00 pg/mL),血清电解质钠126.00 mmol/L↓(正常范围为137.00~147.00 mmol/L)、氯88.00 mmol/L↓(正常范围为99.00~110.00 mmol/L),其余电解质及生化指标(血常规、肝肾功能、甲状腺功能和性激素、血糖、血脂水平)均未见明显异常。磁共振成像(MRI)增强扫描未发现患者垂体及双侧海绵窦区存在确切异常强化灶。
该患者入院诊断为:(1)肺恶性肿瘤(鳞癌);(2)高血压;(3)肾上腺皮质功能减退症(?)。
1.3 治疗过程
入院后,临床药师通过药学问诊发现,该患者近期用药史明确;随后,临床药师进行不良反应关联性评价,以协助医师进行病因诊断。该患者定期复查结果和入院查体结果均显示其肺鳞癌病情稳定,排除原发疾病进展的可能;本次入院后MRI增强扫描未见其垂体及双侧海绵窦区存在确切异常强化灶,排除器质性病变的可能。该患者已规律服用琥珀酸美托洛尔缓释片3年余,该药药品说明书及文献均未提示有类似不良反应;而帕博利珠单抗注射液药品说明书明确提示有irAEs,其内分泌毒性可导致患者肾上腺功能不全。鉴于该患者有明确的ICIs用药史,故临床药师认为肾上腺皮质功能减退病因不能排除帕博利珠单抗致irAEs的可能。患者完善检查后,医师根据临床药师建议并结合患者检查结果,排除其他病因,确诊肾上腺皮质功能减退为irAEs,遂医嘱停用帕博利珠单抗。同时,临床药师建议进行糖皮质激素生理剂量替代治疗[口服氢化可的松片20 mg(上午8时)和10 mg(下午4时)],并通过密切监测患者用药后的临床表现来评估糖皮质激素剂量是否适宜。医师采纳临床药师的建议。患者给药后第5天上午8时,复查示其血浆皮质醇18.70 nmol/L↓,ACTH 5.52 pg/mL,血清电解质钠137.50 mmol/L、氯97.90 mmol/L↓,电解质紊乱情况有所改善。住院期间,该患者多次测量血压,均维持在120/80 mmHg左右;同时,其未出现糖皮质激素常见的不良反应(如兴奋、失眠等)。医师同意其出院,临床药师对其进行如下出院用药教育:(1)院外继续口服氢化可的松片20 mg(上午8时)和10 mg(下午4時);(2)1个月后复查上午8时血浆皮质醇和电解质水平;(3)注意休息,加强营养,避免感染,如有不适应应及时就诊。
2021年6月25日上午8时,患者回院复查示血浆皮质醇22.59 nmol/L↓,ACTH 5.15 pg/mL,血清电解质钠147.00 mmol/L、氯106.00 mmol/L。
2 不良反应评估与用药分析
2.1 肾上腺皮质功能减退的确诊
临床药师查询文献资料发现,在非应激状态下,患者上午8时的基础血浆皮质醇水平等于或低于83.00 nmol/L可确诊为肾上腺皮质功能减退症[4]。肾上腺皮质功能减退症分为原发性和继发性,其中原发性肾上腺皮质功能减退症中最常见的是艾迪生(Addison)病。一般情况下,原发性肾上腺皮质功能减退患者的血浆ACTH水平明显增高,常等于或高于100.00 pg/mL;而继发性肾上腺皮质功能减退患者的血浆ACTH水平常偏低或在正常低水平范围内,且当血浆ACTH水平低于20.00 pg/mL时可排除Addison病,但不能排除轻度的继发性肾上腺皮质功能减退症[5-6]。该患者入院第2天上午8时的血浆皮质醇水平低于83.00 nmol/L,确诊为肾上腺皮质功能减退症;其血浆ACTH水平在正常低水平范围内且低于20.00 pg/mL,同时血清电解质检查示其轻度低钠、低氯,结合该患者自述乏力、纳差等症状,考虑为轻度继发性肾上腺皮质功能减退症。但该患者垂体及双侧海绵窦区未见确切异常强化灶,故应动态随访观察以进一步明确。
2.2 帕博利珠单抗与肾上腺皮质功能减退不良反应的关联性评价
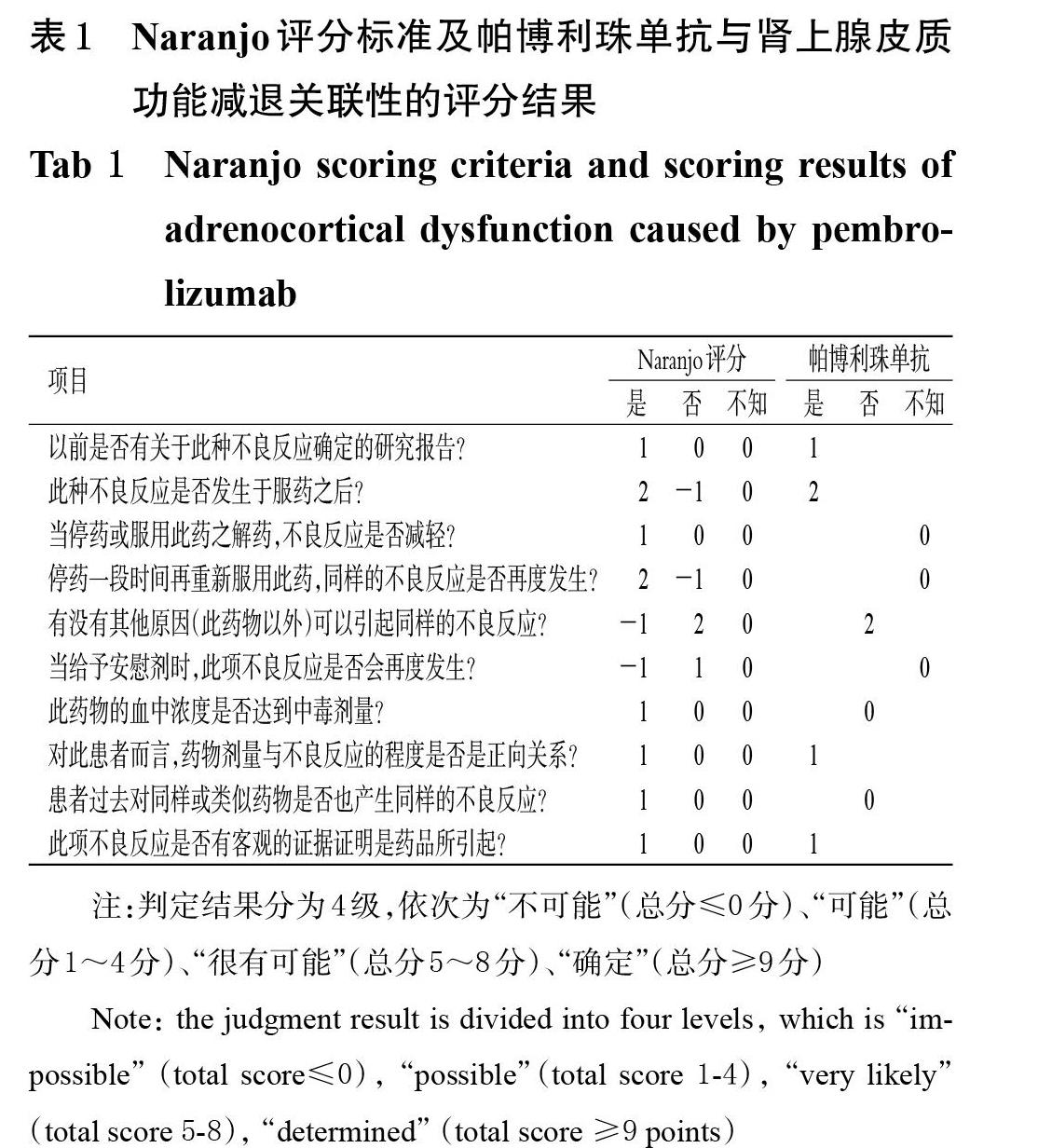
帕博利珠单抗药品说明书对irAEs已有描述,且国内外文献均有相关病例报道[7-9]。临床药师根据Naranjo标准[10]评价不良反应关联性,结果显示,帕博利珠单抗与肾上腺皮质功能减退的关联性评分为7分,即“很有可能”,详见表1。
2.3 帕博利珠单抗致肾上腺皮质功能减退的流行病学特征与发病机制探讨
ICIs相关肾上腺皮质功能减退是较罕见的内分泌irAEs。有研究指出,接受ICIs单药治疗者的irAEs发病率仅为0.7%,而接受ICIs聯合用药治疗者的发病率可达4.2%~7.9%[9]。ICIs通过阻断免疫抑制来活化T淋巴细胞功能,从而增强机体免疫力和对肿瘤细胞的杀伤作用;同时,活化的T淋巴细胞对正常组织的攻击、自身抗体的增加、细胞因子的增多等又有可能诱发自身免疫炎症反应,即ICIs在维持机体免疫系统稳态中的作用失衡,进而诱发一系列irAEs。已有研究报道,ICIs相关肾上腺皮质功能减退是药物诱发自身免疫性肾上腺炎的结果,可能是由自身反应性T淋巴细胞、自身抗体和细胞因子等多种途径共同介导的[11-13]。此外,PDCD1、CTLA4基因多态性和人类白细胞抗原单倍型(包括HLA-DR3-DQ2和HLA-DR4-DQ8)也可能增加了肾上腺皮质功能减退的遗传风险[1],但具体发病机制及高危因素目前尚未明确。还有研究显示,接受超过5 mg/kg伊匹单抗治疗的患者更易发生肾上腺皮质功能减退[1]。肾上腺皮质功能减退可于PD-1受体抑制剂单药治疗几周甚至几个月后出现,中位发生时间在用药后10周。Haanen等[14]报道,帕博利珠单抗致肾上腺皮质功能减退的发生时间可在用药5个月以后,也可发生在撤药后。本例患者在单独使用帕博利珠单抗进行抗肿瘤免疫治疗8个月、累计用药剂量2 000 mg后发生了肾上腺皮质功能减退,与上述文献报道基本一致。
2.4 肾上腺皮质功能减退治疗方案的优化
美国卫生及公共服务部常见不良事件评价标准(common terminology criteria for adverse events,CTCAE)5.0版将肾上腺皮质功能减退分为4个等级,根据患者病情分级及时调整抗肿瘤药物和内分泌药物替代治疗方案[1,15]。本例患者有乏力、纳差等症状,但日常活动不受限,考虑严重程度为2级。根据《免疫检查点抑制剂引起的内分泌系统免疫相关不良反应专家共识(2020)》[1]和免疫治疗相关毒性管理要求[16],ICIs相关肾上腺功能不全治疗应在筛查全垂体轴的基础上进行,同时结合检查结果对症治疗,以补充生理剂量的糖皮质激素为主。与生理剂量相比,超生理剂量的糖皮质激素治疗并不能更好地改善患者的临床症状及缩短腺体功能恢复的时间,同时使用较大剂量的糖皮质激素还有增加感染、高血糖等发生的风险。本例患者乏力、纳差等临床症状较轻,肝肾功能正常,血清钠、氯水平略低于正常范围,临床药师结合患者上述指标水平和文献资料建议选用短效糖皮质激素氢化可的松片进行治疗[17],并根据其药品说明书中的药动学特征,建议在进行生理剂量替代治疗时,于早晨给予较高剂量的氢化可的松片(上午8时20 mg),于下午给予较低剂量的氢化可的松片(下午4时10 mg)。医师采纳临床药师建议。该患者用药期间,临床药师密切监测其症状改善情况、电解质变化情况、糖皮质激素常见不良反应等。
由于替代剂量的氢化可的松吸收快、排出快,与生理皮质醇自然分泌、代谢过程不同,故测定替代治疗后患者的血浆皮质醇和ACTH水平并不能正确反映替代剂量激素治疗的实际效果,故具体疗效的主要判定依据如下:(1)临床上皮质功能减低的表现完全消除,且不出现激素过量征象;(2)上午8时和午夜的血浆ACTH水平降至正常或略低是替代剂量适宜的重要指标;(3)电解质和血压监测是糖皮质激素替代是否适宜的指标,其中血清钠偏低、体位性低血压是糖皮质激素不足的主要表现,相反血压过高则是糖皮质激素过量的征象[17]。本例患者给药后第5天,乏力、纳差症状明显好转,无明显不适;复查血清钠、氯水平均恢复正常,电解质紊乱情况有所改善;住院期间多次测量血压,均维持在120/80 mmHg左右。同时,未监测到患者出现糖皮质激素常见的不良反应。根据患者上述情况,临床药师评估激素替代治疗剂量适宜,建议继续维持原方案进行治疗。医师采纳临床药师建议,并同意患者出院。患者出院1个月后随访,复查血清钠147.00 mmol/L,血清氯106.00 mmol/L,血压115/82 mmHg,电解质、血压均未见明显异常,自述神志清、精神可,无乏力、纳差症状,经评估可以继续接受抗肿瘤免疫治疗(静脉滴注博利珠单抗注射液200 mg,每21天给药1次)。
与其他irAEs不同,内分泌毒性几乎是永久性的,肾上腺皮质功能减退患者通常需要接受长期的生理剂量激素替代治疗,故患者用药依从性对治疗至关重要[1]。治疗前,临床药师对患者及其家属详细讲解激素缺乏的危险性,强调不可自行停药,并告知在应激状态(如感染、呕吐、手术等)时需及时增加剂量(通常为生理剂量的2~3倍),及时复诊、调整剂量以降低肾上腺危象风险。ICIs相关肾上腺皮质功能减退患者在接受激素替代治疗后,无明显临床表现且病情稳定可不必停止免疫治疗,后续每个治疗周期监测相关指标(上午8时血浆皮质醇、ACTH、血清电解质),必要时行影像学检查[11,18],以评估irAEs进展情况及治疗效果。
3 结语
ICIs相关肾上腺皮质功能减退发生较为罕见,初期表现缺乏特异性,易与肿瘤的临床表现混淆而被忽视,故早期的识别和及时的激素替代治疗尤为重要。目前,ICIs相关肾上腺皮质功能减退的病例报道较少且随访时间较短,临床诊治方面尚存在诸多疑惑,亟待加强多学科协作。内分泌专科临床药师不仅要关注内分泌专科药品的安全性问题,亦要关注可能引起内分泌系统相关不良反应的其他专科药品,协助医师及时识别、协同管理并加强患者教育,以避免发生如肾上腺危象等危及生命的严重不良反应。
本文通过介绍临床药师参与1例ICIs相关肾上腺皮质功能减退肺鳞癌患者的诊治过程,通过检查指标评估和不良反应关联性评价以协助医师进行病因诊断,广泛查阅文献资料并结合患者的用药史,提出适宜的用药建议,在患者用药后通过实施药学监护对糖皮质激素剂量进行评估,在确保患者用药安全的前提下,使激素生理剂量替代治疗发挥最佳疗效,为类似不良反应的诊疗提供了参考。基于此,笔者建议在进行ICIs治疗前,应完善患者基线检查,包括体格检查、上午8时血浆皮质醇水平[19];用药期间增加监测上午8时血浆皮质醇水平和血清电解质水平的频次;撤药后至少随访1年,以尽量对ICIs相关肾上腺皮质功能减退做到早发现、早治疗。
综上所述,在ICIs相关肾上腺皮质功能减退肺鳞癌患者的治疗中,临床药师发挥了其药学特长,协助医师制定了适宜的用药方案,对患者及其家属进行了用药宣教,保障了临床治疗的有效性和安全性。
参考文献
[ 1 ] 中华医学会内分泌学分会免疫内分泌学组.免疫检查点抑制剂引起的内分泌系统免疫相关不良反应专家共识:2020[J].中华内分泌代谢杂志,2021,37(1):1-16.
[ 2 ] JORDAN J,ALVIN C,DOUGLAS B. Endocrine toxicities of immune checkpoint inhibitors[J]. Nat Rev Endocrinol,2021,17(7):389-399.
[ 3 ] 劉国强,康朔,王欣晨.帕博利珠单抗一线治疗PD-L1高表达的晚期非小细胞肺癌的药物经济学评价[J].中国药房,2021,32(11):1351-1356.
[ 4 ] 童南伟,邢小平.内科学:内分泌科分册[M].北京:人民卫生出版社,2015:130.
[ 5 ] 廖二元.内分泌代谢病学:上册[M]. 3版.北京:人民卫生出版社,2012:673-674.
[ 6 ] 宁光.内分泌学高级教程[M].北京:人民军医出版社,2011:227-244.
[ 7 ] 孟德辉,王伟兰.帕博利珠单抗致原发性肾上腺功能减退1例及文献分析[J/OL]. 中国药物警戒,2021:1-7[2021- 02-02]. https://kns.cnki.net/kcms/detail/11.5219.R.20210201.
1846.008.html.
[ 8 ] KEI S,KAZUNARI T,TARO H,et al. A case of lung adenocarcinoma with long-term response after late-onset pembrolizumab-induced acute adrenal insufficiency[J]. Case Rep Oncol,2021,14(1):1-7.
[ 9 ] BARROSO-SOUSA R,BARRY W T,CARRIDO-CASTRO A C,et al. Incidence of endocrine dysfunction following the use of different immune checkpoint inhibitor regimens:a systematic review and meta-analysis[J]. JAMA Oncology,2018,4(2):173-182.
[10] 柳丽丽,冯毅,刘文生,等. 1例坎地沙坦致不良反应慢病患者实施药物治疗管理的实践[J].中国药房,2019,30(11):1559-1564.
[11] 樊剑,赵家义,韩一平.免疫检查点抑制剂相关毒性的机制及其治疗的研究进展[J].国际呼吸杂志,2021,41(2):154-160.
[12] 牛志成,王雷,汪治宇.免疫检查点抑制剂相关不良反应的管理专家共识[J].河北医科大学学报,2021,42(3):249-255.
[13] 倪军,张力.肿瘤免疫治疗相关不良反应研究进展[J].中华内科杂志,2021,60(1):84-89.
[14] HAANEN J,CARBONNEL F,ROBERT C,et al. Management of toxicities from immunotherapy:ESMO clinical practice guidelines for diagnosis,treatment and follow-up
[J]. Ann Oncol,2017,28(Suppl 4):iv119-iv142.
[15] 中国抗癌协会肿瘤内分泌专业委员会,重庆市生物医药技术学会肿瘤内分 泌专业委员会.免疫检查点抑制剂主要内分泌不良反应急症处理中国专家共识[J/OL].重庆医科大学学报,2021[2021-03-10]. https://kns.cnki.net/kcms/detail/50.1046.r.20210308.1536.002.html. DOI:10.13406/
j.cnki.cyxb.002758.
[16] 罗景梅,杨中策,潘俐,等.免疫检查点抑制剂所致内分泌不良反应处理流程研究进展[J].解放军医学杂志,2021,46(2):200-206.
[17] 洪磊,邓昂.临床药师参与1例腺垂体功能减退症患者替代治疗用糖皮质激素品种选择的实践与分析[J].上海医药,2017,38(13):59-62.
[18] 汤佳琳,黄镜,王玺,等.程序性死亡蛋白1抗体SHR- 1210治疗晚期实体瘤患者中肾上腺皮质功能减退的临床报道[J].中华肿瘤杂志,2019,41(6):466-470.
[19] 黄光明,贺盛发,黄振光,等. 15例帕博利珠单抗致免疫相关性心肌炎的病例分析[J].中国药房,2021,32(6):729-735.
(收稿日期:2021-07-23 修回日期:2021-10-22)
(编辑:邹丽娟)

