聚鲁米诺修饰电极测定日落黄
姚春雨,代凤婷,王欣玙,王培龙,高慧,刘根,马伟
(淮北师范大学 化学与材料科学学院,安徽 淮北 235000)
0 引言
人工色素一般是通过化学合成方法所制得的有机色素,因其溶解性好、稳定性好、成本低、色泽持久等优点,常常被用作食品添加剂[1-2].此外,人工色素能够耐光照、耐氧化、耐酸碱和微生物污染,可以和食品一起长时间保存[3-4].日落黄(SY)作为一种可食用色素,在一些饮料和甜点中广泛使用[5-7].然而,SY分子中含有偶氮(N=N)官能团和芳香环结构,过多食用,会引起头痛、腹泻、哮喘、过敏、甚至癌变[8-10].因此,为指导食品加工过程中SY的用量,需要建立一种稳定性好、灵敏度高、选择性好的SY检测方法.目前,酶联免疫法[11]、紫外-可见光谱法[12-13]、荧光光谱法[14]、高效液相色谱法[15-16]等多种分析方法已应用于食品中SY的测定.然而,这些方法往往需要昂贵的仪器作为检测平台,检测耗时长且操作繁琐.从检测效果上看,存在灵敏度低、背景干扰严重等问题.而以化学修饰电极为代表的电分析技术凭借其简单快捷的操作、电极制备方式多样以及高灵敏检测的优势,受到广大分析工作者的青睐[17-18].
鲁米诺是一种强化学发光化合物,聚鲁米诺通常是通过化学或电化学方法用单体氧化合成,其聚合过程与苯胺类似,一个鲁米诺分子通过-NH2与另一个鲁米诺分子上的碳原子组成一个聚合单元[19-20].鲁米诺可以在不同材质的电极上形成电化学聚合膜,并表现出良好的电催化性能.比如可以实现对抗坏血酸和烟酰胺腺嘌呤二核苷酸(NADH)的催化氧化[21-22].
本文制备聚鲁米诺修饰玻碳电极(GCE/PLu),该电极制备过程简单,测定SY的灵敏度高,线性范围宽,重现性好,样品分析结果比较理想.GCE/PLu在食品药品分析中的应用前景广阔.
1 实验部分
1.1 仪器与试剂
CHI760电化学分析系统(上海辰华);pHS-3C型酸度计(上海康仪仪器有限公司);三电极系统,玻碳电极或GCE/PLu为工作电极,Ag/AgCl电极为参比电极,铂丝电极为对电极.
鲁米诺和日落黄购买于上海阿拉丁试剂公司,硫酸购买于国药试剂公司.
鲁米诺贮备液:1.00×10-2mol·L-1;日落黄贮备液:5.00×10-3mol·L-1;磷酸盐缓冲溶液(PBS):pH 2.5~9.5,用0.1 mol·L-1磷酸盐按常规方法配制.其它试剂均为分析纯,实验用水为二次去离子水.
1.2 修饰电极的制备
玻碳电极(Ф=3 mm)的预处理按文献[18]进行,然后将该电极放入含1.0×10-3mol·L-1和0.5 mol·L-1H2SO4的溶液中[23],以Ag/AgCl电极为参比电极,铂丝电极为对电极,在电位范围为-0.8~1.2 V,以0.10 V·s-1的扫速循环扫描10周.聚合完成后,用二次去离子水淋洗电极,晾干后使用.
1.3 实验方法
电解池中加入5.0 mL pH 2.5的PBS及5 mL一定浓度的SY标准溶液.GCE/PLu电极、Ag/AgCl电极以及铂丝电极插入其中,进行电化学测定.循环伏安扫描的参数如下,电位范围为0.3~1.1 V,扫描速率为0.10 V·s-1,记录SY的峰电位和峰电流.差分脉冲伏安参数为电位增量:5 mV;脉冲幅度:50 mV;脉冲宽度:60 ms;脉冲间隔:200 ms.
2 结果与讨论
2.1 聚合循环伏安曲线和交流阻抗图谱
图1是鲁米诺在GCE上电化学聚合图,采用循环伏安法连续扫描8圈,其中第1圈在0.57 V和0.82 V左右有明显的的氧化峰,且氧化峰电流较大;在0.68 V和-0.45 V处各有一还原峰.从第2圈开始,峰电流逐渐减小,其中第2圈的氧化峰电流降低较为明显,0.82 V处的氧化峰消失.聚合至第6圈,基本没有变化,说明鲁米诺已稳定地聚合在GCE表面.对裸GCE和GCE/PLu进行电化学阻抗测定,交流阻抗图谱(EIS)如图2所示,高频区GCE/PLu圆弧半径要比裸GCE小很多,说明PLu膜能够有效降低电化学阻抗,促进电子在电极/溶液界面传递.对GCE和GCE/PLu进行SEM表征,如图3所示,GCE表面平整光滑,而GCE/PLu表面比较粗糙,凸起较多.这表明PLu面膜具有较大的比表面积,电活性位点较多.
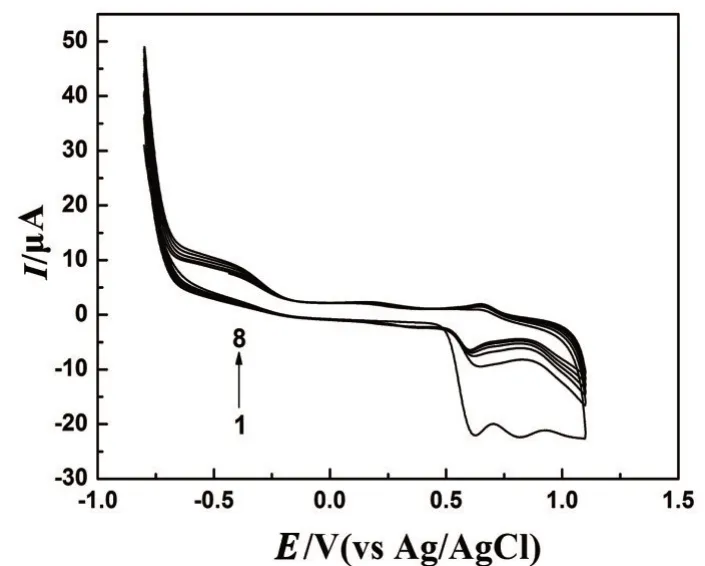
图1 鲁米诺在GCE上的聚合循环伏安曲线
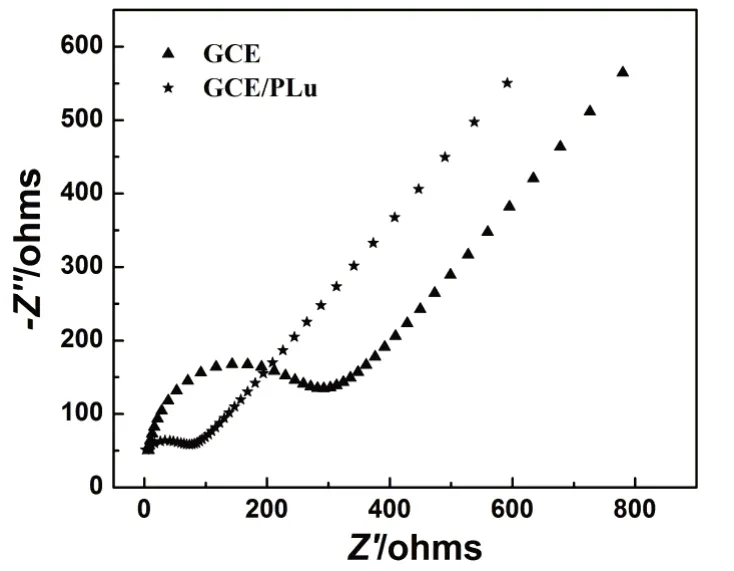
图2 GCE和GCE/PLu在5.0×10-3 mol·L-1 K3[Fe(CN)6]和1.0 mol·L-1 KCl溶液中阻抗谱图

图3 GCE(A)和GCE/PLu(B)的扫描电子显微镜图
2.2 SY在GCE和GCE/PLu上的循环伏安特性
图4为1.00×10-4mol·L-1SY在GCE(a)和GCE/PLu(b)的循环伏安图.其中扫速为0.05 V·s-1,酸度均为pH 2.5.SY在GCE上于0.782 V处有一氧化峰,在GCE/PLu上分别在0.708 V和0.506 V处产生氧化峰和还原峰.其中,GCE/PLu氧化电流远大于GCE,且氧化峰电位较低.说明PLu膜能够有效降低SY的过电位,加速电子在电极/溶液界面上的交换,因此GCE/PLu具有较强的电催化能力.
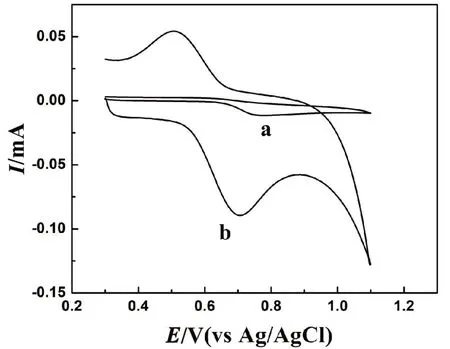
图4 SY在GCE(a)和GCE/PLu(b)上的CV图
2.3 pH的影响
本实验探究不同酸度对1.00×10-4mol·L-1SY的影响.如图5所示,在pH 2.5~9.5范围内,随着pH增加,SY的峰电位负向移动,说明质子参与SY的氧化还原过程.氧化峰电位与pH满足线性方程为E=0.943 3-0.032 53 pH,r=0.990 9.其中,SY在pH 2.5时峰电流最大,所以本实验选择pH 2.5作为测定SY的最佳酸度.
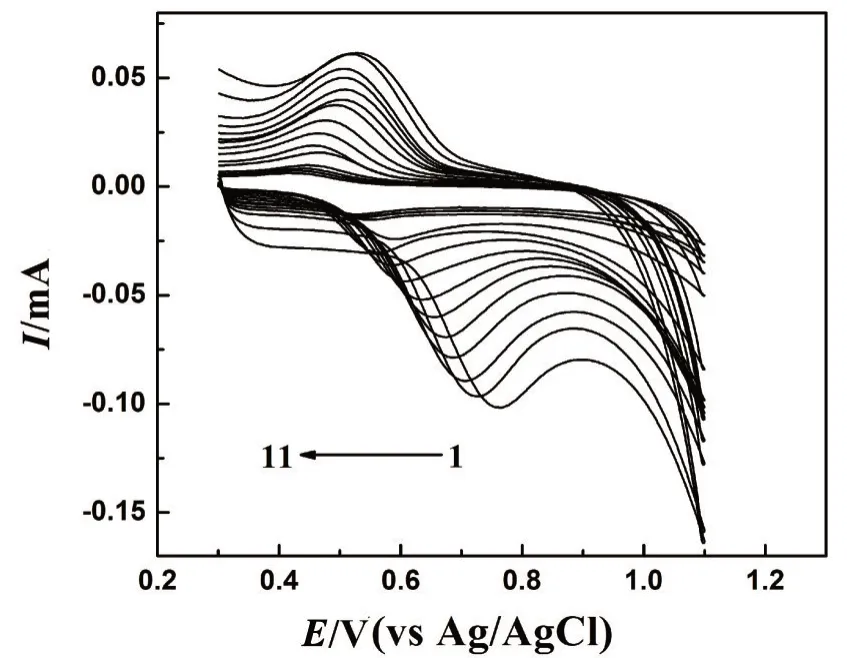
图5 SY在不同pH下的CV图
2.4 扫速影响
图6是不同扫速下1.00×10-4mol·L-1SY循环伏安响应曲线,随着扫描速率的增加,SY的峰电流逐渐增加,同时氧化峰电位正移,还原峰电位负移.在0.02~0.40 V·s-1范围内,其扫速与氧化峰电流满足线性方程I=0.014 26+0.191 6v,r=0.998 4,说明SY在修饰电极上主要受吸附控制.

图6 SY在不同扫速下的CV图
2.5 工作曲线和重现性
在pH 2.5的PBS溶液中,用DPV技术对SY进行测定,结果见图7.氧化峰电流与SY的浓度在5.00×10-7~5.00×10-3mol·L-1范围内呈良好的线性关系,线性方程为lgI=1.029+0.181 6 lgC(I:μA;C:mol·L-1),r=0.990 2,检出限为2.50×10-7mol·L-1.对1.00×10-4mol·L-1的SY进行20次平行测定,峰电流的RSD为3.8%,表明该方法重现性较好.
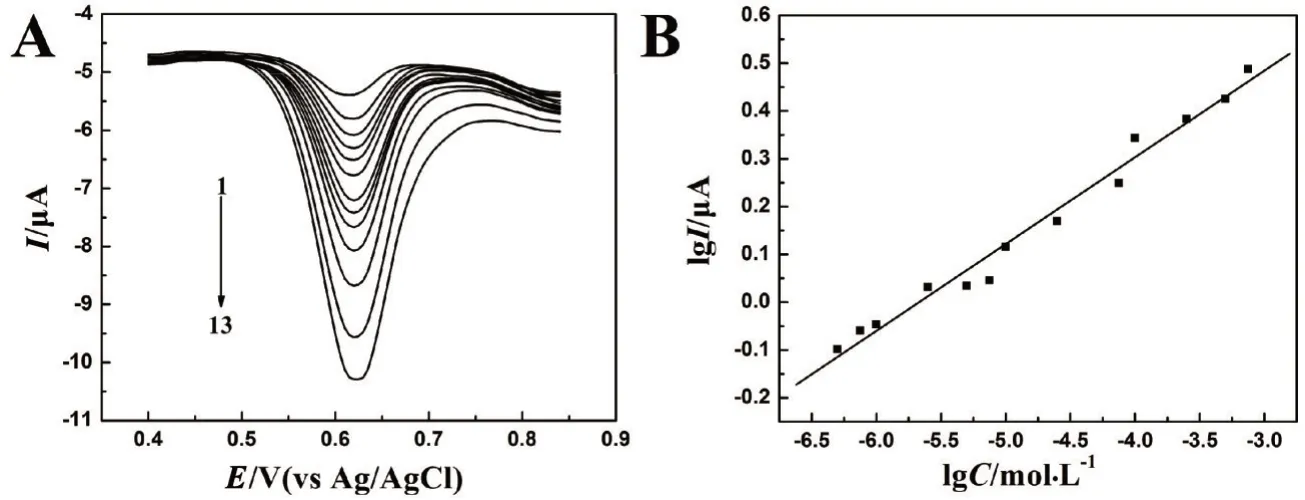
图7 测定SY的DPV曲线(A)及电流与浓度的工作曲线(B)
2.6 干扰实验
5.00×10-4mol·L-1SY溶液中加入50倍浓度的MgCl2、CaCl2、草酸、柠檬酸和抗坏血酸;100倍的L-赖氨酸、L-苯丙氨酸、L-甘氨酸、苋菜红、葡萄糖、蔗糖,SY的DPV信号仍保持在90%以上,说明这些物质对SY的干扰较小.
2.7 样品分析
取5.0 mL芬达橘子汁进行测定,通过标准加入法来评价方法的可行性.计算出实际样品中SY的回收率.如表1,结果表明SY的回收率和精密度均达到较高水平.

表1 饮料中SY测定结果(n=5)
3 结论
本文成功地制备聚鲁米诺修饰玻碳电极,研究日落黄在该电极上的电化学行为,建立差分脉冲伏安法测定日落黄的新方法.这种方法灵敏度高,线性范围宽,对实际样品检测,结果令人满意.

