双去甲氧基姜黄素及姜黄素在SD大鼠体内的药代动力学特征对比研究
侯乐萍 魏晓炎 支玲姣

[摘要] 目的 探討双去甲氧基姜黄素(CurⅢ)及姜黄素(CurⅠ)在SD大鼠体内的药代动力学特征。 方法 选取16只雄性SD大鼠作为研究对象,随机分成甲乙两组,其中甲组大鼠给予双去甲氧基姜黄素混悬液灌服,乙组大鼠给予姜黄素混悬液灌服,测定两种混悬液的性质;于不同时间点抽取大鼠静脉血,利用DAS2.1.1软件计算动力学参数,分析两种药物在大鼠体内的药代动力学特征。 结果 CurⅢ的lgP值、粒径及Zeta电位分别为(0.71±0.04)、(510.35±18.31)nm、(-56.83±-3.44)mV,CurⅠ的lgP值、粒径及Zeta电位分别为(1.62±0.13)、(841.29±26.38)nm、(-75.21±-4.06)mV,两种成分差异有统计学意义;相同条件下,CurⅢ释放速率更快、溶解度更大;CurⅢ的Tmax、MRT0~72 h、MRT0~∞、AUC0~72 h、AUC0~∞分别为(0.76±0.13)h、(8.91±0.54)h、(9.73±0.66)h、(281.02±17.22)μg/(L·h)、(291.27±18.05)μg/(L·h),CurⅠ的Tmax、MRT0~72 h、MRT0~∞、AUC0~72 h、AUC0~∞分别为(0.24±0.02)h、(5.61±0.31)h、(8.37±0.52)h、(171.56±11.16)μg/(L·h)、(190.28±12.38)μg/(L·h),药代动力学参数差异有统计学意义。 结论 与姜黄素相比,双去甲氧基姜黄素水溶性更好、物理稳定性更高,溶解度较大,药物吸收更好,生物利用度较高。
[关键词] 双去甲氧基姜黄素;姜黄素;药代动力学;大鼠
[中图分类号] R943.4 [文献标识码] A [文章编号] 1673-9701(2021)28-0031-04
Comparative study on pharmacokinetic characteristics of dimethoxycurcumin and curcumin in SD rats
HOU Leping1 WEI Xiaoyan2 ZHI Lingjiao3
1.Department of Pharmacy, Chengbei District, Affiliated Hangzhou First People′s Hospital, Zhejiang University School of Medicine, Hangzhou 310000,China; 2.Department of Pharmacy, Zhejiang Cancer Hospital, Hangzhou 310000, China; 3.The 903 Hospital of the Chinese People′s Liberation Army Joint Logistic Support Force, Hangzhou 310004, China
[Abstract] Objective To explore the pharmacokinetic characteristics of dimethoxycurcumin (CurⅢ) and curcumin (CurⅠ) in SD rats. Methods Sixteen male SD rats were selected as the research objects and randomly divided into group A and group B. The rats in group A were drenched with CurⅢ suspension and the rats in group B were drenched with CurⅠ suspension to determine the properties of the two suspensions. Venous blood of rats was extracted at different time points, and kinetic parameters were calculated by means of DAS2.1.1 software to analyze the pharmacokinetic characteristics of the two drugs in rats. Results The lgP value, particle size and Zeta potential of CurⅢ were (0.71±0.04), (510.35±18.31)nm, (-56.83±-3.44)mV, while those of CurⅠ were (1.62±0.13), (841.29±26.38)nm, (-75.21± -4.06)mV, with significant differences between the two ingredients. Under the same condition, the release rate of CurⅢ was faster, and the solubility was greater. The Tmax, MRT0-72 h, MRT0-∞, AUC0-72 h and AUC0-∞ of CurⅢ were (0.76±0.13)h, (8.91±0.54)h, (9.73±0.66)h, (281.02±17.22)μg/(L·h) and (291.27±18.05)μg/(L·h), while Tmax, MRT0-72 h, MRT0-∞, AUC0-72 h and AUC0-∞ of CurⅠ were (0.24±0.02)h, (5.61±0.31)h, (8.37±0.52)h, (171.56±11.16)μg/(L·h) and (190.28±12.38)μg/(L·h), with significant differences in pharmacokinetics parameters. Conclusion Compared with curcumin, dimethoxycurcumin has better water solubility, higher physical stability, higher solubility, better drug absorption and higher bioavailability.
[Key words] Dimethoxycurcumin (CurⅢ); Curcumin (CurⅠ); Pharmacokinetics (PK); Rats
姜黄素类化合物是从姜黄属植物中提取的一种化合物,主要包括姜黄素、脱甲氧基姜黄素、双脱甲氧基姜黄素三种主要的药物成分,该化合物是一种天然的可使用色素,是最有开发价值的天然性色素之一,被广泛应用于食品加工中;同时,这种化合物也具有清除自由基、消炎、抗肿瘤等生理活性,在医学上同样具有广泛的应用。但是,由于这种化合物极性较小、不稳定,在碱性溶液中易降解,所以其生物利用度较低,相关研究发现,双去甲氧基姜黄素与姜黄素具有相类似的生物活性,在防止细胞脂类过氧化物的形成方面效果更好,同时又具有较高的稳定性,因此临床上具有更高的生物利用度[1-3]。对两种化合物的药代动力学特征进行研究对临床用药具有一定的积极作用。本研究主要目的是分析双去甲氧基姜黄素及姜黄素在SD大鼠体内的药代动力学特征,分析试验流程及结果,现报道如下。
1 资料与方法
1.1 一般资料
1.1.1 仪器和设备 液相色谱仪(A1100型):美国Agilent公司;超纯水机(EPED型):南京易普易达科技发展有限公司;旋转蒸发仪(RE52型):上海亚荣生化仪器厂;旋涡混合器(QL901型):海门市其林贝尔仪器制造有限公司;离心机(TDL240B型):上海安亭科学仪器厂;水浴恒温振荡器(THZ 82型):金坛市荣华仪器制造有限公司;研钵等。
1.1.2 药品与试剂 姜黄素,本实验室自制,纯度在90%以上;双去甲氧基姜黄素,本实验室自制,纯度在99%以上;尼群地平(陕西师诺生物科技有限公司),纯度为99.5%;分析纯的乙腈、乙醇、盐酸、冰醋酸(体积分数为5%)、乙酸乙酯、磷酸二氢钾、肝素、无水乙醇、羟甲基纤维素钠等。
1.1.3 研究对象 16只雄性SD大鼠,体重200~300 g,平均(255±21.37)g,由我市药品研发中心提供。
1.2 方法
1.2.1 药物混悬液的制备 分别称取CurⅢ、CurⅠ置于研钵内,充分研磨,称取研磨后的药品加入1~2滴无水乙醇润湿,然后再加入羟甲基纤维素钠(0.5%),使用旋涡混合器混匀,制成CurⅢ、CurⅠ混悬液备用。
1.2.2 血浆样品的采集 取16只SD大鼠[许可证号:SYXK(浙)2019-0012]分为甲乙两组,禁食12 h后,按照50 mg/kg的标准分组灌服上述配制的CurⅢ、CurⅠ混悬液,然后在给药后5、10、15、30、45、60 min等时间点抽取大鼠眼底静脉血,置于肝素化处理的离心管中离心,6000 r/min、离心10 min,吸取上清液,置于 -20℃冰箱备用。
1.2.3 血浆样品预处理 取一2 mL的离心管,分别加入血浆样品200 μL、内标尼群地平工作液100 μL、乙酸乙酯1.0 mL,置于旋涡混合器充分混合2 min,然后离心,12 000 r/min、离心10 min,将离心后的上层有机相转移到另一离心管中,吹干,加入100 μL流动相,使用枪头搅匀复溶,取样复溶后的样品20 μL进样检测。
1.2.4 色谱条件 兩种药物成分色谱条件:ODS色谱柱为250 mm×4.6 mm,5 μm,流动相是体积比为45∶55的乙腈-冰醋酸(体积分数为5%),体积流量为1 mL/min,柱温为30℃,内标为尼群地平,其中CurⅢ测定波长为417 nm,进样20 μL;CurⅠ测定波长为426 nm,进样20 μL[4-5]。
1.2.5 标准曲线的建立 第一步:首先测定空白血浆、血浆样品、空白血浆+对照品+内标检测方法的专属性;第二步:制作CurⅢ、CurⅠ标准液,分别称取CurⅢ、CurⅠ各10.0 mg,内标尼群地平5.0 mg,加入少量甲醇溶解,然后转移至100 mL容量瓶定容、摇匀,于4℃冰箱保存备用;第三步:取上述100 μg/mL的标准液加入适量甲醇溶液稀释成0.5 μg/mL的对照品溶液,取2 mL的离心管加入200 μL空白血浆,加入100 μL尼群地平工作液,然后按照浓度为15、70、105、140、175、245 ng/mL的标准加入相应的对照品溶液,制成标准血浆,将标准血浆预处理后检测,得到标准曲线[6-7]。
1.3 观察指标及评价标准
1.3.1 CurⅢ、CurⅠ混悬液性质测定 测定CurⅢ、CurⅠ的油水分配系数,以油水分配系数比值的对数值lgP表示,lgP 值越小、水溶性越好;用马尔文粒径测定仪测定CurⅢ、CurⅠ的平均粒径和Zeta电位。
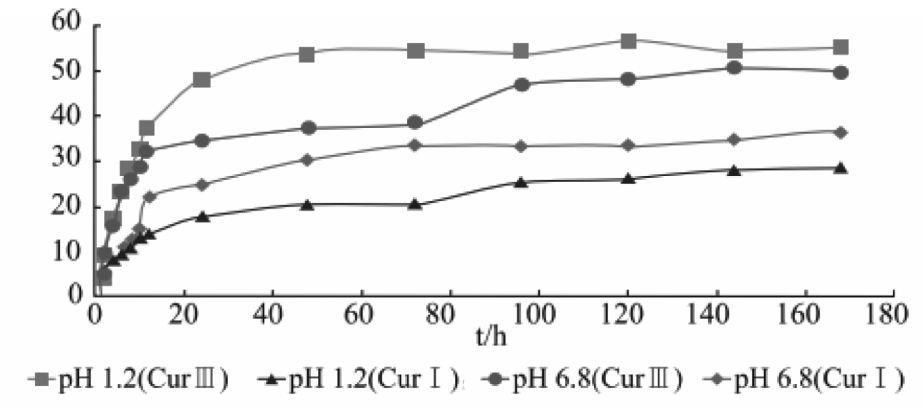
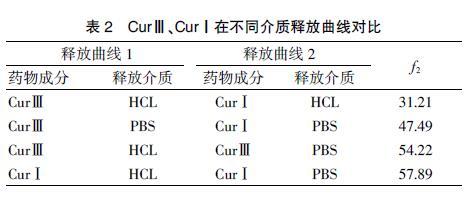
1.3.2 CurⅢ、CurⅠ体外释放行为分析 采用动态透析法测定CurⅢ、CurⅠ的体外释放行为,做法如下:首先选取四种释放介质分别为乙醇(质量分数为20%)、十二烷基硫酸钠(SDS,质量分数为0.5%)、盐酸溶液(HCl,pH值为1.2)、磷酸盐缓冲液(PBS,pH值为6.8),释放介质体积为100 mL;然后分别取1 mL CurⅢ、CurⅠ置于透析袋中,在密闭恒温水浴振荡器中搅拌,分别于1、2、4、8、24、48、72、120、144、168 h取出1 mL介质测定药物累积释放率,需要注意取出的同时,加入等温、等量的相同介质,测定释放介质的药物累积浓度,绘制释放曲线,利用相似因子评价法,比较释放曲线差异,相似因子评价法计算公式见图1,当f2值在0~50时表示两条曲线差异性显著,f2值越接近于100,差异性越小。
1.3.3 药代动力学参数分析 利用DAS2.1.1软件对CurⅢ、CurⅠ的血药浓度-时间曲线进行分析,计算两种药物成分的药代动力学参数,包括用药后最大血药浓度(Cmax)、最大血药浓度达到时间(Tmax)、体内平均滞留时间(MRT)、清除率(CL)、血药浓度-时间曲线下面积(AUC)等。
1.4 统计学方法
将研究所得的所有数据进行统计分析,使用SPSS 20.0统计学软件进行统计分析,计量资料以(x±s)表示,采用t检验,计数资料以[n(%)]表示,采用χ2检验,P<0.05为差异有统计学意义。利用DAS2.1.1软件对CurⅢ、CurⅠ血药浓度-时间关系进行分析,得到两种药物成分在大鼠体内的药代动力学参数。
2 结果
2.1 CurⅢ、CurⅠ混悬液性质分析
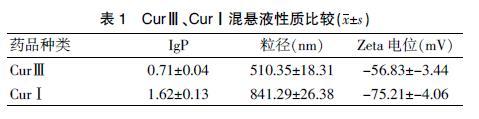
CurⅢ的lgP值、粒径及Zeta电位均远低于CurⅠ,表明CurⅢ的水溶性及物理稳定性显著优于CurⅠ,两种药物成分比较,差异有统计学意义(P<0.05)。见表1。
2.2 CurⅢ、CurⅠ体外释放行为分析
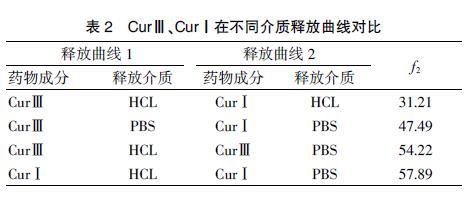
相同条件下,两种药物成分释放速率差异显著,不同pH值时,曲线存在明显差异。见表2、图2。
2.3 CurⅢ、CurⅠ药代动力学分析
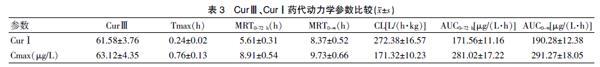
CurⅢ、CurⅠ药代动力学参数差异明显,其中CurⅢ的MRT0~72 h、MRT0~∞分别是CurⅠ的1.59倍、1.16倍;CurⅢ的AUC0~72 h、AUC0~∞分别是CurⅠ的1.64倍、1.53倍;CurⅢ的Tmax是CurⅠ的3.17倍;而Cmax差异较小,差异无统计学意义(P>0.05)。见表3、图3。

3 讨论
姜黄素类化合物是从姜科、天南星科植物中提取出的一种药物成分,是姜黄素、去甲氧基姜黄素及双去甲氧基姜黄素的混合物,其中姜黄素含量约为70%、去甲氧基姜黄素含量约为15%、双去甲氧基姜黄素含量约为15%,姜黄素占比最高,也是姜黄素类化合物主要的功能成分。姜黄素分子结构中含有多个酚羟基,是一种橙黄色结晶粉末、不溶于水,在食品加工中起着着色的作用,在医学上,其具有抗肿瘤、抗炎、抗氧化等多种作用,安全性较好,但其化学结构不稳定,在人体内代谢较快,生物利用度较低;而双去甲氧基姜黄素相对于姜黄素去掉了两个甲氧基,从而改变其性质,提高了水溶性和稳定性,临床应用更广泛[8-12]。

姜黄素分子中含有多个双键,还含有酚羟基和羰基等活性基团,因此具有较高的生理活性,研究表明,姜黄素具有以下生理学作用:①抗肿瘤,姜黄素能够诱导肿瘤细胞的凋亡,抑制肿瘤细胞的增殖,因此具有抗肿瘤的作用;②抗炎,急慢性炎症是心血管疾病,神经退行性疾病等多种疾病的主要致病原因,使用姜黄素对多种病因引起的炎症均能够达到抗炎的作用,具有较大的优势;③抗纤维化,姜黄素能够改变纤维状态,具有明显的抗纤维活性;同时,双去甲氧基姜黄素也具有一系列相类似的药物作用,双去甲氧基姜黄素能够诱导细胞凋亡,能够通过抑制线粒体功能抑制胃癌细胞的生长,能够有效抑制癌细胞在人体内的转移;双去甲氧基姜黄素能够抗纤维化,改变肌纤维状态等,因此其药理作用与姜黄素相一致[13-16]。姜黄素应用广泛,具有较大的开发潜力,既能够作为食品色素应用于食品加工中,又能够作为药物治疗各类疾病,但是,由于姜黄素难溶于水、生物利用度低等物理特性影响了其临床应用,而双去甲氧基姜黄素与姜黄素具有相似的药理特性,同时由于其分子结构改变,物理特性符合利用要求,因此应用相对更加广泛[17-19]。
3.1 CurⅢ、CurⅠ混悬液lgP值、粒径及Zeta电位的性质分析
本研究中,通过对两种成分油水分配系数,结果发现,CurⅢ的lgP值、粒径及Zeta电位均远低于CurⅠ,表明CurⅢ的水溶性及物理稳定性显著优于CurⅠ,两种药物成分比较,差异有统计学意义(P<0.05),这可能是因为CurⅢ去掉两个甲氧基,分子结构改变,其极性、亲水性均明显升高,水溶性较好。
3.2 CurⅢ、CurⅠ在不同pH值时两种药物成分释放速率差异分析
通过对CurⅢ、CurⅠ释放行为的分析,发现在不同pH值条件下,CurⅢ、CurⅠ释放存在差异,这表明CurⅢ的药物吸收度更高,释放比更好,具有更高的生物利用度,利于药物在人体内的吸收[20]。
3.3 CurⅢ、CurⅠ藥代动力学分析
通过对CurⅢ、CurⅠ药代动力学分析,发现CurⅢ的MRT0~72 h、MRT0~∞、AUC0~72 h、AUC0~∞及Tmax均高于CurⅠ,差异有统计学意义(P<0.05),Cmax差异无统计学意义(P>0.05),这可能是由于姜黄素类药物活性较强的原因是由于苯环上-OH以及-OCH具有较强的给电子能力,在CurⅢ中,失去了-OCH,所以其给电子能力减弱,导致其活性较低,稳定性较高。
综上所述,相对于姜黄素,双去甲氧基姜黄素水溶性更好,生物吸收度更高,具有更高的生物利用度。
[参考文献]
[1] 张艳,段雪芹,高刚,等.响应面法优化姜黄素的提取工艺及其抗氧化活性的研究[J].食品工业科技,2015,36(6):269-273.
[2] 黄婧,钱大玮,段金廒,等.银荷降脂方中5种活性成分在大鼠体内的药代动力学研究[J].药物分析杂志,2015, 33(5):867-873.
[3] 刘洁瑜,牛亚伟,李菁,等.姜黄素磷脂干粉工艺及其生物利用度研究[J].中国食品添加剂,2019,21(7):3721-3724.
[4] 陆佳璐,邓丽娜.姜黄素-色氨酸共无定型的制备及其在大鼠体内的药动学研究[J].中国药房,2019,22(17):2348-2354.
[5] 张文焕,刘平香,邱静,等.超高效液相色谱-串联质谱法快速同时测定生姜中10种营养成分[J].色谱,2019, 37(10):1105-1111.
[6] 孙鹏尧,李丹丹,牟德华.HPLC法测定姜黄根茎及姜黄素饮料中姜黄素类化合物的含量[J].食品工业科技,2016,17(21):313-317.
[7] 杨海玲,吴丽丹,覃德杰,等.一测多评法同时测定广西姜黄饮片中3种姜黄素类成分含量[J].药物分析杂志,2016,18(9):1571-1577.
[8] 蔡婧婧,唐晓珍,位思清,等.生姜中姜黄素的匀浆结合有机溶剂法提取工艺优化[J].中国调味品,2018,43(7):832-836.
[9] 高天慧,廖婉,傅超美,等.基于pH值动态变化的川产道地药材蓬莪术醋制前后化学成分差异研究[J].中草药,2017,48(24):5174-5178.
[10] 徐春明,刘亚,陈莹莹,等.姜黄素生理活性、代谢以及生物利用度的研究进展[J].中国食品添加剂,2016,23(9):203-210.
[11] 何丽明,倪赛宏,傅水莲,等.双去甲氧基姜黄素对硫代乙酰胺诱导小鼠肝纤维化的影响及机制[J].中药材,2019,42(2):1031-1032.
[12] 景发,熊书名,李建平.双去甲氧基姜黄素抑制肝癌细胞增殖并诱导凋亡的机制[J].实用临床医药杂志,2016, 20(15):43-46.
[13] 郭清莲,潘凌立,杨立云,等.姜黄素和去甲氧基姜黄素与牛血清白蛋白相互作用热力学行为[J].科学通报,2016, 61(2):3137.
[14] 朱海英,孙红玉,冯光坤,等.姜黄素抑制大鼠脑缺血再灌注损伤内质网应激的研究[J].中华老年心脑血管病杂志,2015,17(4):416-420.
[15] 陈静,张景勍,杨梅,等.双去甲氧基姜黄素与姜黄素的药代动力学比较[J].食品与生物技术学报,2016,35(8):890-895.
[16] 唐艳,杨蓉佳,陳红纲,等.姜黄素对百草枯中毒致肺纤维化大鼠肺功能及TGF-β1、NF-κB表达的影响[J].中华急诊医学杂志,2017,26(4):392-395.
[17] 汪丛丛,庄静,冯福彬,等.姜黄素抑制肺癌细胞血管拟态形成机制探讨[J].中华肿瘤防治杂志,2015,22(4):243-246.
[18] 徐丽丹,王凯旋,季秀梅,等.姜黄素对慢性哮喘大鼠气道炎症及p-ERK1/2表达的影响[J].中华中医药学刊,2015,33(2):419-421,前插14.
[19] 黎星,霍聪,刘艳,等.双去甲氧基姜黄素对星型孢菌素诱导心肌细胞凋亡的影响[J].中华老年多器官疾病杂志,2017,16(1):56.
[20] 何爱文,陈寿权,冷巧云,等.百草枯中毒大鼠急性肺损伤机制及姜黄素的干预研究[J].中华危重症医学杂志(电子版),2016,9(1):14-19.
(收稿日期:2020-10-23)

