美花铁线莲茎乙醇提取物正丁醇萃取部位化学成分的提取和鉴定
王啸洋 卫柯 陆云阳 佟菲 张艳华 汤海峰
毛茛科(Ranuneulaeeae)铁线莲属(Clematis)植物在全世界有370余种,中国约产170种(含变种),全国各地均有分布,以西南和华中地区居多[1-10]。该属在中国民间作为药用的有77种[11],其中川木通(小木通或绣球藤的干燥藤茎)[12]和威灵仙(威灵仙、棉团铁线莲或东北铁线莲的干燥根茎)[12]为《中国药典》2020版收录品种,其他常见的药用品种有百部仙灵(圆锥铁线莲)、黑脚威灵仙(柱果铁线莲)、大木通(钝齿铁线莲)、小木通(毛蕊铁线莲)等,多具有祛风除湿、消肿止痛、舒筋活血、利尿通淋、痛经下乳等功效[13]。现代药学研究表明,本属植物含有三萜皂苷、黄酮、香豆素、木脂素、生物碱等化学成分,具有抗肿瘤、抗炎、镇痛、抑菌等药理作用[14-15]。课题组前期已对多种铁线莲属植物进行了化学成分和药理作用研究,分离鉴定了三萜皂苷、黄酮、木脂素等多种成分,其中部分化合物显示显著抗肿瘤、抗炎、抗心肌缺血等药理活性[16-21]。美花铁线莲(Clematispotaninii)分布于西藏、云南、四川、甘肃、陕西等地,以茎入药,有祛风湿、清肺热、止痢、消食等功效[1]。在前期研究基础上[20],本文继续报道对该植物茎乙醇提取物正丁醇萃取部位化学成分的研究工作,为该植物的进一步开发研究提供理论依据。
1 材料与方法
1.1 仪器与试剂
液相色谱仪为Dionex P680型(美国Dionex公司),配YMC-Pack R&D ODS-A半制备液相色谱柱(20 × 250 mm,5 μm,日本YMC公司);质谱仪为Micromass Quattro(美国Waters公司);气相色谱仪为Finnigan Voyager(美国Finnigan公司),配L-Chirasil-Val气相色谱柱(25 m × 0.32 mm,0.25 μm,美国Agilent公司);旋光仪为Perkin-Elmer 341型(美国Perkin-Elmer公司);核磁共振(nuclear magnetic resonance,NMR)仪为Bruker AVANCE-500型(瑞士Bruker公司)。柱色谱与薄层色谱硅胶(青岛海洋化工厂),反相柱色谱硅胶(ODS-A,日本YMC公司),Sephadex LH-20凝胶柱色谱填料(瑞典GE公司),色谱纯甲醇(天津科密欧化学试剂公司),其他分析纯试剂(天津富宇精细化工公司),水为纯净水。
药材于2015年8月采自陕西省秦岭太白山区域,经陕西中医药大学药学院生药教研室王继涛教授鉴定为毛茛科铁线莲属美花铁线莲Clematispotaninii的茎,标本(20150813)存于空军军医大学药学系中药与天然药物学教研室。
1.2 提取与分离
取美花铁线莲的干燥茎7.5 kg,粉碎成粗粉,加入3倍量70%乙醇加热回流提取3次(每次2小时),合并提取液,减压浓缩得481 g浸膏,浸膏用5 L水分散,依次用等体积石油醚和水饱和正丁醇萃取4次,得正丁醇萃取物170 g。正丁醇萃取物用硅胶柱色谱进行分离,三氯甲烷—甲醇—水(50∶1∶0 ~ 65∶35∶5)梯度洗脱,经薄层色谱检识合并,得到Fr.1~Fr.4四个流份。
Fr.1(4.5 g)用硅胶柱色谱分离,三氯甲烷—甲醇—水(9∶1∶0.02 ~ 8∶2∶0.08)梯度洗脱,得Fr.1.1~Fr.1.6,Fr.1.2和Fr.1.4经Sephadex LH-20凝胶柱色谱(三氯甲烷—甲醇 = 1∶1)分离得Fr.1.2.1~Fr.1.2.8和Fr.1.4.1~Fr.1.4.6;Fr.1.2.3~Fr.1.2.5合并后经重结晶得到化合物1(56.0 mg),Fr.1.4.3~Fr.1.4.5合并后经重结晶得到化合物2(134.0 mg)。
Fr.2(14.2 g)用硅胶柱色谱分离,三氯甲烷—甲醇—水(9∶1∶0.02~8∶2∶0.08)梯度洗脱,得Fr.2.1~Fr.2.5,Fr.2.4经Sephadex LH-20凝胶柱色谱(三氯甲烷—甲醇=1∶1)分离得Fr.2.4.1~Fr.2.4.8,从Fr.2.4.3~Fr.2.4.6合并液中析出白色粉末状物质,为化合物3(45.6 mg)。
Fr.3(26.4 g)用硅胶柱色谱分离,三氯甲烷—甲醇—水(9∶1∶0.02~7∶3∶0.10)梯度洗脱,得Fr.3.1~Fr.3.6,Fr.3.2经Sephadex LH-20凝胶柱色谱(三氯甲烷—甲醇=1∶1)除去水溶性杂质后,用反相ODS柱色谱分离,甲醇—水(3∶7~10∶0)梯度洗脱,得Fr.3.2.1~Fr.3.2.5;其中Fr.3.2.2用半制备高效液相色谱(semi-preparative high performance liquid chromatography,Semi-Prep HPLC)分离(甲醇—水=30∶70),得化合物4(200.0 mg,tR9.3分钟)、化合物5(90.0 mg,tR12.5分钟)和化合物6(20.6 mg,tR14.5分钟)。
Fr.4(42.5g)用硅胶柱色谱分离,三氯甲烷—甲醇—水(9∶1∶0.02~6∶4∶0.5)梯度洗脱,得到Fr.4.1~Fr.4.8,Fr.4.2用Sephadex LH-20凝胶柱色谱(三氯甲烷—甲醇=1∶1)除去水溶性杂质后,经反相ODS柱色谱分离,甲醇—水(2∶8~10∶0)梯度洗脱,得Fr.4.2.1~Fr.4.2.6,其中Fr.4.2.2用Semi-Prep HPLC纯化(甲醇—水=55∶45),得化合物7(122.8 mg,tR8.6分钟)和化合物8(90.2 mg,tR13.7分钟)。
1.3 酸水解和糖基的衍生分析
称取待测化合物5 mg,加入5 mL三氟乙酸溶液(2 mol/L),密闭反应8小时(110 ℃);反应后静置放冷,加入20 mL 纯净水,等体积乙酸乙酯萃取3次,合并水层,浓缩蒸干所得残余物与2 mgL-半胱氨酸甲酯盐酸盐溶于2 mL吡啶,于60 ℃水浴中反应1小时,反应完毕后用氮气吹干;向残余物中加入0.2 mLN-(三甲基硅基)咪唑和2 mL吡啶,60 ℃水浴反应1小时,氮气吹干;残余物用水分散,用等体积环己烷萃取3次,蒸干得糖基的三甲基硅醚化衍生物。
对衍生物进行气相色谱(gas chromatography,GC)分析,载气:氮气;进样量:1 μL;检测器温度:280 ℃;气化温度:250 ℃;程序升温:初始柱温为140 ℃,保持5分钟,以2 ℃/分钟的速度升温到180 ℃,保持5分钟,再以10 ℃/分钟的速升温到320 ℃,保持10分钟。标准糖用上述同样方法衍生并进行分析,根据样品保留时间和峰面积来确定化合物中的糖基种类和含量比例。
2 结果
2.1 结构鉴定
按照1.2所述方法步骤,从美花铁线莲茎乙醇提取物的正丁醇萃取部位共分离鉴定了8个化合物1~8,包括4个三萜类(化合物1、2、7和8)、1个甾醇苷类(化合物3)和3个木脂素类(化合物4、5和6)化合物(图1),所有化合物均为首次从本植物中得到,4为首次从本属植物中发现。
2.2 化合物1
白色针晶,易溶于三氯甲烷,m.p. 256~258℃,Libermann-Burchard反应呈阳性,浓硫酸乙醇溶液(体积分数10%)中显紫色。电喷雾质谱(Electro Spray Ionization-Mass Spectroscopy,ESI-MS)给出[M+Na]+m/z449,结合其13C-NMR(125 MHz, CDCl3)数据推测分子式为C30H50O。该化合物的1H-NMR(500 MHz, CDCl3)给出8个三萜类化合物的特征甲基质子信号:δH0.72 (3H,s,H-24),0.85 (3H,s,H-25),0.86 (3H,d,J=6.5Hz,H-23),0.94 (3H,s,H-29),0.99 (3H,s,H-30),1.00 (3H,s, H-26),1.03 (3H,s,H-27)和1.17 (3H,s,H-28)。
13C-NMR谱及DEPT谱给出30个碳信号,包括8个甲基碳信号、11个亚甲基碳信号、5个次甲基碳信号和6个季碳信号(含1个羰基碳信号),具体如下:δC22.0 (C-1),41.1 (C-2),212.8 (C-3),57.9 (C-4),41.8 (C-5),41.0 (C-6),18.0 (C-7),52.8 (C-8),37.1 (C-9),59.2 (C-10),35.4 (C-11),30.2 (C-12),39.4( C-13),38.0 (C-14),32.5 (C-15),35.7 (C-16),29.7 (C-17),42.5 (C-18),35.1 (C-19),28.0 (C-20),32.2 (C-21),39.0 (C-22),6.6 (C-23),14.4 (C-24),17.6 (C-25),20.0 (C-26),18.3 (C-27),31.8 (C-28),31.5 (C-29),34.8 (C-30)。以上波谱数据与文献报道基本一致[22],故鉴定该化合物为木栓酮。

图1 从美花铁线莲中分离到的化合物1~8的化学结构
2.3 化合物2
白色针晶,易溶于三氯甲烷,m.p. 284~287℃,Libermann-Burchard反应呈阳性,浓硫酸乙醇溶液(体积分数10%)中显紫色。ESI-MS给出[M+Na]+m/z451,结合其13C-NMR(125 MHz, CDCl3)谱推测分子式为C30H52O。该化合物的1H-NMR(500 MHz, CDCl3)给出8个三萜类化合物的特征甲基质子信号:δH0.86 (3H,s,H-24),0.92 (3H,s,H-23),0.94 (3H,s,H-25),0.96 (3H,s,H-30),0.99 (3H,s,H-29),1.01 (3H,s, H-26),1.02 (3H,s,H-27)和1.15 (3H,s,H-28),1个特征的次甲基质子信号δH3.71 (1H,br s,H-3)。
13C-NMR谱及DEPT谱显示,化合物2比化合物1少1个羰基碳信号,多出1个连氧的次甲基碳信号,且化学位移差别主要在A环,具体如下:δC15.6 (C-1),32.2 (C-2),72.6 (C-3),49.0 (C-4),36.8 (C-5),41.7 (C-6),17.4 (C-7),53.0 (C-8),38.2 (C-9),61.2 (C-10),35.4 (C-11),30.5 (C-12),37.7 (C-13),39.5 (C-14),32.8 (C-15),36.0 (C-16),29.8 (C-17),42.7 (C-18),35.2 (C-19),28.0 (C-20),35.0 (C-21),39.1 (C-22),11.5 (C-23),16.2 (C-24),18.1 (C-25),18.5 (C-26),20.0 (C-27),31.9 (C-28),34.8 (C-29),31.6 (C-30)。以上波谱数据与文献报道基本一致[23],故鉴定该化合物为表木栓醇。
2.4 化合物3
白色无定形粉末,m.p. 284~286℃,Libermann-Burchard和Molish反应呈阳性,浓硫酸乙醇溶液(体积分数10%)中显紫色。以3种TLC展开系统(石油醚—丙酮、环己烷—乙酸乙酯和三氯甲烷—甲醇)展开,与β-胡萝卜苷对照品的Rf值和显色反应一致,并且与对照品混合熔点不下降,推测其为β-胡萝卜苷。
该化合物的13C-NMR谱(125 MHz, C5D5N) 数据为δC: 37.6 (C-1),30.3 (C-2),78.4 (C-3),39.8 (C-4),140.8 (C-5),121.7 (C-6),32.3 (C-7),32.0 (C-8),50.4 (C-9),36.7 (C-10),21.1 (C-11),39.2 (C-12),42.4 (C-13),56.7 (C-14),24.5 (C-15),28.6 (C-16),56.4 (C-17),12.1 (C-18),19.3 (C-19),36.3 (C-20),19.1 (C-21),34.4 (C-22),26.5 (C-23),46.0 (C-24),29.5 (C-25),19.9 (C-26),19.4 (C-27),23.5 (C-28),12.1 (C-29),Glc (葡萄糖)C-1~C-6 (102.5,75.4,78.4,71.8,78.1,62.9),与文献数据基本一致[24],故鉴定该化合物为β-胡萝卜苷。
2.5 化合物4
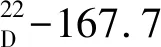
该化合物13C-NMR谱及DEPT谱给出26个碳信号,包括12个隶属于两个芳环的碳信号、6个隶属于六碳糖的碳信号、2个甲氧基碳信号、2个羟甲基碳信号、2个亚甲基碳信号和2个次甲基碳信号,具体如下:δC116.8 (C-1),146.7 (C-2),146.3 (C-3),113.9 (C-4),36.3 (C-5),44.7 (C-6),61.5 (C-6a),45.0 (C-7),61.6 (C-7a),36.3 (C-8),136.7 (C-9),123.0 (C-10),133.5 (C-1’),114.5 (C-2’),150.7 (C-3’),149.1 (C-4’),116.7 (C-5’),122.5 (C-6’),Glc C-1~C-6 (103.1,75.4,79.0,71.7,79.3,62.8),56.3 (3’-OCH3),56.3 (4’-OCH3)。以上信息提示化合物4为由两个苯丙素类分子及一分子葡萄糖组成的木脂素苷类化合物,波谱数据与文献报道基本一致[25],故鉴定该化合物为sargentodoside D。
2.6 化合物5

该化合物的13C-NMR谱及DEPT谱给出32个碳信号,包括12个隶属于两个芳环的碳信号、12个隶属于两组六碳糖的碳信号、2个甲氧基碳信号、1个羟甲基碳信号、2个亚甲基碳信号和3个次甲基碳信号,具体如下:δC139.4 (C-1),111.5 (C-2),149.9 (C-3),147.6 (C-4),116.6 (C-5),119.3 (C-6),83.7 (C-7),54.3 (C-8),60.5 (C-9),135.6 (C-1'),114.2 (C-2'),150.7 (C-3'),146.9 (C-4'),116.9 (C-5'),121.7 (C-6'),33.8 (C-7'),43.5 (C-8'),73.7 (C-9'),Glc I C-1~C-6 (102.8,75.4,79.0,71.7,79.3,62.8),Glc II C-1~C-6 (102.9,75.4,79.1,71.7,79.3,62.9),56.4 (3’-OCH3),56.4 (4’-OCH3)。以上信息提示化合物5为由两个苯丙素类分子及两分子葡萄糖组成的木脂素苷类化合物,波谱数据与文献报道基本一致[26],故鉴定该化合物为落叶松脂醇-4,4’-二-O-β-D-吡喃葡萄糖苷。
2.7 化合物6

分析13C-NMR谱及DEPT谱数据,化合物6比化合物5少1组六碳糖碳信号,具体如下:δC139.3 (C-1),111.2 (C-2),149.7 (C-3),47.5 (C-4),116.3 (C-5),119.2 (C-6),83.7 (C-7),54.3 (C-8),60.2 (C-9),135.6 (C-1’),114.2 (C-2’),150.6 (C-3’),146.7 (C-4’),116.8 (C-5’),121.5 (C-6’),33.7 (C-7’),43.3 (C-8’),73.5 (C-9’),Glc C-1~C-6 (102.8,75.3,79.1,71.1,79.3,62.9),56.3 (3’-OCH3),56.4 (4’-OCH3)。上述波谱数据与文献报道基本一致[26],故鉴定该化合物为落叶松脂醇-4-O-β-D-吡喃葡萄糖苷。
2.8 化合物7

1H-NMR给出6个苷元甲基质子信号:δH0.84 (3H,s,H-29),0.85 (3H,s,H-30),0.96 (3H,s,H-25),1.05 (3H,s,H-26),1.12 (3H,s,H-24)和1.15 (3H,s,H-27);6个糖端基质子信号:δH4.95 (1H,d,J=8.0 Hz,Glc II H-1),5.08 (1H,d,J=6.2 Hz,Ara H-1),5.15 (1H,d,J=8.0 Hz,Xyl H-1),5.86 (1H,s,28-O-Rha H-1),6.23 (1H,d,J= 8.2 Hz,Glc I H-1)和6.35 (1H,s,3-O-Rha H-1);3-O-Rha和28-O-Rha上的甲基质子信号分别为:δH1.51 (3H,d,J=6.2 Hz)和1.67 (3H,d,J=6.1 Hz);苷元特征质子信号:δH3.12 (1H,dd,J=3.6,13.2 Hz,H-18)和5.34 (1H,br s,H-12)。
13C-NMR给出δC:39.2 (C-1),26.9 (C-2),81.3 (C-3),44.0 (C-4),48.2 (C-5),18.6 (C-6),33.2 (C-7),40.4 (C-8),48.5 (C-9),37.3 (C-10),24.1 (C-11),123.2 (C-12),144.4 (C-13),42.4 (C-14),28.6 (C-15),23.7 (C-16),47.5 (C-17),42.0 (C-18),46.7 (C-19),31.2 (C-20),34.3 (C-21),33.2 (C-22),64.3 (C-23),14.3 (C-24),16.5 (C-25),17.9 (C-26),26.4 (C-27),176.9( C-28),33.5 (C-29),24.2 (C-30),Ara C-1~C-5 (105.1,76.0,75.5,69.9,66.4),3-O-Rha C-1~C-6 (101.7,72.4,83.1,73.5,70.3,18.8),Xyl C-1~C-5 (107.6,76.0,78.9,71.6,67.9),Glc I C-1~C-5 (96.0,74.4,79.1,71.2,78.7,69.6),Glc II C-1~C-6 (105.1,75.7,76.6,78.7,77.4,61.6),28-O-Rha C-1~C-6 (103.1,72.8,73.2,74.2,70.6,18.7)。以上波谱数据与文献报道基本一致[29],故鉴定该化合物为sieboldnoside A。
2.9 化合物8

1H-NMR给出7个苷元甲基质子信号:δH0.87 (3H,s,H-25),0.90 (3H,s,H-30),0.91(3H,s,H-29),1.08 (3H,s,H-26),1.15 (3H,s,H-24),1.26 (3H,s,H-27)和1.32 (3H,s,H-23);6个糖端基质子信号:δH4.98 (1H,d,J=7.9 Hz,Glc II H-1),5.05 (1H,d,J=8.0 Hz,Xyl H-1),5.95 (1H,d,J=4.0 Hz,Rib H-1),5.86 (1H,s,28-O-Rha H-1),6.23 (1H,d,J= 8.5 Hz,Glc I H-1)和6.32 (1H,s,3-O-Rha H-1);3-O-Rha和28-O-Rha上的甲基质子信号分别为:δH1.52 (3H,d,J=6.2 Hz)和1.67 (3H,d,J=6.2 Hz);苷元特征质子信号:δH3.14 (1H,dd,J=3.6,13.2 Hz,H-18),3.25 (1H,dd,J=4.2,11.8 Hz,H-18)和5.37 (1H,br s,H-12)。
13C-NMR给出δC:39.3 (C-1),27.0 (C-2),89.1 (C-3),39.9 (C-4),56.4 (C-5),18.8 (C-6),33.3 (C-7),40.3 (C-8),48.5 (C-9),37.4 (C-10),24.2 (C-11),123.2 (C-12),144.4 (C-13),42.5 (C-14),28.6 (C-15),23.7 (C-16),47.3 (C-17),42.0 (C-18),46.6 (C-19),31.1 (C-20),34.3 (C-21),32.9 (C-22),28.5 (C-23),17.6 (C-24),16.1 (C-25),17.8 (C-26),26.4 (C-27),176.9 (C-28),33.4 (C-29),24.1 (C-30),Rib C-1~C-5 (105.0,73.2,69.5,70.9,65.6),Xyl C-1~C-5 (105.7,77.3,80.2,72.0,67.4),3-O-Rha C-1~C-6 (101.8,72.3,81.6,73.1,70.2,18.9),Glc I C-1~C-5 (96.0,74.2,79.0,71.1,78.7,69.6),Glc II C-1~C-6 (105.1,75.7,76.5,78.7,77.3,61.5),28-O-Rha C-1~C-6 (103.1,72.9,73.2,74.3,70.7,18.5)。以上波谱数据与文献报道基本一致[32],故鉴定该化合物为huzhangoside C。
3 讨论
王文采院士等[2]于2005年建立了新的铁线莲属分类系统,认为该属包含4个亚属15组共355种,在此之后,继续对该属品种进行扩展和修订[3-10],现已达到370余种,中国约产170种。据《中国中药资源志要》记载[11],在毛茛科植物中,铁线莲属供药用品种数(77种)仅次于乌头属(82种),已有29个少数民族将其作为药用[13]。可见,本属植物物种丰富,可供药用品种多,《药典》中收录的威灵仙和川木通,其基原植物分别为3种和2种,在实际使用中混用现象较为严重。不同民族对本属植物的药用部位和对应的功能主治也存在较大差别。目前,国内外学者已对20余种本属植物进行过化学成分和药理作用的相关研究,不及本属品种总数十分之一,这些研究表明三萜皂苷、黄酮和木脂素是发挥药效的主要活性成分,但上述成分所发挥的药理作用不尽相同,这也是造成在不同民族药用时功能主治差异的主要原因。因此,有必要进一步拓展本属植物的药效物质基础研究,为民族用药功效的内涵提供科学阐释。
本课题组为首个开展美花铁线莲化学成分研究的团队,本研究在前期工作基础上,综合运用多种色谱分离手段,从该植物的乙醇提取物正丁醇萃取部位分离纯化得到8个化合物,根据波谱数据和理化性质鉴定了它们的化学结构,包括4个三萜类、1个甾醇苷类和3个木脂素类化合物,其中化合物1和化合物2为木栓烷型三萜,化合物7和化合物8为齐墩果烷型三萜皂苷,胡萝卜苷(化合物3)为广泛存在的植物甾醇苷,化合物4为二苄基丁烷型木脂素苷,化合物5和化合物6均为四氢呋喃型木脂素苷,所有化合物均为首次从本植物中分离得到,化合物4为首次从本属分离得到,且所有化合物得量较高,为下一步的药理活性研究提供了保障。本研究结果丰富了铁线莲属植物药效物质基础,为本植物的进一步开发利用提供了实验依据,可为本属植物间的相互替代用药和药效阐释提供参考。

