桑白皮炒制前后HPLC 指纹图谱比较研究*
赵子楠,闫立文,赵 凯,3△
1 北京中医药大学中药学院,北京 100102;2 河北凯盛医药科技有限公司;3 江西欧氏药业有限责任公司
桑白皮又名桑根白皮、白桑皮,为桑科植物桑Morus albaL. 的干燥根皮。始载于《神农本草经》,列为中品。桑白皮性寒味甘,归肺经,具泻肺平喘、利水消肿功效,主治肺热喘咳,水肿,尿少等证[1-2]。现代研究表明,桑白皮的化学成分丰富,主要含有黄酮类、酚酸类、生物碱类等化合物[3]。现代药理学研究表明桑白皮及其活性成分具有抗癌、抗病毒、降血糖、镇痛抗炎、祛痰等多种药理活性[4]。
国家中医药管理局在2018 年4 月公布了《古代经典名方目录(第一批)》(以下简称《目录》),泻白散为《目录》中第40 个处方,处方组成中以桑白皮为君药,其炮制程度被描述为“细锉炒黄”。炒桑白皮为遵古炮制,与我国现行《中华人民共和国药典》(一部)中收载的饮片类型桑白皮和蜜桑白皮不同。炒桑白皮的炮制方式最早出现在宋代《博济方》,曰“剉炒”,后被历代沿用。对于其炮制程度,明代《证治准绳》、清代《小儿药证直诀》聚珍本及现行《 中药炮制经验集成》中均提到为“炒黄”[5-7]。
炮制工艺不同往往带来药效以及化学成分的差异[8-10]。桑白皮化学成分丰富,很难用一种或几种化学成分反映其药材质量,指纹图谱是国内外广泛认可的一种中药质量评价模式。桑白皮的HPLC 指纹图谱多集中于成方制剂以及蜜炙前后的指纹图谱研究,有关炒桑白皮的指纹图谱研究尚未见报道。目前,指纹图谱结合模式识别方法已广泛应用于中药材的质量控制、来源分析及差异标志物筛选等方面,可有效对中药材炮制前后的生品及制品进行判别分析和质量评价[11-13]。
本实验对桑白皮和炒桑白皮指纹图谱进行了比较研究,结合主成分分析PCA 和线性判断分析LDA两种降维分类方法,对其共有的化学组分进行数学分析,尝试探索其化学组分的变化规律[14-16],以期为桑白皮及炒桑白皮质量控制提供参考,给经典名方的研发提供借鉴。
1 材料与方法
1.1 仪器L-3000 型高效液相色谱仪(北京普源精电科技有限公司);YMC Hydrosphere C18(250 mm×4.6 mm,5 μm)色谱柱;CP225D 型电子分析天平[赛多利斯科学仪器(北京)有限公司];电子调温电热套(天津泰斯特仪器有限公司);Anke TDL-16G 型台式离心机(上海安亭科学仪器厂);GR200B型高速粉碎机(合肥荣事达小家电有限公司)。
1.2 试药桑皮苷A 对照品(成都德思特生物科技有限公司,批号:DST190408-068,纯度≥98%);桑根酮C 对照品(成都德思特生物科技有限公司,批号:DST180626-168,纯度≥98%);绿原酸对照品(中国食品药品检定研究院,批号:110753-201415,纯度≥96.2%);桑辛素对照品(成都德思特生物科技有限公司,批号:DST180729-069,纯度≥98%);乙腈为色谱醇(RCIlabscan,批号:19050134);三氟乙酸为分析纯(天津科密欧化学试剂有限责任公司,批号:20190817);水为哇哈哈纯净水。10 批桑白皮药材经河北科技大学李建晨副教授鉴定为桑科植物桑的干燥根皮,样品信息见表1。

表1 桑白皮样品来源
1.3 方法
1.3.1 炮制品的制备 取桑白皮饮片(编号S1~S10),微火炒至表面微黄色或微具焦斑时,取出放凉,得炒桑白皮饮片(编号C1~C10)。分别取桑白皮和炒桑白皮饮片,粉碎,过一号筛,备用。
1.3.2 对照品溶液的制备 分别精密称取桑皮苷A 对照品约20 mg,绿原酸对照品约20 mg,桑根酮C 对照品约10 mg,桑辛素对照品20 mg,置于50 mL 容量瓶中,用甲醇溶解并稀释至刻度,摇匀,作为对照品储备溶液。各分别精密量取桑皮苷A 对照品储备液、桑辛素对照品储备液及绿原酸对照品储备液1 mL,桑根酮C 对照储备液2 mL 置10 mL容量瓶中,用水稀释至刻度,摇匀,即得混合对照溶液,冷藏备用。
1.3.3 供试品溶液的制备 分别精密称取S1~S10,C1~C10 粉末各1.2 g(一号筛),置50 mL 锥形瓶中,精密加入80% 甲醇(体积比)30 mL,水浴回流60 min。过滤,滤液经离心半径4 cm,3000 r/min离心5 min,取上清液过0.4 μm微孔滤膜即得相应的供试品溶液。
1.3.4 色谱条件 色谱柱:YMC Hydrosphere C18(250 mm×4.6 mm,5 μm);体积流量:1.0 mL/min;检测波长:320 nm;柱温:30℃;进样体积:20 μL;流动相:乙腈-水(0.5% 三氟乙酸),梯度洗脱,信号采集时间:105 min。见表2。
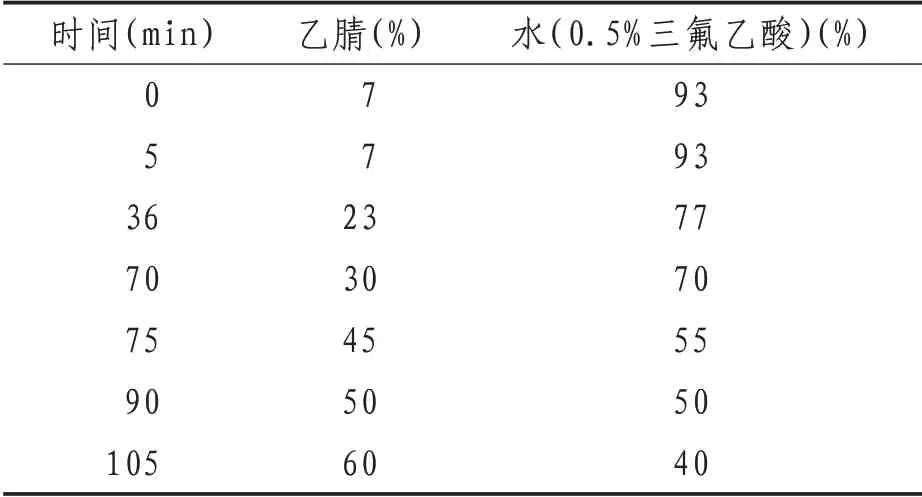
表2 流动相梯度变化
1.4 方法学考察
1.4.1 精密度试验 取同一批炒桑白皮样品(C3),按“1.3.3”项下方法进行制备,按“1.3.4”项下色谱条件连续进样6 次,记录色谱图,采用“中药色谱指纹图谱相似度评价系统”(2012 版)软件进行数据分析,各色谱图的相似度不低于0.995;选择峰面积较大,分离度良好的以7号峰桑根酮C作为参照峰(S),计算各峰的相对保留时间和相对峰面积,结果其RSD 分别小于0.3% 和小于1.5%,符合指纹图谱技术要求,表明仪器精密度良好。
1.4.2 重复性试验 取同一批炒桑白皮样品(C3)6 份,按“1.3.3”项下方法进行制备,按“1.3.4”项下色谱条件检测指纹图谱。采用“中药色谱指纹图谱相似度评价系统”(2012 版)软件进行数据分析,各色谱图的相似度不低于0.995;以7 号峰桑根酮C 为参照峰(S),计算各峰的相对保留时间和相对峰面积,结果其RSD 分别小于0.6%和1.2%,符合指纹图谱技术要求,表明该方法重复性良好。
1.4.3 稳定性试验 取同一批炒桑白皮供试品溶液(C3),于制备后的0、4、10、18、22、34、60 h 进样检测,按“1.3.4”项下色谱条件检测指纹图谱。采用“中药色谱指纹图谱相似度评价系统”(2012版)软件进行数据分析,结果显示,各色谱图的相似度不低于0.995;以7 号峰桑根酮C 为参照峰(S),分别计算各峰的相对保留时间和相对峰面积,结果其RSD 分别小于0.7% 和小于1.5%,表明供试品溶液在60 h内稳定性良好。
1.5 数据分析采用国家药典委员会编制的“中药色谱指纹图谱相似度评价系统”(2012 版)软件、SPSS 22.0 软件及PAST 3 软件对桑白皮及炒桑白皮HPLC的共有峰进行相似度评价、PCA及LDA分析。
2 结果与分析
2.1 指纹图谱的建立将20 批桑白皮、炒桑白皮样品,分别按照“2.3”项下方法制备各供试品溶液,按照“1.3.4”项下的色谱条件进行HPLC 测定与分析,采集105 min色谱图,导入“中药色谱指纹图谱相似度评价系统”(2012 版),分别以C4 和S4的图谱为参照图谱,采用平均数法,对其共有峰进行特征峰匹配,生成各自的对照图谱,均有8 个共有峰。通过与对照品比对,指认出其中两个成分,7号峰为桑根酮C,8号峰为桑辛素,选择分离度良好,峰面积较大,保留时间适宜的7 号峰作为参照峰,分别计算其他共有峰的相对保留时间。见图1—3和表3—4。

表3 炒桑白皮共有峰相对保留时间 min
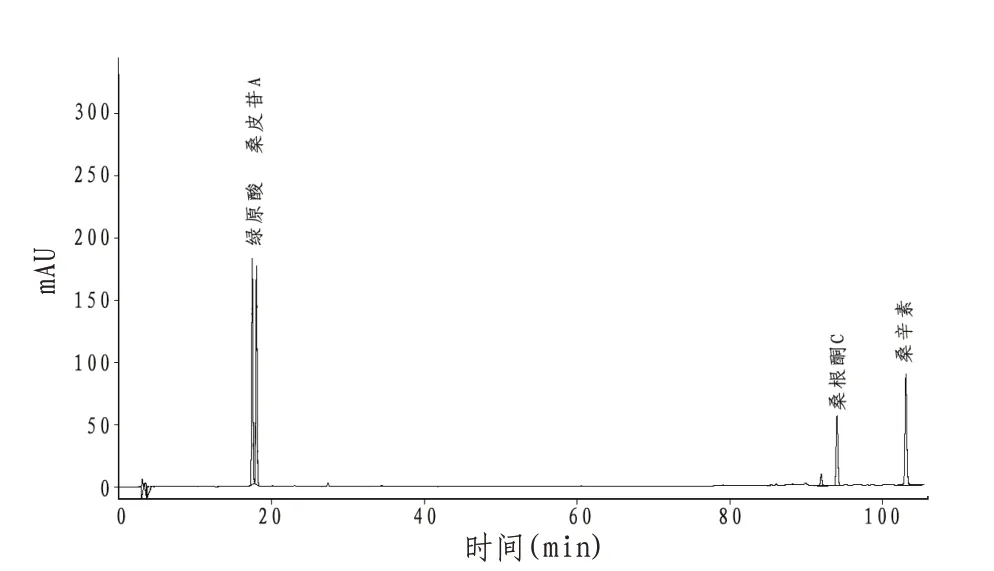
图1 混合对照品溶液HPLC图
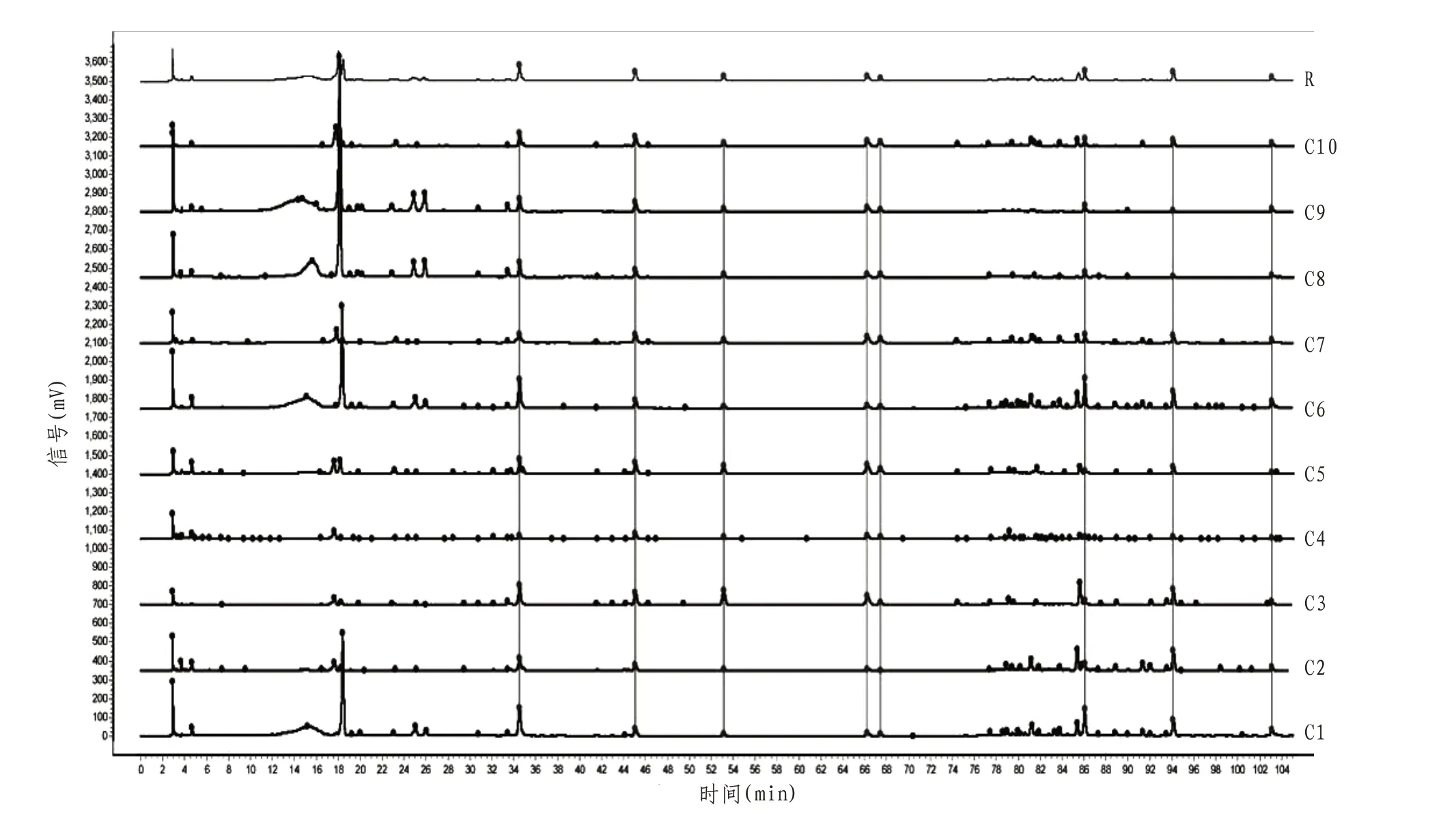
图2 炒桑白皮HPLC指纹图谱

图3 桑白皮HPLC指纹图谱
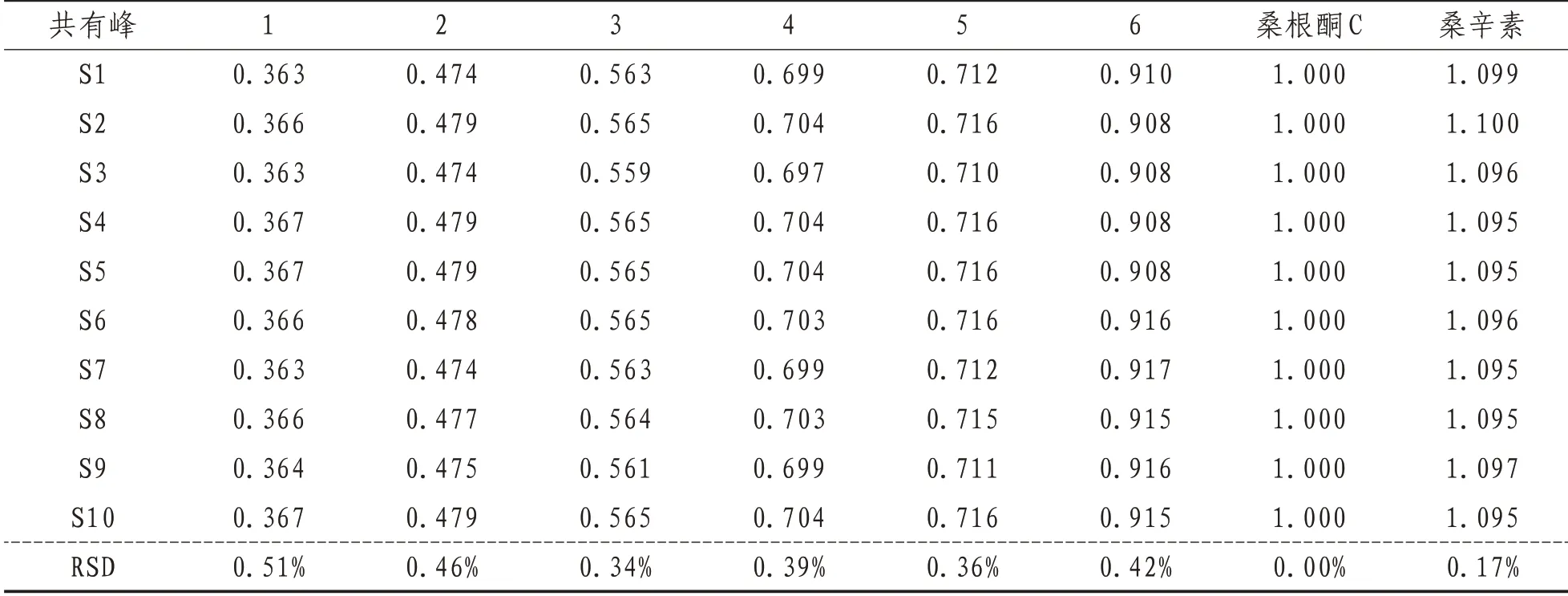
表4 桑白皮共有峰相对保留时间 min
2.2 相似度评价采用“中药色谱指纹图谱相似度评价系统”(2012版)对S1~10、C1~10样品指纹图谱进行相似度分析,可知桑白皮相似度为0.814~0.972,炒桑白皮相似度为0.819~0.972,从相似度波动情况看,炒桑白皮略小于桑白皮,特别是产地为安徽的4 批桑白皮,炒制后相似度差异小于炒制前。说明桑白皮炒制后化学成分发生了一定的变化,经炒制后整体品质趋于稳定和统一。见表5。

表5 桑白皮和炒桑白皮相似度
2.3 主成分分析(PCA)将S1~10、C1~10 样品的色谱图导入“中药色谱指纹图谱相似度评价系统”软件,根据共有峰匹配数据得到一个8×20的共有峰峰面积矩阵,对该数据进行PCA分析,得到主成分的特征值及载荷矩阵。见表6—8。

表6 桑白皮和炒桑白皮共有峰峰面积 mV

表7 桑白皮和炒桑白皮的PCA特征值

表8 桑白皮和炒桑白皮的因子载荷矩阵
选取前两个特征值>1 的成分为主成分,其方差累计贡献值为76.186%,说明前4个因子在反映桑白皮炒制前后与8 个共有成分的相互关系中起主导作用,能够评价桑白皮生品与炒制品的品质。其中,第1 主成分的独立贡献率为48.469%,主要代表第2、3、4、5共有峰的信息,主成分2主要代表第1、6、7、8 共有峰的信息。表明通过PCA 分析降维处理后所提取的主成分能够代表桑白皮指纹图谱中8 个共有峰的主要信息。对前2 个主成分计算得到桑白皮及其炒制品的主成分得分,以主成分1 和主成分2 的得分分别作为X轴和Y轴,得到桑白皮及其炒制品的PCA 投影。可见桑白皮与炒桑白皮未完全分开,存在一定的交叉。S1 和C1,S2和C2,S4和C4,S5和C5的距离较近,说明这几批药材炒制前后变化较小,而其余批次的生品与炒制品距离较远,炒制前后产生的变化较大。把桑白皮和炒桑白皮分别做了凸多边形处理,桑白皮所围成的区域面积略大于炒桑白皮所围成的面积,说明桑白皮批次间的差异略大于炒桑白皮批次间差异。见图4。

图4 桑白皮和炒桑白皮的PCA得分投影图
2.4 线性判别分析(LDA)
2.4.1 桑白皮与炒桑白皮炒制前后线性判别 将表6中共有峰数据分为两组,组1(炒桑白皮),组2(桑白皮),进行线性判别分析,所得模型的准确率为90%,内部交叉验证准确率为45%。
2.4.2 不同产地桑白皮和炒桑白皮的线性判别 将S1~10、C1~10 样品按产地分为5 组进行LDA 分析,所得模型的分类结果准确率为95%,内部交叉验证准确率为55%。共得到4 个判别式函数,前两个函数的方差贡献率累积92.2%,计算桑白皮及其炒制品每一批次在函数1 和函数2 的判别得分,以函数1 为X 轴,函数2 的得分为Y 轴,得到LDA投影图,见图5。
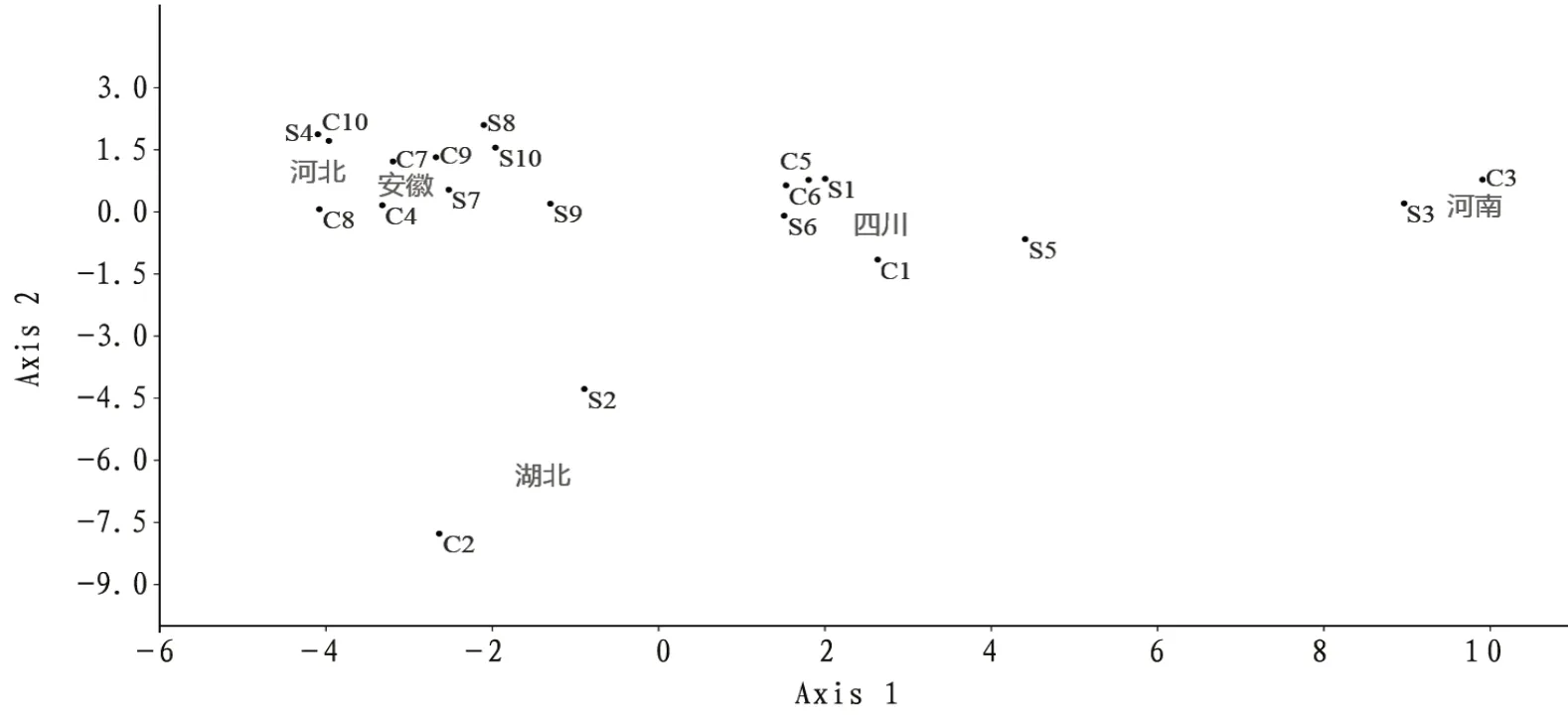
图5 桑白皮和炒桑白皮的LDA分析
可见主成分-线性判别模型对于炒制前后的桑白皮的预测区别精确度低。无法通过主成分-线性判别分析法对二者进行有效区分。
3 讨论
本试验比较了4 个流动相体系:乙腈-水、乙腈-0.1%甲酸水、乙腈-0.5%醋酸水、乙腈-0.5%三氟乙酸水。结果表明,乙腈-0.5% 三氟乙酸水系统为流动相时,各色谱峰分离效果较好,峰型对称且稳定,因此选择乙腈-0.5% 三氟乙酸水系统为流动相。
相似度、PCA及LDA模型三者均可用于桑白皮质量评价分析。桑白皮和炒桑白皮相似度均大于0.80,说明各自组内具有较高的相似性;PCA 和LDA 投影图可见桑白皮和炒桑白皮互相交错的情况,尝试建立的LDA 模型准确率较小,说明这些样品在多个维度上具有较高的相似性,不易找到合适的区分方法,这可能与样品的处理方法有关,目前正在采用冷提取的方式进行研究。
通过本研究结果可知,桑白皮和炒桑白皮二者的指纹图谱保留时间变化不大,峰的个数无明显差异,共有峰的峰面积在炒制前后有所改变,经炒制后整体品质趋向于统一,说明炒制对桑白皮有一定作用,但无明显的趋势呈现,这与李群等[17]对于桑白皮蜜炙前后的指纹图谱研究结果高度相似。桑白皮中发挥止咳平喘作用的关键化合物是东莨菪内酯,徐小飞等[18]发现蜜炙后东莨菪内酯质量分数略有增加,而李群等[17]的研究得出相反结论,发现蜜炙后东莨菪内酯呈下降趋势,提示应结合含量测定对炒桑白皮炮制工艺作进一步深入研究。有文献显示,桑白皮炒制性寒偏平,降气平喘力胜,多用于水饮停肺。蜜炙药味甘,性寒偏润,润肺清热,止咳平喘力强,多用于肺热咳喘[18-19]。提示需通过药理作用来探究经典名方泻白散中使用“蜜桑白皮”和“炒桑白皮”的合理性。
本试验以安徽产桑白皮为主要采集品种,同时收集了四川、河南、河北、安徽等地共10 批样品,涵盖了主产区和道地产区,在产地和质量方面具有代表性。本试验建立了桑白皮及炒桑白皮二者的指纹图谱,并同时进行PCA及LDA分析。探索桑白皮炒制前后的质量变化规律。虽然目前发现二者在化学成分上有较大一致性。但指纹图谱专属性较强,测定方法简便准确,重复性较好,对探索泻白散的桑白皮炒制炮制方式仍有一定的参考意义。而确定炒桑白皮炮制的具体工艺条件对规范炮制方法、提高经典名方泻白散质量非常重要,本课题将进一步深入研究。

