一种改进的休克尔分子轨道模型预测纯碳环分子稳定结构
张亦弛,侯华,王宝山
武汉大学化学与分子科学学院,武汉 430072
休克尔分子轨道(Hückel molecular orbital,HMO)模型是用于处理共轭体系(包括多烯CnHn+2、轮烯CnHn、多环芳烃、Möbius环烃等)的简便方法,它以碳原子p轨道为基函数,只考虑相邻最近的两个C原子之间的共振积分(β),从理论上定性解释了π共轭体系的电子结构特征、离域稳定性、4n+ 2规则等,并在化学研究及结构化学教学中受到广泛关注[1–5]。
然而,HMO在处理一类新型π共轭体系时遇到了困难,它无法正确解释纯碳环C2n的分子结构。碳环是继富勒烯、碳纳米管和石墨烯之后发现的一种新的碳结构[6,7],具有两套相互垂直的π共轭体系,如图1所示。根据HMO理论和4n+ 2规则,C6平面内π键和平面外π键的电子数均为6,该分子应具有芳香性,与苯环类似,其结构应呈现键角平均化的D6h对称性;然而实验与高水平从头算结果均表明键角交替的C6结构更加稳定,分子对称性降为D3h[8–10]。其他纯碳环分子(C2n,n= 2–15)均与C6有类似的结构特征,特别是最新发现的C18分子[11]。高分辨原子力显微镜研究直接证明C18并非全对称的cumulenic结构(D18h),而是键角交替的polyynic结构(D9h),并得到量子化学从头算支持[11,12]。

图1 C6分子的π共轭体系与结构
C2n分子结构对称性降低现象可以用二级Jahn-Teller效应结合高级电子相关计算(例如Diffusion Monte Carlo)加以解释[13],但该方法过于深奥,难以在本科生教学课堂中加以推广。更重要的是,针对纯碳环分子结构的计算结果严重依赖于理论方法,不同理论水平甚至得到截然相反的结论。例如流行的密度泛函理论(DFT)方法预测C18的cumulenic结构更稳定,而耦合蔟(CCSD)方法则支持C18的polyynic结构更稳定[12–14]。因此,需要一种新的简便模型或理论能够正确解释C2n分子结构难题。
HMO理论假设不相邻原子之间的共振积分为零。通常情况下此近似是合理的,因为不相邻原子之间的距离远大于相邻原子的距离。但是,从图1的C6分子结构可以看出:当对称性从D6h降为D3h时,处于间位碳原子之间的距离(1,3)、(1,5)、(3,5)将明显缩短,这些碳原子之间的共振积分显然不宜忽略,其可能是导致C2n分子通过降低对称性而获得额外稳定化能的直接原因。因此,本文针对HMO模型进行了改进,明确考虑间位碳原子之间的共振积分,成功解释了C2n分子的结构特征。
值得指出的是,文献报道了一些改进的HMO模型,包括Pariser-Parr-Pople (PPP)近似、扩展休克尔理论(EHMO)、Wheland模型、ω方法等[15–18]。这些早期的改进方法针对库伦积分、σ电子、重叠积分等进行更复杂处理,虽然可以用于C2n分子的结构与能量计算,但与其他从头算方法类似,均难以给出C2n结构中键角交替规律的物理图像。
1 改进的HMO理论
为了计算积分简便,本文使用对称性匹配的分子轨道。虽然HMO理论可将平面外与平面外π共轭体系统一处理,但因分子对称性发生变化,当考虑间位碳原子共振积分时,需将C2n按C4n与C4n+2两类体系分别处理。设pi为第i个C原子上构成平面内π键的正交归一化原子轨道,以C4和C6为例,推导出包含间位碳原子共振积分的HMO能级公式。
1.1 C4分子
C4分子cumulenic与polyynic结构的点群分别为D4h(正方形)与D2h(菱形),如图2所示。HMO模型仅需考虑点群绕主轴的旋转操作,D4h和D2h对称性约束下的分子轨道均可按照C2点群特征标表的不可约表示进行分类:pʹ1变换至pʹ1或pʹ3,pʹ2变换至pʹ2或pʹ4,因此基轨道可取为(pʹ1,pʹ2),其不可约表示为:


图2 C4分子结构及其对称性

对A、B两种不可约表示的分子轨道分别计算轨道积分:

根据HMO理论,定义:

其中βshort和βlong分别指短对角线和长对角线(即两类间位C原子)pʹ轨道的共振积分。公式(3a–3f)可化简为:

每个不可约表示的分子轨道哈密顿矩阵元分别满足久期行列式:

其中E为分子轨道能级。将(5a–b)分别代入(6a–b)可得:


其中正负号分别对映反键与成键轨道能级。简便起见,取α为相对能量的零点,由共振积分所贡献的能级可分别简化为:
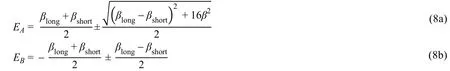
基于以上改进HMO模型的能级公式,可以详细分析C4分子的结构特征:
1) 若令βlong=βshort= 0,即不考虑间位原子轨道共振积分的贡献,则(8a–b)式简化为原始HMO的能级公式,即:

2) 对于D4h对称结构(即图2中正方形),因对角线相等,βshort=βlong,与之相应的分子轨道的能级分别为:

由于所有β积分均为负值,考虑间位共振积分后,A对称性能级降低,然而与此同时B对称性能级将升高相同的能量。因此,D4h结构的总电子能量将不随间位碳原子共振积分的引入而发生变化,与原始HMO结果相同,如图3所示。

图3 C4分子的π电子能级
3) 对于D2h对称结构(即图2中菱形),短对角的两对pʹ原子轨道的相互作用比长对角强,相应的分子轨道能级为:

可以看出,在原始HMO和D4h对称性下简并的EB能级发生了分裂,此时π电子总能量为:

由D4h变为D2h因对称性降低而获得的额外稳定化能为:
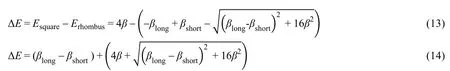
式(14)两个括号内项均为正值,即Erhombus 去对称化的C4n碳环属于D2nh点群,均可简化为C2n子群,而C2n点群特征标表具有与C2点群类似的不可约表示(例如:C2为A和B;C2n为A、B和E)。因此,以上针对C4的改进HMO能级公式适用于所有C4n分子,能够正确揭示C4n结构的键角交替变化趋势。 键角交替的C4n+2碳环分子结构所属的点群为D(2n+1)h,相应的分子轨道可简化为C2n+1子群处理。C2n+1点群的不可约表示包括A和E,与C2n点群相比,缺少了B对称性。因此,C4n+2碳环分子的能级公式与C4n不尽相同。例如,与C4分子不同,C6分子π体系的轨道能级为: 其能级如图4所示。当C6结构从D6h变为D3h时,由于对称性降低而产生的稳定化能为: 图4 C6分子的π电子能级 化简后即得: 可以看出,考虑间位碳原子的共振积分后,降低对称性并不会导致C6分子的简并能级发生分裂,但π电子成键轨道的能级下降,使得键角交替C6分子结构更加稳定。 明确考虑间位碳原子轨道对π共轭体系的贡献,是一种行之有效的HMO理论改进方法。采用改进的HMO模型,发现通过降低分子的对称性,间位碳原子的共振积分可产生额外的稳定化能,获得能量更低的π共轭体系。对于纯碳环分子,改进的HMO模型可以正确预测键角交替结构的能量更低,与高水平从头算或实验观测结果吻合,为理解Jahn-Teller效应中的对称性破损现象提供了新思路。1.2 C6分子




2 结语

