cyclin B1对头颈部鳞状细胞癌生物学特性及细胞焦亡的影响
罗水妹,张琦,黄谊强,谢贤和,2
(1.福建医科大学附属第一医院肿瘤内科,福建医科大学分子肿瘤研究所,福州 350005;2.福建省癌症精准医学重点实验室,福州 350005)
头颈部鳞状细胞癌(head and neck squamous cell carcinoma,HNSC) 是头颈部癌症中最常见的类型。其中,鼻咽癌居首位,统计显示2020年全球鼻咽癌发病13.3万余人,死亡达8万人[1]。尽管鼻咽癌对放射治疗(简称放疗) 相对敏感,但中晚期鼻咽癌放疗后局部复发和远处转移一直是治疗的难点。因此,寻找新的鼻咽癌治疗方法迫在眉睫。
细胞焦亡是一种新的程序性细胞死亡方式,以细胞膜孔形成、细胞肿胀、细胞溶解和炎性细胞因子释放著称[2],是宿主抵御感染和危险信号的关键,近年来已成为肿瘤领域研究热点。cyclin B1是细胞周期G2/M期的关键检查点蛋白,参与有丝分裂过程中染色体凝聚、核膜破裂和纺锤体组装等过程[3],在胃癌[4]、肺癌[5]、食管癌[6]等多种肿瘤中高表达,且与肿瘤恶性表型相关。研究[7]显示,cyclin B1高表达的HNSC患者放疗后局部复发或淋巴结转移风险高于低表达患者,提示cyclin B1高表达可能与HNSC放疗抵抗相关,因此,cyclin B1可能是颇具潜力的肿瘤治疗新靶点。本研究组前期研究[8]显示,敲低cyclin B1可抑制Hela细胞的生长并诱导细胞产生凋亡。此外,靶向敲低鼻咽癌细胞cyclin B1表达可诱导细胞自噬[9]。cyclin B1与细胞焦亡的相关性目前尚未见报道。因此,本研究拟探讨下调cyclin B1对HNSC细胞焦亡的影响,旨在发现HNSC治疗的新靶点和拓宽治疗思路。
1 材料与方法
1.1 数据来源
cyclin B1在HNSC与正常组织的差异表达分析数据来自GEO[10]及UALCAN数据库[11];cyclin B1的免疫组化数据源于Human Protein Atlas(HPA) 数据库[12];cyclin B1与HNSC的生存分析数据源于GEPIA数据库[13];细胞焦亡基因及cyclin B1的表达谱数据来源于OncoLnc数据库[14]。
1.2 实验材料及方法
1.2.1 主要试剂和仪器:人鼻咽癌细胞株CNE-2由福建医科大学附属第一医院中心实验室馈赠。人鼻咽癌细胞株HONE-1购自上海中亚生物公司。cyclin B1及阴性对照(negative control,NC) 的siRNA购自广州市锐博生物科技有限公司。GP-transfect-mate购自中国GenePharma公司。cyclin B1抗体(ab23053)、GSDMD抗体(ab215203)、GSDME抗体(ab215191)、caspase 1(CASP1) 抗体(ab207802)、caspase 3(CASP3)抗体(ab32351) 购自英国Abcam公司。内参β-actin抗体(AF7018)、GAPDH抗体(AF7021) 购自美国Affinity公司。凝胶成像仪(Biosciences AccuriC6型) 购自美国Bio-Rad公司,相差显微镜(IX50/70型) 购自日本Olympus公司。
1.2.2 细胞培养:用含10%胎牛血清、1%双抗(青霉素1 000 U/mL、链霉素0.1 mg/mL) 的RPMI1640培养基,于37 ℃、5%CO2恒温培养人鼻咽癌CNE-2、HONE-1细胞。
1.2.3 细胞转染:取对数生长期细胞(1.5×105/孔) 接种于6孔板,加入无抗完全培养基,融合度为40%时进行转染。以OPTI-MEM分别稀释siRNA和GP-transfect-mate,室温静置5 min,混匀形成转染复合物,室温下再静置20 min后加入至细胞培养基(siRNA终浓度100 nmol/L,GP-transfect-mate按照试剂说明书使用),转染后4~6 h更换为新培养基。cyclin B1-siRNA序列:正义为5’-CCAUGUUUAUUGCAAGCAATT-3’,反义为5’-UUGCUUGCAAUAAACAUGGTT-3’。NC-siRNA序列:正义为5’-UUCUCCGAACGUGUCA CGUTT-3’,反 义为5’-ACGUGACACGUUCGGAG AATT-3’。
1.2.4 蛋白印迹检测:转染48 h后,按常规方法提取细胞总蛋白。上样量为每泳道20 μg,行聚丙烯酰胺凝胶电泳,转膜(0.45 μm PVDF膜),室温封闭1 h,4 ℃孵育一抗过夜,TBST洗膜,室温孵育二抗1h,TBST洗脱,ECL化学发光显影。导出照片后用Adobe Photoshop软件读取各条带灰度值。
1.2.5 高通量全转录本基因芯片检测:将已验证cyclin B1敲低及对照组CNE-2细胞样本送上海市吉凯基因有限公司,进行Clariom D全转录本基因芯片检测,根据检测结果筛选差异表达基因。
1.2.6 相差显微镜检测细胞焦亡形态:细胞转染后48 h置于相差显微镜下,于亮场下观察细胞形态,并拍照记录。
1.2.7 ELISA检测:细胞转染后24 h更换为无血清RPMI1640培养基,再过24 h收集细胞培养上清液,于4 ℃、3 000 r/min离心20 min,取上清按照人白细胞介素(interlukin,IL) -1β ELISA kit(JL13662,江莱生物公司) 操作说明书进行检测。
1.3 统计学分析
利用GraphPad Prism 8进行统计分析,各组间结果比较用t检验,P< 0.05为差异有统计学意义。各基因集交集韦恩图通过EVenn在线可视化工具(http://www.ehbio.com/test/venn/#/)[15]实现。
2 结果
2.1 cyclin B1表达及其与临床特征的关系
GSE12452数据集(https://www.ncbi.nlm.nih.gov/geo/query/acc.cgi?acc=GSE12452)(图1A)、GSE13601数据集(https://www.ncbi.nlm.nih.gov/geo/query/acc.cgi?acc=GSE13601)(图1B) 及UALCAN数据库(http://ualcan.path.uab.edu) 分析(图1C) 显示,HNSC组织cyclin B1的表达水平分别高于正常组织的4.35倍(P< 0.000 1)、5.26倍(P< 0.000 1) 及2.42倍(P< 0.000 1)。HPA数据库[12](https://www.proteinatlas.org/ENSG000 00134057-Cyclin B1/pathology/head+and+neck+cancer) 分析显示,cyclin B1在头颈正常组织中低表达,而在HNSC组织呈中等强度表达(图1D、1F),提示cyclin B1在HNSC中蛋白及mRNA水平均为过表达。UALCAN数据库[11]进一步分析显示,cyclin B1表达水平与HNSC组织分级、肿瘤分期显著相关,组织分级越高,其表达水平越高(图2A),在2、3期患者中表达水平最高(图2B)。

图1 GEO、ULCAN及HPA数据库中cyclin B1在HNSC与正常组织中的表达Fig.1 Cyclin B1 expression in HNSC and normal control group in GEO,ULCAN and HPA databases

图2 cyclin B1表达与临床特征的关系Fig.2 Correlation between cyclin B1 expression and clinical parameters
2.2 cyclin B1表达水平与HNSC的预后显著相关
GEPIA数据库[13](http://gepia.cancer-pku.cn/detail.php) 分析提示,HNSC患者中cyclin B1高表达组(以中位数为分界) 的无病生存期(disease free survival,DFS) 短于低表达组(HR=1.4,P=0.043)(图3)。

图3 cyclin B1表达与HNSC患者DFS的相关性Fig.3 Correlation between cyclin B1 expression and disease free survival in HNSC patients
2.3 cyclin B1与细胞焦亡基因的相关性分析
33个细胞焦亡相关基因、GEPIA数据库[13]及GSE13601数据集筛选差异表达基因取交集结果显示,GEPIA数据库、GSE13601数据集分别筛选出6个(GSDMB,GSDMD,NLRP1,PLCG1,AIM2,IL1B) 和4个(CASP1,CASP4,AIM2,IL1B) 具有差异表达的细胞焦亡基因(图4A、4B)。OncoLnc数据库[14]获取496例HNSC患者cyclin B1及33个细胞焦亡基因表达谱数据分析显示,27.27%(9/33) 的细胞焦亡基因(AIM2,CASP6,GSDMD,NOD2,CASP8,GSDMA,SCAF11,GSDMB,CASP3) 在cyclin B1高表达组与低表达组(以中位数为界) 存在差异表达(图4C),提示HNSC中cyclinB1的表达可能与细胞焦亡生物学过程相关。
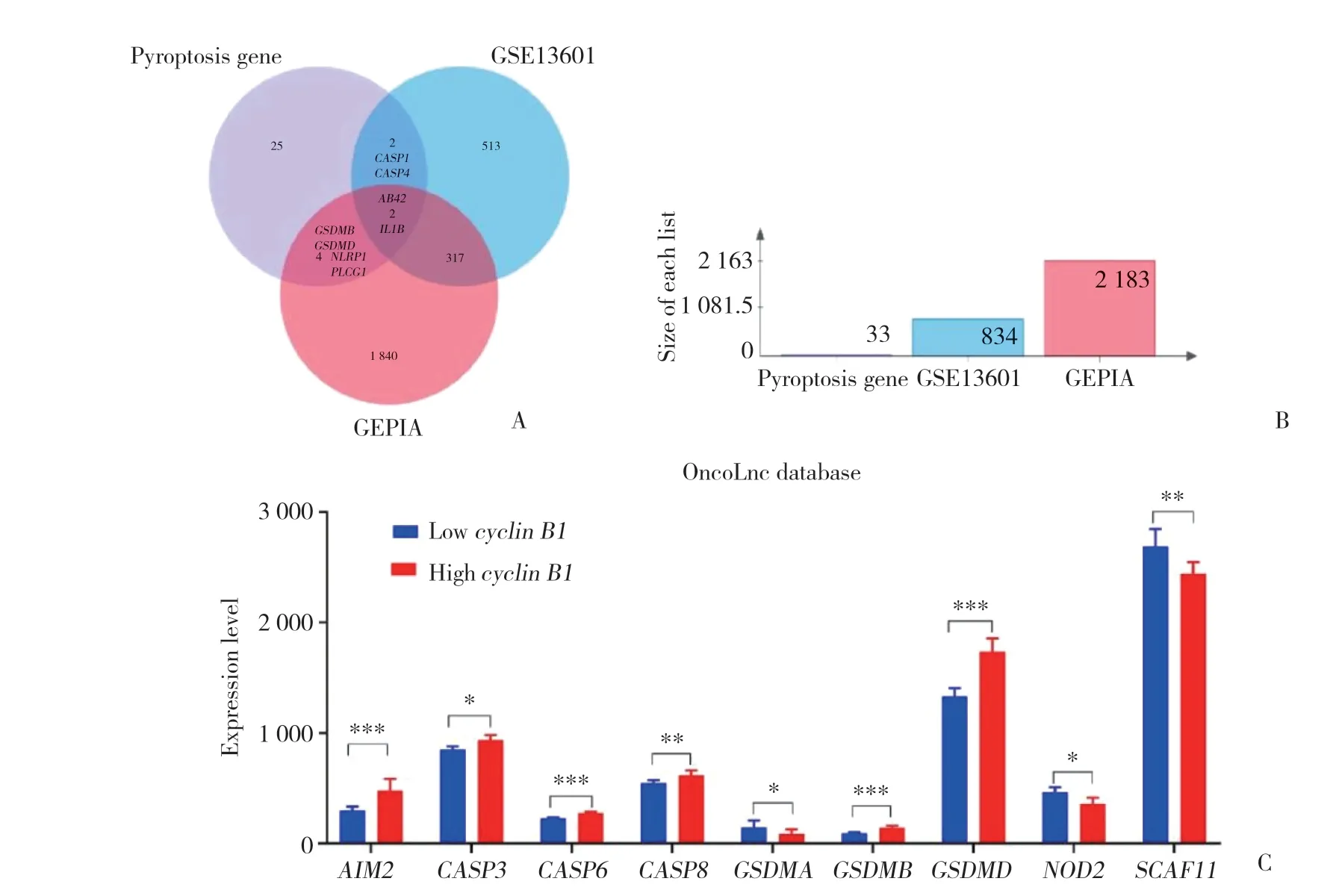
图4 HNSC与正常组织差异表达的细胞焦亡基因及其与cyclin B1表达的相关性Fig.4 Differential expression of pyroptosis genes between HNSC and normal and its correlation with cyclin B1 expression
2.4 cyclin B1与HNSC细胞焦亡的相关性
2.4.1 HONE-1、CNE-2细胞cyclin B1敲低效率检测:HONE-1、CNE-2细胞转染48 h后提取蛋白进行蛋白印迹检测,结果显示,cyclin B1敲低组(转染cyclin B1-siRNA,命名为KD组) 的cyclin B1蛋白表达较对照组(转染NC-siRNA,命名为NC组) 明显减弱,敲低效率分别为61.80%、85.99%(图5A、5B)。
2.4.2 高通量基因芯片检测cyclin B1敲低后差异表达基因:ClariomD全转录本基因芯片检测结果筛选出cyclin B1KD组(n=3) 与NC组(n=3) 差异表达的基因1 480个,其中包括细胞焦亡关键基因CASP1(图5C、5D)。

图5 cyclin B1敲低效率检测及转录组测序筛选差异表达的细胞焦亡基因Fig.5 Detection of cyclin B1 knockdown efficiency and transcriptome sequencing screening of differentially expressed pyrotopia genes
2.4.3 相差显微镜检测细胞焦亡形态:细胞焦亡在光镜下主要表现为细胞肿胀膨大、细胞膜表面可见气泡样突出物。CNE-2、HONE-1细胞分别转染cyclin B1siRNA 48 h后于相差显微镜下观察,可见KD组具有焦亡形态的细胞显著多于NC组(图6)。

图6 相差显微镜下观察HONE-1、CNE-2细胞焦亡形态Fig.6 Pyrophosis morphology of HONE-1 and CNE-2 cells observed by phase contrast microscope
2.4.4 蛋白印迹检测细胞焦亡关键蛋白:转染后48 h,提取蛋白行蛋白印迹实验检测细胞焦亡执行蛋白GSDMD、GSDME前体及裂解片段以及焦亡信号通路的关键分子CASP1、CASP3的前体及裂解片段,结果显示,2组均可检测到CASP1、CASP3裂解片段(图7A、7B),与对照组相比,cyclin B1敲低组的GSDMD、GSDME裂解片断有增加的趋势(图7C、7D)。

图7 蛋白印迹检测转染后48 h CASP1、CASP3蛋白的前体和裂解片段以及GSDMD、GSDME蛋白全长和裂解片段Fig.7 Western blotting detection of precursors and cleavage fragments of CASP1 and CASP3 and full length and cleavage fragments of GSDMD and GSDME 48 h after transfection
2.4.5 ELISA检测IL-1β:转染后48 h收集细胞培养液上清,通过ELISA检测IL-1β,结果显示,2组无统计学差异(P> 0.05),但cyclin B1敲低组的IL-1β水平有较对照组增多的趋势(图8)。

图8 ELISA检测转染后48 h细胞上清中IL-1β水平Fig.8 ELISA dection of IL-1β level in cell supernatant 48 h after transfection
3 讨论
cyclin B1在细胞周期G2/M期转化过程中发挥关键作用,在多种癌组织中异常高表达,从而导致肿瘤细胞增殖失控[3-6]。肿瘤是以细胞增殖、分化与细胞死亡平衡失调为特征的疾病,诱导肿瘤细胞死亡是目前各种抗肿瘤治疗的目的。本课题组前期研究[8]显示,沉默cyclin B1可显著抑制Hela细胞生长并诱导细胞凋亡,而沉默鼻咽癌CNE-2细胞的cyclin B1表达可通过AMPK-ULK1通路触发自噬[9],提示其可能成为肿瘤治疗的潜在靶标。细胞死亡形式主要分为程序性和非程序性细胞死亡两大类。程序性细胞死亡一直是肿瘤领域的研究热点,主要包括细胞凋亡、自噬及焦亡。细胞焦亡作为最新被证实的程序性死亡方式之一,与细胞周期关键检查点分子cyclin B1的关系目前尚未见报道。因此,本研究探讨了cyclin B1对HNSC细胞焦亡的影响,有助于全面揭示cyclin B1在HNSC中发挥的生物学功能,为探讨cyclin B1能否成为肿瘤治疗靶点提供理论依据。本研究通过大数据分析发现cyclin B1在HNSC组织中显著高表达,且与HNSC组织分级和分期显著相关,提示cyclin B1在HNSC的发生、发展中起着重要作用。
细胞焦亡以Gasdermin家族蛋白N端裂解片段在细胞膜上形成1~2 nm孔隙,使膜失去完整性,进而释放出大量炎性细胞因子和炎性细胞内容物为特征[2]。本研究结合GEO、TCGA等数据库分析发现8个细胞焦亡基因在HNSC与正常组织中存在差异表达,提示细胞焦亡可能在HNSC的发生、发展过程中发挥一定作用。此外,本研究还发现9个细胞焦亡相关基因与cyclin B1的表达水平存在相关性,提示cyclin B1表达可能参与HNSC细胞焦亡的生物学过程。据此,进一步以鼻咽癌细胞为研究对象,通过沉默CNE-2细胞的cyclin B1表达后进行转录组测序,结果显示cyclin B1沉默可显著增加细胞焦亡通路关键分子CASP1的表达,也进一步支持了cyclin B1与细胞焦亡存在相关性的结论。
细胞焦亡经典通路中,由NLRP3、NLRC4、AIM2、pyrin和NLRP1组装成的典型炎症小体负责CASP1前体的切割[16-17],而CASP1前体被处理后的裂解片段则可进一步处理GSDMD,使其释放出N端结构域发挥膜穿孔的功能[18],可触发焦亡及诱导炎性细胞因子(IL-1β、IL-18) 的释放[19-20]。另有研究[21]显示,GSDME可被CASP3特异性剪切生成GSDME-N端片段诱导细胞焦亡。本研究通过RNA干扰技术沉默HONE-1、CNE-2细胞cyclin B1后,相差显微镜下观察到cyclin B1敲低组具有焦亡形态的细胞显著多于对照组,ELISA检测结果显示cyclin B1敲低组细胞释放的IL-1β较对照组升高,蛋白印迹结果显示2组均可见CASP1、CASP3裂解片段,与对照组相比,cyclin B1敲低组的细胞焦亡执行蛋白GSDMD-N端片段及GSDME-N端片段有增加的趋势,但2组无统计学差异,因此,cyclin B1参与细胞焦亡生物学过程是否通过经典通路CASP1/GSDMD及CASP3/GSDME途径实现仍无定论。
综上所述,本研究结果显示,cyclin B1在HNSC组织中显著高表达,cyclin B1高表达与HNSC的不良分级、分期及DFS显著相关,且cyclin B1表达与细胞焦亡存在相关性,但其具体机制有待进一步探究。

