大蒜AsPEX7基因的克隆与非生物胁迫响应分析
杨青青 赵永强 刘灿玉 葛洁 陆信娟 张碧薇 杨峰 樊继德


摘要:为了解大蒜PEX7基因及其编码的蛋白质结构特性,分析该基因对不同非生物胁迫的响应情况,从大蒜品种徐紫1号的叶片RNA中克隆获得AsPEX7基因。序列分析结果表明,AsPEX7基因含有1个长度为951 bp的开放阅读框(ORF),编码316个氨基酸,其相对分子质量为35.57 ku,理论等电点为5.55,为亲水性蛋白。氨基酸组成中脂肪族氨基酸的比例最高,其次为碱性氨基酸,酸性氨基酸和芳香族氨基酸最低。AsPEX7蛋白含有25个磷酸化位点,无信号肽和跨膜结构,二级结构由α-螺旋、延伸主链和随机卷曲组成,比例分别为5.06%、40.19%和4715%。实时荧光定量PCR(RT-qPCR)结果显示,在高温(38 ℃)、低温(4 ℃)、干旱(质量体积分数为20%的PEG 6000)和高盐(200 mmol/L NaCl)4种非生物胁迫处理条件下,AsPEX7基因的相对表达水平总体升高,表明该基因可能在抵抗非生物胁迫中发挥重要作用。本研究结果为深入解析PEX7基因调控大蒜生长发育及非生物胁迫的分子机制提供了理论参考基础。
关键词:大蒜;AsPEX7基因;基因克隆;非生物胁迫;表达分析
中图分类号: S633.401 文献标志码: A
文章编号:1002-1302(2022)06-0024-08
收稿日期:2021-06-16
基金项目:江苏省农业科学院探索性颠覆性创新计划[编号:XZ(21)1229];国家特色蔬菜产业技术体系项目(编号:CARS-24-A-07);江苏现代农业产业技术体系建设专项(编号:JATS[2020]043)。
作者简介:杨青青(1994—),女,河南洛阳人,硕士,研究实习员,主要从事大蒜分子生物学研究。E-mail:2521918664@qq.com。
通信作者:樊继德,硕士,副研究员,主要从事大蒜育种与栽培研究。E-mail:fanjide@163.com。
大蒜(Allium sativum L.)属于百合科葱属,喜好冷凉,是多年生宿根作物,其鳞茎、叶片均可作为食用蔬菜,在世界各地普遍种植[1]。在大蒜引种和栽培过程中,非生物胁迫是影响其生长发育以及降低其产量和品质的不利环境因子[2-3]。过氧化物酶体是在真核细胞中普遍存在且具有多种功能的单核细胞器,在保护植物细胞和增强植物对高盐耐受性方面起着重要作用[4-5]。过氧化物酶体合成相关蛋白(peroxisome generate protein)是参与过氧化物酶体生物发生的一类蛋白质,这类蛋白总称为Peroxin,其编码基因为PEX[6]。PEX基因是参与过氧化物酶体形成与增殖的基因,同时也是调控过氧化物酶体代谢活动的重要基因[7]。近年来,越来越多的研究证明,PEX基因也可以调节植物对非生物胁迫的反应[8]。
过氧化物酶体蛋白根据蛋白的分布不同,可以分为合成蛋白、基质蛋白、膜蛋白[9]。在生物体内,过氧化物酶体合成相关蛋白主要参与过氧化物酶体增殖、分化和蛋白转运等过程,已在拟南芥(Arabidopsis thaliana)中鉴定出的PEX蛋白超过30多种[10]。过氧化物酶体的生物发生是由过氧化物酶介导[11]。植物过氧化物酶体含有多种酶,如过氧化氢酶、过氧化物酶和氧化酶[12]。过氧化物酶体也是乙醛酸循环、脂肪酸的β氧化分解、活性氧的调节和次级代谢产物合成的重要部位[13]。以往的研究证明,过氧化物酶体缺乏本身的基因组,因此过氧化物酶体所有的组成蛋白都被编码在核基因组中,并在导入到过氧化物酶体之前被翻译到胞质核糖体上[14]。蛋白质从细胞质到过氧化物酶体的转运依赖于过氧化物酶体输入受体蛋白,肽链上的定位信号(peroxisome targeting singal,简称PTS)负责基质蛋白的转运[15]。目前,2种类型的过氧化物酶体靶向信号PTS1和PTS2已在过氧化物酶体基质酶中鉴定[16]。PEX7是PTS2的受体,由PEX7基因编码[17]。虽然PEX7在蛋白质的运输过程中起着重要的作用,但其调节功能的机制尚不清楚。
在烟草中,转基因植株在遭受H2O2胁迫后,过表达腊梅CpPEX22基因,植株内CAT、POD、SOD的活性和MDA含量都显著增加[18]。转入细叶百合LpPEX7基因的拟南芥,其种子在盐胁迫下发芽率明显高于野生型拟南芥[19]。同样,在拟南芥中,过表达胡杨PePEX11基因,植株抗氧化能力和耐盐性增强[20]。在添加氯化钠或者甘露醇的MS培养基上培养PEX5突变体转基因拟南芥和野生型拟南芥,发现PEX5突变体幼苗的SOD和POD活性显著低于野生型,表明PEX5参与调控拟南芥的抗逆性[21]。大蒜是耐寒性作物,在冷凉的环境下生长良好,高温会造成大蒜的产量和品质下降。目前的研究已经证实PEX7蛋白是合成过氧化物酶体的关键蛋白,但PEX7基因是否参与大蒜对非生物胁迫响应的过程还未有报道,因此研究大蒜AsPEX7基因与逆境胁迫之间是否有一定的应答关系是本研究要解决的问题。本研究从大蒜品种中克隆得到AsPEX7基因,对该基因进行生物信息学分析,利用RT-qPCR检测AsPEX7基因在高温、低温、干旱及高盐4种非生物胁迫下的相对表达水平,为进一步研究AsPEX7基因在大蒜抗逆境方面的代谢途径提供理论基础,并为深入了解AsPEX7基因在大蒜抵抗非生物胁迫中的功能提供依据。
1 材料與方法
1.1 材料及处理
大蒜品种徐紫1号由江苏徐淮地区徐州农业科学研究所园艺研究室保存。试验材料蒜瓣播种于蛭石和有机质配成的混合基质中,17 d之后将大蒜幼苗转移到水培箱,营养液为Hoagland标准营养液配方。缓苗7 d后对大蒜植株进行高温(38 ℃)、低温(4 ℃)、干旱(质量体积分数为20%的PEG 6000)和高盐(200 mmol/L)4种非生物胁迫处理,处理时间分别为0、1、4、8、24、48 h,对照组用ddH2O处理,每个处理3次重复。取大蒜叶片用于 RNA的提取以及cDNA的合成。
1.2 大蒜AsPEX7基因的克隆
基于本课题组的大蒜转录组数据库,通过与其他物种PEX7基因序列BLAST比对分析获得大蒜AsPEX7基因的序列。根据开放阅读框(ORF)序列设计克隆引物,AsPEX7基因正向引物AsPEX7-F:5′-ATCCCCAAATCCCAAGCCCTAAAAAATCAACAG-3′,反向引物AsPEX7-R:5′-AAAATATAAGCTTACCCAAGTGAGAAAA-3′。以徐紫1号的叶片为cDNA模版进行PCR反应。扩增体系总体积 20 μL,包含cDNA模板1 μL、正向引物和反向引物各1 μL、ddH2O 7 μL以及Ex Taq酶10 μL。设置PCR反应条件:94 ℃预变性5 min;94 ℃变性30 s、54 ℃退火30 s、72 ℃延伸60 s,共34个循环;72 ℃延伸10 min。PCR反应产物用质量浓度12 g/L的琼脂糖凝胶电泳进行分离检测,回收产物连接pMD19-T质粒载体,并转化到大肠杆菌DH5α中,挑取单菌落摇菌,经PCR检测后交由南京金斯瑞生物科技有限公司进行测序验证。
1.3 序列分析
通过NCBI (https://www.ncbi.nlm.nih.gov)对获得的目的基因片段的核苷酸和氨基酸序列进行BLAST比较和保守域预测;使用ExPASy蛋白质组分析工具中的Prot-Param (http://www.expasy.ch/tools/protparam.html) 软件对蛋白质相对分子质量、氨基酸构成成分和理论等电点等进行分析;采用DNAMAN软件进行ICE1序列的多重比对及蛋白质的亲水性/疏水性预测;利用MEGA 5.2软件构建蛋白系统进化树[22];利用NCBI CDD数据库大蒜AsPEX7氨基酸序列进行保守域预测;利用SignalP (http://www.cbs.dtu.dk/services/SignalP/)软件进行信号肽分析预测;利用SOPMA 软件对大蒜AsPEX7蛋白进行二级结构预测及分析;跨膜结构域和信号肽预测分别采用TMHMM(http://www.cbs.dtu.dk/services/TMHMM/)[23]和SignalP 4.1(http://www.cbs.dtu.dk/services/SignalP/)软件进行网上运行分析[24]。
1.4 实时荧光定量PCR
使用Real-Time PCR检测系统 (Bio-rad,CFX96,USA) 在96孔板中进行实时定量PCR反应。选用大蒜SNAD基因作为内参基因,其正向引物BD-SAND-F:5′-GCGTCAACGAATGTTCCAATTACCA-3′,反向引物BD-SAND-R:5′-TCTCTTCAGTCTCAACTTCATCAGCAT-3′。用于AsPEX7基因表达分析的正向引物AsPEX7-qF:5′-ACTTCGGAATCCTCGGCAACGG-3′,反向引物AsPEX7-qR:5′-ATCGTAGATGGCGTCGGCTGTG-3′。内参基因与目标基因同时进行扩增,每个样品分别设置3个生物学重复和3个技术重复。PCR反应体系总体积20.0 μL,包含ddH2O 7.2 μL,SYBR Green Ⅰ mix 10.0 μL,cDNA 2.0 μL以及正向荧光定量引物和反向熒光定量引物各0.4 μL。RT-qPCR反应程序:95 ℃预变性30 s;95 ℃变性5 s,60 ℃退火延伸 20 s,共40个循环;通过从65 ℃至95 ℃逐步扩增加热获得熔解曲线。采用 2-ΔΔCT 法计算 AsPEX7基因的相对表达量,并使用SPSS 20. 0 和 EXCEL 2019 软件进行差异显著性分析[25]。
2 结果与分析
2.1 AsPEX7基因的克隆与序列分析
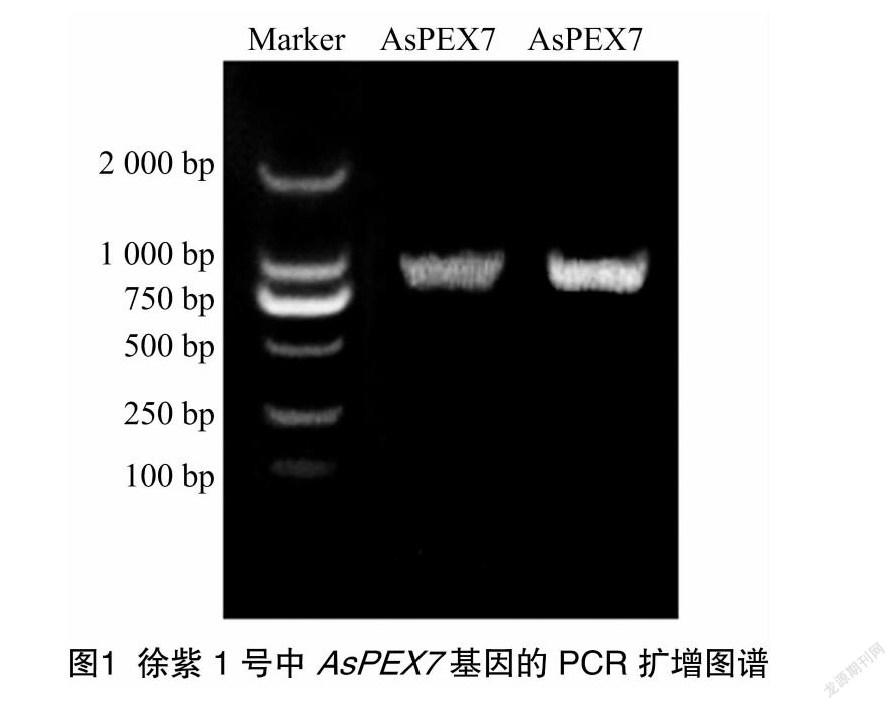
以大蒜未经胁迫处理叶片的cDNA为模版,使用特异性引物AsPEX7-F和AsPEX7-R扩增得到1条长度约 950 bp的目的片段 (图1),片段大小与预期一致。将回收产物依次进行连接、转化及测序,获得AsPEX7基因开放阅读框 (ORF)的序列。测序及分析结果显示,克隆得到的AsPEX7基因含有1个长度为 951 bp的开放阅读框,编码 316个氨基酸(图2)。
2.2 AsPEX7基因的氨基酸序列分析
2.2.1 保守域结构的预测 利用Blast Conserved Domains Search分析大蒜品种徐紫1号AsPEX7基因氨基酸序列的保守域,结果显示,AsPEX7基因的氨基酸序列在第59位至第 306 位氨基酸间含有1个WD40结构域(图3)。
2.2.2 同源性比对分析 将大蒜AsPEX7基因与NCBI数据库中铁皮石斛(Dendrobium catenatum,登录号:XP_020705736.1)、蝴蝶兰(Phalaenopsis equestris,登录号:XP_020576756.1)、银白杨
(Populus alba,登录号:XP_034920855.1)、蒺藜苜蓿(Medicago truncatula,登录号:XP_013462562.1)、香荚兰(Vanilla planifolia,登录号:KAG0484672.1 )、藜麦(Chenopodium quinoa,登录号:XP_021724594.1)和建兰(Cymbidium ensifolium,登录号:QEX51205.1)7种植物PEX7基因编码的氨基酸序列通过DNAMAN进行序列进行比对,结果表明,AsPEX7基因的氨基酸序列与铁皮石斛、蝴蝶兰和银白杨等植物PEX7基因的氨基酸序列一致性较高(图4),表明PEX7具有较高的保守性。
2.2.3 氨基酸组成及理化性质的分析 将AsPEX7蛋白与不同植物PEX蛋白进行氨基酸组成成分及理化性质分析。结果显示,大蒜品种徐紫1号AsPEX7蛋白的相对分子质量为35.57 ku,理论等电点(pI)为5.55。 AsPEX7蛋白和10种植物PEX蛋白氨基酸数量在316~320之间,相对分子质量在35 ku左右,碱性氨基酸的比例总体上高于酸性氨基酸的比例,脂肪族氨基酸的比例明显高于芳香族氨基酸的比例(表1)。
2.2.4 亲水性和疏水性的分析 采用DNAMAN软件对大蒜品种徐紫1号AsPEX7基因的氨基酸序列进行亲水性/疏水性分析(图5)。结果表明,在亲水性区域,第77位丙氨酸(Ala)的亲水性最强,第75位缬氨酸(Val)较强;在疏水性区域,第115位亮氨酸 (Leu)的疏水性最强,第201位酪氨酸(Tyr)、第199位天冬酰胺(Asn)和第142位苯丙氨酸(Phe)的疏水性较强。总体来看,AsPEX7基因的氨基酸序列中的大部分氨基酸为亲水性氨基酸,推测AsPEX7蛋白属于亲水性蛋白(图5)。
2.3 AsPEX7的预测分析
2.3.1 二级结构的预测分析 用SOPMA软件对AsPEX7基因的蛋白质进行二级结构预测,结果表明,该转录因子是由5.06%的α螺旋(alpha helix)、40.19%的延伸主链(extended chain)和47.15%的无规则卷曲(random coil)构成(图6)。总体上看,AsPEX7蛋白主要的二级结构是延伸主链和无规则卷曲。
2.3.2 跨膜结构和信号肽的预测 大蒜AsPEX7蛋白的跨膜结构预测结果表明,AsPEX7基因的氨基酸可能不存在跨膜结构(图7)。跨膜结构分析的结果显示,AsPEX7 蛋白序列不存在信号肽,表明可能不是膜结合蛋白(图8)。研究表明,构成蛋白质跨膜结构的氨基酸大部分为疏水性氨基酸,预测结果也表明AsPEX7蛋白属于亲水性蛋白。
2.3.3 磷酸化位点的预测 大蒜AsPEX7磷酸化位点预测结果表明,AsPEX7基因的氨基酸序列中共有25个磷酸化位点,包括第25、28、67、82、99、119、122、124、139、152、154、156、167、243位共14个丝氨酸磷酸化位点,第6、93、128、142、147、171、195、208、297位共9个苏氨酸磷酸化位点,第148位和第304位共2个酪氨酸磷酸化位点(图9)。
2.4 非生物胁迫下AsPEX7基因的表达
为了分析AsPEX7基因在非生物胁迫下的表达特性,采用荧光定量PCR检测该基因在高温、干旱、低温和高盐下的表达情况,AsPEX7基因的相对表达水平见图10。 结果表明,不同非生物胁迫处理下AsPEX7基因的相对表达水平存在差异。
高温处理1、4、24、48 h时,AsPEX7基因的相对表达水平与处理0 h相比显著升高,分别为处理 0 h 的10.31倍、4.74倍、4.05倍、3.78倍,其中,高温处理 1 h 时AsPEX7基因的相对表达水平最高。但在处理8 h 时,AsPEX7基因的相对表达水平与处理0 h相比略有降低。
干旱处理1、4、8、24 h时,与处理0 h相比AsPEX7基因的相对表达水平逐渐升高,并在处理24 h时达到峰值,分别为处理0 h的1.24倍、2.25倍、446倍、6.80倍;干旱处理48 h,AsPEX7基因的相对表达水平与处理0 h相比明显降低。
低温处理1、4、8 h时,AsPEX7基因的相对表达水平与处理0 h相比显著升高, 分别为处理0 h的3.59倍、5.05倍、8.93倍;低温处理24 h AsPEX7基因的相对表达水平与处理0 h相比无明显变化。
高盐处理1、8、24 h 时,AsPEX7基因的相对表
达水平与处理0 h相比有不同程度的升高,分別为处理0 h的1.98倍、4.46倍、1.07倍,其中,高盐处理8 h 时AsPEX7基因的相对表达水平最高。高盐处理4、48 h时,AsPEX7基因的相对表达水平较处理0 h均略有降低。
3 讨论与结论
非生物胁迫是造成陆生植物生长发育不良和产量下降的主要因素[25-26]。在高温下,植物细胞膜的通透性、抗氧化物系统、渗透调节物质、呼吸作用以及蒸腾作用均会发生改变,且高温下植物通常会出现叶片变黄、坏死、花果脱落等热害病症[27-29]。高盐胁迫会造成土壤中的盐分升高,降低植物根系的吸水能力,造成植物体内水分减少,进而出现萎蔫和死亡的症状[30]。大蒜喜好冷凉的环境条件,其生长适宜温度为12~25 ℃,因此,非生物胁迫会严重影响大蒜的正常生长发育、产量和品质[31]。
本研究从大蒜品种徐紫1号叶片中克隆获得AsPEX7基因,该基因的开放阅读框编码316个氨基酸,其氨基酸序列的第 59位至第 306位氨基酸间含有1个WD40保守域。研究表明,WD40结构域介导蛋白质之间的相互作用,形成复合体结构从而调控下游的基因表达[32]。因此推测,AsPEX7基因可能在非生物胁迫中通过调控下游基因的表达来提高大蒜的抗逆性。与其他植物PEX蛋白的氨基酸序列的多重比对结果表明,PEX蛋白在进化上具有保守性。AsPEX7基因共有25个磷酸化位点,这些磷酸化位点可能在维持蛋白质空间稳定性和调控植物生理生化反应过程中发挥重要作用。跨膜结构和信号肽预测表明,AsPEX7蛋白是不含跨膜结构和信号肽的亲水性蛋白,据此推测AsPEX7蛋白可能是非分泌蛋白。
在真核生物细胞中,过氧化物酶体是一类在物质代谢方面起着重要作用的单核细胞器[33]。植物遭受非生物胁迫时,会产生过量的活性氧,造成氧化损伤,而过氧化物酶体能够通过清除过量的活性氧来调节氧化还原平衡[34]。所有过氧化物酶体基质蛋白都在核基因组中进行编码,由胞质核糖体合成并在PEX蛋白的帮助下转运到过氧化物酶体中[35]。基质蛋白靠自身序列所具有的过氧化物酶体定位信号(PTS)而被识别和转运到过氧化物酶体,PEX5蛋白和PEX7蛋白是分别识别不同的过氧化物酶体靶向信号PTS1和PTS2的受体[34-35]。因此,AsPEX7蛋白作为带有PTS2信号基质蛋白的转运蛋白,对过氧化物酶体的形成起着重要的作用,研究AsPEX7基因的表达特性,对研究大蒜的抗盐碱和高温具有重要的意义。本研究对大蒜进行高温(38 ℃)、低温(4 ℃)、干旱(质量体积分数为20%的PEG 6000)和高盐(0.2 mol/L NaCl)4种非生物胁迫处理,从 AsPEX7基因在胁迫处理后的大蒜叶片中的表达情况来看,AsPEX7基因分别在高温处理的1 h和高盐处理8 h的表达量达到峰值,并且在不同时间AsPEX7基因的表达量总体呈现上调趋势,说明大蒜在受到逆境胁迫时,AsPEX7基因可以启动程序表达来应对环境的改变。
目前,PEX基因在其他作物中大多處于基因克隆分析层面上。并且大蒜的分子遗传研究较为缓慢,因此本试验通过在分子水平上对大蒜AsPEX7基因进行研究,并分析该基因对不同非生物胁迫的响应,为了解AsPEX7基因在大蒜抗逆境胁迫中发挥的作用提供了参考。
参考文献:
[1]梅四卫,朱涵珍. 大蒜研究进展[J]. 中国农学通报,2009,25(8):154-158.
[2]杨献光,梁卫红,齐志广,等. 植物非生物胁迫应答的分子机制[J]. 麦类作物学报,2006,26(6):158-161.
[3]齐 琪,马书荣,徐维东. 盐胁迫对植物生长的影响及耐盐生理机制研究进展[J]. 分子植物育种,2020,18(8):2741-2746.
[4]高飞雁,李 玲,王教瑜,等. PEX基因在过氧化物酶体形成及真菌致病性中的作用[J]. 遗传,2017,39(10):908-917.
[5]An C J,Gao Y F,Li J Y,et al. Alternative splicing affects the targeting sequence of peroxisome proteins in Arabidopsis[J]. Plant Cell Reports,2017,36(7):1027-1036.
[6]孙 艳,孙雪培,姜玲玲,等. 过氧化物酶体生物发生研究进展[J]. 生物学杂志,2015,32(2):83-86.
[7]Hu J P,Aguirre M,Peto C,et al. A role for peroxisomes in photomorphogenesis and development of Arabidopsis[J]. Science,2002,297(5580):405-409.
[8]Islinger M,Voelkl A,Fahimi H D,et al. The peroxisome:an update on mysteries 2.0[J]. Histochemistry and Cell Biology,2018,150(5):443-471.
[9]Koch J,Pranjic K,Huber A,et al. PEX11 family members are membrane elongation factors that coordinate peroxisome proliferation and maintenance[J]. Journal of Cell Science,2010,123(Pt 19):3389-3400.
[10]田国忠,李怀方,裘维蕃. 植物过氧化物酶研究进展[J]. 武汉植物学研究,2001,19(4):332-344.
[11]Cui S K,Fukao Y,Mano S,et al. Proteomic analysis reveals that the rab GTPase RabE1c is involved in the degradation of the peroxisomal protein receptor PEX7 (peroxin 7)[J]. Journal of Biological Chemistry,2013,288(8):6014-6023.
[12]Platta H W,Erdmann R. Peroxisomal dynamics[J]. Trends in Cell Biology,2007,17(10):474-484.
[13]Platta H W,Hagen S,Erdmann R.The exportomer:the peroxisomal receptor export machinery[J]. Cellular and Molecular Life Sciences:CMLS,2013,70(8):1393-1411.
[14]Rodrigues T A,Alencastre I S,Francisco T,et al. A PEX7-centered perspective on the peroxisomal targeting signal type 2-mediated protein import pathway[J]. Molecular and Cellular Biology,2014,34(15):2917-2928.
[15]Francisco T,Rodrigues T A,Freitas M O,et al. A cargo-centered perspective on the PEX5 receptor-mediated peroxisomal protein import pathway[J]. Journal of Biological Chemistry,2013,288(40):29151-29159.
[16]Kiel J A K W,van der Klei I J.Proteins involved in microbody biogenesis and degradation in Aspergillus nidulans[J]. Fungal Genetics and Biology,2009,46(1):S62-S71.
[17]Singh T,Hayashi M,Mano S,et al. Molecular components required for the targeting of PEX7 to peroxisomes in Arabidopsis thaliana[J]. Plant Journal,2009,60(3):488-498.
[18]赵亚虹. 蜡梅过氧化物酶体生成蛋白基因CpPEX22的克隆及功能初步分析[D]. 重庆:西南大学,2013.
[19]何 好,朱国庆,陈诗雅,等. 细叶百合LpPEX7基因克隆及盐胁迫下的表达特性分析[J]. 植物研究,2020,40(2):274-283.
[20]姚 琨,练从龙,王菁菁,等. 胡杨PePEX11基因参与调节盐胁迫下拟南芥的抗氧化能力[J]. 北京林业大学学报,2018,40(5):19-28.
[21]詹 爽,梁绮雯,罗为桂,等. PEX5参与调控拟南芥根系抗逆性的初步研究[J]. 激光生物学报,2019,28(4):336-342.
[22]Tamura K,Peterson D,Peterson N,et al. MEGA5:molecular evolutionary genetics analysis using maximum likelihood,evolutionary distance,and maximum parsimony methods[J]. Molecular Biology and Evolution,2011,28(10):2731-2739.
[23]Ikeda M,Arai M,Lao D M,et al. Transmembrane topology prediction methods:a re-assessment and improvement by a consensus method using a dataset of experimentally-characterized transmembrane topologies[J]. In Silico Biology,2002,2(1):19-33.
[24] Dyrlv Bendtsen J,Nielsen H,von Heijne G,et al. Improved prediction of signal peptides:SignalP 3.0[J]. Journal of Molecular Biology,2004,340(4):783-795.
[25]江海燕,杜菊花,毛 恋,等. 植物响应高温胁迫转录因子研究进展[J]. 分子植物育种,2020,18(10):3251-3258.
[26]Gao Y,Jiang W,Dai Y,et al. A maize phytochrome-interacting factor 3 improves drought and salt stress tolerance in rice[J]. Plant Molecular Biology,2015,87(4/5):413-428.
[27]徐 海,宋 波,顾宗福,等. 植物耐热机理研究进展[J]. 江苏农业学报,2020,36(1):243-250.
[28]李 丽,刘双清,杨远航,等. 热激转录因子在植物抗非生物胁迫中的功能研究进展[J]. 生物技术进展,2018,8(3):214-220.
[29]宋有金,吴 超. 高温影响水稻颖花育性的生理机制综述[J]. 江苏农业科学,2020,48(16):41-48.
[30]Parihar P,Singh S,Singh R,et al. Effect of salinity stress on plants and its tolerance strategies:a review[J]. Environmental Science and Pollution Research International,2015,22(6):4056-4075.
[31]侯進慧,刘春雷. 我国大蒜资源深加工与产业化研究进展[J]. 生物资源,2020,42(1):36-42.
[32]严 莉,陈建伟,王翠平,等. 基于转录组信息的黑果枸杞WD40蛋白质家族分析[J]. 核农学报,2019,33(3):482-489.
[33]Hu J P. Plant peroxisomes:small organelles with versatility and complexity[J]. Journal of Integrative Plant Biology,2019,61(7):782-783.
[34]Mittler R,Vanderauwera S,Gollery M,et al. Reactive oxygen gene network of plants[J]. Trends in Plant Science,2004,9(10):490-498.
[35]Kunze M,Malkani N,Maurer-Stroh S,et al. Mechanistic insights into PTS2-mediated peroxisomal protein import[J]. Journal of Biological Chemistry,2015,290(8):4928-4940.

