一种新HBsAg化学发光试剂盒的研制
沈冬 温江涛
[摘要] 目的 评价一种新HBsAg化学发光定量试剂盒主要性能指标。 方法 对2019年8月16日至2020年1月15日南京医科大学附属苏州科技城医院5035例阴性体检标本、209例阴性住院患者标本和101例潜在交叉反应样本进行了检测。对30个血清盘和434份预选阳性标本(包括基因型和亚型)进行敏感度检测。对25个突变株进行检测。对不同基因型进行敏感度试验。对25例HBsAg阳性和27例HBsAg阴性血清/血浆样本进行血清-血浆等效性检测。 结果 该HBsAg试剂盒检测特异度为99.96%,敏感度为100.00%。在30个血清盘中,该试剂与雅培HBsAg试剂敏感度相同,比列出的最不敏感试剂早123 d,平均提前4.1 d。突变株的检测能力相同。稀释基因型组中每个样本的敏感度均<0.13 IU/ml。所有配对样本均显示血清-血浆等效性。结论 该HBsAg定量試剂性能优良,适合临床应用。
[关键词] HBsAg;化学发光;定量分析;特异度;敏感度
[中图分类号] R392.3 [文献标识码] B [文章编号] 1673-9701(2022)07-0126-05
Performance of a new chemiluminescent HBsAg quantitative assay
SHEN Dong WEN Jiangtao
Department of Clinical Laboratory, the Affiliated Suzhou Science & Technology Town Hospital of Nanjing Medical University, Suzhou 215153, China
[Abstract] Objective To evaluate the main performance indicators of a new HBsAg chemiluminescence quantitative kit. Methods From August 16, 2019 to January 15, 2020, 5,035 negative physical examination specimens, 209 negative inpatients′ specimens, and 101 potential cross-reactive specimens were tested in our hospital. Sensitivity testing was performed on 30 serum plates and 434 pre-selected positive samples (genotype and subtype). Twenty-five mutant strains were tested. Sensitivity tests were performed for different genotypes.Serum-plasma equivalence tests were performed on 25 HBsAg-positive and 27 HBsAg-negative serum/plasma samples. Results The detection specificity and the sensitivity of the HBsAg kit were 99.96% and 100.00%, respectively. In the 30 serum plates, the reagent had the same sensitivity as the Abbott HBsAg reagent, 123 days earlier than the least sensitive reagent listed, and 4.1 days earlier on average. The detection ability of mutant strains was the same. The sensitivity of each sample in the diluted genotype group was <0.13 IU/ml. All matched samples showed serum-plasma equivalence. Conclusion The HBsAg quantitative kit has excellent performance and is suitable for clinical application.
[Key words] HBsAg; Chemiluminescence; Quantitative analysis; Specificity; Sensitivity
乙型肝炎病毒(hepatitis B virus,HBV)是肝硬化和肝细胞癌的主要病因[1-3]。在HBV感染窗口期乙型表面抗原(hepatitis B surface antigen,HBsAg)水平低于检测限[4]。也有报道丙肝病毒(hepatitis C virus,HCV)/艾滋病病毒(human immunodeficiency virus,HIV)共感染可导致HBsAg检测不到[5]。HBsAg免疫逃逸突变,特别是在“a”决定簇内,可能改变蛋白质的抗原性,导致抗-HBs抗体中和HBsAg失败。HBsAg突变有三种主要形式:氨基酸替换、插入和缺失[6]。最具特征的逃逸突变是G145R[7]。HBsAg检测敏感度不断提高可降低输血相关性乙肝的感染。近年来,定量HBsAg免疫分析已广泛应用于临床[8-11]。高敏感度和特异度、突变检测能力和定量化是HBsAg检测的主要发展趋势。本研究是一种新型吖啶酯标记的化学发光免疫分析方法,用于定量测定人血清和血浆中的HBsAg,现报道如下。
1 资料与方法
1.1 一般资料
5035例阴性标本来自医院体检样本,雅培(Architect)HBsAg检测结果均为阴性。209例阴性住院患者标本。101份具有潜在交叉反应的HBsAg阴性样本,包括:血管炎患者(6例)、类风湿因子(8例)、胶原病患者(3例)、多产孕妇(6例)、高IgG/IgM患者(8例)、流感疫苗接种者(6例)、慢性肾功能不全患者(6例)、梅毒患者(7例)、艾滋患者(6例),丙型肝炎患者(7例)、EB病毒患者(5例)、巨细胞(8例)、带状疱疹患者(5例)、单纯疱疹病毒患者(5例)、甲型肝炎患者(6例)、戊型肝炎患者(8例)和桥本甲状腺炎患者(1例)。
所有标本冻存于-20℃冰箱。避免反复冻融。本研究经南京医科大学附属苏州科技城医院医学伦理委员会批准(批准文号:IRB2021046),参与者均签署知情同意书。
1.2 方法
全自动化学发光分析仪和试剂盒由苏州长光华医生物生物工程有限公司(Hybiome)研发生产。Hybiome HBsAg分析是一种化学发光免疫分析两步法,使用生物素化的抗乙肝表面抗体(hepatitis B surface antibody, HBs)小鼠单克隆抗体和吖啶标记的抗HBs山羊多克隆抗体捕获和检测人血清或血浆中的HBsAg。
1.3 观察指标及评价标准
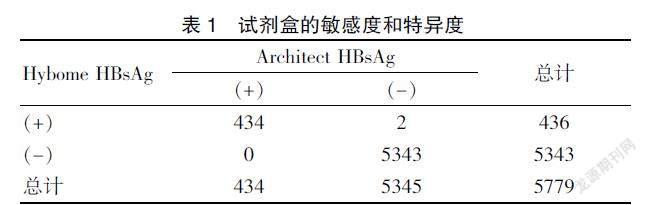
1.3.1 方法学比对 用Architect HBsAg试剂检测乙肝五项的5779份标本,经Hybiome HBsAg检测系统检测并与雅培结果比对,出现不一致结果用罗氏Elecsys HBsAg Ⅱ试剂复核。敏感度=真阳性例数/(真阳性例数+假阴性例数)×100%,特异度=真阴性例数/(真阴性例数+假阳性例数))×100%。
1.3.2 定量检测的相关性分析 将434例阳性标本在Architect和Hybome两个检测系统上的定量结果进行相关性分析。
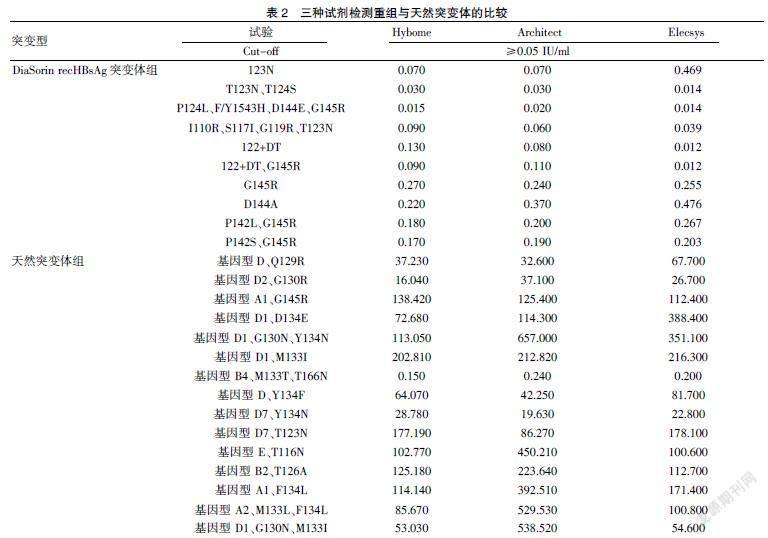
1.3.3 突变样本检出率 用Hybiome HBsAg、Architect HBsAg和Elecsys HBsAg-Ⅱ检测15个天然突变体和10个DiaSorin-rec HBsAg突变体(重组)。
1.3.4 血清盘 30个市售血清盘来自Zeptometrix(27个)、Seracere(2个)和Biomex(1个)。将Hybiome与Architect HBsAg同时检测的结果进行比较,并与最低和最敏感的检测数据进行比较。
1.3.5 不同基因型的检测效率 HBV基因型小组(PEI6100/09):该小组由10个基因型组成:A1、A2、B2、C2、D1、D2、D3、E、F2和H。
1.3.6 血清-血浆等效性 HBsAg阴性血清/血浆对:收集同一HBsAg阴性受试者(27例)的血清和血浆(枸橼酸钠、K2EDTA、K3EDTA、肝素锂、CPD、CPDA、肝素钠、ACD-B、草酸钾/氟化钠)。收集到同样的25例HBsAg阳性血清/血浆对。用已知的HBsAg阳性样本对每个样本进行加标(加标率为0.25%~10.00%),以获得分布在诊断范围内的不同HBsAg浓度的25个样本。
1.4 统计学方法
本研究使用保罗埃利希研究所建立的两次测定之间的时间延迟计算模型。与平行参考试剂Architect HBsAg定量法比较计算总数,并与最敏感和最不敏感测定法比较计算总延迟天数。使用SPSS 13.0统计学软件计算平均值、标准差、变异系数(CV)、回归斜率和相关系数。
2 结果
2.1 方法学比对
采用Hybiome HBsAg和Architect HBsAg同时检测5779份标本,结果表明,两种试剂的阳性符合率为100.00%(434/434),阴性符合率为99.96%(5343/5345),总符合率为99.96%(5777/5779)。有两个不一致的样本,经试验确认,一例为阴性,另一例为阳性。因此,Hybiome HBsAg试剂的敏感度和特异度分别为99.77%(434/435)和99.98%(5343/5344)。见表1。
2.2 两种HBsAg定量方法的相关性分析
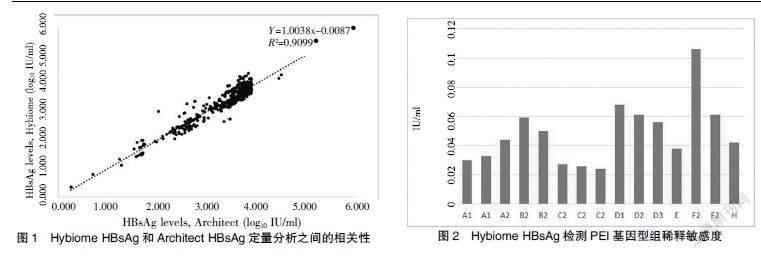
Hybome HBsAg检测与Architect HBsAg定量检测的相关性分析(n=434)。X和Y轴分别为Architect和Hybiome的HBsAg水平。两种分析方法相关性很高(r=0.953)。见图1。
2.3 HBsAg天然和重组突变样本的检测
用Hybiome HBsAg、Architect HBsAg和Elecsys HBsAg-Ⅱ(瑞士罗氏公司)检测DiaSorin-rec HBsAg突变体和天然突变体。三种试剂漏检了T123N、T124S和P124L、F/Y1543H、D144E和G145R重组突变体。对15个天然突变体均无漏检,且浓度相近。见表2。
2.4 血清盘
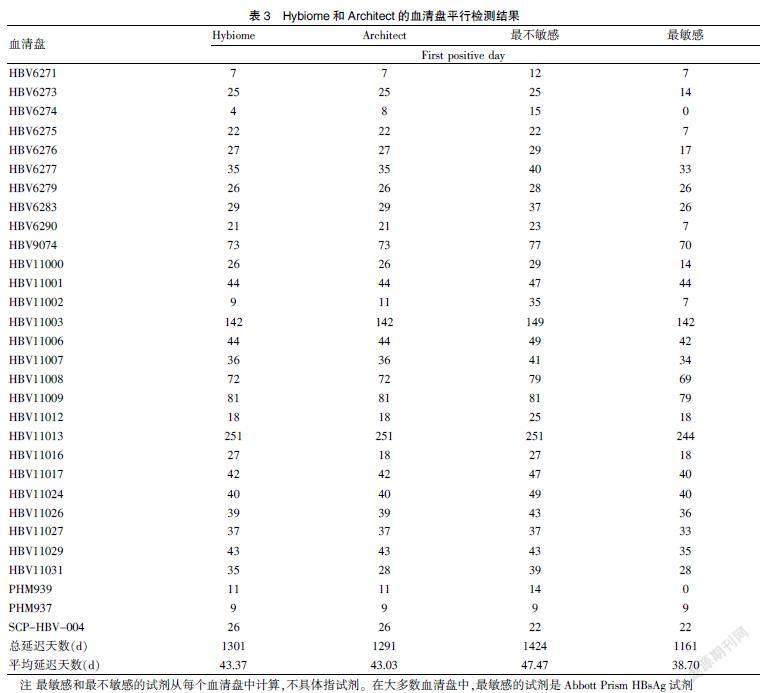
共有30个商品化血清盘(1个Biomex、2个SeraCare和27个ZeptoMetrix)。用Hybome HBsAg和Architect HBsAg同时检测。将Hybiome HBsAg与Architect HBsAg的结果进行比较,并与最低和最敏感的检测数据进行比较。保罗埃利希研究所也采用了这一原则。因此,Hybome HBsAg检测试剂盒与最低和最敏感的HBsAg检测之间的总延迟天数和平均延迟天数见表3。Hybome HBsAg总延迟天数为1301 d,比Abbott Architect HBsAg晚10 d,比最不敏感试剂早123 d,比最敏感試剂晚140 d。
2.5 不同基因型的检测效率
第一國际参考组(PEI 6100/09)的HBV基因型检测,每个小组的最低浓度仍与HBsAg检测试剂盒反应。见图2。结果表明,所有基因型的检测效率基本相同。所有基因型在浓度<0.13 IU/ml时均能检出。
2.6 血清-血浆等效性
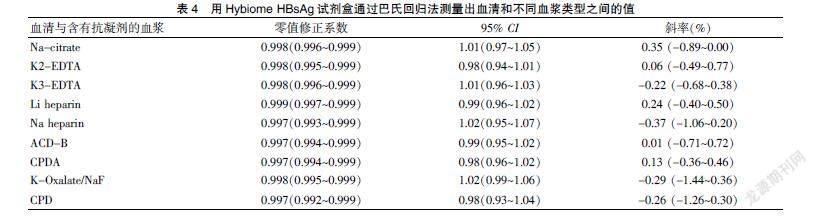
用Hybiome HBsAg试剂盒检测27例阴性血清和血浆(枸橼酸钠、K2EDTA、K3EDTA、肝素锂、CPD、CPDA、肝素钠、ACD-B、草酸钾/氟化钠)。所有样本均为阴性,即值<0.05 IU/ml。检测25个加标血清和血浆(柠檬酸钠、K2EDTA、K3EDTA、肝素锂、CPD、CPDA、肝素钠、ACD-B、草酸钾/氟化钠),所有样本均阳性,即值≥0.05 IU/ml。为了评估血清和不同血浆基质之间的测量值是否存在差异,根据CLSI EP09-A3分析数据,结果(估计值和95%置信区间)。见表4。
所有血浆类型的估计相关系数均为1.00(介于0.997~0.999之间)。估计的回归斜率在0.98和1.02之间变化。因此,含柠檬酸钠、K2EDTA、K3EDTA、肝素锂、CPD、CPDA、肝素钠、ACD-B和草酸钾/氟化钠抗凝剂的血清和血浆可被认为是等效的,适用于Hybiome HBsAg试剂盒进行检测。
3 讨论
HBV是全球报道的最常见的病毒感染。HBsAg是HBV感染的关键标志物,在HBV感染过程中首先出现在受感染的血清中。但在HBV感染窗口期或存在HBsAg突变时HBsAg很难被检测出来。许多研究表明,血清HBsAg浓度与HBVDNA有很好的相关性,尤其是HBeAg阳性患者。此外,血清HBsAg浓度与肝脏HBV-DNA和cccDNA相关性良好,优于血清HBV-DNA,提示血清HBsAg可作为肝脏cccDNA的间接标志物。HBsAg检测试剂盒是识别HBV感染者的一线筛查工具。近年来,定量HBsAg免疫分析已广泛应用于临床。高敏感度和特异度、突变检测能力和定量化是HBsAg检测的主要发展趋势。
HBsAg检测的高敏感度可提高血液安全性,降低输血传播乙肝病毒感染的风险。HBsAg测试之间的分析敏感度差异非常大,可达300倍(0.013~4.000 IU/ml)。本次实验中,新开发的 Hybiome HBsAg试剂盒检测显示,与血清盘中非常敏感的替代检测相比,其敏感度高。这意味着Hybiome可以尽快检测出HBV感染。
研究报道HBV基因型和亚型变异会影响HBsAg的敏感度[12-13]。然而,Hybiome HBsAg试剂盒没有遗漏任何阳性样本。除了早期感染的窗口期外,HBsAg检测可能由于突变而漏检,包括改变HBsAg抗原性的“a”决定簇突变。关于特定人群中突变频率的数据很少,例如,泰国个体的突变频率为0.1%[14]。在东南亚,HBsAg阳性献血者中HBV突变的频率在1.0%~3.7%之间[15]。G145R突变比较常见[16-18],表明它是最常见的突变,需要在分析设计中加以考虑。许多试剂商已经优化了他们的HBsAg检测方法,使用多个捕获的抗野生和变异HBV的单克隆抗体代替一个单克隆抗体,并用多克隆抗体代替单克隆示踪抗体[19-20]。多克隆示踪剂抗体在提高突变检测能力的同时,也限制其特异性。Hybiome HBsAg试剂盒中两个HBsAg抗体至少各自包含一种抗S蛋白单克隆抗体,两种抗S蛋白单克隆抗体针对的HBsAg的表位不同,本研究的试剂盒在国际上尚属首例,在检测HBsAg时具有高灵敏感度和准确度,极大提高了HBsAg突变株的检出能力。Hybiome与其他CE标记的检测试剂盒相比,几乎是最好的,包括雅培PRISM HBsAg试剂盒和罗氏HBsAg Ⅱ试剂盒。
Hybiome HBsAg试剂盒检测特异度高达99.96%,超过欧盟标准的99.5%,无天然或重组突变假阴性。在30个血清盘中,Hybiome HBsAg检测试剂盒与Architect HBsAg参考检测试剂盒具有相似的敏感度。这几乎是最敏感的发光标记分析。所有基因型均在<0.13 IU/ml浓度下检测到。
本研究建立的化学发光定量检测试剂盒采用国际主流试剂通用的两步法检测,可以极大地降低HOOK效应。而且敏感度高,特异度好,各性能指标均可满足临床需求,摆脱了冗长的传统手工操作。相对进口试剂价格便宜,有助于推动国产发光试剂在临床上的大规模应用。根据上述结果,本研究得出结论,国产Hybiome HBsAg检测试剂性能优良,适合临床应用,完全可替代进口试剂。
[参考文献]
[1] Chang TS,Yang YH,Chen WM,et al.Long-term risk of primary liver cancers in entecavir versus tenofovir treat-ment for chronic hepatitis B[J].Trial Sci Rep, 2021,11(1):1365.
[2] Chaturvedi VK,Singh A,Dubey SK,et al. Molecular mec-hanistic insight of hepatitis B virus mediated hepat-ocellular carcinoma[J].Microb Pathog,2019,128:184-194.
[3] Yang F,Ma LT,Yang Y,et al. Contribution of hepatitis B virus infection to the aggressiveness of primary liver cancer:A clinical epidemiological study in eastern China[J]. Front Oncol,2019,9:370.
[4] Cheng J,Dai Y,Yan L,et al. Clinical characteristics and correlation analysis of subjects with chronic hepatitis B virus(HBV) infection and sustained low levels of hepatitis B surface antigen (HBsAg)[J]. Med Sci Monit,2018,24:1826-1835.
[5] Carretero C,Herraiz M.Chronic hepatitis B virus infection[J]. An Sist Sanit Navar,2004,27(Suppl 2):27-32.
[6] Rajput MK. Mutations and methods of analysis of mutations in Hepatitis B virus[J].AIMS Microbiol,2020,6(4):401-421.
[7] Konopleva MV,Belenikin MS,Shanko AV,et al. Det ection of S-HBsAg mutations in patients with hematologic malignancies[J].Diagnostics (Basel),2021,11(6):969.
[8] Vachon A,Osiowy C. Novel biomarkers of hepatitis B virus and their use in chronic hepatitis B patient manag-ement[J].Viruses,2021,13(6):951.
[9] Liu YY,Veeraraghavan V,Pinkerton M,et al. Viral bio markers for hepatitis B virus-related hepatocellular carc-inoma occurrence and recurrence[J].Front Microbiol,2021, 12:665 201.
[10] Cao J,Gong J,Tsia H, et al. Prediction model of HBsAg seroclearance in patients with chronic HBV infection[J]. Biomed Res Int,2020,2020:6 820 179.
[11] Yang RF,Cui LY,Liu Y,et al. A hook-effect-free homo geneous light-initiated chemiluminescence assay:Is it reliable for screening and the quantification of the hepatitis B surface antigen?[J].Ann Transl Med,2020,8(9):606.
[12] Pronier C,Candotti D,Boizeau L,et al. The contribution of more sensitive hepatitis B surface antigen assays to detecting and monitoring hepatitis B infection[J].J Clin Virol,2020,129:104 507.
[13] Limeres MJ,Gomez ER,Noseda DG,et al.Impact of hepa titis B virus genotype F on in vitro diagnosis:Detection efficiency of HBsAg from Amerindian subgenotypes F1b and F4[J]. Arch Virol,2019,164(9):2297-2307.
[14] Louisirirotchanakul S,Kanoksinsombat C,O'Charoen R,et al. HBsAg diagnostic kits in the detection of hepatitis B virus mutation within "a" determinant[J].Viral Immunol,2006,19(1):108-114.
[15] Kuhns MC,Mcnamara AL,Holzmayer V,et al. Frequency of diagnostically significant hepatitis B surface antigen mutants[J].J Med Virol,2007,79(1):5.

