基于甲酸的硝酸亚铈微波脱硝前驱体的制备
贾红伟,李 斌,贾艳虹,于 婷,何 辉
中国原子能科学研究院 放射化学研究所,北京 102413
乏燃料后处理是从反应堆卸出的乏燃料中提取铀钚等元素,是实现核能可持续发展的重要环节[1]。目前,乏燃料后处理普遍采用溶剂萃取PUREX流程,该流程以磷酸三丁酯为萃取剂,利用铀钚以及裂片元素萃取行为差异实现铀钚的分离[2-3]。在该流程中经过钚纯化得到较为纯净的硝酸钚溶液,为满足贮存要求以及使用需要,需经过钚尾端转换环节将硝酸钚溶液转化成PuO2固体形式。当前钚尾端主要采用将硝酸钚先沉淀后煅烧的工艺,该工艺相对成熟,生产过程稳定,具有一定的净化效果,产品活性好,能满足后续工艺要求,但该工艺存在工序复杂、产生废液量大、对料液要求高的问题,因此有必要寻找一种条件温和的硝酸钚转化成二氧化钚的钚尾端工艺。
钚的直接脱硝主要目的是在一个容器中完成硝酸钚溶液的浓缩、结晶及转化操作,最终得到PuO2固体。该工艺可通过避免或减少在不同容器与设备间材料转移,最大程度降低了钚的损失。但直接脱硝时,缺少对煅烧前物料状态的控制,最终产物PuO2易出现结块且粒度分布不均的问题。甲酸是一种一元羧酸,可与硝酸和硝酸盐反应,将硝酸根转化为氮氧化物逸出,常用于溶液脱硝以降低溶液酸度[4-8]。在煅烧前将物料与甲酸反应生成煅烧前驱体,利用煅烧前驱体在煅烧过程中具有遗传性的特点[9],通过控制前驱体的粒径和形貌来进一步调节煅烧后产物的粒径和形貌。
与常规加热相比,微波加热具有加热均匀、升温速率快、加热效率高的特点,因此本工作通过微波加热溶液。Ce3+的离子半径(103.4 pm)与Pu3+的离子半径(100.0 pm)相近,且铈在4f电子体系中所占的位置与钚在5f电子体系中所占的位置相似,研究中多以铈作为钚的模拟材料,因此本工作拟以硝酸亚铈溶液模拟硝酸钚(Ⅲ)溶液,微波加热使硝酸亚铈溶液蒸发结晶,再通过结晶产物与甲酸反应生成煅烧前驱体,研究甲酸浓度、甲酸用量对煅烧前驱体的粒径与形貌的影响,并对煅烧前后的颗粒粒径与形貌进行比对研究。
1 实验部分
1.1 试剂与仪器
六水合硝酸亚铈(纯度为99.95%)、甲酸(质量分数为88%),上海麦克林生化科技有限公司;硝酸(优级纯),国药集团化学试剂有限公司。
硝酸亚铈溶液模拟硝酸钚(Ⅲ)溶液,其中铈离子浓度为0.21 mol/L,硝酸浓度为1.5 mol/L。
MKX-G1C1C型微波浓缩热解仪,青岛迈可威微波创新科技有限公司,输出微波功率为0~800 W,微波频率为2 450 MHz;SX-G07103型箱式纤维电阻炉,天津市中环实验电炉有限公司;D8 Advance型 X射线衍射仪(XRD),布鲁克(北京)科技有限公司;Bettersize 2600E 型激光粒度仪,丹东百特仪器有限公司;TESCAN-VEGA3型扫描电子显微镜,泰斯肯贸易(上海)有限公司。
1.2 实验方法
1.2.1实验方法及步骤 取100 mL配制好的硝酸亚铈的硝酸溶液置于石英烧杯中,在800 W微波功率下加热,待溶液蒸发浓缩并结晶成固体且温度恒定后,加入甲酸(甲酸浓度为8~23 mol/L、HCOOH和Ce的摩尔比为6∶1~24∶1)加热至68 ℃并保持恒温,待反应完全后加热至110 ℃将溶液蒸发殆尽,最终得到粉末状前驱体,并对所得前驱体的粒径和形貌进行分析,将甲酸铈在500 ℃进行煅烧1 h,对煅烧前后的粒径和形貌进行比对。
1.2.2分析方法 通过X射线衍射仪确定粉末的结构,通过激光粒度仪测量颗粒的粒径,通过扫描电镜(SEM)观察颗粒的形貌。
2 结果与讨论
2.1 产物的确定
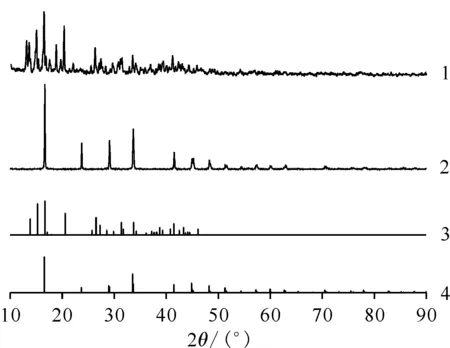
1——微波加热产物;2——添加甲酸后产物;3——PDF#43-0944,Ce(NO3)3·2H2O;4——PDF#49-1245,Ce(HCOO)3图1 微波加热产物和添加甲酸后产物的XRD图Fig.1 XRD of product after heating by microwave and product after adding formic acid reaction
分别对微波加热后的产物和添加甲酸后的产物进行表征,得到的XRD衍射图示于图1。由图1可知:微波加热后产物与二水合硝酸亚铈标准XRD谱图(PDF#43-0944)衍射峰吻合,证明该产物为二水合硝酸亚铈;添加甲酸后的产物与无水甲酸铈标准XRD谱图(PDF#49-1245)衍射峰吻合,证明该产物为无水甲酸铈。这说明,在800 W功率下,加热硝酸亚铈的硝酸溶液得到的产物为二水合硝酸亚铈,且不会发生分解,而添加甲酸后,二水合硝酸亚铈与甲酸发生反应式(1)。继续微波加热,溶液中的硝酸和过量的甲酸反应分解为气体逸出,最终得到无水甲酸铈固体粉末。
Ce(NO3)3·2H2O+3HCOOH=
Ce(HCOO)3↓+3HNO3+2H2O
(1)
从式(1)中可得到理论上甲酸与铈离子的摩尔比为3∶1,为保证硝酸亚铈完全转化为甲酸铈并保证反应后的溶液具有一定的酸度,实验时甲酸过量,以甲酸与铈离子的摩尔比为3∶1为1倍甲酸用量,6∶1为2倍甲酸用量,以此类推,以甲酸倍数用量来说明甲酸的过量程度。
2.2 甲酸浓度对前驱体粒度的影响
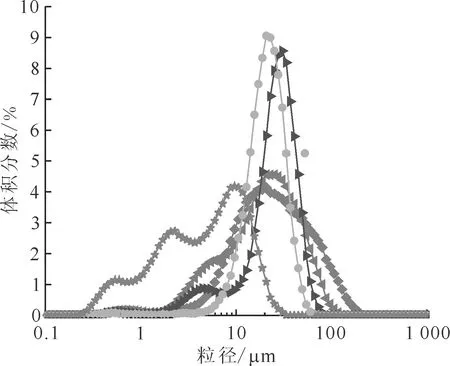
6倍甲酸用量甲酸浓度,mol/L:◆——8,◀——12,▶——16,●——20,★——23图2 不同甲酸浓度下制备的甲酸铈粒径分布Fig.2 Particle size distribution of cerium formate prepared under different formic acid concentration
二水合硝酸亚铈与甲酸在微波加热条件下发生反应最终产物的粒径分布图示于图2。从图2可以看出:添加甲酸后,生成的甲酸铈为粉末状,甲酸浓度为8 mol/L时,甲酸铈粒径分布区间为0.30~200 μm,存在超过100 μm的大颗粒;随着甲酸浓度升高,甲酸铈的最大粒径逐渐减小,甲酸浓度为23 mol/L时最大粒径仅为32 μm;甲酸浓度从8 mol/L增加到20 mol/L时,粒径分布范围减小,粒径分布更为集中,粒径分布曲线由发散型转为收缩型。
在甲酸的用量相同时,甲酸浓度高,单位体积内甲酸分子增加,单位体积内与甲酸反应的硝酸根也会增加。根据文献报道,甲酸浓度越高、硝酸根浓度越大脱硝速率越快[4, 10-11],甲酸与二水合硝酸亚铈的反应加快,这使得溶液中生成的晶核更多,反应时间缩短,晶核的生长时间短,形成的颗粒粒径变小。因此,为获得粒径较小的颗粒,应选择高浓度的甲酸。
2.3 甲酸过量程度对前驱体粒度的影响
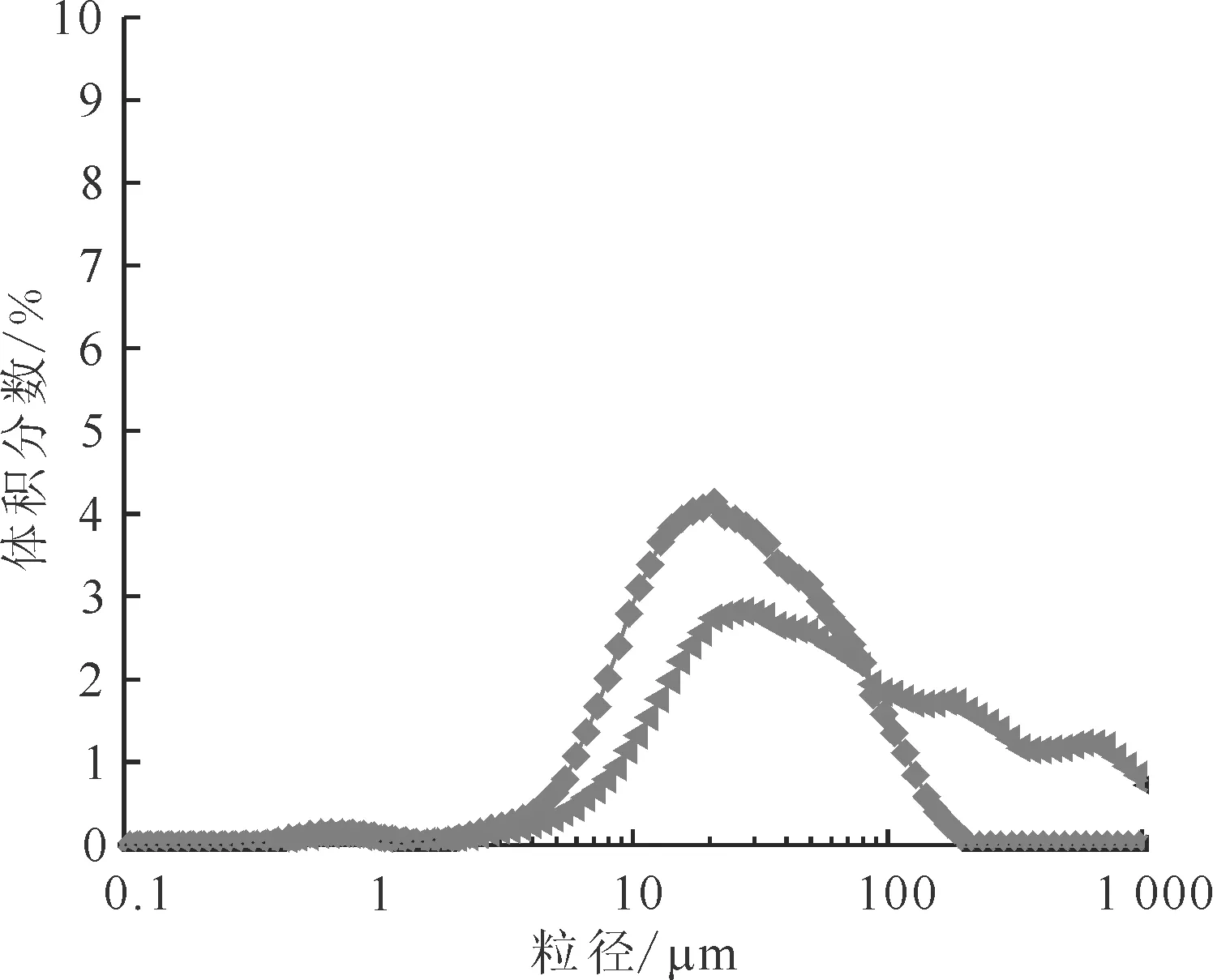
甲酸用量:◆——6倍,◀——8倍图3 8 mol/L甲酸制备的甲酸铈粒径分布Fig.3 Particle size distribution of cerium formate prepared by 8 mol/L formic acid
当甲酸浓度为8、12、16、20 mol/L和23 mol/L时,不同甲酸用量下制备的甲酸铈粒径分布图示于图3—7。由图3—7可知:当甲酸浓度为8 mol/L、4倍甲酸用量时,生成的甲酸铈前驱体粘结成块且会粘在容器上,无法测量粒度;当甲酸浓度为8~16 mol/L时,增加甲酸用量,会使得颗粒粒径整体呈增大的趋势;当甲酸浓度为20 mol/L时,生成的颗粒粒径较好,最大粒径为69 μm;当甲酸浓度为23 mol/L时,整体粒径偏小,但存在少量大于100 μm的颗粒。这说明甲酸用量与前驱体粒径的关系受甲酸浓度的影响,当甲酸浓度在8~16 mol/L时,甲酸用量增加,反应后甲酸剩余量增加,甲酸铈在甲酸溶液中加热时,会因为溶液中水的氢键架桥作用而产生团聚现象[12-13]。低浓度下,甲酸用量越多,溶液中水的总量越大,在蒸干过程中会造成团聚现象更为严重,导致一些较大的颗粒出现。而甲酸浓度高于20 mol/L时,甲酸与硝酸铈在常温下即可剧烈反应,增加甲酸用量,会导致反应时生成更多的晶核,缩短了反应时间,晶核生长时间短,生成很多的细颗粒。因此,甲酸浓度为16~20 mol/L、6倍甲酸用量的反应条件较为适宜。
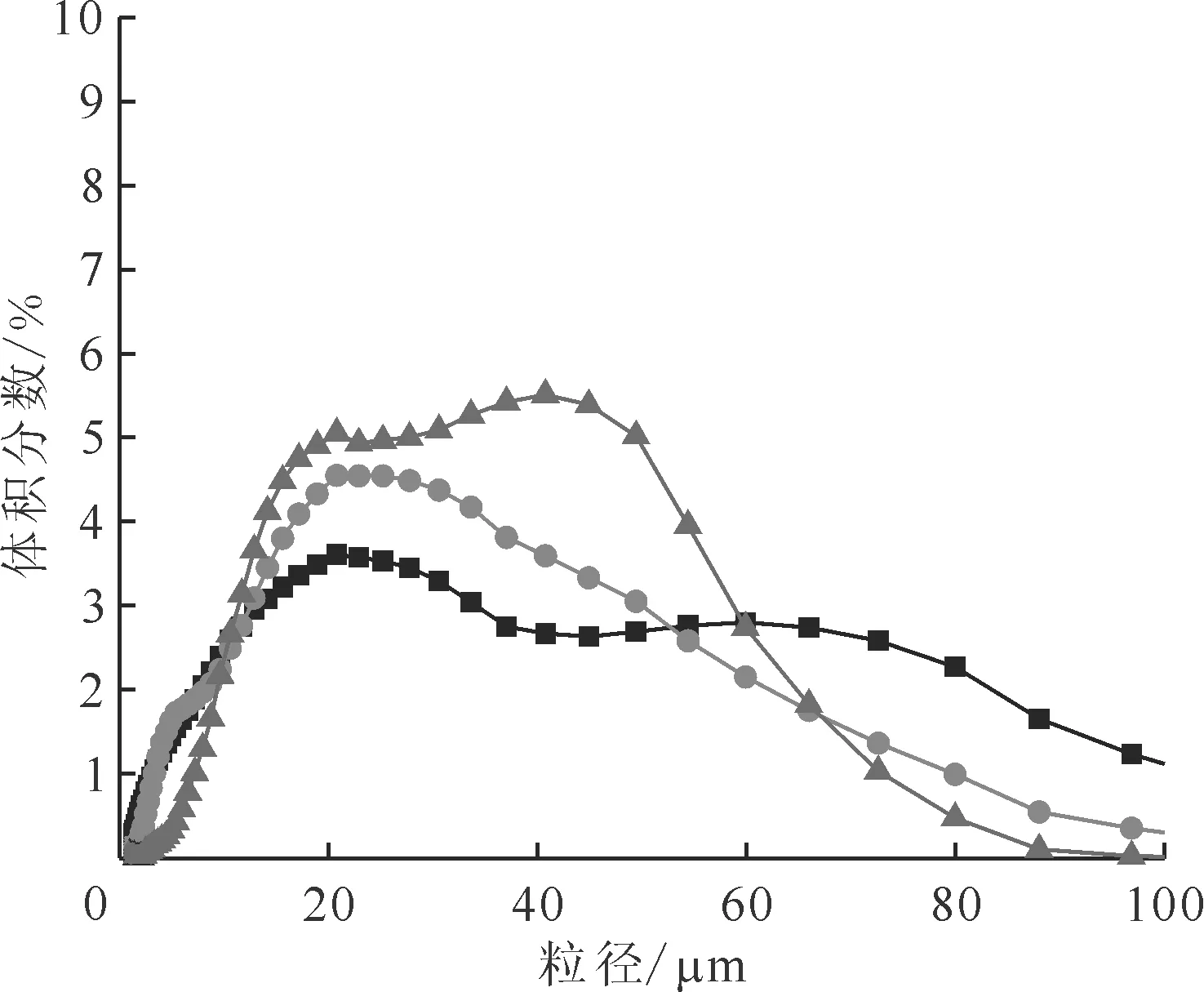
甲酸用量:■——4倍,●——6倍,▲——8倍图4 12 mol/L甲酸制备的甲酸铈粒径分布Fig.4 Particle size distribution of cerium formate prepared by 12 mol/L formic acid
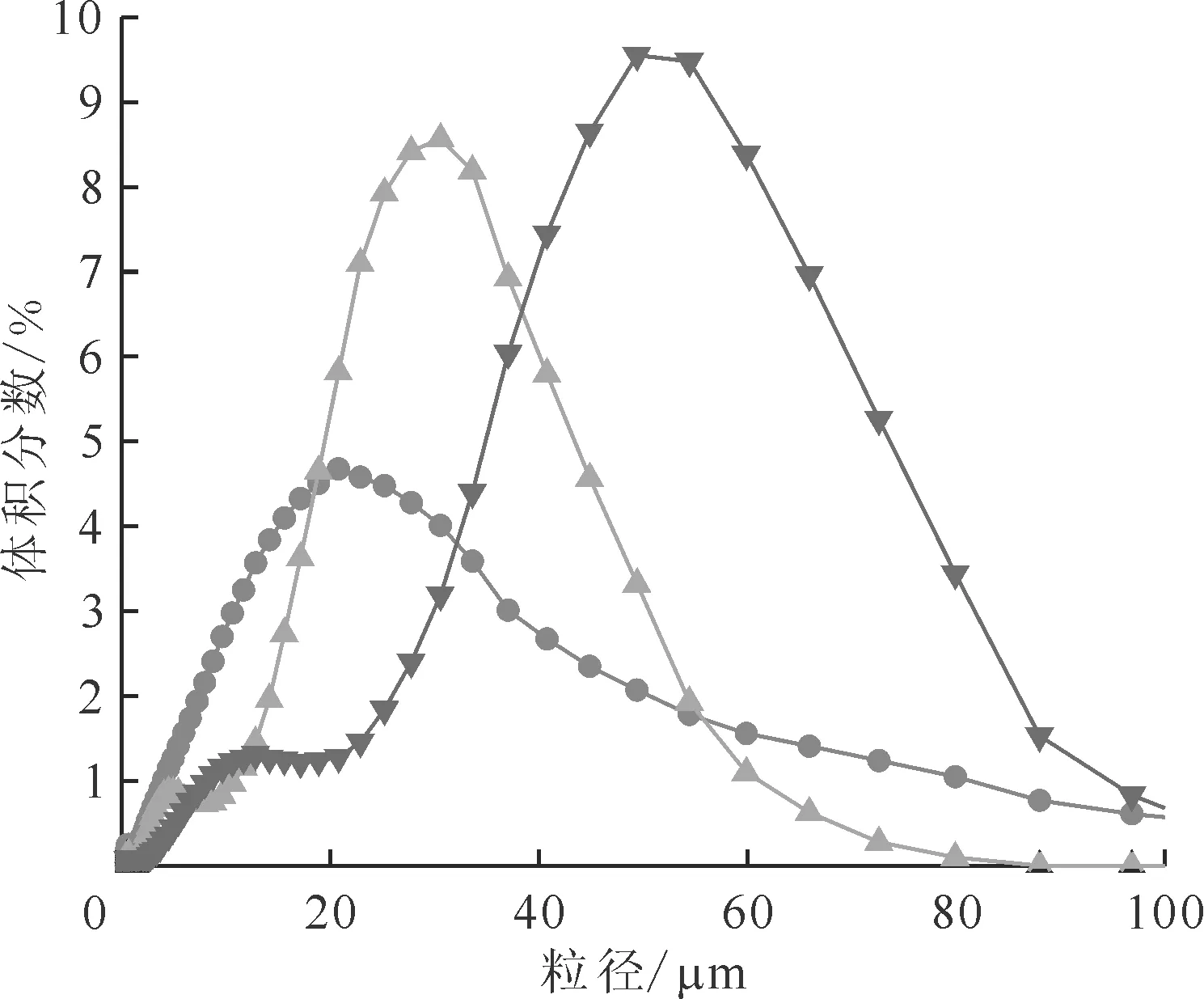
甲酸用量:●——4倍,▲——6倍,▼——8倍图5 16 mol/L甲酸制备的甲酸铈粒径分布Fig.5 Particle size distribution of cerium formate prepared by 16 mol/L formic acid

甲酸用量:▲——4倍,▼——6倍,◆——8倍图6 20 mol/L甲酸制备的甲酸铈粒径分布Fig.6 Particle size distribution of cerium formate prepared by 20 mol/L formic acid
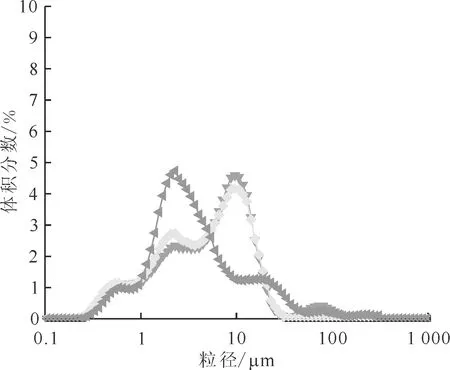
甲酸用量:▼——4倍,◆——6倍,◀——8倍图7 23 mol/L甲酸制备的甲酸铈粒径分布Fig.7 Particle size distribution of cerium formate prepared by 23 mol/L formic acid
2.4 不同甲酸浓度下的前驱体颗粒形貌
图8为不同甲酸浓度下的前驱体颗粒SEM图。由图8可知,硝酸亚铈与甲酸反应生成了棒状甲酸铈颗粒。甲酸浓度低于16 mol/L时,棒状颗粒较长,很多棒状颗粒团聚在一起;甲酸浓度为16 mol/L时,反应生成的甲酸铈颗粒更倾向于以一个中心点向四周生长,颗粒较小;甲酸浓度达到20 mol/L及以上时,此时生成的棒状颗粒进一步减小,团聚体是不规则的球体。这说明棒状颗粒的长度与甲酸浓度有关,甲酸浓度越高,反应越剧烈,晶核生长时间越短,棒状颗粒越短。甲酸浓度低时,在溶液蒸发结晶的过程中,许多棒状颗粒与水通过氢键形成架桥现象,使颗粒团聚;而甲酸浓度高时,常温下甲酸即可与二水合硝酸亚铈反应,反应剧烈,在短时间内生成大量的晶核,缩短了反应时间,使得生成的甲酸铈颗粒很小,剧烈的反应还使得相邻的晶核无序地结合在一起。因此,根据颗粒的粒径分布和SEM图,最佳工艺条件确定为甲酸浓度为16~20 mol/L、6倍甲酸用量,此时反应在可控范围内且得到的颗粒粒径适中。
2.5 煅烧前后的粒径与形貌对比
分别选取6倍甲酸用量下、甲酸浓度为16 mol/L和20 mol/L时生成的甲酸铈,将其在500 ℃下煅烧1 h,得到煅烧产物二氧化铈,产物粒径分布示于图9。由图9可知:16 mol/L甲酸形成的颗粒煅烧后大粒径颗粒减少,中等粒径颗粒增加;而20 mol/L甲酸形成的颗粒煅烧后1.0~10 μm粒径的颗粒明显减少,而粒径小于0.30 μm的颗粒急剧增加。结合图8可知,16 mol/L的甲酸浓度下形成的颗粒有些为两个小团聚体粘接在一起形成的大团聚体,在煅烧过程中,前驱体会分解,生成气体逸出,可能会造成这部分颗粒在连接处断裂分开,形成两个小的团聚体颗粒,使得大颗粒分解为中等颗粒;而20 mol/L甲酸时,煅烧前前驱体颗粒是甲酸与二水合硝酸亚铈在较为剧烈的反应条件下得到的团聚体,晶粒生长时间短,结合力较弱,在煅烧后逸出气体的过程中,很多细小的颗粒会在外力的作用下从团聚体中分离出来,造成粒径小于0.30 μm的细小颗粒增加。但从整体的粒度分布区间来看,煅烧后的颗粒粒径与煅烧前的颗粒粒径接近或稍小一些。

6倍甲酸用量甲酸浓度,mol/L:(a)——8,(b)——12,(c)——16,(d)——20,(e)——23图8 不同甲酸浓度下的前驱体SEM图Fig.8 SEM images of precursors under different concentrations of formic acid
两组甲酸铈前驱体煅烧前后的SEM图示于图10。由图10可知,煅烧不改变颗粒的形貌。16 mol/L甲酸制备得到的甲酸铈为棒状颗粒的团聚体,经过煅烧后,颗粒仍为棒状结构,团聚体的大小也没有明显改变;20 mol/L甲酸制备得到的甲酸铈为晶粒很小的颗粒的团聚体,形状不规则,经过煅烧后,颗粒的形状也没有明显改变。但正如图9所示的粒径分布,500 ℃下煅烧后,会有一定的粒径小于0.30 μm的细颗粒生成。

6倍甲酸用量■——16 mol/L甲酸,煅烧前;●——16 mol/L甲酸,500 ℃煅烧后;▲——20 mol/L甲酸,煅烧前;▼——20 mol/L甲酸,500 ℃煅烧后图9 煅烧前后的粒径对比图Fig.9 Comparison of particle sizebefore and after calcination

6倍甲酸用量制备条件:(a)——16 mol/L甲酸,煅烧前;(b)——16 mol/L甲酸,500 ℃煅烧后;(c)——20 mol/L甲酸,煅烧前;(d)——20 mol/L甲酸,500 ℃煅烧后图10 煅烧前后的SEM对比图Fig.10 Comparison of SEM before and after calcination
3 结 论
通过开展甲酸与硝酸亚铈溶液蒸发结晶产物在微波加热条件下反应的研究,得到以下结论:
(1) 硝酸亚铈溶液微波加热后得到块状的二水合硝酸亚铈,添加甲酸后得到粉末状的甲酸铈前驱体;
(2) 甲酸铈的颗粒状态与甲酸添加量和甲酸浓度有关,生成的甲酸铈颗粒为棒状结构,甲酸浓度越高,长度越短,形成的团聚体粒径也越小;甲酸浓度为16~20 mol/L、HCOOH/Ce摩尔比为18时,反应在可控范围内且得到的颗粒适中,此时为最佳反应条件;
(3) 甲酸铈颗粒经过煅烧后,颗粒的形貌基本不变,粒径大体相同,但会产生少量的小于0.30 μm的细颗粒,生成甲酸铈时甲酸的浓度越高,反应越剧烈,煅烧时越容易产生细颗粒。

