[Cu6(dmpymt)6]簇基纳米MOFs催化可见光诱导醇脱氢反应
张梦娟,王利利,代永康
(亳州学院 中药学院,安徽 亳州 236800)
醇被选择性氧化为羰基化合物是大规模合成商业化学品过程中极为普遍的有机转化。此转换可以通过无机氧化剂的氧化和金属催化醇的有氧氧化实现。而这两种方法具有较差的官能团耐受性并会产生有毒有害的废弃物[1-2]。金属催化的醇的无受体脱氢(acceptorless dehydrogenation of alcohols, AAD)以氢气为副产物,避免了醛的进一步氧化。因此,从原子经济性和氧化选择性的角度考虑,醇的无受体脱氢(AAD)无疑是一个优良的可行方案[3-4],更为重要的是,从生物质中析氢可用于备受关注的化学能的存储[5-6]。据我们所知,在无外加氧化剂的条件下,金属配合物催化醇的脱氢反应已得到了广泛研究,但此方法一般需要较高的反应温度活化催化剂。因此,室温常压条件下,非均相光催化剂催化可见光诱导的AAD反应是一个节能、环境友好的策略。到目前为止,人们的研究主要集中在Pt、Pd、Au、Rh和Ni纳米粒子负载的无机半导体作为光催化剂实现醇脱氢反应[7]。
与传统的半导体材料相比,光活性的金属-有机框架(metal organic framework, MOF)不仅有丰富多彩的结构化学和可见光吸收,而且其功能团可灵活调控。据报道,某些修饰的MOFs材料可用于醇的光氧化和质子还原反应[8-9]。小分子光催化剂如膦修饰的Rh/Pd/Pt、Rh卟啉化合物和多金属氧酸盐在紫外光的照射下可以催化醇脱氢反应[10]。Bernhard等人报道使用RhIII(dtbbpy)2I2]+(dtbbpy = 4,4′-di-tert-butyl-2,2′-bipyridine)作为可见光催化剂,实现了醇的脱氢反应[11]。大多数的研究集中在含Ru、Ir、Re等贵金属配合物基团的MOFs光催化剂的合成与应用上,而对于将地球上含量高、毒性小、易合成的金属配合物可见光催化剂引入到MOFs材料中的研究却非常少。寻找高效、廉价、非均相的可见光催化剂,将太阳能有效地转化为化学能仍然是一个挑战。
2-巯基嘧啶(Hdmpmt = 4,6-dimethylpyrimi-dine-2-thiol)金属配合物将是合成MOFs可见光催化剂潜在的前躯体。此类化合物的荧光寿命长,在可见光区域有吸收,是潜在的优良光敏剂[12-16];若能将这类簇合物组装成MOFs结构,将是合成非均相可见光催化剂的有效手段,如何将这些簇合物组装成MOFs材料,是合成非均相光催化剂的关键。
2-巯基嘧啶金属簇合物中没有配位的N原子可与金属离子进一步配位反应,从而组装成簇基金属-有机框架结构,不仅丰富无机-有机杂化材料的结构化学,也提高了簇合物的可见光催化效率。为合成出高活性、廉价的非均相可见光催化剂提供更多的机会。
1 实验部分
1.1 实验仪器和试剂
化合物1根据文献方法合成[16]。所用溶剂均通过标准方法进行蒸馏纯化,其他药品和试剂均通过购买得到未经过进一步纯化、所得产物经过硅胶色谱柱进行分离提纯。C、H、N的元素分析测试在Carlo-Erba CHNO-S元素微分析仪上进行;红外光谱采用固体样品KBr压片在型号为Varian 1000 FT-IR光谱仪(4000~400 cm-1)上测得;核磁共振谱1H NMR和13C NMR在室温条件下由型号为Varian UNITYplus-400或者Bruker 600 MHz仪器上的核磁共振仪测得,化学位移是以CD3Cl或者DMSO-d6的溶剂峰信号作为基准;粉末X-射线谱图是在X'Pert PRO SUPERA旋转阳极X射线衍射仪上测得的;高分辨质谱是在GCT-TOF仪器上测得的;荧光发射光谱在室温下由型号为FLS980稳态荧光光谱仪上测得的;UV-Vis光谱是在室温条件下型号为Shimadzu UV-3150紫外光谱仪上测得;扫描电镜图谱(SEM)是用HITACHI S-4700型电子显微镜测得的;X射线光电子图谱(XPS)的测试是在ESCALAB 250Xi型光谱仪上完成的。
1.2 实验步骤
1.2.1 化合物{[Cu6(dmpymt)6]2[Cu2(μ-I)2]4(CuI)2}n(2)的合成
向一根直玻璃管(长20 cm,内径7 mm)中加入1 (10.2 mg, 0.05 mmol)的三氯甲烷(CHCl3, 2 mL)溶液,随后缓慢加入CHCl3(1 mL)和乙腈(MeCN,1 mL)的混和溶剂作为缓冲层。最后将碘化亚铜(CuI, 19.0 mg, 0.1 mmol)的MeCN (2 mL)溶液缓慢覆盖到上述缓冲层上面进行扩散。封口后,在室温静置数天,析出黄色块状晶体2。抽滤收集晶体2,先后用MeCN和乙醚 (Et2O)充分洗涤,最后置于空气中干燥。化合物2的产率:12.7 mg (75% 基于S计算) C72H84Cu22I10N24S12元素分析:理论值:C 19.94, H 1.95, N 7.75%;实验值:C 20.18, H 1.75, N 7.66%。红外光谱(KBr压片, ν/cm-1):1585 (s), 1526 (m), 1431 (m), 1385 (w), 1345 (m), 1254 (s), 1135 (w), 878 (w), 571 (w)。
化合物2的纳米粒子的制备:向1 (10.2 mg, 0.05 mmol)的CHCl3(2 mL)溶液中快速加入CuI (19.0 mg, 0.1 mmol)的MeCN (2 mL)溶液,反应液会立即变成黄色悬浊液。快速将生成的黄色固体进行离心分离,先后用MeCN和Et2O充分洗涤,在空气中自然干燥,最终产物即是2的纳米粒子。
1.2.2 化合物{[Cu6(dmpymt)6]2[Cu2(μ-I)2]4}n(3)的合成
方法一:将反应物1 (10.2 mg, 0.05 mmol)、三苯基膦碘化亚铜(Ph3P)CuI (22.7 mg, 0.05 mmol)以及乙腈(1 mL)和甲苯(toluene, 1 mL)加入Pyrex耐压管中。密封后加热到120 ℃恒温反应24 h,之后再以每小时降低5 ℃的速度降至室温,得到橙色块状晶体3。所得晶体先后用MeCN和Et2O,在空气中干燥。化合物3的产率:14.0 mg (89% 基于S计算) C72H84Cu20I8N25S12CH3CN元素分析:理论值:C 22.16, H 2.19, N 9.08%;实验值:C 22.58, H 2.25, N 8.60%。红外光谱(KBr压片, ν/cm-1):1587 (s), 1522 (m), 1426 (m), 1353 (m), 1259 (s), 1177 (w), 1027 (w), 882 (w), 841 (w), 560 (w)。
方法二:与方法一合成步骤基本相同,只是将反应物1 (10.2 mg, 0.05 mmol)和(Ph3P)CuI (22.7 mg, 0.05 mmol)换成CuI (19.0 mg, 0.1 mmol)和Hdmpymt (7.0 mg, 0.05 mmol)。产量:7.4 mg (产率为45%,基于S计算)。
化合物3的纳米线的制备:向1 (20.3 mg, 0.1 mmol)和(Ph3P)CuI (45.3mg, 0.1 mmol)的乙腈(4 mL)和甲苯(4 mL)混合溶液中加入聚乙烯吡咯烷酮(PVP, 100 mg)。混合物在120 ℃以适当的转速快速搅拌24 h。反应结束后,待体系温度降至室温,离心得到橙色固体产物,依次用蒸馏水和乙醇各洗三次,最后在60 ℃真空烘箱干燥12 h,最终得到3的纳米线。
1.2.3 光催化醇无受体脱氢反应的一般步骤
在氮气氛围下,将醇 (0.2 mmol),3 (4.1 mg), 氢氧化钾(KOH, 0.04 mmol) 以及6.0 mL MeCN加入35 mL的石英管中。密封后,用氮气球鼓入氮气,室温条件在蓝色LEDs灯的照射下搅拌反应。反应结束后,向其中加入10 mL水并用二氯甲烷CH2Cl2萃取 (3 × 10 mL)。合并有机相并用无水硫酸钠干燥后减压蒸馏,得到的粗产物用硅胶色谱柱分离提纯。
2 结果与讨论
2.1 化合物2和3的合成与表征
Cu6(dmpymt)6(1)中存在的未参与配位的N原子,还可以进一步与金属离子发生配位反应。令我们高兴的是,室温条件下1与CuI在MeCN和CHCl3中反应得到一个三维的簇基配位聚合物{[Cu6(dmpymt)6][Cu2(μ-I)2]2(CuI)·3CH2Cl2}n(2·3CH2Cl2)。
1与(Ph3P)CuI在乙腈和甲苯中120 ℃条件下发生溶剂热反应得到另一个三维化合物{[Cu6(dmpymt)6][Cu2(μ-I)2]2·0.5MeCN}n(3·0.5MeCN)。单晶衍射分析表明,2·3CH2Cl2属于四方晶系,P41212空间群。在2·3CH2Cl2中,每个“Cu6(dmpymt)6”单元通过四个“Cu2(μ-I)2”与其他四个相同单元相互连接形成一个二维的面,面与面之间再通过N—Cu—N键连接成一个三维网络结构(图1)。化合物3属于单斜晶系,C2/c空间群。3中每个“Cu6(dmpymt)6”单元可以作为四面体节点,通过N—Cu(μ-I)2Cu—N的桥连与邻近的其他四个单元相互连接成一个三维网络(图2)。“Cu6(dmpymt)6”单元中的六个(2)或四个(3)dmpymt配体以μ—(κ1—N,κ1—N′,κ3—S)的配位模式桥连四个铜(I)原子,其他的dmpymt以μ—(κ1—N,κ3—S)的配位模式桥连三个铜(I)原子。如果将每个“Cu2(μ-I)2”或者“CuI”看作是2-connecting节点,那么“Cu6(dmpymt)6”可简化为6-或者4-connecting节点,三维的拓扑结构可以描述为{(8)(8)(812·123)} (2)和{(8)(84·122)} (3)(图1d和图2c)。

图1 (a) 2中最小结构单元;(b) [Cu6(dmpymt)6]与[Cu(μ-I)]2组成2中沿bc面延伸的二维网络结构;Color codes: Cu (cyan), I (pink), S (yellow), N (blue), C (black);(c) 2的三维网络结构;(d) 2的拓扑结构(红色代表4-connected Cu6(dmpymt)6;绿色Cu2I2 linking;紫色[CuI] units)

图2 (a) 3的三维网络结构;(b) 3的拓扑结构(颜色说明与图1描述一致)

图3 化合物2(左)和3(右)的PXRD谱图
化合物2和3均能在含氧和潮湿条件下稳定存在,并且不能溶于常见的有机溶剂CHCl3、甲醇(MeOH)、MeCN、N,N-二甲基甲酰胺(DMF)和二甲亚砜(DMSO)等。它们的元素分析测试结果均符合各自的分子式。如图3所示,化合物2和3的粉末X射线衍射(PXRD)谱图与单晶数据模拟的结果相匹配。氮气氛围下,热重分析(TGA)表明这两个化合物都具有较高的热稳定性,在大约280 °C时骨架开始坍塌(图4)。
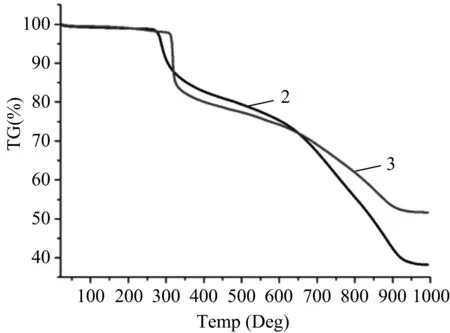
图4 化合物2和3的热重曲线图
[Cu6(dmpymt)6]和CuI在CHCl3和MeCN中室温搅拌生成2的纳米粒子。在耐压玻璃管中,[Cu6(dmpymt)6]、(Ph3P)CuI和PVP于乙腈和甲苯混合溶液中120 ℃加热搅拌24 h可制备3的纳米线。所制备的2和3纳米粒子的PXRD谱图分别与其单晶数据模拟的结果相匹配(图3)。如图5a所示,它们的SEM图像表明2的纳米粒子的形状近似于球形,粒径大约在50~100 nm之间。纳米粒子3生长成纳米线,它的宽度为50~100 nm,长度为十几微米(图5b)。X射线光电子能谱(XPS)表征了两个化合物中存在的元素及其价态。XPS谱图(图6)中,在结合能931.9 eV (2)或者932.2 eV (3)和951.8 eV (2)/952.1 eV (3)的峰,分别对应于Cu 2p3/2和Cu 2p1/2,相应地Cu的价态为一价。

图5 2 (a)和3 (b)纳米结构的SEM图像

图6 2 (a)和3 (b)的XPS谱图
2.2 化合物1,2和3的光学性质
如图7所示,1表现出紫外可见光吸收并在480 nm可见光处仍有吸收。由1自组装得到的2和3呈现出相似的吸收带。与1相比,它们在可见光的吸收范围更宽并且吸收峰有轻微红移。在室温下,我们测试了它们的固体荧光发射。在波长420 nm光的激发下,1在742 nm处有一个强荧光发射峰(图8),量子产率为36.23%。1在CHCl3中只能发出极弱的荧光,量子产率为4.37%。因此1可以作为聚集诱导发光材料[17]。此类化合物的荧光发射极有可能来自配体到金属的电荷转移(LMCT)和(或者)金属到配体的电荷转移(MLCT),可能还涉及金属中心的电荷转移(ds/dp)。在相同的测试条件下,化合物2的荧光发射与3相似,由于3具有较短的Cu…Cu键,所以3的最大发射峰的位置会蓝移至677 nm处。2和3的量子产率均高于1,分别高达42.47%和55.28%。除此之外,我们还测试了1,2和3的固体荧光寿命,分别是3.6,4.1和7.1 μs。如图9所示,相比于1,化合物2和3表现出较强的光电流响应,说明2和3具有较高的电荷分离效率。以上结果表明,簇合物的自组装不仅可以扩展自身的吸收范围而且能提升其荧光性质。由紫外漫反射数据推算出它们的能隙值分别为2.20 eV (2),2.20 eV (3)和2.02 eV (3)(图10)。吸收数据(α/S)是通过Kubelka-Munk方程计算得到:
其中,α是吸收系数,S是散射系数,R是特定能量下的反射率[18](P408)。

图7 室温下化合物1、2和3的固体紫外可见吸收光谱
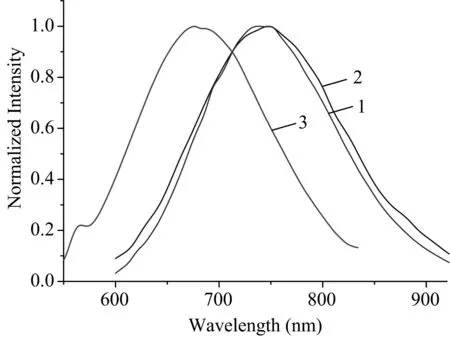
图8 室温下化合物1、2和3的固体荧光发射光谱(λex=420 nm)

图9 化合物1、2和3的瞬时光电流响应

图10 化合物1、2和3在室温下的固体紫外漫反射(以硫酸钡为背景)
2.3 光催化醇的无受体脱氢反应的条件优化
基于这些化合物的光化学性质,我们对其在蓝色LEDs灯下光催化醇的无受体脱氢反应展开了研究。以1-苯乙醇1aa为反应底物,最初的反应条件设置如下:室温下,氮气氛围中,1-苯乙醇(1aa,0.2 mmol),纳米粒子2 (NPs 3)或者NPs 3作为催化剂(10 mol% Cu),氢氧化钾(10 mol%)于乙腈中,蓝色LEDs灯照射6小时,可以分别得到95%和98%的苯乙酮(2aa)(表1,entries 1和2)。在相同的反应条件下,如果将2或者3的晶体研磨成粉末作为催化剂,分别给出80%和82%的2aa。为了验证反应过程中有氢气产生,我们用导管将光反应体系连通到含有Pd/C和4-甲氧基苯乙烯的乙酸乙酯溶液中,经气质联用(GC-MS)检测,乙酸乙酯溶液中有还原产物4-甲氧基苯乙烷生成,这一结果印证该光反应过程中确实有氢气产生。使用1作为催化剂,可以得到60%的目标产物(entry 3)。由于3具有较窄的能隙值,其纳米粒子表现出最高的催化活性。CuI表现出很差的催化活性(entry 4)。为了验证该反应经历了光诱导过程,空白实验研究结果表明:光催化剂和光源是实现该无受体脱氢反应的必要条件,缺一不可(entries 5和6)。除KOH以外,甲醇钠NaOMe,叔丁醇钾tBuOK,氢氧化钠NaOH,氢氧化锂LiOH,碳酸铯Cs2CO3,碳酸钾K2CO3和磷酸钾K3PO4都表现出较差的效果(entries 8-14)。在其他有机溶剂中反应, 2aa的产率较低(94% (toluene); 32% (四氢呋喃THF); 40% (DMF); 20% (CHCl3)) (entries 15-18)。在异丙醇中,该反应根本不能进行(entry 19)。
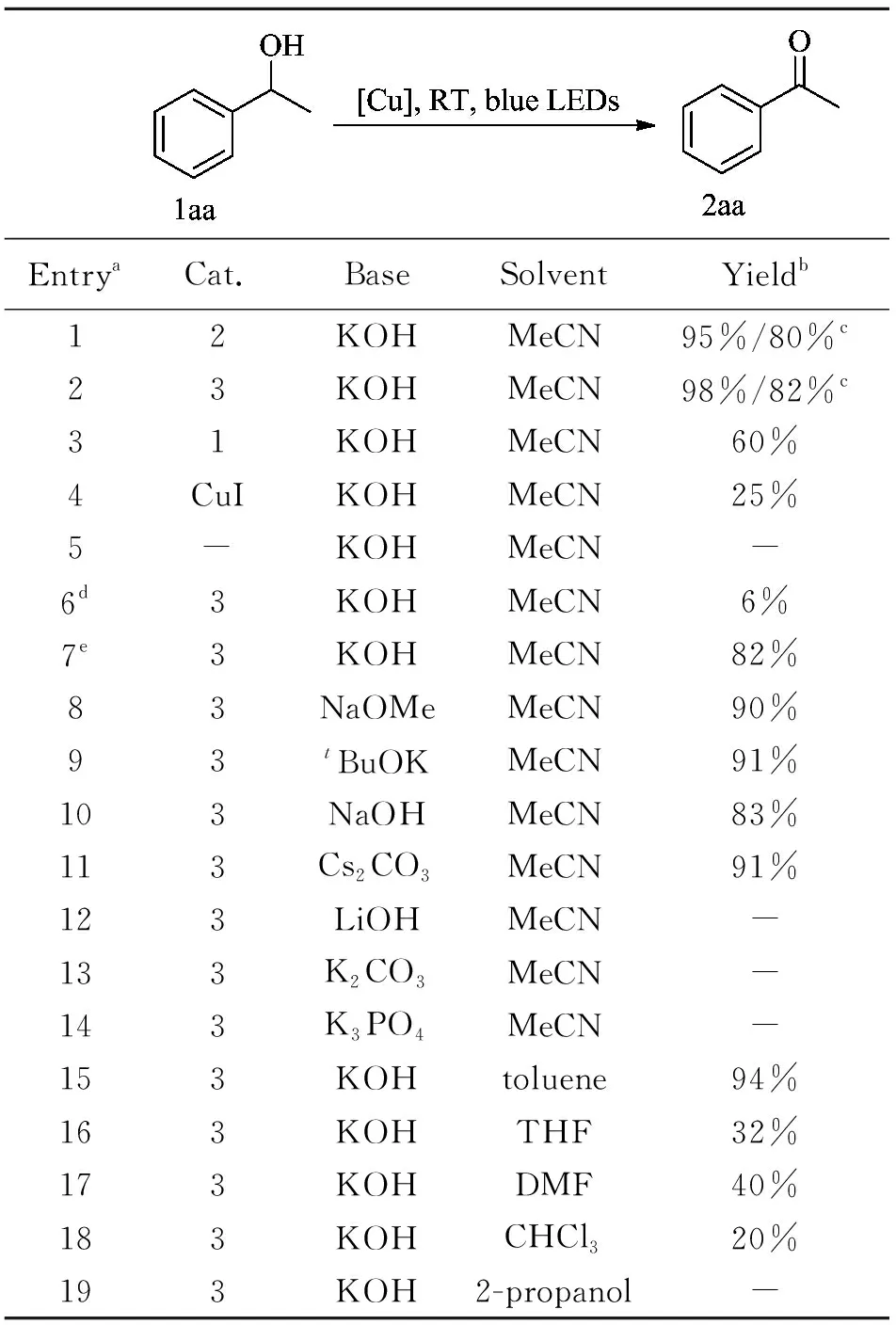
表1 醇脱氢反应的条件优化
2.4 底物拓展
在获得最优的反应条件之后,我们考察了可见光诱导醇脱氢反应的底物范围。如表2所示,所考察的二级醇底物都能顺利地发生无受体脱氢反应,以高收率得到相应的酮。1-苯乙醇衍生物苯环上的取代基电子效应对反应活性有一定的影响:苯环上带有给电子以及电中性取代基的1-苯乙醇能很顺利地发生脱氢反应,在反应5~6 h后得到酮的分离收率高达93%~99%(2aa-2ac, 2am, 2aq, Ⅲ2aw, 2ax);当苯环上带有拉电子取代基时,醇需要更长的反应时间完成转化(2ad, 2ae, 2ah, 2ai)。取代基的位阻效应对醇的反应性的影响微乎其微。带有间甲基和邻甲基的1-苯乙醇都可以高效地转化为对应的产物2aj (99%)和2al (96%)。对于二级杂环醇,1-thiophen-2-yl-ethanol和1-pyridin-3-yl-ethanol等都能顺利地分别转化为2ap (92%)和2ao (90%)。环己醇发生无受体脱氢反应生成2ay。该催化体系同样适用于一级醇的无受体脱氢反应,但其反应性低于相应的二级醇。苄醇类的底物需要反应10 h,得到中等或高分离收率的目标产物。苄醇苯环上有吸电子基团时会钝化该脱氢反应,需要更长的反应时间(14 h)实现较高的收率(2bd (86%),2be (89%), 2bg (87%),2bl (89%))。肉桂醇顺利地发生脱氢反应生成肉桂醛(2bm-2bo)。含杂原子的3-吡啶甲醇和2-噻吩甲醇等也是可以兼容的底物,脱氢得到相应的产物(2bk, 87%; 2bp, 89%)。一级脂肪醇也能发生完全转化(2bq, 2br)。

表2 3的纳米粒子光催化醇的无受体脱氢反应a
2.5 催化剂的循环实验
我们测试了NPs 3催化1-苯乙醇无受体脱氢反应的循环实验(图11),每一次循环反应结束以后,把NPs 3从催化体系中离心分离,依次用MeCN、H2O和Et2O洗涤并干燥,随后继续用于催化反应。由每次循环后NPs 3的粉末X射线衍射谱图可知,催化剂3的框架结构在反应过程中始终保持稳定(图12)。我们测试了第四次循环反应后NPs 3的SEM图,发现纳米粒子发生了明显的聚集(图13)。实验结果表明,经过4轮的催化循环后,NPs 3只能将大约79%的1-苯乙醇转化为苯乙酮(图11),每次循环后,纳米粒子会不可避免地发生团聚,导致其催化活性发生一定程度的失活。以上结果表明,光催化反应极有可能是在3纳米粒子的表面进行的。基于现有的研究结果,我们提出了如图14所示的可能反应机理,在可见光的照射下,NPs 3中会产生光生电子,结合原位生成的Cu-H/NH(SH)双氢物种实现醇的脱氢反应。

图11 NPs 3 在可见光照射下催化1-苯乙醇脱氢反应的循环实验
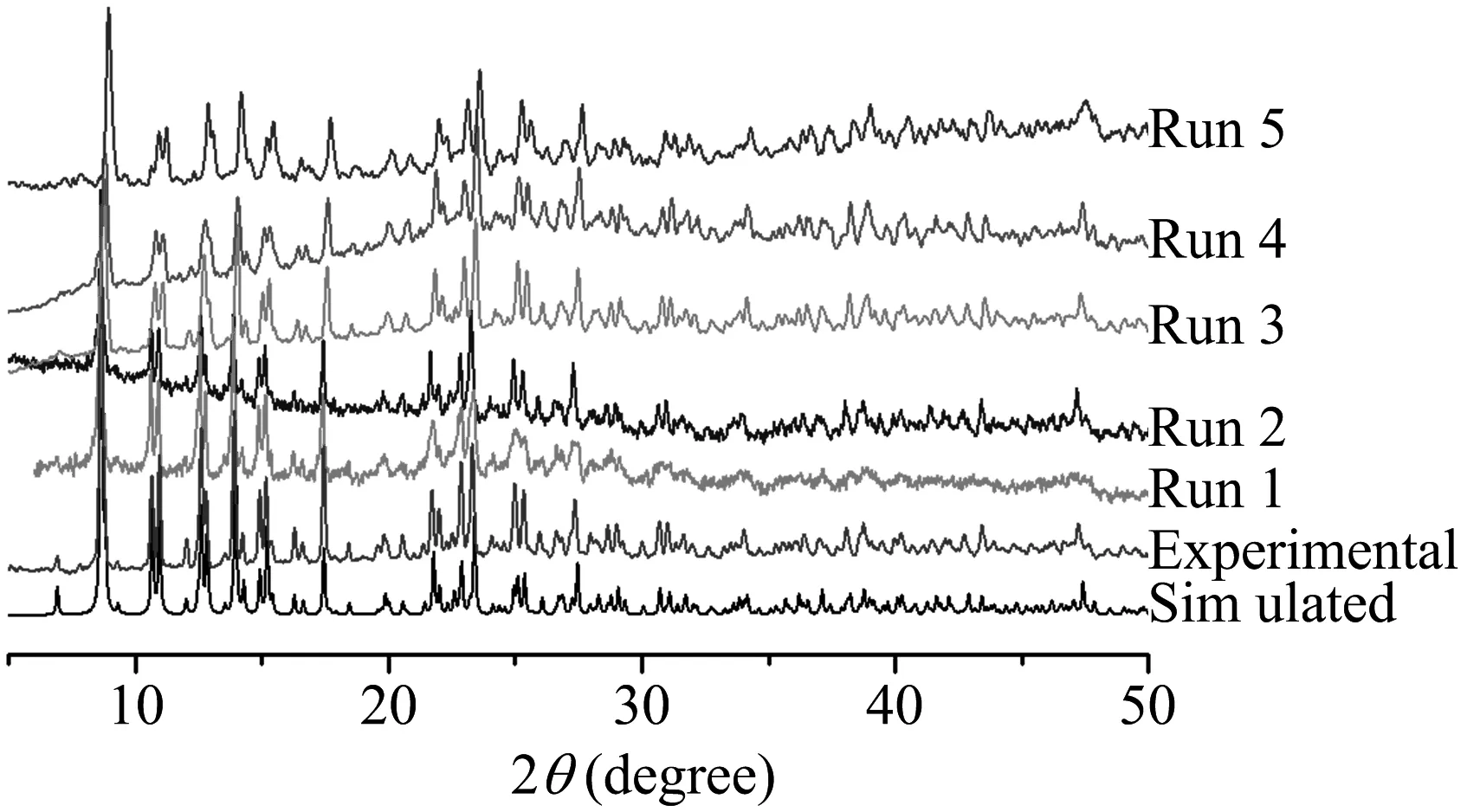
图12 NPs 3的单晶数据模拟、制备和催化循环后的PXRD图谱

图13 第四轮催化循环反应后NPs 3的SEM图

图14 光催化醇的无受体脱氢反应的可能机理
3 总结
本文使用[Cu6(dmpymt)6]作为前驱体分别与CuI和(Ph3P)CuI反应直接合成双功能簇基金属-有机框架结构{[Cu6(dmpymt)6]2[Cu2(μ-I)2]4(CuI)2}n(2)和{[Cu6(dmpymt)6]2[Cu2(μ-I)2]4}n(3)。MOFs 2和3既可以作为光敏剂又可以作为ADD催化剂,在蓝色LEDs灯的照射下,对于光催化醇的无受体脱氢反应表现出更高的催化活性。在温和的条件下,各种类型的二级醇,一级醇、烯丙基醇以及脂肪醇均能够转化成相应的酮或醛。除此之外,自组装得到的非均相光催化剂经多次循环使用后,依然保持着较高的催化活性。

