痒疹样营养不良型大疱性表皮松解症1例并文献复习
李杏杏,孔姝敏,曹育春,孙小燕
(华中科技大学同济医学院附属同济医院皮肤科,湖北 武汉 430030)
1 临床资料
患者女,41岁。“四肢及躯干丘疹、结节伴瘙痒10余年。”患者10余年前无明显诱因四肢出现丘疹、结节,偶见水疱,伴剧烈瘙痒。期间上述症状反复发作,患者多次于当地医院就诊,按“结节性痒疹”予以治疗,上述皮损无好转,逐渐增多加重,并向躯干部发展。患者既往体健,家族中无类似病史。皮肤科情况:躯干、四肢见散在分布黄豆至指甲盖大小丘疹、结节,其上可见散在抓痕、结痂,皮损以四肢伸侧及背部为重,对称分布,境界清楚,未见糜烂、溃疡等。双膝内侧及双足底见新发对称分布壁厚水疱,疱液澄清。双足趾甲萎缩,轻度嵌入,部分趾甲增厚、混浊(图1a-1c)。甲板真菌检查为阴性。患者陈旧性皮损主要为苔藓样斑块或痒疹样结节样改变,皮损组织病理检查结果示:角化过度,颗粒层增厚,棘层呈轻度假上皮瘤样增生,棘细胞间水肿。真皮浅中层胶原增生肥厚,血管扩张、充血。(见图2a、2b)患者新发皮疹可见壁厚水疱,皮损组织病理检查示:表皮下水疱形成。真皮浅深层血管周围及胶原束间可见稀疏至中等密度的淋巴细胞、中性粒细胞浸润(图2c、2d)直接免疫荧光示:IgG,IgA,IgM,C3均为阴性。
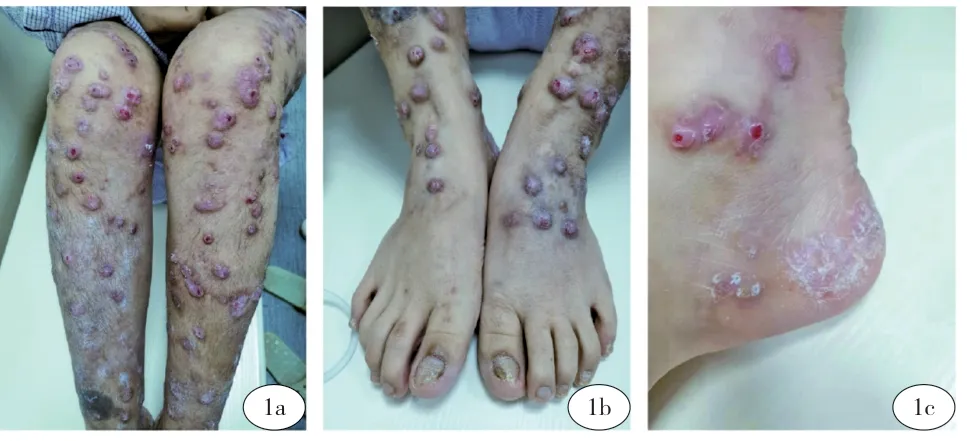
图1:痒疹样营养不良型大疱性表皮松解症患者皮损表现

图2:痒疹样营养不良型大疱性表皮松解症患者皮损病理表现(HE染色)
诊断:痒疹样营养不良型大疱性表皮松解症。
治疗:主要为对症支持治疗,如口服抗组胺药物缓解瘙痒,外用糖皮质激素等。加用阿维A胶囊及甲氨蝶呤口服治疗,患者病情可得到一定程度控制。本例患者尚未发现癌变倾向,需长期随访。
2 讨论
痒疹样营养不良型大疱性表皮松解症(dystrophic epidermolysis bullosa pruriginosa,DEBP)是 营 养 不良型大疱性表皮松解症中一种罕见的临床亚型,由1994年McGrath等[1]首次报道,迄今为止,已有记录的DEBP病例不到200例[2]。与大多数遗传性疾病不同,DEBP的症状和体征通常在成年期才出现。Hayashi报道[3]一例患者在71岁时才出现DEBP的临床表现。一些DEBP患者在成年后直接出现典型皮损而无任何其他大疱性表皮松解症的临床表现。其皮损常表现为逐渐于双胫或四肢伸侧缓慢出现的痒疹样改变、苔藓样斑块、萎缩性瘢痕,同时伴有轻度的甲营养不良,如甲萎缩或甲板不规则增厚。脚趾甲营养不良通常在婴儿期就出现,并且在大多数的DEBP病例中都能看到。极少数DEBP患者还可以在典型临床表现的基础上出现白色丘疹样皮疹[4]。因为长期搔抓损伤,完整的水疱是很少看到的,这增加了诊断的困难。该型常伴发剧烈瘙痒,这种瘙痒可以发生在皮肤表现之前,也可以与皮损同时出现。
DEBP在光镜下可见典型的表皮下水疱或裂隙、角化过度、纤维化、粟丘疹和少量淋巴细胞浸润。嗜酸性粒细胞浸润是EB常见的光镜下表现。然而,在遗传性大疱性表皮松解症(epidermolysis bullosa,EB)中观察到明显的炎症浸润,包括嗜酸性粒细胞,这个特征可能会被忽视,并被误诊为获得性自身免疫性大疱性疾病。DEBP电镜下的组织病理学分析常显示在真皮表皮连接处有数量减少和结构改变的锚原纤维。突变分析示:VII型胶原蛋白基因(COL7A1)突变。根据临床特征性病变、创伤性起疱史、显性或隐性遗传的有类似皮肤表现的家族史以及光镜或电镜下的组织学图像可诊断DEBP。突变分析是确诊遗传性EB的金标准[2]。临床上诊断的困难在于不同的发病年龄,罕见完整的大疱,组织学上的不明确,以及易与其他皮肤疾病的相混淆。DEBP的鉴别诊断包括肥厚性扁平苔藓、皮肤淀粉样变、慢性单纯性苔藓、结节性痒疹。本例患者新发皮损及病理均可见水疱,陈旧皮损病理示胶原增生肥厚,合并甲改变,尽管未行COL7A1基因突变检测,仍根据临床表现及病史诊断为DEBP。
EB的临床表现取决于特定基因的分子畸变及影响皮肤黏膜脆性超微结构的异常平面位置。目前已发现十余个基因的致病变异与EB相关,包括COL17A基因[5]。COL17A基因编码突变影响VII型胶原蛋白的功能及稳定表达,导致皮肤脆性增加,引起DEBP的典型临床表现。其致病遗传变异的具体性质决定了此类EB亚型的表型,即VII型胶原蛋白残余量或残余功能决定了疾病严重程度是轻中度,其症状受常年剪切力作用后逐渐加重。
长期反复剪切力造成的皮肤真表皮分离,以及之后机体对伤口愈合的修复机制是慢性炎症的原因之一。另外,在VII型胶原蛋白缺失的小鼠模型中可发现成纤维细胞中转化生长因子b1和成纤维细胞生长因子2表达升高以及真皮中胶原酶表达增加[6],提示VII型胶原蛋白异常可以参与细胞因子相关的慢性炎症。营养不良性EB的复发性炎症、瘢痕化和纤维化晚期可导致挛缩和假并指的形成,从而显著增加疾病的严重程度并降低生活质量。临床前研究显示磷酸二酯酶-4抑制剂能够抑制EB的炎症因子水平从而改善患者症状和生活质量[7]。
DEBP发展为皮肤鳞状细胞癌(SCC)的风险随着伤口的严重程度和皮疹持续时间增加而增加。大疱性性表皮松解症继发的SCC通常比非EB的SCC更具侵袭性,需注意此类患者的定期随访和评估。有关DEBP的治疗目前并没有公认能治愈或较好疗效的方法。其临床治疗的主要目的是缓解瘙痒,预防及减少瘢痕形成,改善患者的生活质量。既往的治疗包括局部和全身使用糖皮质激素、口服维甲酸、紫外线光疗或者全身使用环孢素、氨苯砜、沙利度胺等[8]。然而,这些治疗手段的疗效都差强人意。近年来,临床前研究开始致力于转化疗法[9],包括从细胞和基因水平纠正编码异常的蛋白、补充缺乏蛋白等方法,直接或间接地纠正潜在的分子病理学,从而有望获得更有效和持久的治疗。

