La2 O3 在LiF⁃NaF 熔盐体系中的溶解行为
熊志伟, 刘爱民, 刘玉宝, 王 旭, 石忠宁
(1. 东北大学 多金属共生矿生态化冶金教育部重点实验室, 沈阳 110819; 2. 包头稀土研究院 白云鄂博稀土资源研究与综合利用国家重点实验室, 包头 014030; 3. 江西理工大学 材料冶金化学学部, 江西 赣州 341000)
氢能作为一种清洁、绿色、高效的二次能源,对我国实现碳达峰与碳中和具有重要意义.氢能的储藏与运输是尤为关键的一步,镧镍系列合金具有不易粉化的特点[1-6],是一种优良的储氢材料.此外,在加工钢、铁等金属制品的过程中添加金属镧,利用其稀土微合金化的作用来细化组织或捕捉氢等有害元素,可极大提升合金的高温强度与耐腐蚀性.因此,金属镧在储氢材料、合金材料等方面得到广泛应用,其需求量逐年上升[7].
目前,制备金属镧的方法主要有熔盐电解法和金属热还原法.相较于金属热还原法,熔盐电解法具有可连续生产、经济方便及无需金属还原剂等优势,是工业生产金属镧的主要方法[8].根据熔盐体系不同,熔盐电解法可进一步分为氯化物体系熔盐电解法与氟化物体系熔盐电解法.与氯化物体系熔盐电解相比,氟化物体系熔盐电解法的电流效率与稀土回收率较高,在解决槽体材料耐氟盐腐蚀等问题之后得以迅速发展,现已达到工业化稳定生产水平[9-12].
稀土氧化物是氟化物熔盐体系电解制备稀土金属的原料,其在熔盐体系中的溶解度是影响电解过程的关键因素[9].从已有研究中可知,稀土氧化物在熔融氟化物中的溶解度通常很低,大部分低于10%(质量分数,下同)[13].Porter 等[14]使用石墨滤棒从稀土氧化物饱和的熔盐中提取样品进行化学分析,测量了1 073 ~1 223 K 下CeO2在CeF3⁃BaF2⁃LiF 熔盐体系中的溶解度,以及La2O3在LiF⁃LaF3和LiF⁃LaF3⁃BaF2熔盐体系中的溶解度,结果表明CeO2与La2O3在上述熔盐体系中的溶解度均小于5%.Ambrová 等[15]通过热分析法测量了La2O3在熔融碱性冰晶石中的溶解度,发现La2O3在碱性冰晶石中溶解度较高且为化学溶解,在锂冰晶石的共晶点温度下溶解度可高达19.12%.Ambrová 等[16]通 过 热 分 析 法 测 量 了La2O3分别在LiF,NaF,KF 一元体系和LiF⁃NaF⁃KF 三元共晶体系的溶解度,结果表明La2O3在上述熔盐中溶解度为1.1% ~2.4%且SLiF>SNaF>S(LiF⁃NaF⁃KF)eut>SKF.Pshenchny 等[17]比 较 了873 ~1 073 K 下La2O3,Sm2O3和Ho2O4分 别 在LiF⁃ZrF4,NaF⁃ZrF4,NaF⁃ZrF4与KF⁃ZrF4共晶熔盐体系中的溶解度,结果表明La2O3的溶解度为0.262%~2.057%,且在LiF⁃ZrF4熔盐体系中的溶解为化学溶解.
通过对LiF⁃NaF 熔盐体系物理化学性质的研究[18],发现其初晶温度较低,但关于La2O3在LiF⁃NaF 熔盐体系中的溶解度和溶解机制的研究尚未有报道.本文中采用等温饱和法研究La2O3在LiF⁃NaF 熔盐体系中的溶解度,确定La2O3在LiF⁃NaF 熔盐体系中的溶解平衡时间,进一步探究La2O3在不同熔盐组分和温度下与溶解度的关系,并结合XRD 物相分析,揭示La2O3在LiF⁃NaF熔盐体系中的溶解机制.
1 实 验
LiF(质量分数≥99.9%),NaF(质量分数≥99%),La2O3(质量分数≥99.99%)等实验试剂均购买于上海阿拉丁生化科技股份有限公司.试剂放置在干燥箱中,150 ℃下干燥24 h,充分脱除吸附的水分后以待实验使用;使用粒度为25 μm 的碳化硅砂纸打磨若干不锈钢棒,去除不锈钢棒表面氧化层,用酒精擦拭后进行烘干,并放置在干燥处,以待实验中用于提取上清液.
主要设备有高温电阻炉与自制加料装置,如图1 所示.采用等温饱合法测定La2O3在LiF⁃NaF熔盐体系中的溶解度[19].将一定质量配比的LiF,NaF 混合均匀放入石墨坩埚中,再将石墨坩埚放入铁坩埚中,并在高温电阻炉中加热到所需温度,保温一段时间直至熔盐完全熔化;然后将过量的La2O3加入熔盐中,在预定温度保温溶解一段时间后,取熔盐上层清液,冷却后研磨成粉状制样.采用电感耦合等离子体原子发射光谱法对样品中镧的质量分数进行测定,再通过计算得出La2O3在此熔盐体系中的质量分数.整个实验过程在氩气保护性气氛下进行.

图1 实验装置图Fig.1 Diagram of experimental setup
2 结果与讨论
2.1 La2O3 溶解平衡时间测定
为测定La2O3在LiF⁃NaF 熔盐体系中的溶解度,需先确定La2O3在此熔盐体系中的溶解平衡时间,再研究温度、熔盐组分等条件对La2O3溶解度的影响.
在温度为680 ℃、熔盐配比量为60%LiF⁃40%NaF(摩尔分数,下同)的条件下,采用控制变量法研究熔盐体系中La2O3的溶解平衡时间,结果如图2 所示.在恒定温度680 ℃下,随着溶解时间的延长,熔盐中La2O3质量分数逐渐增大,达到溶解平衡时,La2O3质量分数约为1.75%.在溶解过程的前120 min,熔盐体系中La2O3质量分数快速增大,说明La2O3在此时间段的溶解速度较快,平均溶解速度约为0.87%/h;在120 min 之后,La2O3质量分数不再增大,恒定在1.75%左右,说明此时熔盐中的 La2O3达到了溶解平衡. 使用ExpAssoc 模型对数据进行非线性拟合,R2=0.977 02,相关性较好,具体方程式如下所示:

图2 LiF⁃NaF 熔盐体系中La2O3 质量分数与溶解时间的关系(在680 ℃)Fig.2 The relationship between the mass fraction of La2O3 and the dissolution time in the LiF⁃NaF molten salt system(at 680 ℃)
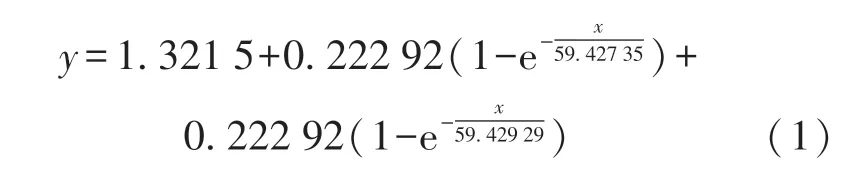
综上所述,在温度为680 ℃的条件下,La2O3经120 min 溶解后达到饱和状态,此时可认为在120 min 之后熔盐中La2O3质量分数等于其在此条件下的溶解度.根据La2O3溶解平衡时间测定的实验,可确定接下来溶解度实验的取样时间,以期提高实验数据准确性与实验效率.
2.2 La2O3 在LiF⁃NaF 熔盐中的溶解机制
Stefanidaki 等[20]通 过 研 究Nd2O3在NdF3⁃LiF⁃KF⁃MgF2熔盐中的溶解机制,发现在溶解过程中产生了含有Nd 的氟氧络合物;Ambrová等[15]通过对La2O3在M3AlF6(M=Li,Na,K)熔盐中溶解机制的研究,发现在溶解过程中产生了氟氧络合物LaOF.由此可见,稀土氧化物在熔盐体系中溶解过程变化较为复杂,其溶解行为往往不是单一形式,通常是物理溶解与化学溶解同时进行.
在实验中,首先将质量分数为5%的La2O3加入完全融化的60%LiF⁃40%NaF 熔盐中,在680 ℃下溶解超2 h 达到溶解平衡状态,此时取熔盐上清液在室温下冷却并制样,然后对试样进行XRD分析,结果如图3 所示.

图3 LiF⁃NaF 熔盐上清液的XRD 图谱Fig.3 XRD pattern of LiF⁃NaF molten salt supernatant
从图3 中可以发现,物相中存在LaOF,NaF,LiF,La2O3相.其中,NaF,LiF,La2O3相为配制熔盐添加的物质,而LaOF 相可以断定为新生成的物质.XRD 测试结果表明,溶解过程中既存在物理溶解也存在化学溶解.LaOF 的形成可以通过如下反应解释[16].

2.3 LiF⁃NaF 熔盐组分对La2O3 溶解度的影响
采用控制变量法,考察LiF⁃NaF 相图共晶点(61% LiF⁃39% NaF,649 ℃) 附 近 熔 盐 组 分 对La2O3在LiF⁃NaF 熔盐中溶解度的影响,实验结果如图4 所示.

图4 La2O3 在LiF⁃NaF 熔盐中的溶解度与熔盐中LiF 摩尔分数的关系Fig.4 The relationship between the content of molten salt components and the dissolved amount of La2O3
随着LiF⁃NaF 熔盐中LiF 摩尔分数的增加,La2O3在熔盐中的溶解度先增大后减小.当熔盐组分为60%LiF⁃40%NaF 时,La2O3的溶解度达到最大值,这是因为此时LiF⁃NaF 熔盐的初晶温度接近于共晶温度.当LiF 摩尔分数小于60%时,相同温度下熔盐的过热度会随着LiF 摩尔分数增加而升高,使得溶解度随着LiF 摩尔分数的增加而增大.当LiF 摩尔分数大于61%时,相同温度下熔盐的过热度会随着LiF 摩尔分数的增加而降低,使得La2O3在熔盐中的溶解度随着LiF 摩尔分数增加而减小.
2.4 温度对La2O3 在LiF⁃NaF 熔盐中溶解度的影响
为了确定溶解平衡后La2O3的溶解度与温度之间的变化规律,采用控制变量法,探究不同配比LiF⁃NaF 熔盐体系下La2O3溶解度与温度(680 ~900 ℃)的关系,结果如图5 所示.

图5 不同配比LiF⁃NaF 熔盐体系中La2O3 的溶解度与温度的关系Fig.5 The relationship between the solubility of La2O3 and temperature in the LiF⁃NaF molten salt system with different proportions
从图5 可以看出,在一定配比的熔盐体系中,当溶解达到平衡之后,La2O3的溶解度随着温度的升高而增大.首先,对于化学溶解反应而言,升高温度对吸热反应[21]有正向促进作用,会进一步加速溶解.其次,LiF 能有效降低熔盐熔点,从而在熔盐温度升高的过程中使得熔盐的内部结构变得松散,导致熔盐体积增大,熔盐中阴阳离子间作用力减弱及微观结构孔隙增加,有利于La2O3溶解.
对实验数据进行线性拟合,结果如图6 所示,发现温度与溶解度之间呈现较好的线性关系.
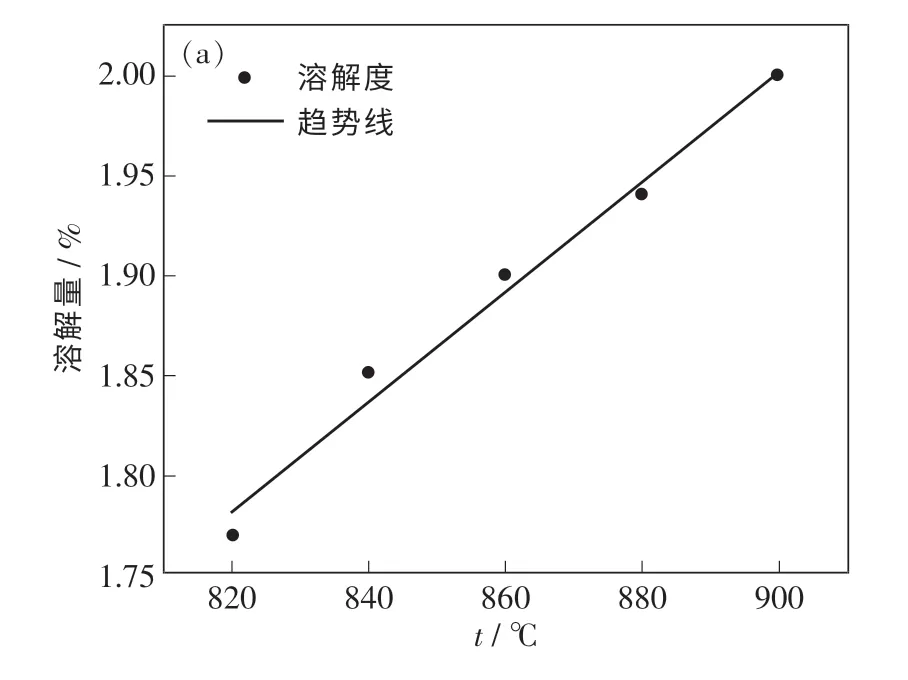

图6 温度-溶解度数据拟合Fig.6 Temperature⁃solubility data fitting
其具体线性方程与决定系数R2如下:

式中:S为La2O3溶解度,%;t为摄氏温度,℃.
拟合结果表明,LiF 摩尔分数、NaF 摩尔分数、温度均与La2O3溶解度密切相关.虽然较高的温度能提高La2O3的溶解量,过大的过热度可增大La2O3溶解速率,从而有效提升电解效率,但温度过高会使电解质中的LiF 与NaF 大量挥发,对人体产生危害,同时也会造成电解质的浪费.此外,在电解过程中,过高的温度会消耗大量电能,损失不必要的电解成本,出于实际生产考虑,过热度应控制在30 ℃以内.
2.5 溶解过程焓变的计算
从热力学角度来解释,La2O3的溶解过程可以简单地认为是La2O3从固态向溶解态的转变.由此,该过程可表示为

式中:T为热力学温度,K.
结 合 图7 所 示, 拟 合 直 线 的 斜 率a=-0.954 58 ± 0.022 817, 截 距b=1.956 21 ±0.036 07,溶解度的自然对数与热力学温度的倒数呈现较好的线性关系(R2=0.991 37).

图7 La2O3 在LiF⁃NaF 熔盐体系中溶解度的自然对数与温度倒数的关系Fig.7 The relationship between the natural logarithm of the solubility of La2O3 in LiF⁃NaF molten salt system and the reciprocal temperature
当溶解达到平衡时,吉布斯自由能可以通过反应的平衡常数K来表示:


3 结 论
(1)在温度达到680 ℃时,La2O3在LiF⁃NaF熔盐体系中溶解平衡时间为120 min 左右.
(2)La2O3在LiF⁃NaF 熔盐体系中溶解包括物理溶解与化学溶解, 其中化学反应为:La2O3+2MF ══2LaOF+M2O(M=Li,Na).
(3)相同温度条件下,La2O3溶解度会随着LiF 摩尔分数的增加表现出先升高后降低的趋势,在熔盐比例60%LiF⁃40%NaF 时达到峰值.
(4)相同熔盐组分条件下,La2O3溶解度会随着温度的上升而增大;溶解过程La2O3(s)→La2O3(溶解态)为吸热过程.

