藤茶总黄酮提取工艺优化与抗氧化 活性物质基础研究
◎ 许陈思菡,沈周媛,袁琢越,路 璐,向延卫,丁 越
(上海中医药大学,上海 201203)
藤茶,学名显齿蛇葡萄,由被子植物门木兰纲芸香目葡萄科蛇葡萄(Ampelopsis grossedentata)的嫩茎叶加工而成,盛产于我国湖北、湖南、江西以及福建等南方各地[1-2]。藤茶性凉,味甘淡,有清热解毒、消肿利咽、消痈散结的功效,可用于治疗口腔溃疡、咽喉肿痛、感冒发热、湿热黄疸、目赤肿痛和痈肿疮疖等症状[3]。现代研究表明藤茶具有较好的抗氧化、抗肿瘤、抗炎抑菌、抗流感、降血压、降血脂及保肝等多种保健功效和药理作用,是一种极具开发潜力的中草药[4-10]。黄酮类化合物是藤茶中最主要的成分,藤茶中的黄酮含量是目前被研究的植物中最高的,因此藤茶又被称为“黄酮之王”[11]。藤茶中总黄酮含量高达45.52%,其中二氢杨梅素的含量达藤茶总黄酮含量的58.10%~58.80%[12]。目前,藤茶产品开发尚处于初级阶段,以茶类产品为主,即冲泡型商品。然而藤茶晒干后,其表面的白霜会导致冲泡后外观及口感不佳。从藤茶的开发利用来讲,藤茶提取物应用到食品中安全健康,具有广阔前景。本研究采用紫外分光光度计法检测藤茶及其提取物中总黄酮含量,并对藤茶的水提工艺进行优化,测定藤茶提取物及其主要活性成分的抗氧化活性,研究藤茶的抗氧化的物质基础,以期为藤茶的进一步研究和开发提供理论依据。
1 材料与方法
1.1 材料与试剂
藤茶原茶,市售湖南张家界野生特级藤茶(批号:20210816)。
1,1-二苯基苦基苯肼(DPPH),购自上海鸿永生物科技有限公司;芦丁标准品(纯度92.6%,供UV检测),购自中国食品药品检定研究院;抗坏血酸(维生素C),购自国药集团化学试剂有限公司;二氢杨梅素标准品(纯度98.38%,供HPLC测定)、杨梅素标准品(纯度99.69%,供HPLC测定)、檞皮素标准品(纯度98.05%,供HPLC测定)、橙皮素标准品(纯度98.60%,供HPLC测定)和芹菜素标准品(纯度98.03%,供HPLC测定),均购自上海鸿永生物科技有限公司。乙醇、甲醇、硝酸铝、氢氧化钠和亚硝酸钠均为分析纯,均购自国药集团化学试剂有限公司。
1.2 仪器与设备
JFSD-100-II微型高速粉碎机,上海嘉定粮油仪器有限公司;YH系列电热器,500 mL,江苏近湖镇教学仪器厂;DK-S24电热恒温水浴锅,上海精密实验设备有限公司;XS105电子天平,梅特勒-托利多集团;UV2550紫外分光光度计,日本岛津公司;酶标仪,BioTek;SB5200D超声波清洗机,宁波新芝生物科技股份有限公司。
1.3 实验方法
1.3.1 藤茶总黄酮水提工艺研究
(1)提取方法。取50 g藤茶,加入适量的水煎煮,合并几次水煎液,过滤。
(2)单因素实验设计。取50 g藤茶,分别加入不同料液比1∶10、1∶20、1∶30、1∶40和1∶50(g∶mL)的水煎煮1.0 h、1.5 h、2.0 h和2.5 h,煎煮1、2、3次,合并水煎液,过滤,采用直接测定法测定藤茶水煎液中藤茶总黄酮的浓度,并计算总黄酮提取率,考察不同料液比、不同提取时间、不同提取次数对藤茶总黄酮提取率的影响。
(3)水提工艺正交试验设计。采用L9(34)正交试验表,考察料液比(1∶20、1∶30、1∶40)、提取时间(1.0 h、1.5 h、2.0 h)和提取次数(1次、2次、3次)3个因素,以总黄酮提取率为考察指标,分别采用直观分析和正交分析进行水提工艺条件的优选,确定最佳水提提取工艺。
1.3.2 藤茶中总黄酮含量测定方法的建立与比较
(1)二氢杨梅素标准品溶液制备精密称定适量二氢杨梅素标准品,用95%乙醇溶解并定容于25 mL容量瓶中,配成0.499 6 mg·mL-1的标准品溶液,备用。
(2)样品溶液制备称取5 g藤茶,10倍量75%乙醇浸泡18 h,超声1 h,过滤,取1 mL滤液于50 mL容量瓶中,95%乙醇定容,然后取5 mL于50 mL容量瓶中,95%乙醇稀释至刻度线,备用。
(3)直接测定法精密吸取藤茶样品溶液2.5 mL于25 mL容量瓶中,另取0.5 mL二氢杨梅素标准品溶液于另一个25 mL容量瓶中,并采用95%乙醇定容,摇匀后静置10 min,在200~700 nm波长进行扫描,根据扫描光谱图,确定该方法的最适吸收波长为294 nm。然后分别准确吸取0.250 mL、0.375 mL、0.500 mL、0.625 mL和0.750 mL二氢杨梅素标准品溶液于5个不同25 mL容量瓶,95%乙醇定容,摇匀,静置10 min,在此方法最适吸收波长处测定吸光度,绘制标准曲线,测定藤茶样品溶液的吸光度并计算其中藤茶总黄酮的含量。
(4)硝酸铝-亚硝酸钠-氢氧化钠[Al(NO3)3-NaNO2-NaOH)]比色法(简称硝酸铝法)。精密吸取藤茶样品溶液1.5 mL于25 mL容量瓶中,另取0.25 mL二氢杨梅素标准品溶液于另一个25 mL容量瓶中,加入5 mL蒸馏水,摇匀后加入1 mL 5% NaNO2溶液摇匀并静置6 min,加入1 mL 10% Al(NO3)3溶液摇匀静置6 min,加入10 mL 10 mol·L-1NaOH溶液,加蒸馏水至刻度线后摇匀静置15 min,在200~700 nm波长进行扫描,根据扫描光谱图,确定该方法的最适吸收波长为324 nm。然后分别准确吸取0.15 mL、0.20 mL、0.25 mL、0.30 mL和0.35 mL二氢杨梅素标准品溶液于25 mL容量瓶,按上述方法进行处理,在此方法最适吸收波长处测定吸光度,绘制标准曲线,测定藤茶样品溶液的吸光度并计算其中藤茶总黄酮的含量。
1.3.3 藤茶总黄酮水提物及其主要化合物抗氧化活性评价
(1)DPPH溶液的制备。精密称取DPPH试剂适量,加乙醇溶解配制成0.65 mmol·L-1。
(2)样品溶液的制备。精密称取2.00 mg藤茶提取物,加入乙醇溶液,定容至10 mL,恒温超声提取30 min,冷却至室温,用50%乙醇逐级稀释成系列浓度的样品溶液。
(3)对照品溶液的制备。精密称取芦丁、抗坏血酸、二氢杨梅素、杨梅素、槲皮素和橙皮素适量,加入二甲基亚砜适量配成20 mmol·L-1母液,用50%乙醇逐级稀释成系列浓度的对照品溶液。
(4)抗氧化活性的测定。精密量取10 μL样品提取液和对照品溶液,分别加入有100 μL DPPH溶液的96孔板中,充分混匀,加入140 μL的50%乙醇,室温避光反应1 h,混匀,在517 nm下测定吸光度。以加入50%乙醇溶液为空白对照,各平行3份。并计算抑制率:
式中:A1为样品溶液的吸光度;A0为空白对照溶液的吸光度。
分别以各样品溶液浓度和抑制率进行线形回归,并计算抑制率为50%时,待测样品的浓度值,即半抑制浓度IC50。
2 结果与分析
2.1 方法学考察
2.1.1 线性关系考察
分别准确吸取0.250 mL、0.375 mL、0.500 mL、0.625 mL和0.750 mL二氢杨梅素标准品溶液于25 mL容量瓶,95%乙醇定容,摇匀,静置10 min,在最适吸收波长处(294 nm)测定吸光度,以吸光度(Y)对各对照品浓度(X)进行线性回归。
分别准确吸取0.15 mL、0.20 mL、0.25 mL、0.30 mL和0.35 mL二氢杨梅素标准品溶液于25 mL容量瓶,加入5 mL蒸馏水,摇匀后加入1 mL 5% NaNO2溶液摇匀并静置6 min,加入1 mL 10% Al(NO3)3溶液摇匀静置6 min,加入10 mL 10 mol·L-1NaOH溶液,加蒸馏水至刻度线后摇匀静置15 min,在最适吸收波长处测定吸光度(324 nm),以吸光度(Y)对各对照品浓度(X)进行线性回归,评价两种检测方法的线性关系。
直接测定法和硝酸铝法的线性关系见表1,以二氢杨梅素标准品溶液的系列浓度(µg·mL-1)为横坐标,吸光度为纵坐标绘制标准曲线,分别得到两种方法相应的线性回归方程。直接测定法在线性范围为4.996 ~ 14.988 μg·mL-1时,R2为 0.999 3,线性关系较好;硝酸铝法在线性范围为2.998~6.994 μg·mL-1时,R2为0.999 7,线性关系较好。

表1 两种测定方法的线性关系表
2.1.2 精密度实验
准确移取上述藤茶样品溶液2.5 mL和1.5 mL,分别按照1.3.2项下2种方法进行处理,然后在各方法的最大吸收波长处(294 nm和324 nm),在2 min内对同一样品溶液连续测定6次,计算测定吸光度的平均值和RSD值。直接测定法和硝酸铝法测定藤茶样品溶液总黄酮的精密度实验中,RSD值分别为1.4%和1.8%,均小于3%,说明采用紫外分光光度计测定总黄酮精密度较好。
2.1.3 重复性实验
分别按照1.3.2项下2种方法处理藤茶样品溶液各5份,然后测定各藤茶样品中总黄酮的含量,并计算其平均值和RSD值。结果表明,直接测定法和硝酸铝法测定藤茶样品溶液中总黄酮的含量分别为0.069 mg·mL-1和 0.083 1 mg·mL-1,RSD 值分别为 2.1%和2.4%,均小于5%,在误差允许范围内,说明采用上述两种方法测定藤茶提取液中总黄酮的含量,均有较好的重复性。
2.1.4 稳定性实验
准确移取藤茶样品溶液2.5 mL和1.5 mL,分别按照1.3.2项下2种总黄酮含量测定方法进行处理,然后在 0 h、0.5 h、1.0 h、1.5 h、2.0 h、2.5 h、3.0 h、3.5 h和4.0 h时,在各方法最大吸收波长处测定一次吸光值,共测定9次,计算各方法测定吸光度的平均值和RSD值。稳定性实验显示,直接测定法在4 h内的稳定性最好,RSD值仅为1.3%,硝酸铝法在4 h内的稳定性最差,RSD值为7.8%,而在1.0 h内的RSD值为2.1%,说明硝酸铝法在1.0 h内基本稳定。由此可见,直接测定法建立的总黄酮测定方法稳定性更好。
2.1.5 加标回收率实验
准确移取藤茶样品溶液1.25 mL和0.75 mL各9份藤茶样品溶液,按照80%、100%和120%比例分别加入一定量的二氢杨梅素标准品溶液后,分别按照1.3.2项下2种总黄酮含量测定方法进行处理,分别在上述方法中最大吸收波长处(294 nm和324 nm)测定藤茶样品溶液的吸光值,并计算其加样回收率和RSD值。结果表明,采用直接测定法测定藤茶总黄酮的含量平均加样回收率为100.5%,RSD为4.2%(表2);采用硝酸铝显色法测定藤茶总黄酮的含量平均加样回收率为102.8%,RSD为6.2%(表3),两种方法中硝酸铝显色法测定误差较大。结合方法学考察结果,最终选择直接测定法测定样品中总黄酮的含量。
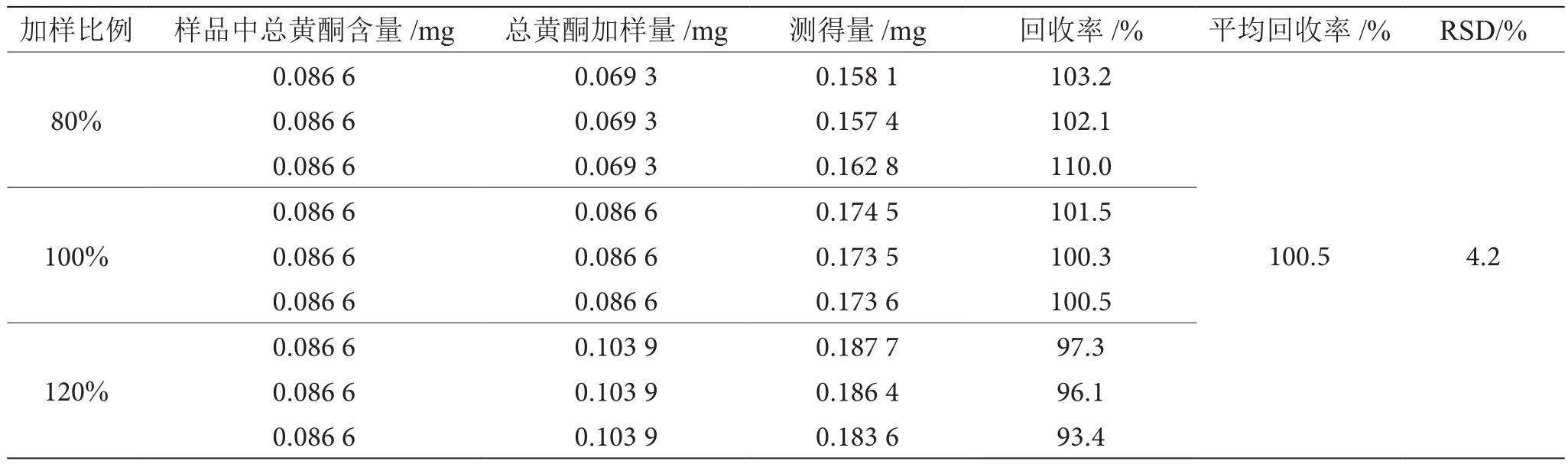
表2 直接测定法加标回收率实验结果表

表3 硝酸铝法加标回收率实验结果表
2.2 藤茶总黄酮水提工艺研究
2.2.1 提取溶剂量的初步考察
取50 g藤茶,分别加入不同料液比(1∶10、1∶20、1∶30、1∶40和1∶50)的水煎煮2 h,煎煮2次,合并水煎液,过滤,采用直接测定法测定藤茶水煎液中藤茶总黄酮的浓度,并计算总黄酮提取率。
由图1可知,随着提取液加入量的增加,藤茶总黄酮提取率先上升后逐渐下降,当料液比为1∶40时,总黄酮提取率达到最高。继续增加提取液用量,总黄酮提取率不再升高,考虑到提取液增多,使得浓缩时间变长,降低了提取效率。综合考虑经济效益,提取料液比选择1∶40最佳。
2.2.2 提取时间的初步考察
实验考察不同提取时间(1 h、1.5 h、2 h和2.5 h)对藤茶总黄酮提取效率的影响。由图2可知,随着提取时间的增加,总黄酮提取率先升高后降低,当提取时间达到2 h时,总黄酮提取率最高。综合考虑,初步确定提取时间为2 h。
2.2.3 提取次数的考察
实验考察不同提取次数(1次、2次、3次)对藤茶总黄酮提取效率的影响。由图3可知,随着提取次数的增加,总黄酮提取率先升高后降低,提取次数为2次时,总黄酮提取率最高。综合考虑,初步确定提取次数为2次。
2.2.4 水提工艺正交试验及方差分析
采用L9(34)正交试验表,考察料液比(1∶20、1∶30、1∶40)、提取时间(1.0 h、1.5 h、2.0 h)和提取次数(1次、2次、3次)3个因素,以总黄酮提取率为考察指标,进行水提工艺条件的优选,确定最佳水提提取工艺。正交实验结果见表4,方差分析见表5。
由表4可知,在不考虑交互作用的情况下,影响水提工艺的因素主次顺序为料液比>提取时间>提取次数。由表5可知,料液比对总黄酮提取率有显著性影响,而提取时间、提取次数在考察范围内影响不显著。因此,藤茶总黄酮提取的最佳工艺条件为A3B3C2,即选用料液比1∶40,提取2 h,提取2次。
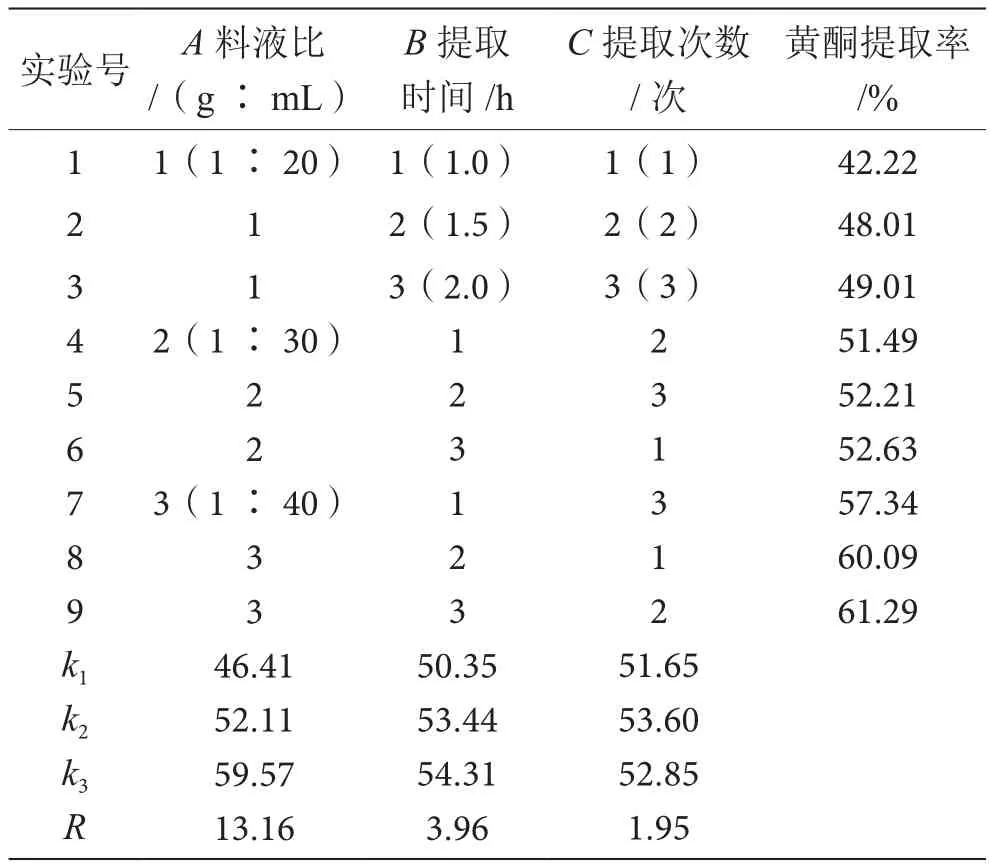
表4 正交试验结果表
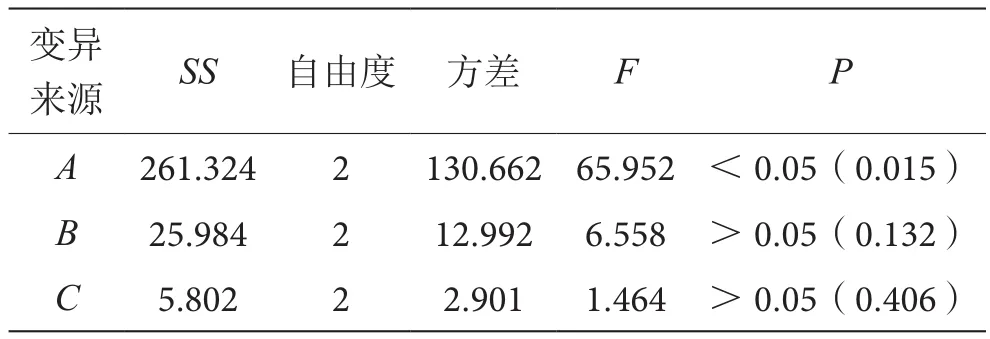
表5 正交试验方差分析表
2.2.5 最佳工艺验证实验
由表6可知,按照最佳提取溶液开展验证实验,3次实验藤茶总黄酮提取率分别为62.61%、62.40%和61.66%,说明该工艺稳定可行。
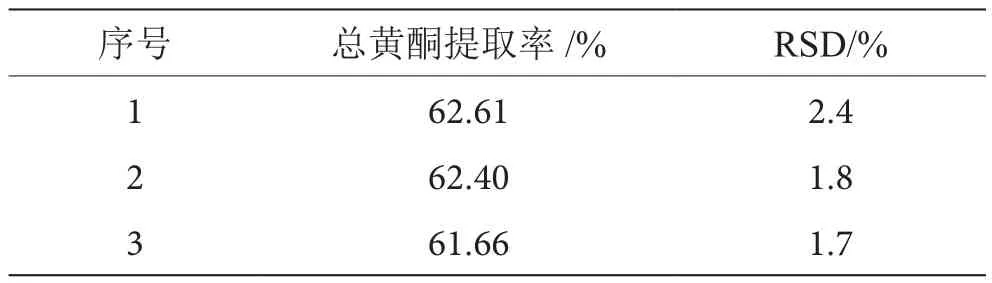
表6 重复性试验结果表
2.3 测定结果
由表7可知,藤茶水提物对DPPH自由基清除能力强弱与黄酮含量呈正相关性,表明藤茶提取物中黄酮类化合物的抗氧化活性占主导地位。藤茶总黄酮水提物IC50=0.176 mg·mL-1,总黄酮DPPH自由基清除能力略低于维生素C(IC50=0.147 mg·mL-1),高于芦丁(IC50=0.192 mg·mL-1)。藤茶中主要的4种黄酮类单体化合物均有较强的清除作用,对DPPH自由基清除能力随着浓度的增加而增强。对DPPH自由基清除能力为杨梅素>槲皮素>二氢杨梅素>维生素C>橙皮素。

表7 藤茶总黄酮提取物和主要黄酮类单体化合物抗氧化活性结果表
3 结论
本文以二氢杨梅素为对照品,选用直接测定法和硝酸铝法对藤茶中总黄酮含量进行测定,结果表明两种测定方法相对应的最适吸收波长分别为294 nm和324 nm。在该波长下,直接测定法和硝酸铝法测定藤茶总黄酮,在 4.996 ~ 14.988 μg·mL-1和 2.998 ~ 6.994 μg·mL-1线性关系良好;精密度、重复性良好;稳定性结果表明,直接测定法在4 h内的稳定性最好,硝酸铝法在1.0 h内基本稳定,4 h内的稳定性较差。同时,加标回收率实验结果表明采用硝酸铝显色法测定藤茶总黄酮的含量平均加样回收率为102.8%,RSD为6.2%,两种方法中硝酸铝显色法测定误差较大,最终选择直接测定法测定藤茶中总黄酮的含量。
藤茶总黄酮是藤茶中主要活性成分,采用水提法制备藤茶总黄酮,采用单因素和正交实验得到的最佳提取工艺为料液比1∶40,提取2 h,提取2次。3次验证性实验表明,所制备藤茶水提物中总黄酮提取率分别为62.61%、62.40%和61.66%,说明该工艺稳定可行。运用DPPH法对藤茶水提物及其黄酮类单体成分的自由基清除能力进行评价,结果表明,藤茶水提物对DPPH自由基清除能力强弱与黄酮含量大小呈正相关性,对DPPH自由基清除能力略高于芦丁。藤茶中主要的4种黄酮类单体化合物均有较强的清除作用,对DPPH自由基清除能力随着浓度的增加而增强,对DPPH自由基清除能力为杨梅素>槲皮素>二氢杨梅素>维生素C>橙皮素,其中杨梅素、二氢杨梅素和槲皮素可能是藤茶抗氧化的主要化学成分。
藤茶作为一种保健茶,在民间饮用历史可上溯到神农尝百草时期。我国最早的诗歌总集《诗经》称之为古茶勾藤。它不仅是一种纯天然的绿色饮料,更是一种药效保健性能很强的茶中奇葩。藤茶素有“黄酮之王”的称号,本文通过提取工艺优化,可以使藤茶总黄酮提取率达到60%以上,同时藤茶提取物可以迅速溶解到溶液中,服用后发挥抗氧化、抗炎的功效。藤茶提取物对DPPH自由基清除能力强弱与黄酮含量大小呈正相关性。目前已证实自由基氧化损伤与衰老及多种疾病相关,当体内自由基产生过多或/和清除过少时都会打破人体内自由基平衡,使多余的自由基攻击人体内的生物膜,造成体内脂质、蛋白质、核酸、酶等生物大分子的氧化损伤,破坏细胞结构和功能完整,从而影响人体正常新陈代谢、产生疾病[13]。因此,藤茶作为一种营养价值较高的药用原料,具有很高的开发利用价值。

