腹腔镜超声引导下肝肿瘤消融术的模型及进针设计
张 寅,赵玲玲,吴 贤,王 奕,苏卫民,谢炳銮
(1.浙江中医药大学附属温州中医院普通外科,浙江 温州,325000;2.上海交通大学医学院附属同仁医院肝胆外科)
对于小肝癌,消融可达到与手术切除相似的效果,但安全性更高[1-3]。消融有经皮、开腹、腹腔镜3种方式。腹腔镜超声(laparoscopic ultrasound,LUS)引导下肝脏肿瘤消融术与经皮超声引导具有相似的适应证[4]。LUS引导消融治疗原发性肝癌具有较多优势,尤其在排除遗漏病灶、提高特殊部位肝癌的完全消融率等方面优势明显[5]。经LUS引导,微波针可精确、安全地放置于大血管周围,针对血管周边长径<4 cm的肿瘤,可极大地发挥腹腔镜的优势[6-9]。但LUS下消融是在腹腔镜与LUS的联合视角下进行的,需要一定的三维观念来规划穿刺路径。本文主要探讨LUS下肝肿瘤消融的进针方法及消融的3D模型。
1 资料与方法
1.1 临床资料 回顾分析2019年11月至2021年8月为24例肝肿瘤患者行LUS引导下微波消融术的临床资料,术前取得患者及家属的知情同意及医院伦理学委员会的批准。24例患者中男19例,女5例,32~72岁;Child A级21例、B级3例;其中慢性乙型肝炎16例,肝硬化10例;5例有腹部手术史;肿瘤(多发则为主瘤)直径0.9~4.2 cm。患者均无肝外转移、门静脉或其他大血管癌栓。
1.2 手术方法 全麻下行LUS引导微波消融术。全身麻醉,腹腔镜下先分离腹腔粘连,检查有无腹腔内转移,根据需要离断相应肝周韧带,扫描肝脏,确定肿瘤位置及有无新发肿瘤,使用全氟丁烷微球超声造影剂,予以保护肿瘤周围脏器,肿块穿刺活检,然后在LUS引导下多角度消融,一般使用1根微波针3~4个角度消融,肿瘤直径达到3 cm时,我们采用双针多角度消融,注意针道消融。灶区降温后,再次超声造影观察有无残留。
1.3 观察指标 记录术前及术后第2天的生化、血常规结果,记录消融前病灶,术后1个月复查MRI了解消融效果。
1.4 统计学处理 采用SPSS 22.0软件进行数据分析,计量资料符合正态分布者以均数±标准差表示,采用配对t检验;不符合正态分布者用M(P25,P75)表示,采用配对秩和检验。
2 结 果
本组24例消融病例,共30个病灶,无中转开腹,1例术中同时行腹腔镜胆囊切除术。术中出血少,均无术中输血。术后均未见明显出血、黄疸、肠道损伤、腹壁灼伤、膈顶损伤等。术后1个月复查增强MRI,23例患者的肝肿瘤达到完全消融,1例门脉右前支与右后支分叉处肿瘤不完全消融,加以介入栓塞治疗,效果满意。术前仅部分患者甲胎蛋白、癌胚抗原升高,随访过程中继续监测。白细胞、血生化丙氨酸转氨酶较术前升高,差异有统计学意义(P<0.05);见表1。术后2周内肝功能各指标恢复正常。
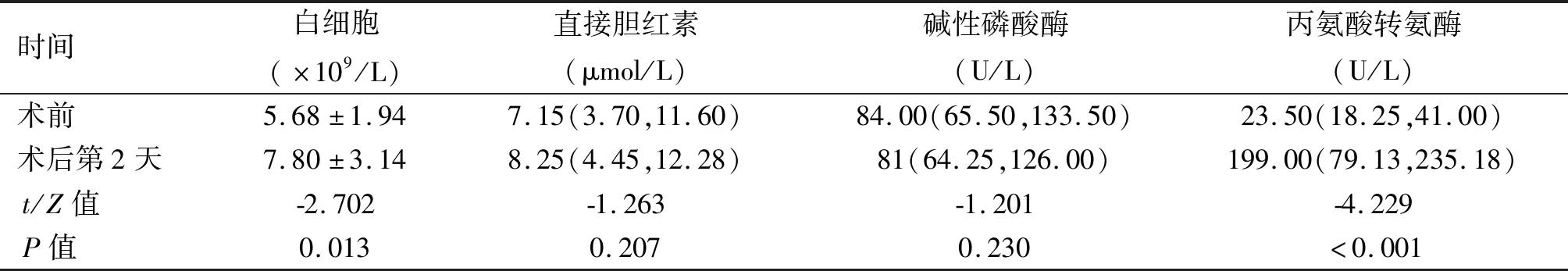
表1 手术前后患者化验指标的变化情况
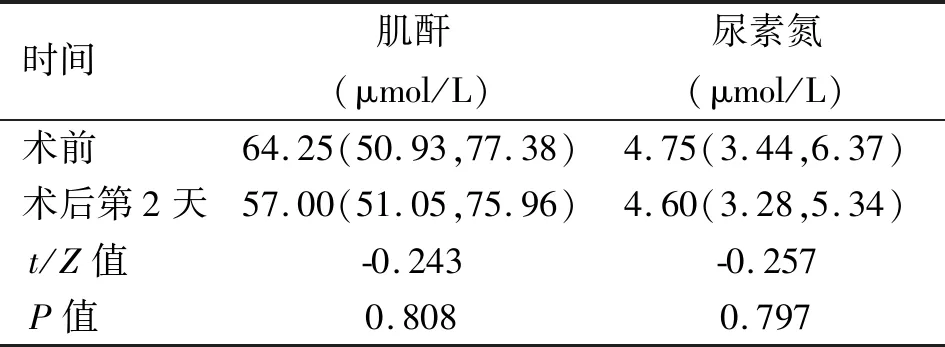
续表1
3 讨 论
3.1 LUS下消融的安全性及治疗效果 LUS引导下微波消融治疗肝癌较手术切除、经皮消融具有优越性[10-11],其优点包括微创、直观,对组织深度、层次、结构性质敏感,可防止腹壁的热灼伤等,且患者满意度、接受度均较高,依从性好。本研究为24例肝肿瘤患者行LUS引导下微波消融术,术后均未见明显出血、黄疸、肠道损伤、腹壁灼伤、膈顶损伤等表现,消融率达95.8%(23/24),疗效肯定。消融治疗本身可重复性强,可分次治疗,提高了安全性,亦可与其他治疗方式,如肝动脉化疗栓塞等联合应用,治疗效果更佳[12-13],本研究中1例血管旁肿瘤消融后予以动脉栓塞达到根治效果。
3.2 LUS下消融进针方法及消融效果 LUS引导肝肿瘤消融不但需要外科医生具有较好的三维解剖、立体视觉,同时应掌握熟练的超声操作技巧及判识读片能力,对术者综合要求较高[4]。本文重点讨论LUS引导消融术中Trocar位置选择、多角度穿刺消融的问题。
3.2.1 Trocar位置的选择 《腹腔镜超声在肝脏外科的应用专家共识》[4]中建议,根据肝脏肿瘤位置选择LUS进入腹腔的Trocar位置及进针点,并可利用肝脏影像三维重建软件规划LUS位置及进针点(图1a~图1c)。我科采用3孔法施术,进镜与进LUS的Trocar位置较固定(图1d),不随肿瘤位置做大的变化。LUS的Trocar位置,我们基本选在剑突下方,只要LUS的Trocar不影响腹腔镜对LUS探头及消融针的观察即可。因此,对S4段肝肿瘤,LUS的Trocar可能遮挡腹腔镜的观察视野,左右略移动Trocar即可。
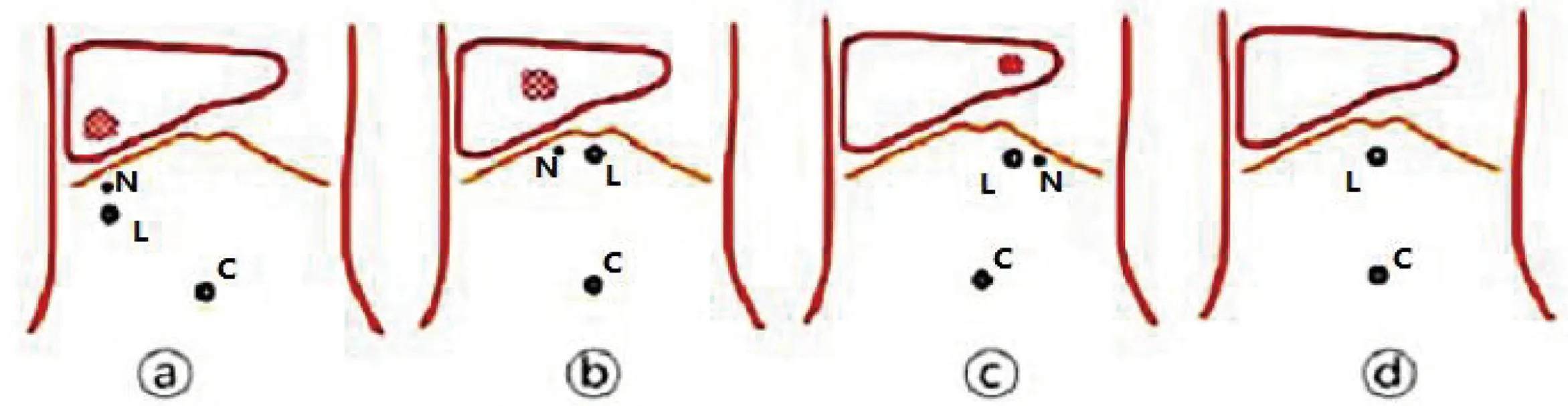
图1 ⓐⓑⓒ:2017专家共识[4]中建议的Trocar布局;ⓓ:笔者采用的Trocar布局[C:进镜Trocar;L:进LUS的Trocar;N:消融针进针点;图片源自腹腔镜超声在肝脏外科的应用专家共识(2017)[4]]
3.2.2 多角度穿刺、消融 经皮超声消融时,消融针可全针道显示在超声扫描平面上,但目前的LUS引导下消融基本不能实现全针道显示。
3.2.2.1 先找针、再找针尖 LUS下消融找针时需要注意3方面:(1)进针方向:LUS下消融针是在LUS探头的侧方进针,同2017指南[4]一样,建议穿刺方向与超声扫描方向的夹角尽量小一点(图2∠AOB、∠AOC)。如图2所示,BO方向进针,∠AOB角度较小,消融针在肝内的距离短;CO方向进针,∠AOC角度大,消融针在肝内进针距离较长(图3的白色线条)。消融针在肝内的针道越长,越难把控,找针难度大,进针不满意时调整穿刺点后再找针的难度也高。(2)消融针在LUS下显示为一个点或一小段(图3),但见到消融针后必须探查到针尖才可以消融,可通过轴向转动(图3)或平移探头(图4)进行观察,再参考消融针入肝距离,确定针尖所在。如图4(2B)所示,消融针与肿瘤很近,但不可执行消融,因为针尖距肿瘤较远。(3)LUS扫描平面,与探头、肝脏的接触面垂直向下不是同一概念,如图3所示,探头位置不变,但探头轴线转动后,探头的扫描平面逐渐在变化。

图2 不同角度下进针(当前超声扫描平面向下。L:腹腔镜探头;A:探头的扫描面;B、C:消融针,白色线为消融针在肝内的针道;O:B、C 2根消融针与A平面的交点)
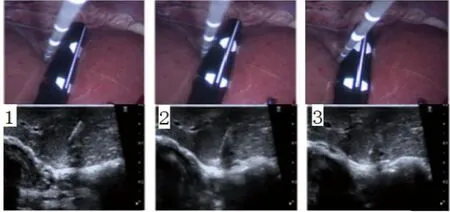
图3 LUS探头逆时针轴线转动及对应的超声影像
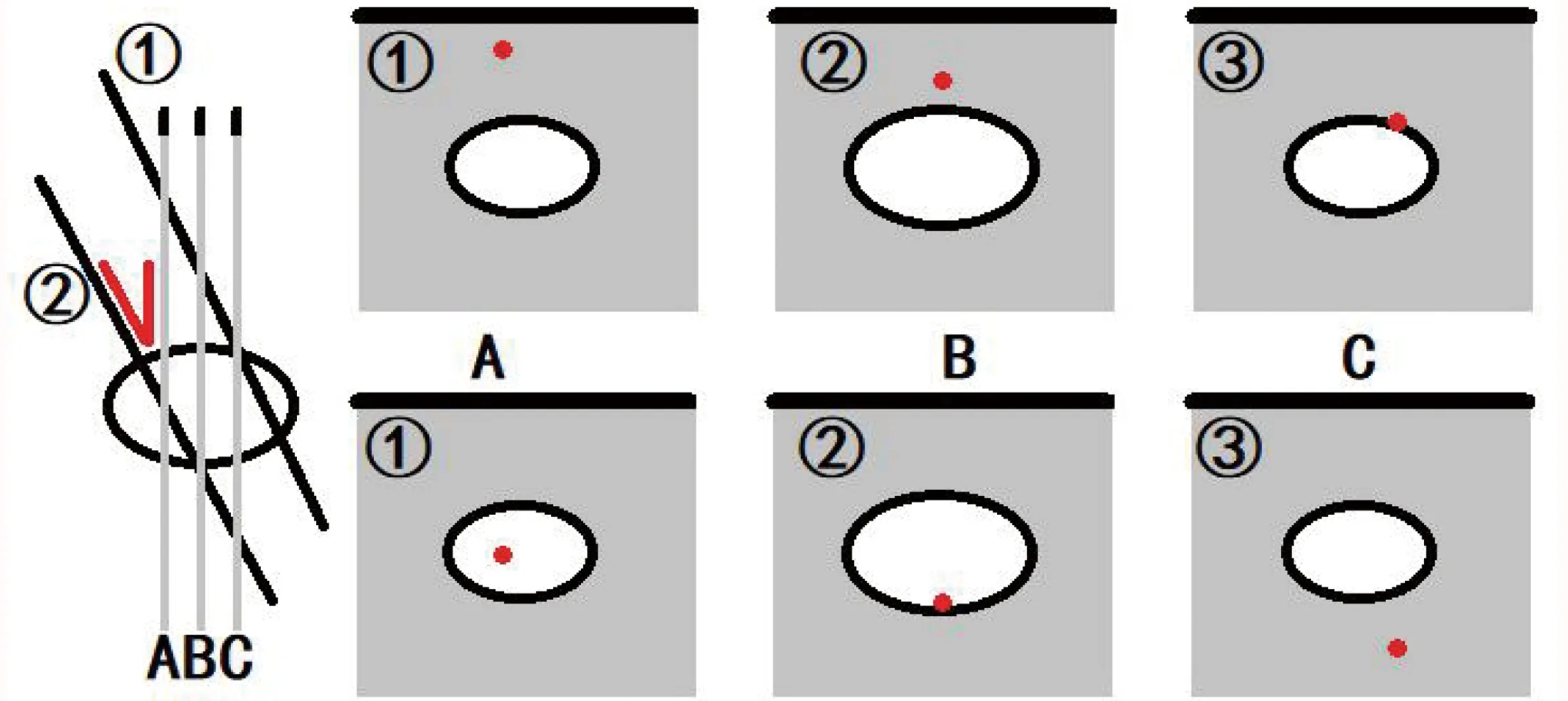
图4 LUS侧面进针在不同超声扫面平面ABC上的结果(见到针在肿块内,针尖可能已穿过肿块,不可盲目消融;①②:消融针;红点:超声下消融针显示)
总之,超声下找到消融针、针尖,即完成了消融的重要一步,然后根据肿块位置、发现的消融针位置进行微调,即能得到满意的消融位点。LUS下穿刺需要一定的学习曲线。在肝内穿刺路径越长,难度越高,需要较高的三维空间思维来规划皮肤、肝脏穿刺点,还需要注意针道消融。
3.2.2.2 消融针穿刺设计 如图5所示,经皮超声下消融时,针道均显示在超声图像上,因为消融针在超声的扫描屏幕内(图5-2);而LUS下消融,消融针由超声探头的侧面进针,因此超声下只看到一个点(图5-4、5、6)。假设:(1)消融范围为直径3 cm的球形;(2)经皮超声下与LUS下消融具有相同的超声探头侧面观角度(图5,∠1=∠2);(3)经皮超声下消融与LUS下消融具有相同的消融针针尖位置(O点),我们就可得到一个三维模型,用以计算各角度观察时消融球的中心位置(图6-1、2)。如图6所示,我们将长方体沿2条对角棱切开(图6-1),得到一个直角的楔形体(图6-2),其中OA=OB=3 cm,OA代表经皮超声下消融针,OB代表LUS下的消融针,OA、OB代表两个消融范围的直径;楔形体正面同超声扫描平面,棱OA°与超声探头长轴平行。然后我们可计算出由超声探头侧面、上方、后方观察时的消融中心点位置。

图6 经皮超声与LUS消融模型(OA、OB:消融有效范 围的最大径,OA=OB=3 cm)
如图7-1所示,在探头侧面观察时,OA、OB投影在楔形体的正面,且投影在同一棱OA上。OB的投影为OB°,因此OA较OB°长。侧面观察,OA消融球的中心点在OA连线的中点,OB消融球的中心点在OB°连线的中点,均有相同的O点,因此侧面观察时,OB消融球的中心点较OA消融球的中心点更靠近O的位置。结论:在上述假设条件下,由超声探头侧面观察时,LUS下消融范围的中心点距针尖(O点)较经皮超声消融近,因此图5-4的消融范围是正确的。
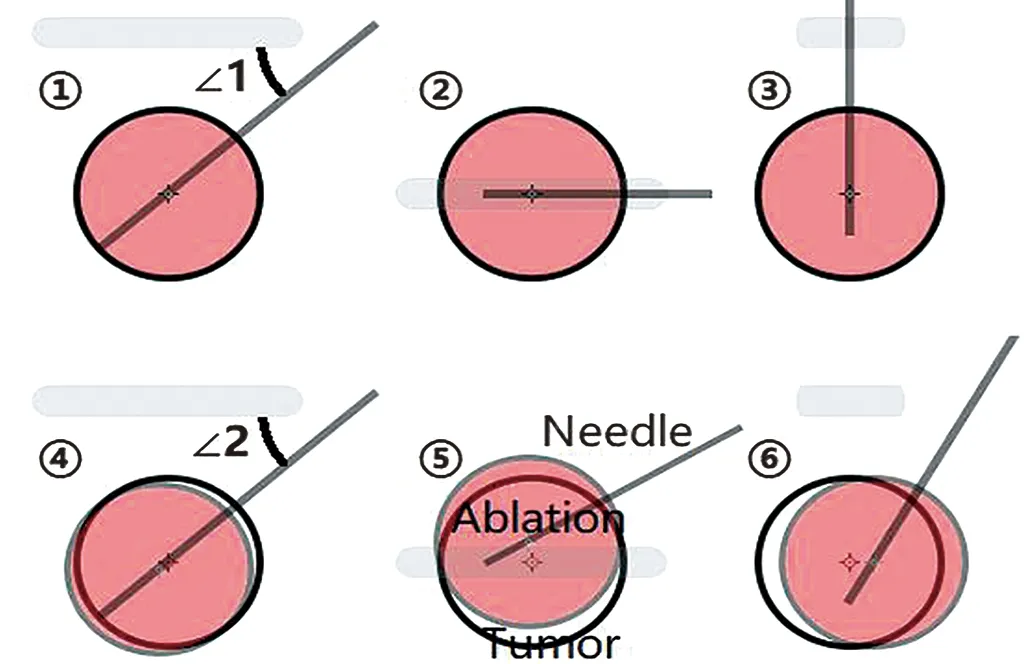
图5 1~3:经皮超声消融,侧面、上方、后方观察;4~6: LUS下消融,侧方、上方、后方观察(肿瘤直径3 cm; 粉红色部分为消融有效范围;∠1=∠2)
如图7-2所示,在探头上方观察时,OA、OB投影在楔形体的下面;而且是在OA°棱上。OA的投影为OA°,OB的投影为OC。根据勾股定理,直角三角形△OAA°、△OBC中,OA=OB,AA°>BC,因此OC>OA°。结论:在假设条件下,由超声探头上方观察时,LUS下消融范围的中心点距针尖(O点)较经皮消融远。进一步研究,我们可利用直角三角的勾股定理计算OC在OA°的投影长度及在OA°这个棱的消融范围。

图7 ①:LUS下从探头的侧面观察消融最大径;②:LUS 下由探头上方观察时消融最大径。
如图8所示,在探头后面观察时,OA、OB投影在楔形体的右侧面。OA的投影为AA°,OB的投影为A°D。根据勾股定理同样可以得出A°D>AA°。结论:在假设条件下,由超声探头后面观察时,LUS下消融范围的中心点距针尖(A°点)较经皮消融远。
通过图5~图8,我们可以直观地了解到同一针尖位置,经皮超声与LUS下的不同消融结果,也可通过三角函数估计出被LUS探头扫描到的消融针进针距离。通过图5-4、6的LUS下侧面观察沿肿瘤中心方向进针,我们可见肿块底部未能消融,而因为消融后局部气化的超声图像的影响,我们很难对此超声位置下的肿块底部正中进行消融。因此,我们推荐,先将超声探头放到肿瘤最大径,在扫描面最底部先消融(图9)。然后消融针前移1.5 cm或在最远处消融(图10)。结合图9、图10我们发现超声探头的进针侧基本完全消融,仅在探头侧面观察时探头的前下方局部未消融(图11),这时我们将超声探头向远离进针侧方向移动1.5 cm后,重复上述步骤。

图8 LUS下由探头后方观察时消融最大径
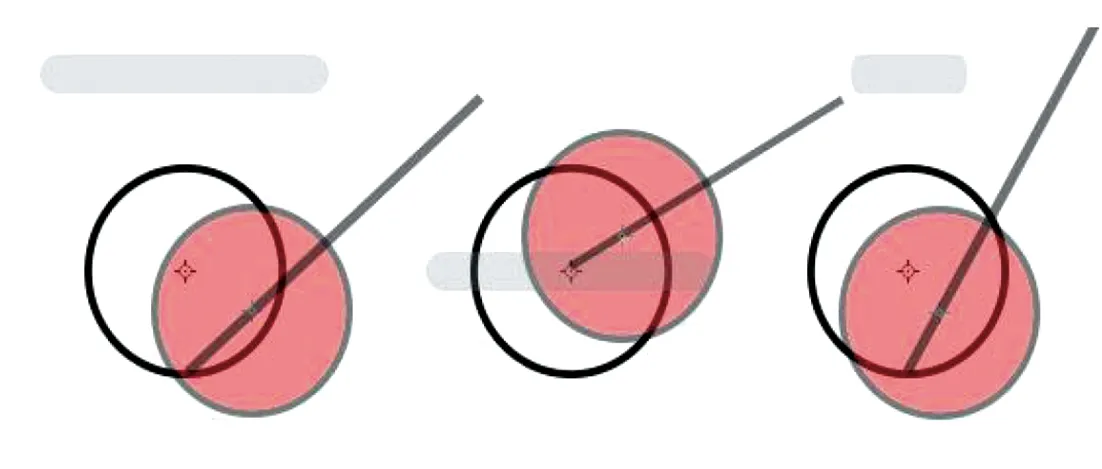
图9 第1针(由侧面、上方、后方观察:进针侧前上方、外侧未消融)
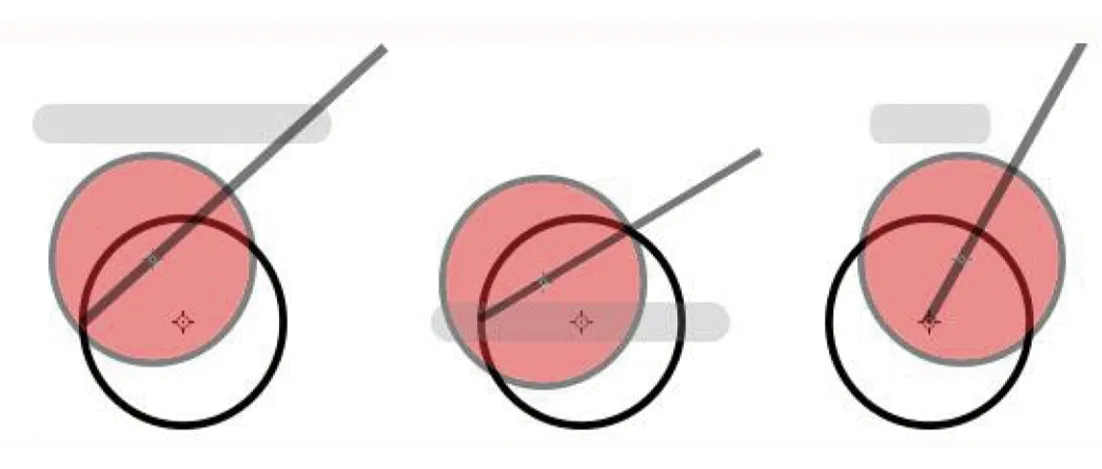
图10 第2针(由侧面、上方、后方观察)
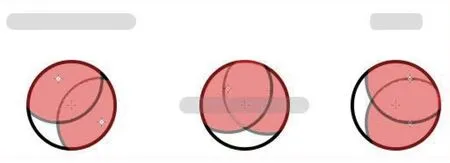
图11 第1、2针后的消融范围(侧面、上方、后方观察)
对于直径>3 cm的肝癌,建议同侧双针进行消融(图12),间距建议1.5 cm。
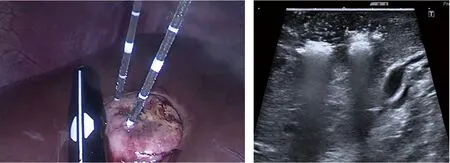
图12 腹腔镜膈面肝肿瘤消融及LUS图
总之,LUS引导下肝肿瘤消融是安全、有效的。但腹腔镜及LUS下的侧面进针,需要良好的三维概念,需要经过一定的学习曲线再开展此技术。随着穿刺经验的积累,可明显缩短手术时间,提高消融效率,灭活效果显著[14-15]。但应严格把握手术指征,注意患者能否耐受全麻手术及腹腔粘连情况,如有自发性腹膜炎病史、腹腔灌注化疗病史,应加强手术的安全、保证消融的完全彻底。本模型对于单一位点的消融范围解释的比较透彻,但对多针消融时的重叠范围还需要计算机技术的支持与完善。

