布地奈德直肠用脂质体温敏凝胶制备工艺的研究
杨东亮,马瑞丽,赵宇郁,滕亮,马桂芝*,高晓黎(. 新疆医科大学第一附属医院药学部,乌鲁木齐80054;. 新疆医科大学 药学院,乌鲁木齐 800;. 庆阳市中医医院药剂科,甘肃 庆阳 745099)
溃疡性结肠炎(UC)是结直肠的一种慢性免疫介导的炎症性疾病[1],病因尚不明确,且暂无法治愈,如果不及时治疗,可导致黏膜损伤及结直肠癌等致命并发症[2]。在全球范围内,UC 的发病率呈上升趋势[3],近二十余年来,我国UC的就诊人数快速增长[4]。UC 一般均以连续性分布的方式,从直肠向近端结肠扩展,在中国病变的主要部位为直肠、直-乙状结肠、左侧结肠。糖皮质激素是活动期UC 诱导缓解治疗的重要药物,临床常口服或静脉给予糖皮质激素,但全身用药易出现药物不良反应并存在诸多限制,且局部药物浓度低[5]。布地奈德(budesonide,Bud)是第二代皮质类固醇类激素,具有局部抗炎作用强,全身不良反应少的优点,可有效缓解轻中度UC 患者的症状[6]。
目前,临床常使用吸入用Bud 混悬剂灌肠[7],但混悬剂几乎没有生物黏附性,在肠道保留时间短,且几乎不溶于水、局部吸收差,影响疗效。故本研究利用脂质体的特性增加药物溶解度、提高黏膜滞留性能、升高靶部位浓度、减少药物入血[8];同时,利用温敏凝胶常温下为液态、体温下为凝胶的特点,促进药物的均匀分布、提高局部黏附性能,以对抗肠道的自蠕动[9-10]。本研究将Bud 制备成脂质体后再进一步制成脂质体温敏凝胶,使其兼顾脂质体和温敏凝胶的优势:给药前为液体状态,到达给药部位后均匀分布,后迅速相变为凝胶黏附于肠黏膜,进一步通过脂质体实现靶向作用,提高疗效,降低不良反应。
1 仪器与试药
1.1 仪器
LC-20AD 高效液相色谱仪(日本岛津公司);New Classic MS 分析天平(梅特勒-托利多公司,d =0.01 mg);KQ5200DE 型数控超声波清洗器(昆山市超声仪器有限公司);Zetasizer Nano ZS 纳米激光粒径测定仪(英国马尔文仪器有限公司);PS-1000 磁力搅拌器(东京理化器械株式会社);3-18KS 台式高速冷冻离心机(SIGMA公司);VCX500 超声波细胞破碎仪(Sonics &Materials Inc);TP-6 智能透皮试验仪(天津市鑫洲科技有限公司);PHSJ-3F 雷磁pH 计(上海仪电科学仪器有限公司);NDJ-5S 数字式黏度计(上海菁海仪器有限公司);Milli-Q 艾柯超纯水仪(美国密理博公司)。
1.2 试药
Bud 对照品(上海源叶生物科技有限公司,批号:Y13J7C9082,纯度≥ 98%);Bud 原料药(山东泰华生物科技有限公司,批号:20190906,纯度≥ 99%);大豆磷脂(批号:SYSO-200401)、胆固醇(批号:B80859)(上海艾伟拓医药科技有限公司);泊洛沙姆407、泊洛沙姆188(北京索莱宝科技有限公司);羟丙基甲基纤维素(上海麦克林生化科技有限公司);醋酸纤维素膜(孔径:0.45 µm,尺寸:50 mm)(上海市新亚净化器件厂);甲醇为色谱纯,水为超纯水,其他试剂均为分析纯。
2 方法与结果
2.1 Bud 的含量测定
2.1.1 色谱条件 色谱柱为Agilent SB-C18(250 mm×4.6 mm,5 μm),以甲醇-水(72∶28)为流动相等度洗脱,检测波长260 nm,进样量10µL,流速1 mL·min-1,柱温25℃。
2.1.2 溶液的配制 取Bud 对照品适量,精密称定,置25 mL 量瓶中,加甲醇超声溶解并定容,即得质量浓度为196.4 µg·mL-1的对照品储备液。精密移取对照品储备液适量,用甲醇依次稀释为0.38、0.77、1.53、3.07、6.14、12.28、24.55、49.1、98.2 µg·mL-1的系列对照品溶液。
分别取Bud 对照品溶液、Bud 脂质体、Bud脂质体温敏凝胶1.0 mL,甲醇定容,超声,以0.22 µm 微孔滤膜滤过,取续滤液,即得供试品溶液。
制备不含Bud 的空白脂质体、空白脂质体温敏凝胶,各取1.0 mL,甲醇定容,超声,以0.22 µm微孔滤膜滤过,取续滤液,即得阴性样品溶液。
2.1.3 专属性考察 取Bud 对照品、供试品及阴性样品溶液各10 μL,进样分析,记录色谱图,结果见图1,基质对Bud 测定无干扰[11]。

图1 Bud 脂质体及Bud 脂质体温敏凝胶的HPLC 图Fig 1 HPLC chromatogram of Bud liposomes and Bud liposome temperature sensitive gel
2.1.4 线性关系考察 测定系列对照品溶液,以峰面积(Y)对Bud 质量浓度(X)进行线性回归,得回归方程Y=1.59×104X+1.993×103(r=0.9999)。结果表明,Bud 在0.38 ~98.2 µg·mL-1与峰面积线性关系良好。
2.1.5 方法学考察 取供试品溶液连续测定6 次,测得精密度RSD为0.30%。于常温下供试品分别放置0、2、4、6、8、10、12 h,测得稳定性RSD为1.1%。平行制备6 份供试品溶液,测得重复性RSD为1.7%。精密量取已知浓度样品9 份,加低、中、高浓度对照品溶液,测得平均加样回收率在98.7%~100.2%,RSD均<2.0%。
2.2 Bud 脂质体的制备
2.2.1 制备工艺优选指标 以包封率、载药量和粒径作为考察指标,综合分析。结合层次分析法确定的权重系数,得到综合评分Y=包封率/包封率最大值×0.7306+载药量/载药量最大值×0.1884+粒径最小值/粒径×0.0810[11]。
2.2.2 Bud 脂质体的制备工艺 根据Bud 性质,采用逆向蒸发法制备Bud 脂质体。精密称取Bud原料药、胆固醇和大豆磷脂适量于250 mL 圆底烧瓶中,加入20 mL 氯仿超声使其溶解,再按有机相与水相的体积比加入超纯水,水浴超声10 min形成稳定的W/O型乳液,40℃下减压蒸发除去有机溶剂,加入超纯水,继续旋转蒸发,于冰浴条件下超声,即得Bud 脂质体,于3 ~5℃保存[12]。
2.2.3 Bud 脂质体制备工艺单因素的考察 测定各脂质体包封率、载药量和粒径,以综合评分Y为指标,按“2.2.2”项下方法考察膜材比(3∶1、6∶1、9∶1、12∶1 和15∶1)、脂药比(2∶1、6∶1、10∶1、14∶1 和18∶1)、有机相与水相比例(V有机/V水相为2∶1、3∶1、4∶1、5∶1 和6∶1)、乳化时间(6、8、10、12 和14 min)、孵育温度(20、30、40、50 和60℃)、分散时间(10、15、20、25和30 s)等因素对Bud 脂质体综合指标的影响。结果,在膜材比为9∶1、脂药比为6∶1、V有机/V水相为4∶1、乳化时间12 min、孵育温度50 ℃、分散时间15 s 时,所制脂质体包封率较高。
2.2.4 星点设计-效应面法优化制备工艺 在单因素试验的基础上,选取脂药比和V有机/V水相两个对指标影响较大的因素,设计二因素三水平的星点设计-效应面法优化Bud 脂质体制备工艺。因素水平见表1,以综合评分Y为考察指标,按照星点设计-响应面法设计进行试验见表2、图2,方差分析结果见表3。

表3 方差分析Tab 3 Analysis of variance
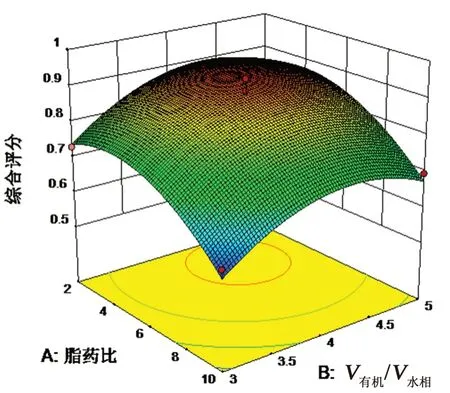
图2 Bud 脂质体制备工艺优化的效应面图Fig 2 Response surface for optimization of preparation process of budesonide liposomes

表1 星点设计-效应面法的因素水平表Tab 1 Factor and level of central composite design-response surface method
采用Design-Expert 10.0.7 软件对表2数据进行拟合,得到综合评分Y的回归方程为Y=0.8897 - 0.0854A+ 0.0527B- 5.9275AB-0.0874A2-0.0902B2,模型P<0.01,与数据的拟合度好,误差低,可用于进一步分析与检测。通过Design-Expert 10.0.7 软件对优选的制备工艺条件进行预测,A=4.5∶1,B=4.0∶1,Y的预测值为0.92。应用Design-Expert 10.0.7 软件对优选的制备工艺条件进行预测,A=4.5∶1,B=4.0∶1,Y的预测值为0.92。结合实际操作条件,初步确定优选工艺参数为:脂药比4.5∶1,V有机/V水相=4.0∶1,按照优选参数,采用逆向蒸发法制备3 批Bud 脂质体。结果表明,3 批样本的包封率为(82.15±0.34)%、载药量为(12.71±0.34)%、粒径为(273.8±3.4)nm、Y为(0.95±0.01),说明工艺稳定可行,重现性好。

表2 星点设计-效应面法的结果Tab 2 Central composite design-response surface method
2.3 Bud 脂质体温敏凝胶的制备
采用冷溶法制备Bud 脂质体温敏凝胶。精密称取泊洛沙姆407(P407)、泊洛沙姆188(P188)和羟丙基甲基纤维素(HPMC)适量,在磁力搅拌下缓慢加入到一定量的脂质体中,搅拌均匀后,于4 ℃下静置溶胀24 h,即得。
2.4 Bud 脂质体温敏凝胶工艺优选指标
2.4.1 胶凝温度 采用试管倒置法[13]测定胶凝温度。试管中加2 mL 凝胶溶液,插入温度计,置恒温水浴锅中,从25 ℃开始缓慢升温,每隔0.2 ℃将试管倾斜180°以观察溶液的流动情况。溶液不流动时的最低温度即为胶凝温度,重复3次取平均值。
2.4.2 累积释放度的测定 采用Franz 扩散池对药物的累积释放度进行测定[14]。供给池和接收池间以半透膜隔离。向接收池中加入恒温至37.5℃的磷酸盐缓冲液(PBS,pH 7.4)释放介质,将Franz 扩散池置于37.5℃恒温水浴磁力搅拌器中。取Bud 脂质体温敏凝胶1.0 mL,加入到供给池中,放置10 min,待凝胶胶凝后开始搅拌。分别于0.5、1、2、4、6、8、10、12 h 各取样0.4 mL,同时补充恒温介质0.4 mL。按“2.1.1”项下方法测定Bud含量。
2.4.3 评价指标——综合评分法 以胶凝温度(Y1)和累积释放度(Y2)的综合评分(Y)为评价指标[15],其中:
Y1=胶凝温度/32 ℃,Y1评分实行分段评分,即:当Y1≥1时,Y1评分=1/Y1×80;当Y1<1 时,Y1评分=Y1×80;
Y2=∣Q2h-20%∣+∣Q6h-50%∣+∣Q12h-80%∣,Y2评分=Y2min/Y2×20;
Y=Y1评分+Y2评分。Y值越大指标越好。其中,Q2h、Q6h、Q8h分别为2 h、6 h、8 h 后的累积释放度;Y2min为Y2最小值。
2.5 单因素对处方用量的考察
2.5.1 P407 用量的考察 固定处方中其他用量,分别加入14%、16%、18%、20%、22%、24%的P407 制备Bud 脂质体温敏凝胶,测定胶凝温度分别为38.8、36.2、33.5、31.0、30.0、29.0℃。表明随着P407 用量的增加,胶凝温度逐渐降低,当P407 的用量小于16%时,温敏凝胶在37℃仍未发生胶凝。
2.5.2 P188 用量的考察 固定处方中其他用量,分别加入1%、2%、3%、4%、5%、6%的P188制备Bud 脂质体温敏凝胶,测定胶凝温度分别为28.9、30.8、33.5、35.5、37.2、39.0℃。表明随着P188 用量的增加,胶凝温度逐渐增大,当P188 的用量大于5%时,温敏凝胶在37.5℃仍未发生胶凝。
2.5.3 HPMC 用量的考察 固定处方中其他用量,分别加入0.2%、0.4%、0.6%、0.8%、1%的HPMC 制备Bud 脂质体温敏凝胶,测定胶凝温度分别为34.3、34.0、33.8、33.6、33.5℃。表明随着HPMC 用量的增加,胶凝温度逐渐减小,但减小的趋势不显著。
2.6 正交试验优选温敏凝胶的处方组成
根据单因素试验,确定各因素的水平,以“2.4.3”项下Y为综合评价指标,进行L16(45)正交试验,因素水平见表4,正交试验结果见表5,方差分析见表6。

表4 正交试验设计的因素水平(%)Tab 4 Factor and level of orthogonal test (%)
由表5及表6中可知,处方中各因素对Bud脂质体温敏凝胶质量的影响程度依次为AB >A >C >B,优选水平组合为A3B3C1,即优选处方为P407 用量20%、P188 用量4%、HPMC 用量0.4%。

表5 正交试验设计与结果Tab 5 Orthogonal test

表6 方差分析Tab 6 Variance analysis
2.7 最佳工艺的验证
按优化的最佳工艺条件平行制备3 批样品,平均胶凝温度为(33.1±0.1)℃;平均体外累积释放度Q2h(13.6±0.2)%、Q6h(41.6±0.4)%、Q12h(72.6±1.1)%;平均综合评分(90.12±0.43);分别用超纯水将3 批样本稀释10 倍,置于NDJ-5S数字式粘度计样品池中,通过Zetasizer Nano ZS纳米激光粒径测定仪对其粒径和Zeta 电位进行测定,每个样平行测3 次。分别用超纯水将3 批样本稀释10 倍,置于NDJ-5S 数字式粘度计样品池中,通过Zetasizer Nano ZS 纳米激光粒径测定仪对其粒径和Zeta 电位进行测定,每个样平行测3次。平均粒径为(285.2±6.7)nm,平均Zeta 电位为-(45.8±5.3)mV,分布见图3。制备的脂质体的平均粒经和平均Zeta 电位分别为(273.8±3.4)nm 和-(31.9±2.16)mV,可知制成脂质体温敏凝胶后粒径和Zeta 电位绝对值有增大的趋势,但影响不明显。经验证该Bud 脂质体温敏凝胶在体温条件下能迅速胶凝,且累积释药性能良好。

图3 Bud 脂质体温敏凝胶的粒径(A)和 Zeta 电位分布(B)Fig 3 Particle size(A)and Zeta potential distribution(B)of Bud liposome temperature sensitive gel
2.8 稳定性初步考察
按最佳处方工艺制备Bud 脂质体温敏凝胶,置密闭西林瓶中,于4℃冰箱避光保存,分别于第0、15、30、45、60日取样,观察外观性状,测定胶凝温度及药物含量。结果表明在考察的时间范围内,Bud 脂质体温敏凝胶外观、胶凝温度、含量、粒径和Zeta 电位无明显变化,可满足后续药效学和药动学的研究要求。
3 讨论
Bud 为亲脂性药物,几乎不溶于水,难以有效分散于水溶性凝胶中,故将其包裹于脂质体,以有效分散于温敏凝胶中,从而发挥缓释、局部靶向作用[16]。Bud 脂质体温敏凝胶,在常温下为自由流动的液体,在灌肠后可快速均匀分布于降结肠、乙状结肠、直肠,后在体温调节下迅速胶凝,黏度升高以对抗肠道自蠕动。另外,脂质体还可提高局部黏膜的滞留量,减少全身作用[8]。包封率、载药量、粒径、分散指数、电位等均为评价脂质体制备工艺的指标,一方面指标过多容易导致试验难度增加;另一方面,预试验中各考察因素对分散指数和电位并无显著影响,故选择包封率、载药量和粒径为指标,采用加权后综合评分进行全面评价,不仅能全面反映各检测指标对脂质体的重要程度,也能直观反映整体制备工艺[11]。
胶凝温度是温敏凝胶的一个重要指标,温敏凝胶灌肠后,若在病灶部位短时间内不能相变,会因肠道自蠕动作用而漏出,且凝胶所载药物会发生突释,降低制剂的缓释作用,因此选择胶凝温度在30 ~34℃为宜[16]。为保证该直肠给药系统在室温下为液态,便于给药和分布,进入直肠后迅速的胶凝,本研究以32℃为胶凝温度的参考温度[17]。然而,制剂质量的好坏不只取决于胶凝温度,还与合适温度下药物能否充分释放有关。故本研究在单因素筛选出各基质的合理范围后,继以胶凝温度和累积释放度的综合评分为指标,使优选出的Bud 脂质体温敏凝胶在生理温度下迅速胶凝,发挥良好的释药作用。
在筛选处方时,P407 的质量分数影响最为显著,这与P407 在处方中的作用与贡献是一致的。泊洛沙姆分子是排列整齐的Z 字形结构。当温度升高时,Z 字形结构可能转变为缠绕紧密的折叠结构,而且缠绕越来越紧密,形成更黏稠的凝胶[18]。P407 是由聚氧乙烯(PEO)、聚氧丙烯(PPO)组成的PEO-PPO-PEO 非离子型三嵌段共聚物,其中PEO 与PPO 的质量比为7∶3。加入P188 后,相对增加了PEO 的比例而降低了PPO的比例,升高了体系的胶凝温度。但P188 的用量过大时,本身已胶束化的P188 分子亦可参与凝胶构成,又导致体系胶凝温度降低。因此要调节P407 的胶凝温度需选择P188 合适的用量[19]。本研究还发现P407 与P188 存在较为显著的交互作用,其对指标的影响甚至大于P407 与P188 各自的影响。
虽然本研究对该直肠定向给药制剂进行了初步研究,但对于其生物有效性、安全性尚待进一步研究,以期为UC 患者提供可靠的药物制剂。