中医辨证用药联合针灸、耳穴压豆治疗睡眠呼吸暂停综合征的效果分析
莫寒茹
(广州市中西医结合医院呼吸内科,广东广州 510800)
睡眠呼吸暂停综合征(obstructive sleep apnea syndrome,OSAHS)是一种睡眠障碍性疾病,表现为打鼾、呼吸表浅或呼吸暂停等症状[1]。研究显示,本病患者睡眠状态下氧通气不足,机体氧化与抗氧化系统失衡、诱发氧化应激反应和全身炎症反应,对全身组织系统造成危害,甚至引发低氧血症、高碳酸血症等,严重者可能导致死亡[2]。目前,临床将本病全身、低度、慢性、非感染性的炎症反应伴随细胞因子分泌异常作为研究的重点,西医治疗主要以持续气道正压通气(CPAP)及手术治疗为主,但CPAP存在价格昂贵、复位率高的问题,且大多数患者手术意愿较低,导致西医疗效不能令人满意[3]。中医认为,本病与痰湿内阻密切相关,责之于脾、肺两脏,痰湿内生,阻滞气机升降,痰气上扰清窍,脑髓失养,发为嗜睡、健忘等症状,而痰湿阻滞肺道、鼻咽,则呼吸受限,引发打鼾时停时止症状[4]。中医通过辨证用药、针灸、耳穴贴敷等方法,能发挥综合疗效,提高症状缓解效果[5]。本研究进一步分析中医治疗OSAHS的效果,现报道如下。
1 资料与方法
1.1 一般资料 选取2019年10月至2021年12月广州市中西医结合医院收治的60例OSAHS患者为研究对象,按照随机数字表法分为观察组和对照组,各30例。观察组患者中男性22例,女性8例;年龄24~67岁,平均年龄(43.25±10.84)岁;病程6个月~5年,平均病程(2.93±1.16)年。对照组患者中男性23例,女性7例;年龄22~68岁,平均年龄(43.72±11.21)岁;病程6个月~6年,平均病程(3.22±1.43)年。两组患者一般资料比较,差异无统计学意义(P>0.05),组间具有可比性。本研究经广州市中西医结合医院医学伦理委员会批准,患者及其家属均对研究知情并签署知情同意书。纳入标准:①符合《成人阻塞性睡眠呼吸暂停基层诊疗指南(实践版·2018)》[6]中OSAHS的诊断标准;②中医辨证属于鼾证中的痰湿内阻证;③低通气指数(AHI)>5次/h;④年龄20~70岁。排除标准:①合并严重心、肝、肾疾病;②呼吸道占位性病变、先天鼻咽结构异常;③免疫、神经、血液等系统疾病;④精神或认知障碍;⑤治疗依从性差。
1.2 治疗方法 对照组患者使用常规健康指导联合CPAP治疗,设置起始压力4~5 cmH2O(1 cmH2O=0.098 kPa),后根据患者睡眠状况调整参数,维持血氧饱和度>90%,治疗时间≥5 h/d;治疗期间给予患者针对性健康指导,叮嘱患者严禁饮酒、饮茶及咖啡,禁用镇静催眠类药物,侧卧位睡眠,可适当抬高床头,白天避免过度劳累,控制饮食,积极减肥等。在此基础上,观察组患者使用中医方法治疗:①自拟中药方。组方:药用黄芪30 g,苍术15 g,竹茹15 g,浙贝母15 g,厚朴10 g,法半夏10 g,枳实10 g,陈皮10 g,胆南星10 g,石菖蒲10 g,茯苓10 g,威灵仙10 g,炙甘草6 g,大枣6枚,生姜3片。1剂/d,加1 000 mL水煎煮取药汁300 mL,150 mL/次,2次/d,早晚服用。②针灸。选取曲池、丰隆、足三里、太冲、廉泉、天突等穴位,使用一次性针灸针,直刺进针,施以平补平泻法,留针30 min,期间行针1~2次,1次/d,共治疗14 d。③耳穴压豆。选择心、脾、肺、交感、神门、皮质下、三焦、肾上腺、小肠、胃等耳穴,用王不留行籽贴压,每穴按压30 s/次,共3~5 min,两耳交替按压,5次/周,共治疗2周。两组患者均治疗2周后评价疗效。
1.3 观察指标 ①比较两组患者临床疗效。采用多导睡眠监测仪(北京怡和嘉业,型号:YH-2000A型)检测AHI。临床控制:中医证候积分下降>95%,AHI<5次/h,血氧饱和度>90%;显效:70%≤中医证候积分降低≤95%,AHI≤15次/h或减少超过50%,血氧饱和度在85%~90%;有效:30%≤中医证候积分降低<70%,AHI减少20%~50%,血氧饱和度在80%~84%;无效:中医证候积分降低<30%,AHI减少<20%,血氧饱和度<80%,或病情进一步加重[7]。总有效率=(临床控制+显效+有效)例数/总例数×100%。②比较两组患者治疗前后症状指标。采用PSG(美国凯迪泰公司,型号:SW-SM 2000 CB型)检测AHI、微觉醒指数(MAI)、呼吸紊乱时最低氧饱和度(LSaO2)。③比较两组患者血清炎症因子水平。治疗前后检测血清炎症因子,抽取患者外周静脉血3 mL,以3 000 r/min离心10 min,取上清液,采用酶联免疫法检测超敏C反应蛋白(hs-CRP)、白细胞介素-1(IL-1)、白细胞介素-6(IL-6)、肿瘤坏死因子-α(TNF-α)。④比较两组患者治疗前后嗜睡、疲乏、睡眠及生活质量。Epworth嗜睡量表(ESS)[8]、疲乏严重度量表(FSS)[9]评估嗜睡及疲乏程度:前者分为8个项目,每项0~3分,<6分为正常,得分越高嗜睡越严重;后者有9个条目,得分越高,疲劳程度越严重。采用匹茨堡睡眠指数(PSQI)、Calgary睡眠呼吸暂停生活质量指数(SAQLI)[10]评估睡眠及生活质量:前者包含19个自评和5个他评条目,总分0~21分,得分与睡眠质量呈反比;后者总分0~7分,得分与生活质量呈正比。
1.4 统计学分析 采用SPSS 22.0统计学软件进行数据处理。计数资料以[例(%)]表示,组间比较采用χ2检验;计量资料以()表示,组间比较行独立样本t检验,组内比较行配对样本t检验。以P<0.05为差异有统计学意义。
2 结果
2.1 两组患者临床疗效比较 观察组患者治疗有效率明显高于对照组,差异有统计学意义(P<0.05),见表1。

表1 两组患者临床疗效比较 [例(%)]
2.2 两组患者治疗前后症状指标比较 两组患者治疗后AHI、MAI水平均低于治疗前,LSaO2水平高于治疗前,差异有统计学意义(P<0.05),观察组患者治疗后AHI、MAI水平均低于对照组,LSaO2水平高于对照组,差异有统计学意义(P<0.05),见表2。
表2 两组患者治疗前后症状指标比较()

表2 两组患者治疗前后症状指标比较()
注:与同组治疗前比较,*P<0.05。AHI:低通气指数;MAI:微觉醒指数;LSaO2:最低氧饱和度。
组别 例数 AHI(次/h) MAI LSaO2(%)治疗前 治疗后 治疗前 治疗后 治疗前 治疗后观察组 30 39.43±15.28 22.30±10.62* 15.37±3.82 10.23±3.54* 83.37±5.24 91.16±4.78*对照组 30 39.72±15.61 31.68±11.29* 15.90±4.18 13.72±10.43* 82.95±5.46 87.49±5.15*t值 0.303 9.385 0.531 4.493 0.585 4.367 P值 0.794 0.001 0.632 0.001 0.602 0.001
2.3 两组患者治疗前后炎症因子水平比较 两组患者治疗后hs-CRP、IL-1、IL-6、TNF-α水平明显低于治疗前,且观察组低于对照组,差异有统计学意义(P<0.05),见表3。
表3 两组患者治疗前后炎症因子水平比较()

表3 两组患者治疗前后炎症因子水平比较()
注:与同组治疗前比较,*P<0.05。hs-CRP:超敏C反应蛋白;IL-1:白细胞介素-1;IL-6:白细胞介素-6;TNF-α:肿瘤坏死因子-α。
组别 例数 hs-CRP(mg/L) IL-1(pg/L) IL-6(ng/L) TNF-α(ng/L)治疗前 治疗后 治疗前 治疗后 治疗前 治疗后 治疗前 治疗后观察组 30 22.54±2.81 9.02±1.92* 20.67±3.9214.53±3.28* 57.17±5.90 38.23±4.28* 38.97±3.71 27.50±3.18*对照组 30 22.13±2.6914.38±2.34* 20.45±4.0318.15±3.67* 56.84±5.65 44.62±5.19* 39.32±4.14 33.16±4.23*t值 0.414 5.267 0.252 4.362 0.297 6.394 0.352 5.564 P值 0.703 0.001 0.948 0.001 0.934 0.001 0.835 0.001
2.4 两组患者治疗前后嗜睡、疲乏、睡眠及生活质量评分比较 两组患者治疗后ESS评分、FSS评分、PSQI评分明显低于治疗前,SAQLI评分明显高于治疗前,差异有统计学意义(P<0.05),观察组患者治疗后ESS评分、FSS评分、PSQI评分明显低于对照组,SAQLI评分明显高于对照组,差异有统计学意义(P<0.05),见表4。
表4 两组患者治疗前后嗜睡、疲乏、睡眠及生活质量评分比较(分,)
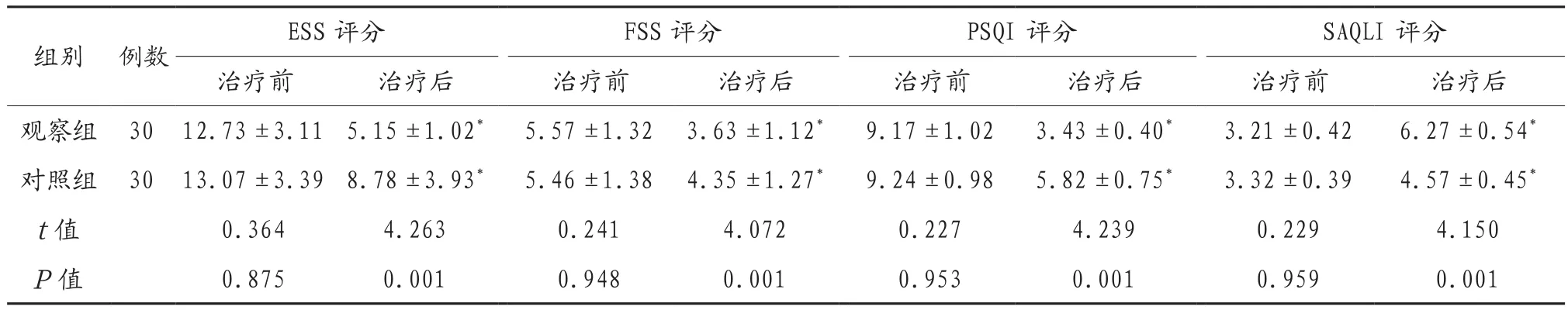
表4 两组患者治疗前后嗜睡、疲乏、睡眠及生活质量评分比较(分,)
注:与同组治疗前比较,*P<0.05。ESS:Epworth嗜睡量表;FSS:疲乏严重度量表;PSQI:匹茨堡睡眠指数;SAQLI:Calgary睡眠呼吸暂停生活质量指数。
组别 例数 ESS评分 FSS评分 PSQI评分 SAQLI评分治疗前 治疗后 治疗前 治疗后 治疗前 治疗后 治疗前 治疗后观察组 30 12.73±3.11 5.15±1.02* 5.57±1.32 3.63±1.12* 9.17±1.02 3.43±0.40* 3.21±0.42 6.27±0.54*对照组 30 13.07±3.39 8.78±3.93* 5.46±1.38 4.35±1.27* 9.24±0.98 5.82±0.75* 3.32±0.39 4.57±0.45*t值 0.364 4.263 0.241 4.072 0.227 4.239 0.229 4.150 P值 0.875 0.001 0.948 0.001 0.953 0.001 0.959 0.001
3 讨论
OSAHS的发病机制复杂,一般认为与气道解剖异常、神经肌肉功能失调等有关,导致睡眠时上气道通路狭窄,氧通气不足,使机体处于间歇性缺氧状态,进而降低睡眠质量,引发白天嗜睡、疲劳等症状,严重者发生血氧饱和度明显下降、低氧血症,甚至诱发心脑血管疾病。本病与年龄有一定相关性,年龄越大,发病风险越高。研究显示,本病患者长期处于缺氧状态,提升血液中碳酸浓度,增加中性粒细胞应激性,提高交感神经兴奋性,诱发机体释放炎症因子和细胞因子,对全身组织器官均有一定损伤,使机体处于慢性、微炎症状态[11]。
CPAP是主要的治疗工具之一,通过持续的正压通气,可升高上气道管内压,扩张上气道,达到解除睡眠时气道阻塞、避免呼吸暂停的目的,具有无创、高效、安全的优点。但CPAP的弊端也很明显,仅可短期使用,较难做到长期治疗[12]。
中医认为,该病的发病与脾、肺两脏密切相关。脾虚则痰湿内生,气机升降失常,使得痰浊上逆犯肺,壅塞肺道,而肺气虚则水液输布不利,加重痰湿阻滞,还可引发血瘀阻滞,使得病情缠绵难愈,逐渐加重[13]。临床将本病多辨证为痰湿内阻证,治疗当以燥湿化痰、理气和中为大法。
本研究根据辨证使用自拟中药方,方中黄芪益气健脾,通利水湿;苍术、茯苓健脾燥湿;厚朴、法半夏燥湿化痰、降逆止呕;竹茹、浙贝母清热化痰;枳实、陈皮理气和中、行气导滞;胆南星、石菖蒲豁痰开窍;威灵仙祛风通络、消积化痰;炙甘草、大枣、生姜健脾温中、调和诸药。全方共奏健脾利湿、理气化痰之效[14]。研究显示,本方可改善气道内环境,抑制气道炎症,减少多种炎症因子的释放,降低毛细血管通透性,减轻气道阻塞症状,改善睡眠质量[15]。针灸、耳穴贴敷均是重要的中医外治方法,通过循经取穴,能激发经气,调和脾胃功能,促进气血运行,从而改善颈部肌肉活动,辅助抑制气道阻塞,提升整体疗效[16-17]。
本研究结果显示,观察组患者临床疗效、症状指标、炎症因子、嗜睡、疲乏、睡眠及生活质量等均优于对照组。证实通过中医辨证,结合内服和外治治疗OSAHS,能针对个体化病机特点优化治疗方案,提升病情控制效果,有效抑制炎症反应,促进症状缓解,改善睡眠及生活质量。
综上所述,中医治疗OSAHS的效果确切,能有效缓解症状,抑制炎症反应,提高睡眠及生活质量,值得临床使用。

