氯化铝盐析曲线的绘制及其对晶体纯度的影响
许立军,刘瑞平,王永旺,陈 东,张云峰,图 亚
(1.神华准能资源综合开发有限公司,内蒙古 鄂尔多斯 010300;2.国家能源集团煤炭伴生资源综合利用研究中心,内蒙古 鄂尔多斯 010300)
国家能源准能集团以准格尔矿区的高铝粉煤灰为原料,采用“一步酸溶法”工艺生产冶金级氧化铝,将原料粉煤灰与盐酸溶液按照一定比例加热溶出获得AlCl3浸出液,经固液沉降分离、除杂、蒸发结晶、焙烧等工序,最终生产出冶金级氧化铝一级品[1-2]。传统蒸发结晶方式是采用加热的方式使溶剂汽化,使溶液由不饱和变为饱和,继续蒸发,过剩的溶质就会呈晶体析出。盐析结晶是指向AlCl3溶液中通入气体HCl,利用AlCl3在酸性条件下溶解度随酸度的提高而降低的特性,使AlCl3晶体自发析出的过程。美国矿务局[3]以高岭土为原料提取氧化铝过程中采用盐析结晶方式。除此之外,加拿大orbite公司、英国伯明翰大学等[4-8]均进行过盐析结晶技术方面的研究工作。本文以氯化铝的浸出原液、除杂精制液为实验原料,开展在不同酸度下的盐析结晶实验研究,最终获得盐析曲线并探讨影响晶体纯度的主要因素。
1 实验部分
1.1 实验原料
实验以“一步酸溶法”工艺过程中的粉煤灰HCl浸出原液、除铁精制液为原料,分别进行盐析实验,详细成分分析见表1、表2。采用的HCl气体为化学纯。
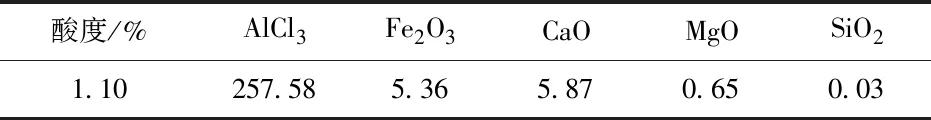
表1 浸出原液成分分析结果 g/L
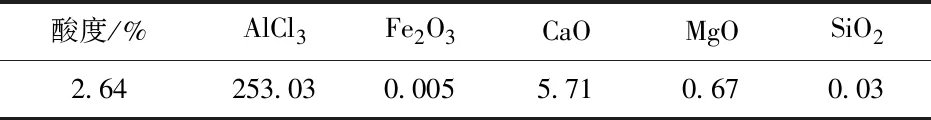
表2 除铁精制液成分分析结果 g/L
1.2 实验方法
室温条件下,将HCl气体通入200 mL原料溶液中进行盐析,盐析装置采用流水冷却,解决盐析过程中HCl气体的溶解放热,以提高HCl气体吸收效率,盐析尾气经NaOH溶液吸收中和后统一处理。将盐析后溶液和六水氯化铝晶体进行固液分离,并分别对液样和固样进行分析。
采用化学滴定法测试溶液酸度;采用ICP-OES分析六水氯化铝晶体及溶液中的Al、Fe、Ca、Mg等离子。
2 结果与讨论
2.1 浸出原液盐析
从图1和图2中可以看出:浸出液原液通入HCl后,随溶液酸度的提高,溶液中AlCl3浓度降低,这是因实验过程中AlCl3转变为六水氯化铝结晶(AlCl3·6H2O)从溶液中大量析出,降低了溶液中AlCl3浓度。当溶液酸度达到23.12%时,溶液中AlCl3浓度已由浸出原液的257.58 g/L降低至74.24 g/L,AlCl3·6H2O晶体析出率已经达到了84.15%。与AlCl3浓度降低对应的是:AlCl3·6H2O晶体析出率随溶液酸度的增加而提高,即晶体析出率与溶液酸度呈正比关系。
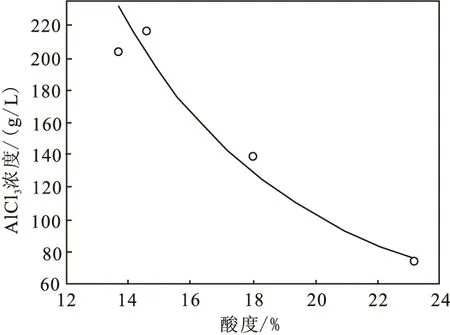
图1 酸度-氯化铝浓度曲线(盐析后液)
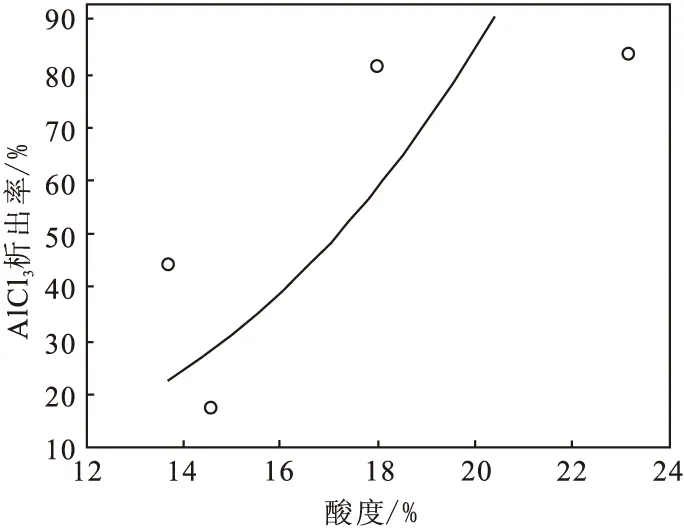
图2 酸度-氯化铝析出率曲线
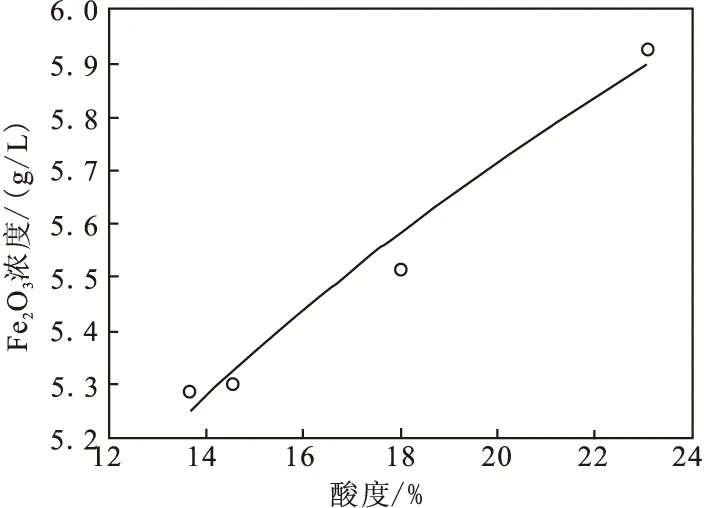
图3 酸度-氧化铁浓度曲线(盐析后液)
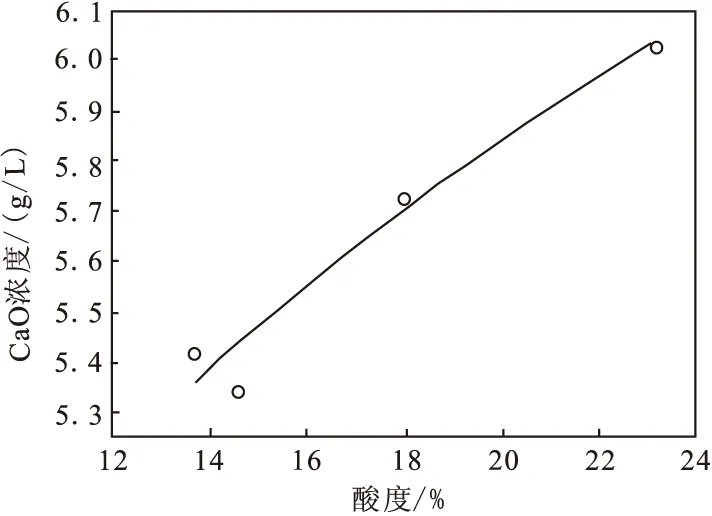
图4 酸度-氧化钙浓度曲线(盐析后液)
随着AlCl3·6H2O晶体的析出,Fe、Ca、Mg、Si等杂质也发生相应的变化,研究其在盐析过程中的行为,有利于提高AlCl3·6H2O晶体纯度。
从图3~图5中可以看出:盐析后溶液中的Fe2O3、CaO、MgO杂质浓度随酸度的升高而逐渐升高,但与盐析前原液相比,各种杂质浓度变化幅度较小。其原因是AlCl3在转变为AlCl3·6H2O晶体的过程中,消耗部分溶剂,使得溶剂中的各种物质浓度升高。而图6中盐析后溶液中杂质SiO2浓度并未随酸度的提高而有所变化。分析主要原因是:与其他杂质相比,盐析前溶液中的SiO2含量较低,AlCl3·6H2O晶体析出过程中消耗的溶剂量对SiO2浓度影响较小。
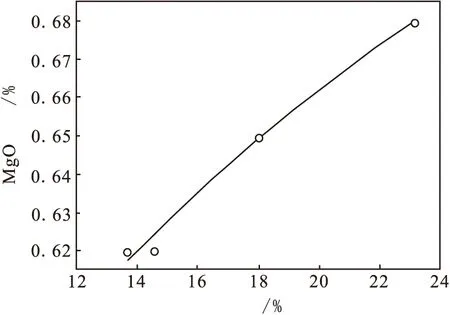
图5 酸度-氧化镁浓度曲线(盐析后液)
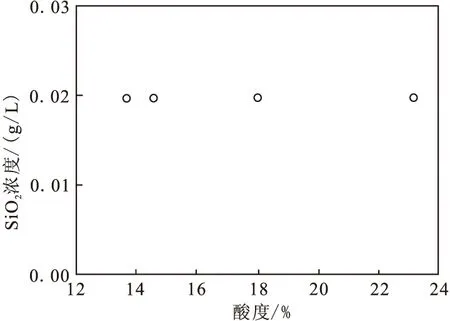
图6 酸度-氧化硅浓度曲线(盐析后液)
所以,浸出原液盐析后溶液酸度范围为13.64%~23.12%时,对应溶液中AlCl3浓度范围为216.67~74.24 g/L、CaO浓度范围为5.35~6.03 g/L、MgO浓度范围为0.62~0.68 g/L、AlCl3·6H2O晶体析出率为44.41%~84.15%。
盐析结晶具有液中晶体可以自发结晶析出的优势,从而降低传统蒸发结晶的能量消耗。单纯从析出率上考虑,氯化铝析出率越高越有利于工业生产;从产品纯度方面考虑,浸出原液中的杂质保留于盐析后液中越多越有利于提高产品纯度。另外,在盐析后溶液酸度相同的条件下,盐析后AlCl3溶液-AlCl3·6H2O晶体之间达到溶解-结晶平衡,溶液中AlCl3溶解度维持不变,因此高浓度的AlCl3原液有利于提高氯化铝的析出率、降低单位晶体产出中HCl气体的消耗量。
2.2 除铁精制液盐析
直接采用粉煤灰浸出液原液进行盐析结晶,获得的晶体中杂质含量较高。将浸出原液进行除铁后,获得除铁精制液后继续进行盐析结晶实验。除铁精制液成分见表2。从表中可以看出:除铁精制液中AlCl3、CaO、MgO、SiO2浓度非常接近于浸出原液。
从图7~图10中可以看出:除铁精制液盐析后,溶液中铝、钙、镁等物质含量变化趋势与浸出原液盐析结晶趋势一致。由于本次实验原料为除铁精制液,盐析后溶液中铁浓度较低,均与原液接近。当盐析后溶液酸度范围为13.42%~23.35%时,对应此时溶液中AlCl3浓度范围为198.49~51.52 g/L、CaO浓度范围为5.29~5.96 g/L、MgO浓度范围为0.63~0.68 g/L、AlCl3·6H2O晶体析出率为25.48%~87.28%。与浸出原液盐析结晶相比较,数值略有波动,但波动总体不大。
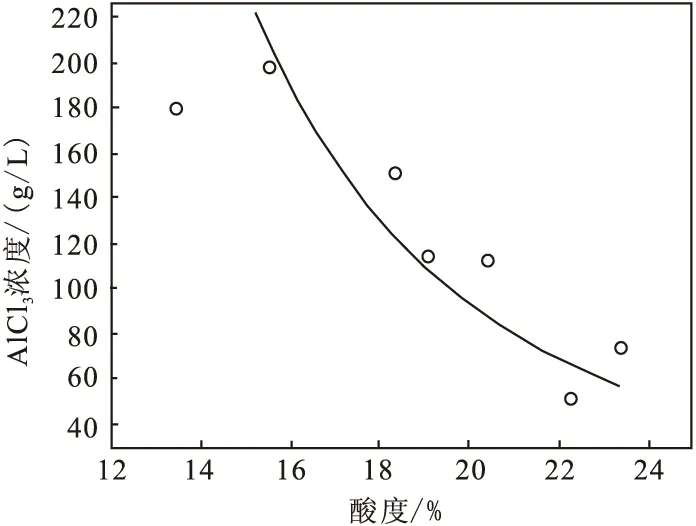
图7 酸度-氯化铝浓度曲线(盐析后液)
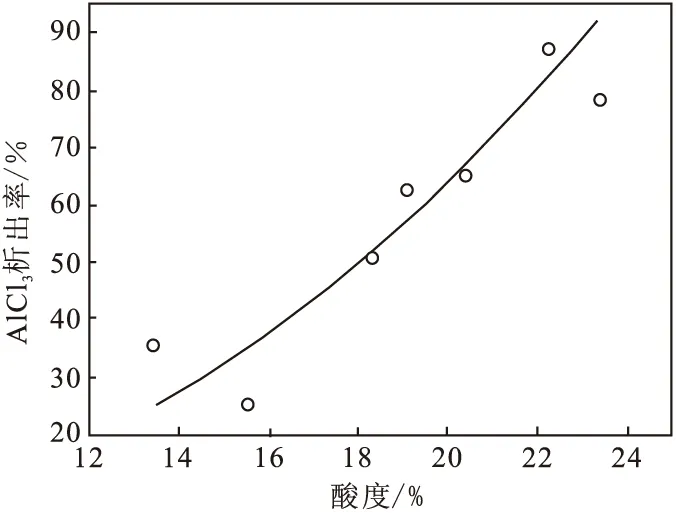
图8 酸度-氯化铝析出率曲线
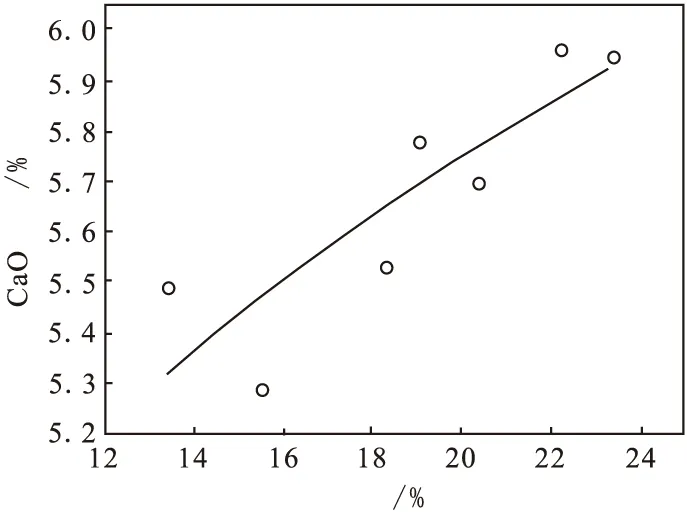
图9 酸度-氧化钙浓度曲线 (盐析后液)
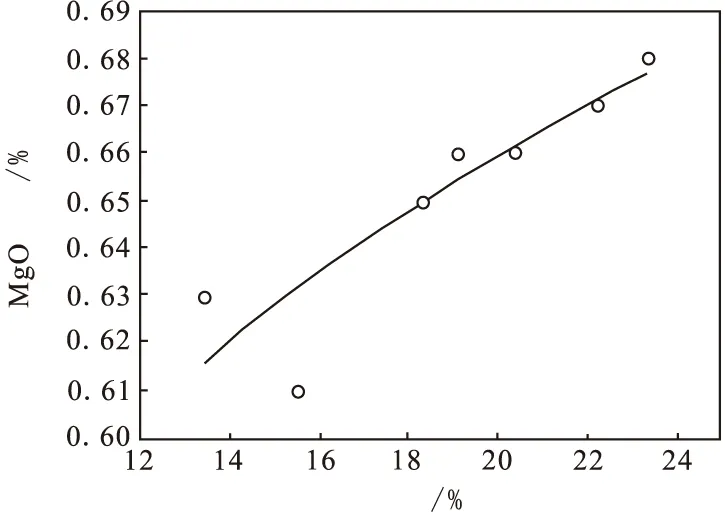
图10 酸度-氧化镁浓度曲线(盐析后液)
通过多次对浸出原液和除铁精制液进行盐析实验,获得盐析后溶液酸度、AlCl3浓度等实验数据,最终绘制出“一步酸溶法”工艺条件下的AlCl3溶液的盐析曲线,为工业化生产提供参考依据。
从图11和图12中可以看出:当盐析后溶液中的酸度范围为13.42%~34.42%时,对应盐析后溶液中AlCl3浓度范围为216.67~3.18 g/L,AlCl3·6H2O晶体析出率为35.87%~98.08%。

图11 酸度与溶液中AlCl3浓度曲线
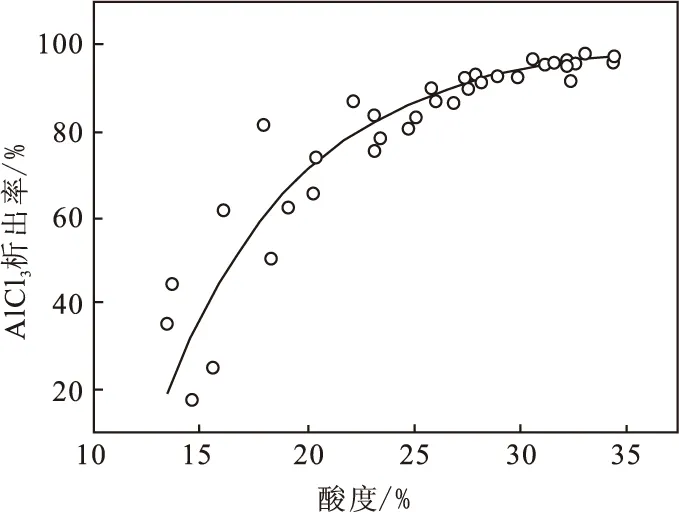
图12 酸度与AlCl3晶体析出率曲线
3 盐析晶体纯度分析
从表3看出:浸出原液析出的AlCl3·6H2O晶体中,主要杂质为Ca、Fe,,其中Fe2O3含量0.11%~0.13%,CaO含量0.13%~0.17%,K、Na、Mg、Si等杂质含量较低,晶体纯度可达99.64%~99.70%。

表3 浸出原液盐析AlCl3·6H2O晶体纯度分析
“一步酸溶法”生产氧化铝工业中,产出的AlCl3·6H2O晶体为氧化铝生产的中间品,AlCl3·6H2O晶体经高温焙烧发生分解反应,生成Al2O3、HCl、H2O,其他杂质在焙烧后也转变为相应的氧化物,最终产品为Al2O3。按化学反应计算,每焙烧4.74吨AlCl3·6H2O晶体,可生成1吨Al2O3。实际工业生产过程中,因晶体中含有约5%附液,每生产1吨氧化铝需焙烧晶体总量约4.9吨。若将浸出原液直接进行盐析,获得的晶体直接焙烧后氧化铝产品中Fe2O3含量0.54%~0.64%,造成产品中Fe2O3含量超标,Al2O3产品无法达到冶金级氧化铝一级品要求(Fe2O3含量≤0.02%)。
从表4看出:除铁精制液盐析出的AlCl3·6H2O晶体中铁含量仅为0.0001%~0.0002%,焙烧后,氧化铝中Fe2O3含量约0.0005%~0.001%,完全满足冶金级氧化铝一级品的要求。另外,AlCl3·6H2O晶体中主要杂质为CaO,含量0.13%~0.20%。
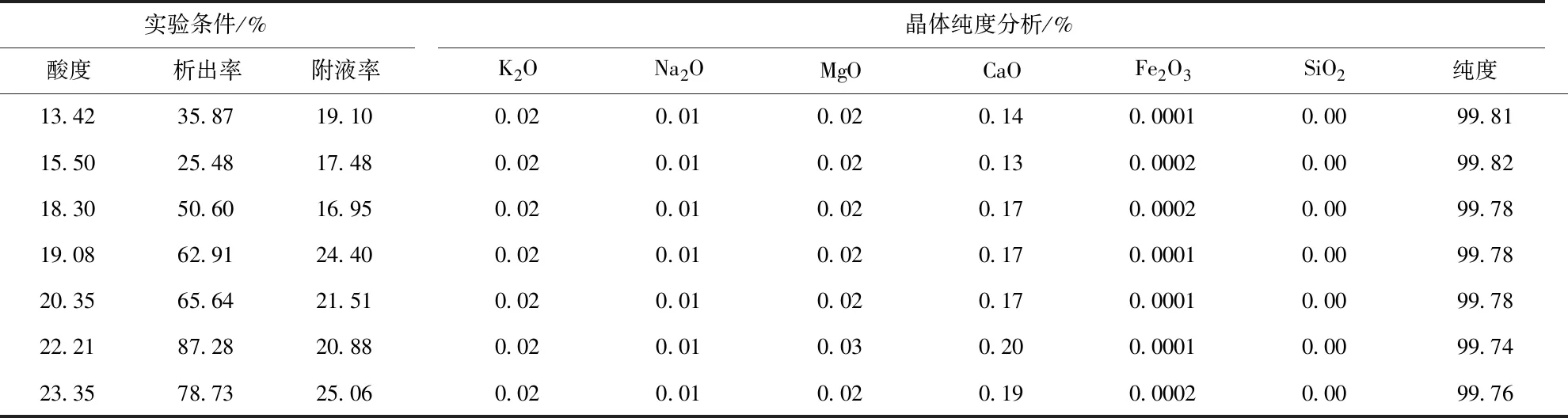
表4 除铁精制液盐析AlCl3·6H2O晶体成分分析
造成盐析后晶体中含有杂质物质的主要原因,盐析结束后,固液混合物需进行分离,这使得晶体中不可避免的夹带一定的溶液(附液),而溶解于晶体附液中的杂质离子会影响晶体纯度。
影响晶体纯度的主要因素有:附液率、原液中杂质离子浓度和盐析酸度(析出率)。附液率越高,单位晶体中的杂质含量越高,是影响晶体纯度的最直接因素。原液中杂质离子浓度和盐析酸度(析出率)均会影响盐析后溶液最终的杂质离子浓度,从而影响产品纯度。除上述因素外,另一个可能影响晶体纯度的因素是在盐析过程中,可能因溶液中各种离子间的相互影响,使溶液中的杂质与AlCl3一样,生成相应的水合晶体而析出[9-10],如:FeCl3·6H2O、CaCl2·4H2O等。
为进一步明确晶体中杂质来源,以CaO为例,开展实验研究。提高浸出原液中CaO杂质浓度,并进行盐析实验。假设晶体中杂质全部来源于附液,结合晶体附液率、盐析后液中CaO浓度等,计算理论上晶体中CaO含量。将理论计算与实验测试结果进行对比分析,结果见表5。
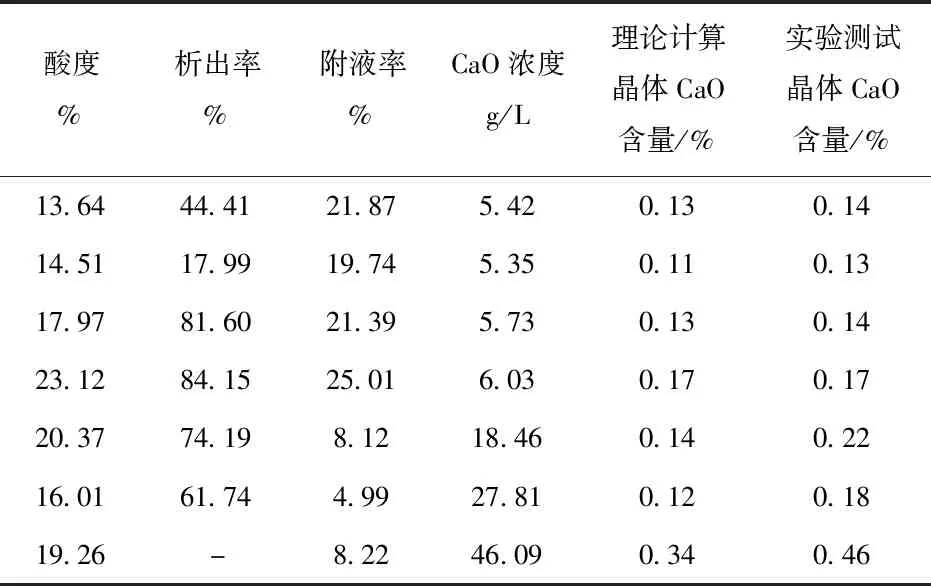
表5 理论计算及实验测试晶体中CaO含量分析
从表5看出:若盐析后溶液中CaO浓度较低时(5~6 g/L),理论计算值与实际值非常接近或一致,说明此时晶体中绝大部分CaO杂质来源于晶体附液;当溶液中CaO浓度提高后,理论计算值与实际值偏差较大,说明当溶液中CaO浓度较高,盐析过程中杂质可能出现了共结晶而析出。
4 结 论
(1)采用盐析结晶技术可以使溶液中的氯化铝析出,从而降低生产能耗。
(2)直接采用浸出原液获得的结晶氯化铝产品,焙烧后氧化铝中Fe2O3含量0.54%~0.64%,无法达到冶金级氧化铝一级品要求(Fe2O3含量≤0.02%);除铁后精制液获得的结晶氯化铝,焙烧后氧化铝中Fe2O3含量约0.0005%~0.001%,完全满足冶金级氧化铝一级品的要求。
(3)盐析后,影响晶体中杂质来源主要为附液,应尽可能降低晶体附液量。
(4)在盐析结晶过程中,当盐析后液中CaO浓度较低时(5~6 g/L),晶体纯度与理论值一致,但当盐析后液中杂质离子浓度较高时,实际晶体纯度与理论计算值发生较大偏差,这可能存在其他杂质离子共结晶的缘故,需要进一步实验研究。
(5)通过实验数据获得了“一步酸溶法”工艺条件下,盐析结晶过程中酸度与晶体析出率关系曲线,为工业化生产提供指导。

