毛细管气相色谱法检测环氧氯丙烷及其微量组分
胡 芳,于旺堂,张卫东
1.河南佰利联新材料有限公司,河南焦作454191;2.原阳县公共检验检测中心,河南新乡453500
环氧氯丙烷(ECH)是一种易挥发、有毒、不稳定的无色液体,具有类似氯仿和醚的气味,能与多种有机溶剂如乙醇、乙醚、氯仿、三氧乙烯、四氯化碳混溶,微溶于水,20℃时在水中的溶解度为6.6%(质量分数)。ECH分子结构中具有不对称碳原子,一般以含有等量右旋和左旋结构的外消旋混合物的形式存在。ECH是精细化工耗氯产品,也是一种重要的有机化工原料,以其作为原料生产的环氧树脂、增塑剂、胶黏剂、氯醇橡胶等精细化工产品又广泛应用于食品、涂料、交通运输、医药、电子电器、轻工和化工等领域。目前,国内外ECH工业生产方法主要有丙烯高温氯化法、醋酸丙烯酯法、丙烯醛法、甘油法和过氧化氢法[1-7]。其中,醋酸丙烯酯法、丙烯醛法、过氧化氢法生产ECH工艺在中国乃至全球所占比例较少,国内采用丙烯高温氯化法生产ECH的装置产能占比约为40%,而采用甘油法生产ECH的装置产能占比已达到了60%[6],源于甘油原料丰富,价格仅为丙烯的2/3,废水量为丙烯法的1/10,既经济又环保,可实现绿色清洁生产。甘油法采用甘油作为原料,工艺过程主要包括盐酸解析、甘油氯化制二氯丙醇、二氯丙醇环化生产ECH,反应原理见式(1)~(3)[8-9]。因生物柴油副产甘油的产量快速攀升,甘油法生产ECH的成本大幅下降。相对丙烯高温氯化法和醋酸丙烯酯法,甘油法不需使用剧毒氯气和次氯酸,操作条件缓和、对设备要求大大降低、安全可靠、污染大大降低,也不需昂贵的催化剂,既经济又环保,甘油法生产的ECH产品具有较强的市场竞争力。因此,本文针对甘油法生产的ECH,采用毛细管气相色谱法监控ECH生产过程的产品和最终产品品质。据文献[8]报道,某公司曾采用Rtx-WAX(60 m×0.25 mm,0.25 μm)聚乙二醇色谱柱气相色谱法检测甘油法生产ECH的中间产品二氯丙醇,采用Rtx-5(60 m×0.32 mm,1.00 μm)5%苯基-95%甲基聚硅氧烷色谱柱气相色谱法检测甘油法生产ECH的最终产品,采用氢火焰离子化(FID)检测器和峰面积归一化定量方法,基本可以满足中间产品及最终产品的分析要求,但是2种毛细管气相色谱法的分析时间均超过45 min。在此基础上,本文选取OV-1701(30.0 m×0.25 mm,1.00 μm)7%氰丙基-7%苯基-86%甲基聚硅氧烷色谱柱,对甘油法生产ECH的中间产品及最终产品进行毛细管气相色谱法分析,以期缩短分析时间,且能有效地分离甘油法所制得的中间产品二氯丙醇、最终成品环氧氯丙烷及可能存在的主要杂质,从而提高毛细管气相色谱法检测环氧氯丙烷及其微量组分的工作效率。


1 实验部分
1.1 主要仪器和试剂
GC-2014C型气相色谱仪,日本岛津公司;WYB-1A型静音无油空气泵、SPGH-300型高纯氢气发生器,优莱博技术(北京)有限公司。
ECH(99%)、1-氯-2-丙醇(95%)、缩水甘油(96%)、1,3-二氯丙醇(99%)、2,3-二氯丙醇(97%)和3-氯-1,2-丙二醇(98%),阿法埃莎(中国)化学有限公司;甲醇,色谱纯,国药集团化学试剂有限公司。
1.2 色谱操作条件
色谱柱为美国Ohio Valley Specialty公司的OV-1701(30.0 m×0.25 mm,1.00 μm)7%氰丙基-7%苯基-86%甲基聚硅氧烷,进样口温度220℃,检测器温度350℃。柱箱温度程序:初温100℃,保持1 min,然后以15℃/min升到180℃,保持5 min。载气为99.99%以上高纯N2,H2流量为40 mL/min,空气流量为400 mL/min。分流进样,分流比为50∶1,进样量为0.2 μL。
1.3 校正溶液与待测溶液的配制和检测
1)准确称取ECH、1-氯-2-丙醇、缩水甘油、1,3-二氯丙醇、2,3-二氯丙醇和3-氯-1,2-丙二醇标准品各1.000 0 g(精确至0.000 1 g),分别置于10 mL容量瓶中,用甲醇稀释并定容至刻度,即为单一标样,用于各组分的定性。
2)参照GB/T 13097—2015[10]用称量法配制甘油法氯化样品、ECH样品的校准溶液,每个标准品的称量精确至0.000 1 g,并计算各自的质量分数,精确至0.000 1%。所配制的校准物质的含量应与待测氯化样品、ECH样品中各组分相近。氯化样品校准溶液的配制:将1,3-二氯丙醇标准品90.000 0 g置于试剂瓶中,依次加入2,3-二氯丙醇5.000 0 g、3-氯-1,2-丙二醇1.000 0 g以及ECH 4.000 0 g,摇匀。ECH样品校准溶液的配制:将ECH标准品100.000 0 g置于试剂瓶中,依次加入1-氯-2-丙醇、缩水甘油、1,3-二氯丙醇、2,3-二氯丙醇和3-氯-1,2-丙二醇各0.005 0 g,摇匀。
3)准确称取1.000 0 g(精确至0.000 1 g)氯化样品和ECH样品的校准溶液以及某公司2022年3月28日某批次的氯化样品和ECH样品,分别置于10 mL容量瓶中,用甲醇稀释并定容至刻度,分别得到氯化样品和ECH样品校正溶液、氯化样品和ECH样品待测溶液,采用带校正因子的面积归一化法检测甘油法生产ECH的中间产品及最终产品。
2 结果与讨论
2.1 定性分析
在1.2节的色谱条件下,检测ECH、1-氯-2-丙醇、缩水甘油、1,3-二氯丙醇、2,3-二氯丙醇和3-氯-1,2-丙二醇单一标样,得出相应物质的相对 保 留时间 依 次为3.754、4.017、4.205、6.477、7.076和7.775 min,各物质的保留时间相差较大,不易交叉干扰,可以用来检测氯化装置、环化装置、产品罐区的有机样品,如中间产品主要成分为二氯丙醇的氯化样品、最终产品主要成分为ECH的环化样品和ECH产品。
2.2 定量分析
待仪器稳定、基线平直后,手动进样0.2 μL,分别检测甘油法氯化样品的校正溶液和待测溶液、ECH样品的校正溶液和待测溶液。根据相对保留时间定性分析样品中的组分,根据校正面积归一法确定各组分的含量。甘油法生产ECH的校正溶液中,中间产品及最终产品各组分的相对保留时间和校正因子分别见表1和表2,待测溶液中氯化样品、ECH样品气相色谱仪测试结果分别见图1和图2。由表1和表2可知:中间产品中ECH、1,3-二氯丙醇、2,3-二氯丙醇和3-氯-1,2-丙二醇的相对保留时间依次为3.755、6.457、7.050和7.767 min;最终产品中ECH、1,3-二氯丙醇和2,3-二氯丙醇的相对保留时间依次为3.748、6.477和7.076 min。与图1、图2中相关物质的相对保留时间相比可知,在相同测试条件下,校正溶液、待测溶液中各物质的保留时间与单一标样的保留时间基本一致,存在0.001~0.020 min偏差。将中间产品和最终产品的校正因子设定到相应产品的定量分析中,按照式(4)计算出校正后产品中各组分的质量分数,但各被测物质的质量分数(w)未扣除色谱仪无法识别的水分。由图1和图2可知:某公司2022年3月28日某批次的氯化样品中ECH、1,3-二氯丙醇、2,3-二氯丙醇和3-氯-1,2-丙二醇的质量分数依次为3.97%、90.83%、4.73%和0.47%;ECH样品中ECH、1,3-二氯丙醇和2,3-二氯丙醇的质量分数依次为99.65%、0.19%和0.01%,未识别的2种杂质的总质量分数约0.15%。
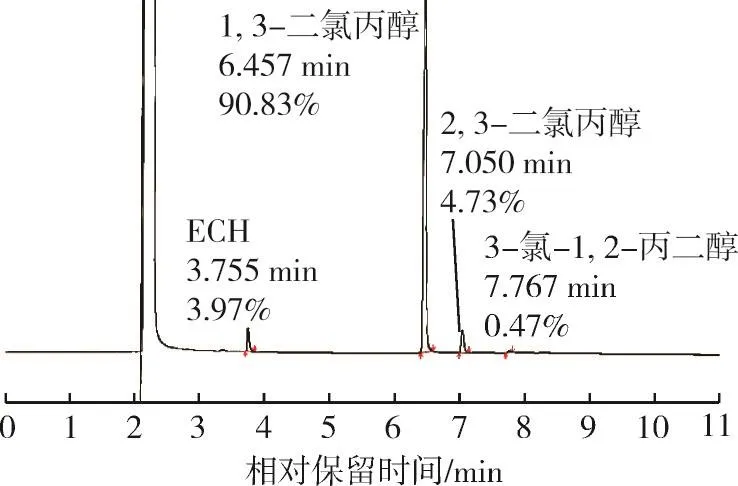
图1 待测溶液中氯化样品的色谱图

图2 待测溶液中ECH样品的色谱图
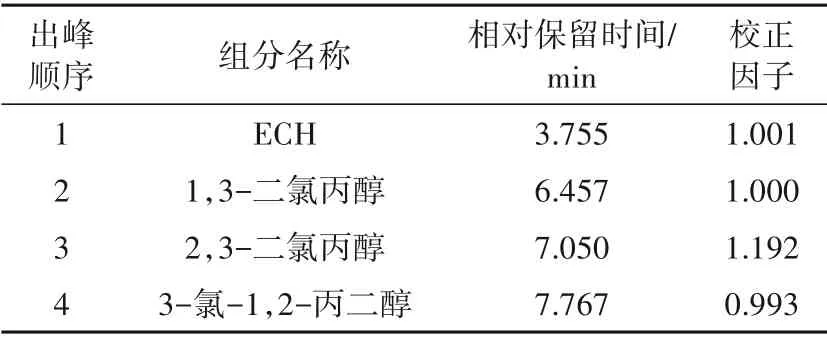
表1 中间产品各组分相对保留时间及校正因子

表2 最终产品各组分相对保留时间及校正因子

式中:Ai为某组分色谱峰面积;fi为某组分的校正因子。
2.3 精密度试验
氯化样品和ECH样品的待测溶液在相同的色谱条件下平行测定8次,计算各组分的质量分数,结果如表3所示。由表3可知:氯化样品中ECH、1,3-二氯丙醇、2,3-二氯丙醇和3-氯-1,2-丙二醇的平均质量分数依次为3.94%、90.82%、4.70%和0.49%,其中二氯丙醇总质量分数为95.52%;ECH样品中ECH、1,3-二氯丙醇和2,3-二氯丙醇的平均质量分数依次为99.64%、0.18%和0.02%,未识别的2种杂质的总质量分数约0.16%。各组分的相对标准偏差为0.01%~0.05%,精密度较好。
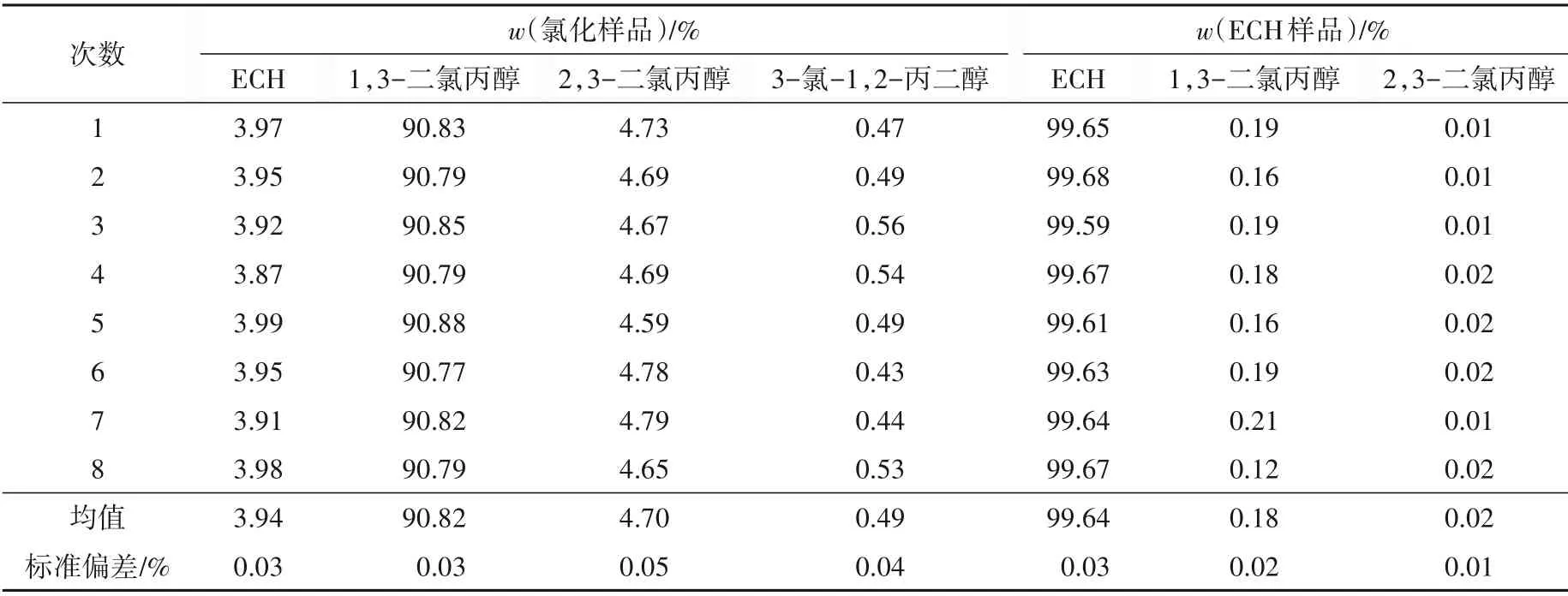
表3 精密度试验结果
2.4 准确度试验
分别称取1.000 0 g(精确至0.000 1 g)氯化样品待测溶液4份和ECH样品待测溶液3份,加入一定量的各组分标准物,分别置于10 mL容量瓶中,用甲醇稀释并定容至刻度,相同色谱条件下平行测定3次。根据加标前后校正面积归一法先计算出对应样品中各组分质量的本底值和测定值,再计算加标回收率,结果见表4。由表4可知:氯化样品待测溶液中ECH、1,3-二氯丙醇、2,3-二氯丙醇和3-氯-1,2-丙二醇质量的本底值分别为39.4、908.2、47.0和4.9 mg,对应加标量依次为50.0、450.0、100.0和10.0 mg;ECH样品待测溶液中ECH、1,3-二氯丙醇和2,3-二氯丙醇质量的本底值分别为996.4、1.8和0.2 mg,对应加标量依次为500.0、5.0和5.0 mg。根据平行测定3次计算加标回收率,最终得到平均加标回收率为98.7%~100.3%。

表4 加标回收率试验结果
3 结论
1)选 择OV-1701(30.0 m×0.25 mm,1.00 μm)7%氰丙基-7%苯基-86%甲基聚硅氧烷色谱柱,采用升温程序:初温100℃,保持1 min,以15℃/min升到180℃并保持5 min。进样口温度220℃,分流进样,分流比为50∶1,FID检测器,检测器温度350℃,进样量0.2 μL。在此色谱条件下,能快速有效地分离样品中ECH、1-氯-2-丙醇、缩水甘油、1,3-二氯丙醇、2,3-二氯丙醇和3-氯-1,2-丙二醇组分。
2)ECH、1-氯-2-丙醇、缩水甘油、1,3-二氯丙醇、2,3-二氯丙醇和3-氯-1,2-丙二醇的相对保留时间依次为3.754、4.017、4.205、6.477、7.076和7.775 min,各物质的保留时间相差较大,不易交叉干扰。
3)中间产品中ECH、1,3-二氯丙醇、2,3-二氯丙醇和3-氯-1,2-丙二醇的保留时间依次为3.755、6.457、7.050和7.767 min;最终产品中ECH、1,3-二氯丙醇和2,3-二氯丙醇的保留时间依次为3.748、6.477和7.076 min。与单一标样中对应组分的保留时间存在0.001~0.020 min的偏差,属正常现象。
4)经检测,2022年3月28日某公司某批次的氯化样品含1,3-二氯丙醇和2,3-二氯丙醇的总质量分数为95.52%,ECH样品含ECH的质量分数为99.64%,该方法操作简单、相对标准偏差为0.01%~0.05%、加标平均回收率为98.7%~100.3%。

