冻干口崩片的质量评价研究
李思潼,薛婉莹,李红鑫,孙常胜,吴婧楠,邱旖,吴雪纯,蒋巧萍,宇泉霖,孙腾跃,张欣悦,张金玲,蔡程科*,王洪飞*(.北京中医药大学中药学院,北京 0488;.北京量子高科制药科技有限公司,北京 000)
冻干口崩片(lyophilised orally disintegrating tablets)是指将特制配方溶液通过冷冻干燥技术制备得到的一种新剂型,与传统压片法制备的口崩片相比,其具有高孔隙率、崩解迅速、辅料用量少、生物利用度高的特点。服用时仅通过唾液即可在口腔中快速崩解,无需用水送服。其活性成分可直接通过口腔黏膜快速吸收,避免肝脏首过效应,特别适用于老人、儿童、精神类疾病以及吞咽困难的患者,可以极大地提高这些人群的服药依从性。
冻干口崩片始载于2015年版《中国药典》,2020年版《中国药典》对其要求为:“除冷冻干燥法制备的口崩片外,口崩片应进行崩解时限检查(通则0921)。采用冷冻干燥法制备的口崩片可不进行脆碎度检查”。冻干口崩片在国内正处于快速发展阶段,然而对其进行质量评价的研究较少,其质量较轻,具有疏松多孔的骨架结构,现有标准及相关研究中用于经典片剂的质量评价方法并不完全适用于冻干口崩片。
本研究选取了10 种具有代表性的冻干口崩片(包含化药类、中药类、蛋白类等),对其进行多角度的质量评价研究,并找出合适的评价方法,为冻干口崩片及其相关剂型药物的质量表征与评价提供有效可行的新模式和新方法,也为口腔崩解片相关质量标准的制订提供参考。建立冻干口崩片的质量评价体系,可以科学、规范地评价产品的质量水平,更能在生产中准确把控产品的质量,切实引导市场选择导向,为这一新剂型的发展奠定了基础。
1 材料
1.1 试药
透明质酸钠冻干泡腾片(批号:20210531,规格:15 mg)、胶原蛋白肽透明质酸钠冻干含化糖(批号:20220107,规格:50 mg)、百荷冻干含化糖(批号:20210913,规格:50 mg)、地龙蛋白含化糖(批号:20200805,规格:30 mg)、氯雷他定口崩片(批号:ZS2101002,规格:10 mg)(陕西量子高科药业有限公司);对乙酰氨基酚口崩片(自制,批号:20210810,规格:100 mg);霍山石斛口崩片(批号:20210428,规格:20 mg,自制);桑葚口崩片(批号:20210823,规格:60 mg)、他达拉非口崩片(批号:20210818,规格:20 mg)、银杏叶冻干口崩片(批号:20210928,规格:40 mg)(北京量子制药科技有限公司)。
氯雷他定对照品(批号:100615-201103,纯度:99.8%,中国食品药品检定研究院);乙腈、甲醇(色谱纯,Fisher Scientific 公司);磷酸(分析纯,无锡市亚泰联合化工有限公司);二乙胺(分析纯,天津市大茂化学试剂厂);卡尔费休试剂(国家化学试剂质检中心);无水甲醇(分析纯,天津市致远化学试剂有限公司);纯净水(杭州娃哈哈集团有限公司)。
1.2 仪器
电子天平(BT25s,北京赛多利斯仪器系统有限公司);口崩片崩解仪(KB-1,天津市天大天发科技有限公司);卡尔费休水分测定仪(MA-1,上海本昂科学仪器有限公司);药品稳定性试验箱(Labone-300CGS,北京兰贝石恒温技术有限公司);高性能全自动压汞仪[AutoPore V9605,麦克默瑞提克(上海)仪器有限公司];全自动真密度分析仪(Ultrapyc 5000)、全自动比表面积和孔径分析仪(Autosorb-IQ-MP)[安东帕(上海)商贸有限公司]。
2 方法与结果
2.1 冻干口崩片质量评价
2.1.1 外观评测 10 批冻干口崩片,每批随机抽取20 片,分别置于自制外观评测装置(见图1)的固定白色光源、纯色背景下,固定角度观察片剂。设计5 个评价指标:颜色、形态、裂边、融化、黏片。分别要求片剂颜色均匀;呈圆形、饱满光洁;无裂片、裂边;无底融化、中心融化;没有与包材粘连残留的现象。记录每批20 片中合格片剂的数量,合格一个记1 分,单个评测项低于15 分即为此项不达标,5 个评测指标中存在2 项及以上不达标即为样品不合格。各批冻干口崩片的外观评测结果如表1 所示。
表1 外观评测结果
Tab 1 Appearance evaluation
类别 样品颜色 形态 裂片 融化 黏片化药类 氯雷他定口崩片2020202020他达拉非口崩片2020202020对乙酰氨基酚口崩片2020202020中药类 百荷冻干含化糖920162020霍山石斛口崩片2020202010桑葚口崩片2020202020银杏叶冻干口崩片2020181920蛋白类 胶原蛋白肽透明质酸钠冻干含化糖202020 320地龙蛋白含化糖1520202020其他透明质酸钠冻干泡腾片 2020202020
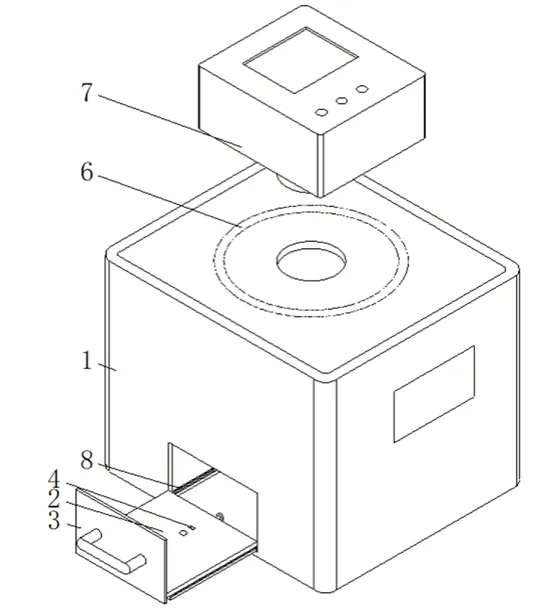
图1 冻干口崩片外观评测装置Fig 1 Appearance evaluation device for lyophilised orally disintegrating tablets
从评测结果可得,化药类冻干口崩片多呈白色至类白色,中药类多为黄色或棕色,10 批冻干口崩片均为圆形片,片面饱满光洁,但中药类与蛋白类冻干口崩片更容易出现裂片或融化现象,顶部突起黏附顶铝的现象可通过调整灌装量解决。10 批冻干口崩片外观评测均合格。
2.1.2 片重差异 根据2020年版《中国药典》对于片重差异测定法的要求,对10 批冻干口崩片每批随机抽取20 片,精密称定总重量,求得平均片重后,再分别精密称定每片的重量,每片重量与平均片重比较,超出重量差异限度的不得多于2 片,并不得有1 片超出限度1 倍。平均片重或标示片重0.3 g 以下的重量差异限度为±7.5%。片重差异计算公式:

图2 氯雷他定口崩片(左)与银杏叶冻干口崩片(右)的外观Fig 2 Appearance of loratadine orally disintegrating tablet(left)and ginkgo leaf lyophilised orally disintegrating tablet(right)
片重差异(%)=(单片重-平均片重)/平均片重×100%
各批冻干口崩片的试验结果如表2 所示。由表2 可以看出,10 批冻干口崩片的片重差异均合格。冻干口崩片的片重较轻,大多为19 ~108 mg,通过片重与规格的比较可以发现其辅料用量很少,药物活性成分(API)占比很大,这也是冻干口崩片的优势之一。
表2 片重差异测定结果
Tab 2 Tablet weight difference
类别样品规格/mg平均片重/mg超限数 结果化药类 氯雷他定口崩片1019.030合格他达拉非口崩片2039.190合格对乙酰氨基酚口崩片100108.060合格中药类 百荷冻干含化糖5052.070合格霍山石斛口崩片2023.681合格桑葚口崩片6066.760合格银杏叶冻干口崩片4067.290合格蛋白类 胶原蛋白肽透明质酸钠冻干含化糖5076.611合格地龙蛋白含化糖3057.290合格其他透明质酸钠冻干泡腾片1526.841合格
2.1.3 崩解时限 根据2020年版《中国药典》口崩片崩解时限检查法的要求,使用口崩片崩解仪测定崩解时限,将崩解篮固定于支架上,浸入1000 mL 杯中,杯内盛有温度为(37±1)℃的水约900 mL,调节水位高度使崩解篮最低位时筛网在水面下(15±l)mm,启动仪器。取本品1 片,置崩解篮中进行检查,应在60 s 内全部崩解并通过筛网,如有少量轻质上漂或黏附于不锈钢管内壁或筛网,但无硬心者,可作符合规定论。重复测定6 片,均应符合规定。如有1 片不符合规定,应另取6 片复试,均应符合规定。各批冻干口崩片的测定结果如表3 所示。
表3 崩解时限测定结果(s)
Tab 3 Disintegration time (s)
类别样品1 23456均值化药类 氯雷他定口崩片1 111111他达拉非口崩片1 111111对乙酰氨基酚口崩片97 95 107 117 105 92 102.2中药类 百荷冻干含化糖10 685446.2霍山石斛口崩片3 222332.5桑葚口崩片2 111121.3银杏叶冻干口崩片 11 96 10498.2蛋白类 胶原蛋白肽透明质酸钠冻干含化糖4 646655.2地龙蛋白含化糖4 644454.5其他透明质酸钠冻干泡腾片59 64 57 62 67 55 60.7
由表3 可以得出,透明质酸钠冻干泡腾片与对乙酰氨基酚口崩片崩解时限大于60 s,不合格,其余均在10 s 内崩解。规格小的冻干口崩片一般情况下的崩解速度稍快于大规格冻干口崩片。
2.1.4 水分测定 参照2020年版《中国药典》中水测定法第一法(费休氏法)进行测定,取适量样品,放入研钵中充分研磨,精密称定重量后,快速放入卡尔费休水分测定仪中测定水分,记录测定结果,每批平行测定3 次,结果见表4。
由表4 可以得出,大部分冻干口崩片的含水量在0.5%~5%,但百荷冻干含化糖含水量远高于平均水平。化药类含水量均在2%以下,中药类与蛋白类含水量高一些,大部分为3%~5%,中药由于其成分复杂,水分不易除去,在生产过程中更难制备。
2.1.5 引湿性试验 根据2020年版《中国药典》中9103 药物引湿性试验指导原则,结合实际生产情况,设计了引湿性试验。取具塞玻璃称量瓶,于试验前一日置于药品稳定性试验箱内,设置温度为(25±1)℃,湿度为(40±2)%,精密称定称量瓶质量(m
),每批各取10 片样品,平铺于上述称量瓶中,精密称定质量(m
),将称量瓶敞口,并与瓶盖同置于上述恒温恒湿条件下,分别于1 h、2 h 取出称量瓶,盖好称量瓶盖子,精密称定质量(m
)。增重百分率计算公式:增重百分率(%)=(m
-m
)/(m
-m
)×100%测定结果如表4 所示。由表4 可以看出,冻干口崩片1 h 与2 h 的增重百分率相差不大,说明其吸水过程主要发生在前1 h,在1 ~2 h 期间,吸水较少。10 批冻干口崩片的2 h 增重百分率为0.15%~8.74%,其中化药类的增重百分率很低,为0.15%~0.16%,中药类增重百分率较高,为2.85%~8.74%,蛋白类的增重百分率为0.67%~3.97%。
表4 水分、引湿性试验测定结果
Tab 4 Moisture and hygroscopicity test
类别样品含水量/%增重百分率/%1 h2 h化药类氯雷他定口崩片1.660.100.16他达拉非口崩片1.600.130.15对乙酰氨基酚口崩片0.510.160.16中药类百荷冻干含化糖11.048.248.74霍山石斛口崩片3.072.852.85桑葚口崩片4.193.173.35银杏叶冻干口崩片5.175.926.86蛋白类胶原蛋白肽透明质酸钠冻干含化糖5.000.110.67地龙蛋白含化糖1.693.793.97其他透明质酸钠冻干泡腾片3.566.856.85
2.1.6 真密度测定 试验前应将全自动真密度分析仪,以及试验材料、用具处于试验室恒温环境下放置24 h 以上。准备开始测定样品的真密度,首先打开氦气阀,调压力为0.13 ~0.14 MPa,打开仪器电源,预热30 min,使仪器恒温,然后对仪器进行校准。校准完成后,取适量样品,精密称定,放入样品池内进行测定,依次测定10 批样品,结果如表5 所示。10 批冻干口崩片的真密度较为接近,在1.473 ~1.862 g·cm。
2.1.7 比表面积测定 使用氮气吸附法测定冻干口崩片的比表面积,首先开启氮气瓶的主阀,确认压力不低于5 MPa,再将加压阀压力调至0.08 MPa,然后开启仪器,准备做样品的前处理,取适量样品放入提前称好重量的样品管中,一起精密称定并记录,再将样品管安装在脱气站上,进行脱气处理,脱气完成后,将样品管取下精密称定,再将样品管安装在分析站上,进行测试,记录试验结果,依次测定10 批冻干口崩片,结果如表5 所示。
从表5 可以看出,剔除偏离较大的数据(百荷)后,冻干口崩片的比表面积为1.431 ~5.192 m·g,化药类平均比表面积高于中药类,百荷冻干含化糖比表面积较低,推测为冻干曲线不合适,在冻干过程中没有形成孔道。
2.1.8 孔隙率测定 使用压汞仪来测定冻干口崩片的孔隙率,将仪器打开后,取适量样品装入样品管中,然后将样品管密封,精密称定总重量并记录,把检测套加在样品管头上锁住,然后进行低压孔隙分析测试以及高压孔隙分析测试,依次测定10 批样品,结果如表5 所示,剔除偏离较大的数据(百荷冻干含化糖)后,10 批冻干口崩片的平均孔径大小为10 254.31 ~29 207.12 nm,孔隙率为76.76%~86.98%。
表5 物理常数测定结果
Tab 5 Physical constants
类别样品真密度/(g·cm-3) 比表面积/(m2·g-1) 平均孔径/nm孔隙率/%化药类氯雷他定口崩片1.8624.33614 039.3786.95他达拉非口崩片1.6615.19210 254.3180.29对乙酰氨基酚口崩片1.7132.77929 207.1276.76中药类百荷冻干含化糖1.6040.14658 411.9365.96霍山石斛口崩片1.7563.37124 401.386.98桑葚口崩片1.5851.43124 059.9984.62银杏叶冻干口崩片1.5442.06010 944.7381.49生物类胶原蛋白肽透明质酸钠冻干含化糖1.4732.01211 114.2378.83地龙蛋白含化糖1.5973.15717 072.6581.75其他透明质酸钠冻干泡腾片1.7884.58411 655.9177.81
2.1.9 加速试验 取氯雷他定口崩片300 片放置在温度(40±1)℃,湿度(75±5)%的恒温恒湿箱中6 个月,分别于0、1、2、3、6 个月取样,测定其外观、含量、有关物质、水分、崩解时限。试验结果如表6 所示。
表6 加速试验测定结果
Tab 6 Accelerated test
检测项 外观评分单一杂质/% 总杂质/% 含量/%水分/%01000.100.30102.802.40 11000.060.20103.402.20 2 980.060.20100.402.40 3 990.060.20101.302.40 6 980.070.30101.702.50
① 外观、水分、崩解时限测定:外观测定方法按“2.1.1”项下方法;水分测定按“2.1.4”项下方法;崩解时限测定按“2.1.3” 项下方法。
② 含量测定:照高效液相色谱法(《中国药典》2020年版四部通则0512)测定。色谱柱用十八烷基硅烷键合硅胶为填充剂;流动相为乙腈-甲醇-0.02%的二乙胺溶液(50∶20∶30)(用磷酸调pH 值至4.0±0.1);检测波长247 nm;进样量20 μL;流速1.0 mL·min;柱温25℃。
测定法:取本品10 片(相当于氯雷他定100 mg),置100 mL 量瓶中,加水5 mL,超声处理2 min,加流动相80 mL,再超声处理15 min,加流动相稀释至刻度,作为储备液;精密量取储备液10 mL,置50 mL 量瓶中,加流动相稀释至刻度,用聚四氟乙烯滤膜滤过,取续滤液作为供试品溶液。另精密称取105℃干燥至恒重的氯雷他定对照品适量,加流动相溶解并稀释成每1 mL中含氯雷他定0.1 mg 的溶液,作为对照品溶液。分别吸取供试品溶液和对照品溶液各20 μL 注入液相色谱仪,记录色谱图,按外标法以峰面积计算,即得。
③ 有关物质测定:记录色谱图至主峰保留时间的3 倍,供试品溶液色谱图中如有杂质峰,各杂质峰面积的总和不得大于对照溶液主峰面积(1.0%),单个杂质峰的峰面积不得大于对照溶液主峰面积的0.5 倍(0.5%)。
2.2 各评测结果相关性分析
将上述结果导入SPSS 20.0 进行相关性分析,首先对8 组数据的正态分布进行分析,符合正态分布的组别使用Pearson 相关性分析,不符合正态分布的组别使用Spearman 相关性分析,结果如表7 所示:水分含量与比表面积成强负相关关系;水分含量与引湿性成极强正相关关系;崩解时限与孔隙率成强负相关关系;真密度与比表面积成强正相关关系。
表7 评测结果相关性分析
Tab 7 Correlation analysis of evaluation
注(Note): <0.05, <0.01。
项目比表面积平均孔径孔隙率水分崩解时限片重引湿性真密度比表面积1平均孔径-0.4181孔隙率0.486-0.1271水分-0.697*0.030-0.1881崩解时限-0.3220.237-0.687*0.2431片重-0.5300.030-0.3210.1640.5351引湿性-0.3900.237-0.5120.796**0.473-0.1451真密度0.696*0.2240.304-0.564-0.116-0.582-0.2061
3 讨论
考虑到国内已上市的冻干口崩片品种较少,本研究除选取已上市产品外,其余冻干口崩片均采用与已上市药品相同的制备工艺得到。因此,可以保证其质量稳定可靠。且选取的品种类别涵盖范围较广,得到的质量评价结果具有较高的可信度与普适性。自冻干口崩片收载于2015年版《中国药典》以来,其质量评价的发展比较缓慢,国内研究大多为对于某一种产品的崩解时限、溶出度、含量测定等,进行质量评测,本文针对这一剂型进行系统性的质量评价研究,为其质量标准的制定提供了新方法、新思路。
冻干口崩片容易出现颜色不均匀、裂片、底部融化、中心融化、黏片等现象。冻干口崩片片型的好坏与其冻干前溶液均匀度、处方、冻干曲线等因素有关,出现裂片现象可适当增加黏合剂进行改善,出现融化现象可适当调整冻干曲线。图3、图4 为冻干口崩片的三维显微结构图与切片图,可看见其疏松多孔的骨架结构,API 均匀的分布在骨架结构上,这也是其可以快速崩解的原因。
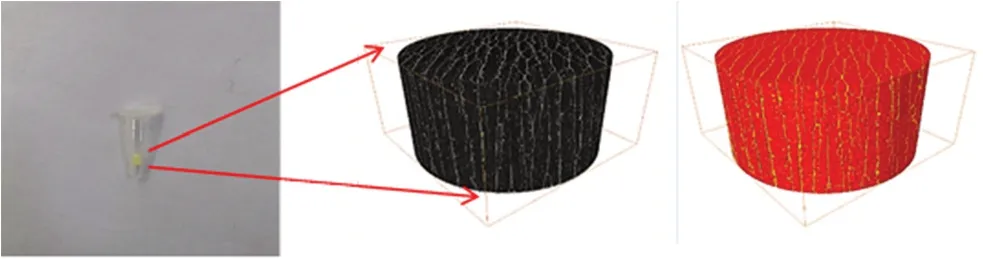
图3 氯雷他定口崩片在X 线三维显微镜下的结构Fig 3 Structure of loratadine orally disintegrating tablets under X-ray three-dimensional microscope

图4 氯雷他定口崩片在X 线三维显微镜下的切片图Fig 4 Sectional view of loratadine orally disintegrating tablet under X-ray three-dimensional microscope
2020年版《中国药典》规定冷冻干燥法制备的口崩片可不进行崩解时限检查,但是在研究中发现,也存在几种冻干口崩片的崩解时限超出了药典规定的60 s,经过多次试验,推测崩解慢与其规格较大或者原料的黏性大有关。
从相关性分析可以看出,水分含量与比表面积成负相关、与引湿性成正相关,水分含量越低的冻干片比表面积越大,引湿性越弱,因此可以通过控制冻干口崩片的水分,从而来保证其质量;崩解时限与孔隙率成负相关,孔隙率越高的冻干口崩片崩解速度越快,因此可以通过增大孔隙率的方法来加快其崩解的速度。
本研究通过对外观、片重差异、崩解时限、水分、真密度、比表面积、孔隙率、引湿性试验的评测,可以初步判断冻干口崩片的质量优劣。但是这些方法评价标准的制订还需积累更多的数据。药品审批过程中涉及到的一些方法也可用于质量评价,如口感、口味,含量均匀度,有关物质,溶出度,溶出曲线,稳定性试验等。质量评价研究可以帮助快速发现和解决在研发、生产过程中遇到的问题,从而保证产品的质量。准确客观的冻干口崩片质量评价方法,可以为其质量标准的建立提供依据,推动冻干口崩片剂型的发展,服务更多的患者,提高其用药依从性。

