基于中医辨证保健理论探索辅助降血糖功能评价方法
孟 靓 王景霞 孟智睿 魏益谦 邵紫萱 李 丽 高学敏 张建军
(北京中医药大学,北京,100029)
糖尿病前期是一种糖代谢异常的状态,介于糖代谢正常状态和糖尿病之间[1]。如果不采取有效干预措施,处于糖尿病前期状态的人群会有很大概率发展成为糖尿病患者[2]。目前我国糖尿病前期人群约为4.934亿,且呈逐年高速增长态势[3]。我国糖尿病患者中,2型糖尿病占90%以上[4]。2型糖尿病绝大多数是可以预防的,对于处在糖尿病前期的亚健康人群来说,通过早期干预,控制血糖和糖耐量的进一步受损,降低患病风险,减少治疗花费的经济负担,具有重要的现实意义。
保健食品是指具有特定保健功能的食品,适宜于特定人群食用,可以调节机体功能,不以治疗疾病为目的[5]。我国保健食品特定的27个功能中就有“辅助降血糖”,在降低疾病风险、预防糖尿病方面发挥着重要的作用[6]。中药保健食品是以中医药理论为指导,结合现代药理学、药剂学、营养学、食品学等各学科的最新研究进展,以含有中药、中药提取物、药食两用等原料为主,研制而成的功能类保健食品[7]。中药保健食品可依托中医辨证理论的指导,精细划分保健食品适宜人群的范围,使其更加有针对性发挥保健效能,充分体现“辨证”特色[8]。但是在目前的保健食品研发过程中,保健功能的评价却不能体现中医的辨证特点,国家2012年发布的《辅助降血糖保健功能评价方法》中,辅助降血糖功能评价方法有2种,一种是损伤胰岛高血糖模型,另一种是胰岛素抵抗糖脂代谢紊乱模型[9]。这2种方法虽然建立了高血糖模型,但是均不能体现中医证候特点,只能评价某一中药保健品的降血糖功能,这就使因人制宜的精准化及个性化保健无法实施,如果使用不对症的保健食品盲目保健,则还可能适得其反危害机体健康[10]。
糖尿病前期属于中医“脾瘅”范畴,属未病阶段,如不及时干预则可转为“消渴”,脾瘅可认为是消渴前期,根据中医辨证可分为湿热蕴脾、肝郁气滞、脾虚湿盛和气阴两虚4个证型,不同证型的人群临床表现是不同的,所选择的中药必然不同[11]。本研究以辅助降血糖保健功能为切入点,依据中医对糖尿病前期的认识,通过建立“气阴两虚型高血糖动物模型”,探索符合中医辨证特点的保健食品功能评价体系,为研发辅助降血糖辨证保健产品提供方法学参考。
1 材料与方法
1.1 材料
1.1.1 动物 选取45只雄性SD大鼠(北京维通利华实验动物技术有限公司,许可证号:SCXK(京)2016-0006),体质量(160±20)g,饲养于无特定病原体(Specific Pathogen Free,SPF)级屏障环境中,大鼠维持饲料由北京科澳协力饲料有限公司提供。特殊高脂饲料(猪油10%、蔗糖15%、蛋黄粉%、酪蛋白5%、胆固醇1.2%、胆酸钠0.2%、碳酸氢钙0.6%、石粉0.4%、鼠维持饲料52.6%)由斯贝福(北京)生物技术有限公司提供。整个实验过程中大鼠自由饮水,室温20~22 ℃,相对湿度为60%~70%,灯照周期为12 h,7:00至19:00灯照,19:00至第2天7:00黑暗。本研究通过北京中医药大学医学与实验动物伦理委员会审批(伦理审批号:BUCM-4-2019110201-4032)。
1.1.2 药物 十味消渴胶囊(天津中新药业集团股份有限公司,生产批号:09950063)。
1.1.3 试剂与仪器 试剂:血清总胆固醇(Total Cholesterol,TC)试剂盒(长春汇力生物技术有限公司,批号:2019009)、三酰甘油(Triacylglycerol,TG)试剂盒(长春汇力生物技术有限公司,批号:2019008)、高密度脂蛋白(High-Density Lipoprotein,HDL)试剂盒(长春汇力生物技术有限公司,批号:2019007)、低密度脂蛋白(Low-Density Lipoprotein,LDL)试剂盒(长春汇力生物技术有限公司,批号:2019011)、空腹胰岛素(Fasting Insulin,FINS)试剂盒(优尔生生物科技有限公司,批号:L191102001)、三碘甲状腺原氨酸(Triiodothyronine,T3)试剂盒(优尔生生物科技有限公司,批号:L191114551)、甲状腺素(Thyroxine,T4)试剂盒(优尔生生物科技有限公司,批号:L191104072)、环磷酸腺苷(Cyclic Adenosine Monophosphate,cAMP)试剂盒(优尔生生物科技有限公司,批号:L191114614)、环磷酸鸟苷(Cyclic Guanosine Monophosphate,cGMP)试剂盒(优尔生生物科技有限公司,批号:L191008130)、L-甲状腺素钠试剂盒(BioRuler,美国,批号:r5703),D(+)-无水葡萄糖试剂盒(国药集团化学试剂有限公司,批号:20181205)。仪器:电子天平(梅特勒-托利多仪器上海有限公司,型号:PL-203)、超声细胞粉碎机(宁波新芝生物,型号:JY92-IIn)、台式高速冷冻离心机(力康,中国香港,型号:Neofuge 15R)、涡旋混合器(武汉赛维尔生物科技有限公司,型号:MX-F)、全自动研磨仪(武汉赛维尔生物科技有限公司,型号:KH-Ⅲ)、自动洗板机(深圳雷杜生命科技,型号:RT3100)、酶标检测仪(BioTeK,德国,型号:EPoch)、全自动生化分析仪(深圳雷杜生命科技,型号:Chemray240)。
1.2 实验方法
1.2.1 药品制备 十味消渴胶囊灌胃药制备:拆去胶囊外壳,称取适量药物粉末,放入烧杯中,根据大鼠灌胃量(1 mL/100 g)加入适量蒸馏水,搅拌至完全溶解均匀。灌胃用葡萄糖溶液制备:取适量葡萄糖,放于烧杯中,根据大鼠灌胃量(2.5 g/kg)加入适量无菌水,搅拌混合均匀,直至葡萄糖完全溶解。注射用T4混悬液制备:取适量L-甲状腺素钠,放于烧杯中,根据大鼠注射剂量(0.2 mg/kg)加入蒸馏水,摇晃均匀即得。
1.2.2 分组及给药 雄性SD大鼠45只,体质量(160±20)g,适应性喂养5 d后,禁食过12 h后,使用便携式血糖测定仪取尾静脉血测量血糖值,测定灌胃葡萄糖前(即0 h)血糖值,再测定灌胃2.5 g/kg BW葡萄糖后0.5 h、2 h血糖值,作为该批次动物基础值[9]。以0 h、0.5 h血糖水平分为3个组,即空白组、模型组、阳性组(十味消渴胶囊1.32 g/(kg·d),相当于人7.92 g/d)、每笼饲养6只。从实验开始第一天给每组动物进行预防给药,灌胃时间连续33 d(给药体积:1 mL/100 g)。空白组不做处理,模型组给予同体积溶剂,阳性组予以灌胃十味消渴胶囊溶液。
1.2.3 造模方法 参考《保健食品检验与评价技术规范2003》辅助降血糖功能评价方法中的胰岛素抵抗糖脂代谢紊乱模型,建立由高脂饲料喂养、劳倦伤脾、T4皮下注射、联合链脲佐菌素(Streptozotocin,STZ)注射造成气阴两虚型胰岛素抵抗糖脂代谢紊乱大鼠模型[9]。适应性喂养5 d后,开始造模,造模周期维持33 d:1)各组给予维持料饲养,1周后模型组、阳性组更换高热能饲料,喂饲3周。2)负重游泳力竭运动:在实验8~21 d灌胃给药结束1 h后进行负重力竭游泳,在大鼠尾根部负荷其体质量10%的铅块,放入0.8 m×0.8 m×1 m的游泳桶内,水深0.7 m,水温(20±5)℃,使大鼠在水中不能用尾巴接触桶底,每桶放置2只。力竭标准:游泳动作明显失调,不能再坚持;大鼠鼻尖没入水里超过3 s不能回到水面,停止游泳,及时捞出,吹干毛发。3)T4皮下注射:在实验22~28 d下午14:00进行上颈部皮下注射T4混悬液(0.2 mg/kg)。4)在实验第28天T4注射结束后,模型组、阳性组禁食24 h(不禁水),在实验第29天给予2% STZ溶液(30 mg/kg)一次性腹腔注射(现用现配,取适量STZ,锡纸避光于冰块中保存,用0.1 mol/L柠檬酸-柠檬酸钠缓冲液在冰浴中配置溶液,pH=4.5),以1 mL/100 g体质量的剂量进行注射。注射后继续给予高热量饲料喂饲5 d。
1.2.4 模型判定 实验结束后,各组动物禁食12 h,检测空腹血糖(Fasting Blood Glucose,FBG)、糖耐量、血清胰岛素及TC、TG水平。测定FBG即给葡萄糖前(0 h)血糖值,阳性组给予十味消渴药液,模型组给予同体积溶剂,空白组不做处理,15 min后各组灌胃葡萄糖2.5 g/kgBW,测定给葡萄糖后0.5 h、2 h的血糖值,模型组FBG值≥10 mmol/L或0.5 h、2 h任一时间点血糖升高或血糖曲线下面积(Area Under The Curve,AUC)升高,与空白组比较有显著性差异,判定糖代谢紊乱模型成立[9]。模型组血清TC或TG明显升高,与空白组比较,差异有统计学意义(P<0.05),判定脂代谢紊乱模型成立[9]。
1.2.5 检测指标与方法
1.2.5.1 大鼠证候表征的观察 大鼠造模前和造模后证候表征比较,即大鼠毛色、尿量、排便情况、自主活动的表现。运用电子称,在实验第33天给各组大鼠称体质量。每日观察记录各组大鼠的肛温、摄食量、饮水量、排尿量、排便量。
1.2.5.2 血糖测定及相关指数计算 用血糖试纸,按说明书操作,尾尖静脉取血测FBG值。AUC=(0 h血糖+0.5 h血糖)×0.5/2+(2 h血糖+0.5 h血糖)×1.5/2;胰岛素抵抗指数(Homeostasis Model Assessment of Insulin Resistance,HOMA-IR)=(FBG×FINS)/22.5;胰岛B细胞功能指数(HOMA-β)=20×FINS/(FBG-3.5);胰岛素敏感指数(Insulin Sensitivity Index,ISI)=Ln(l/FINS×FBG)。
1.2.5.3 大鼠负重游泳力竭运动时间 实验第34天早晨进行最后1次负重游泳力竭运动,记录负重游泳时间。
1.2.5.4 脏器指数、血脂、环核苷酸等指标的检测 实验第33晚灌胃结束后禁食不禁水,于第34天早晨进行最后1次负重游泳力竭运动,30 min后处死动物并取材。巴比妥钠麻醉,腹主动脉取血,3 000 r/min、离心半径2 cm环境下离心10 min,取上清液,4 ℃保存待测,取胸腺、脾脏并称重,计算各组大鼠胸腺、脾脏指数,脏器指数=脏器重(g)/体质量(g)。采用比色法在全自动生化仪上测各组血清TC、TG、LDL、HDL。采用酶联免疫吸附试验法检测血清T3、T4、FINS、cAMP和cGMP的含量,并计算cAMP/cGMP比值。

2 结果
2.1 各组大鼠一般状况比较 实验期间观察大鼠的状态,力竭游泳结束后,大鼠懒动无力,便溏,爪色青紫。注射T4后,大鼠情绪出现躁动,毛发枯黄,易脱落,饮水量、进食量增加,舌红,小便黄,大便稍变干。注射STZ后,毛发枯黄无光泽,易脱落,饮水量、进食量显著增加,舌色鲜红,小便多,大便干,色黑,呈现出气阴两虚的证候表征。给药后,阳性组大鼠毛发光泽度增强,脱落减少,自主活动正常,舌色红,爪色淡红,大便干,色黑。
2.2 各组大鼠体质量比较 对实验第1天和实验第33天的大鼠体质量进行比较,实验第33天,与空白组比较,模型组大鼠体质量显著降低(P<0.01)。阳性组与模型组比较,差异有统计学意义(P<0.01)。见表1。

表1 各组大鼠体质量比较
2.3 各组大鼠FBG比较 给药33 d后,与空白组比较,模型组大鼠FBG显著升高,差异有统计学意义(P<0.01)。与模型组比较,阳性组大鼠FBG显著降低,差异有统计学意义(P<0.05)。见表2。
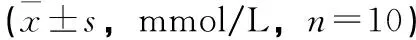
表2 各组大鼠FBG比较
2.4 各组大鼠饮水量、进食量、排尿量、排便量、肛温比较 与空白组比较,模型组大鼠饮水量、进食量、排尿量、排便量、肛温显著升高,差异有统计学意义(P<0.01)。与模型组比较,阳性组能使大鼠饮水量、进食量、排尿量、排便量、肛温降低,差异有统计学意义(P<0.01)。见表3。
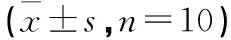
表3 各组大鼠饮水量、进食量、排尿量、排便量、肛温比较
2.5 各组大鼠糖耐量比较 与空白组比较,模型组大鼠AUC显著升高(P<0.01)。与模型组比较,阳性组大鼠AUC显著降低(P<0.01),差异有统计学意义。见表4。
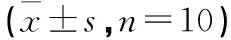
表4 各组大鼠糖耐量及AUC比较
2.6 各组大鼠FINS比较 与空白组比较,模型组大鼠FINS显著降低,差异有统计学意义(P<0.01)。阳性组大鼠FINS显著升高,与模型组比较,差异有统计学意义(P<0.01)。见表5。
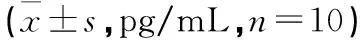
表5 各组大鼠FINS比较
2.7 各组大鼠HOMA-IR、HOMA-β、ISI比较 与空白组比较,模型组大鼠HOMA-IR显著升高,HOMA-β、ISI显著降低(P<0.01)。与模型组比较,阳性组大鼠HOMA-IR显著降低,HOMA-β、ISI显著升高(P<0.01),差异有统计学意义。见表6。
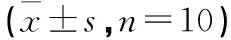
表6 各组大鼠HOMA-IR、HOMA-β、ISI比较
2.8 各组大鼠血脂四项比较 与空白组比较,模型组大鼠TC、TG、LDL显著升高,HDL显著降低,差异有统计学意义(P<0.01)。与模型组比较,阳性组大鼠TC、TG、LDL显著降低(P<0.01),HDL显著升高,差异有统计学意义。见表7。
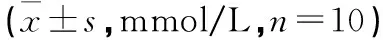
表7 各组大鼠血脂四项比较
2.9 各组大鼠T3、T4比较 与空白组比较,模型组大鼠T3、T4显著升高,差异有统计学意义(P<0.01)。与模型组比较,阳性组大鼠T3有下降趋势,T4显著降低(P<0.01)。见表8。
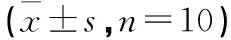
表8 各组大鼠T3、T4比较
2.10 各组大鼠cAMP、cGMP的影响 与空白组比较,模型组大鼠cAMP显著升高、cGMP显著降低、cAMP/cGMP显著升高(P<0.01)。与模型组比较,阳性组大鼠cAMP显著降低、cGMP显著升高、cAMP/cGMP显著降低(P<0.01,P<0.05)。见表9。
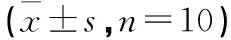
表9 各组大鼠cAMP、cGMP、cAMP/cGMP的影响
2.11 各组大鼠脾脏、胸腺指数比较 与空白组比较,模型组大鼠脾脏指数、胸腺指数显著降低(P<0.01)。与模型组比较,阳性组大鼠脾脏指数、胸腺指数显著升高,差异有统计学意义(P<0.01)。见表10。
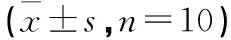
表10 各组大鼠脾脏、胸腺指数比较
2.12 各组大鼠力竭游泳时间比较 与空白组比较,模型组大鼠力竭游泳时间显著降低,差异有统计学意义(P<0.01)。阳性组能延长大鼠力竭游泳时间,与模型组比较差异有统计学意义(P<0.01)。见表11。
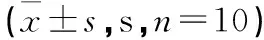
表11 各组大鼠力竭游泳时间比较
3 讨论
针对目前保健食品功能评价方法缺少中医功效评价,不能体现证候特点的问题,要实现辨证保健,就要先建立高血糖的证候模型。而糖尿病中医证候动物模型的建立周期较长,6~10周才能造成气阴两虚证,且模型的动物状态损伤较重,并不适合保健食品的功能评价,所以建立合适的中药类保健食品的降血糖功能评价方法至关重要[12]。本研究基于此,拟在2012年版辅助降血糖功能评价方法的基础上,结合中医对消渴症前期未病阶段的认识,建立气阴两虚型胰岛素抵抗糖脂代谢紊乱动物模型,探索适合中药保健食品辨证保健的辅助降血糖的评价方法[9]。
3.1 气阴两虚型胰岛素抵抗糖脂代谢紊乱模型造模方法的依据 糖尿病前期归于中医“脾瘅”范畴,主要由肺、脾、肾脏腑功能失调所致,但其根源在于脾胃功能受损。中医干预治疗时应注重辨证,首先应辨虚实:实证以湿热蕴脾、肝郁气滞为主,虚证以脾虚湿盛、气阴两虚为主。气阴两虚证是一种介于气虚和阴虚之间的复合证候,即气虚与阴虚的表现同时并见[13]。气虚,则体力下降,倦怠懒动,乏力懒言;阴虚,则五心烦热,咽干颧红,形体消瘦[14]。本实验采用比较经典的中医气虚证和阴虚证的造模方法,即强迫大鼠进行负重力竭游泳2周模拟中医劳倦伤脾所致气虚,并甲状腺素注射1周造成甲亢型阴虚,同时参考国家食品药品监督管理局2012年发布的《辅助降血糖功能评价方法》中糖脂代谢紊乱模型造模方法,即高脂喂养结合STZ注射,造模周期共33 d,建立多因素复合、病证结合、适合辨证保健的“气阴两虚型高血糖动物模型”[9,15-16]。
3.2 气阴两虚型胰岛素抵抗糖脂代谢紊乱模型大鼠血糖、血脂、胰岛素比较 实验结果表明,模型组大鼠FBG平均值为15.68 mmol/L,且0.5 h、2 h的血糖升高、血糖曲线下面积与空白组比较,均有显著性差异,判定糖代谢紊乱模型成立。模型组大鼠血清TC、TG、LDL显著升高,HDL显著降低,与空白组比较有显著性差异,判定脂代谢紊乱模型成立。同时,与空白组比较,模型组大鼠血清FINS显著降低,HOMA-IR显著升高,ISI、HOMA-β显著下降,说明模型组大鼠处于胰岛素抵抗状态。根据以上结果判断胰岛素抵抗糖脂代谢紊乱模型复制成功。
3.3 气阴两虚型胰岛素抵抗糖脂代谢紊乱模型大鼠中医证候表征比较 在本实验中,与空白组比较,模型组大鼠出现多饮、多食、多尿的“三多一少”症状,饮食量、饮水量、排尿量都显著升高,肛温也明显升高,能食,精神不振,毛发枯黄,无光泽,易脱落,体质量下降,舌色淡红等症状,与临床上气阴两虚证的症状相符,说明模型大鼠表现出气阴两虚证的证候表证。
cAMP与cGMP对细胞反应具有拮抗性的调节作用,与中医“阴”和“阳”的特点相似。测定血浆cAMP、cGMP水平及其比值,可以作为帮助判断临床辨证阴虚、阳虚的客观指标[17]。研究认为cAMP/cGMP升高说明机体处于一种阴虚状态[18]。T3、T4作为下甲状旁腺功能亢进轴中甲状腺分泌的关键激素,具有调节机体产热和能量代谢的作用,研究显示阴虚患者血清中T3、T4明显升高,T3、T4可能是阴虚证的证候指标之一[19]。有研究认为T3、T4可作为阴虚内热型糖尿病的证候指标[20-21]。在本实验中,模型组大鼠cAMP升高而cGMP降低,cAMP/cGMP比值显著升高,T3、T4显著升高,表明本实验模型组大鼠出现阴虚证候。
脾气虚则机体运化失常,线粒体能量代谢损伤,氧化磷酸化产生的ATP减少,产能减少,推动机体生命活动的能力下降,引起免疫器官萎缩,导致免疫功能低下,血清细胞因子水平降低[22-23]。在本实验中,模型组大鼠的脾脏指数、胸腺指数均显著降低,且模型组大鼠力竭游泳时间明显缩短,显示其耐力也明显下降,说明本实验模型组大鼠处于气虚证的状态。
3.4 以方测证 “以方测证”是依据“方证相应”理论,根据方剂的药物组成及效用,来推测其所治疗对象的病机或症状的方法[24]。以方测证作为一种中医认识病证的手段,一直是中医临床和基础研究中的重要方法之一[25]。以相应的方剂干预不同阶段的证,可使疾病的治疗更为精确,证和方是密不可分的[26]。在中医“证”的实验研究中,建立稳定的某一证候模型,再用相对应的基本方药进行干预,如果能改善或消除模型的症状和某些检测指标,则可佐证此模型成立[27-29]。
由于目前已上市的中药保健产品只有保健功能,没有证候的概念,不能作为阳性药物。故本实验以治疗消渴病气阴两虚证的十味消渴胶囊为阳性药物。十味消渴胶囊是已经上市的降糖中药复方制剂,由人参、黄芪、白术、山药、玉竹、熟地黄、麦冬、牛膝、茯苓、泽泻等药味组成,功能是益气养阴,生津止渴,主治消渴病气阴两虚证[30]。实验结果显示,十味消渴胶囊能显著增加气阴两虚型高血糖大鼠体质量,降低FBG,改善糖耐量,延长力竭游泳时间,提高机体耐力,降低血清中T3、T4的水平,降低环核苷酸系统cAMP、cAMP/cGMP比值,升高HDL含量,降低LDL、TG、TC的水平,提高血清中胰岛素含量,改善胰岛素抵抗,以及改善大鼠的气阴两虚证候的状态。十味消渴胶囊对模型大鼠各个指标都具有改善作用,以方测证,也佐证了本研究建立的气阴两虚型高血糖大鼠模型符合中医理论,与相应的中医证候一致,说明该造模方法是切实可行的。
本研究基于辨证保健的理念,根据中医对糖尿病前期气阴两虚证的认识,在保健食品《辅助降血糖功能评价方法》(2012年)的基础上,即高脂喂养结合STZ注射,造模周期共33 d,叠加力竭游泳和T4注射,建立多因素复合的病证结合“气阴两虚型高血糖动物模型”,造模设计在思路和方法上符合中医基本理论,且造模周期较短。判定指标在《辅助降血糖功能评价方法》(2012年)的基础上增加了中医气阴两虚证候的表证和指标,既能评价辅助降血糖的功能,又能评价益气养阴的中医功效,体现了中药保健食品辨证保健的特点。希望能在此模型的基础上,研究相应保健产品的干预作用,进一步验证辅助降血糖功能评价方法的可行性,为建立具有中医辨证特点的保健食品功能评价方法提供科学依据,以期在科学的评价方法基础上研发辨证保健食品,真正实现辨证保健,精准保健。

