Cuギ金属有机骨架中配位环境对类Fenton反应活性的影响
郭 彬 杨 静 卢文欣 王 鹏
(山东科技大学化学与生物工程学院,青岛266590)
随着超分子化学的发展,化学家们基于传统的配位化学中配位键的连接方式和配体配位取向的空间伸展调控,采用自组装的方式获得了环状、笼状等离散型配位分子结构,以及一维到三维的聚合型配位聚合物和多孔的金属有机骨架(metal-organic frameworks,MOFs)等新型结构的化合物。随着晶体学分析测试技术的提高和人们对其性质的不断研究,这些化合物的应用也从可调谐发光、二阶非线性光学、均相催化[1-2]等领域发展到了小分子气体吸附、存储与分离、选择性分离[3-6]乃至非均相催化领域[7-11]。MOFs是多孔结构的配位聚合网络(coordination polymerization networks,CPNs),由配位中心的金属阳离子或离子簇和有机配体组装聚合反应而构成,是一种具有周期性的晶态的多孔材料。MOFs不仅结合了有机配体和金属离子各自的特性且表现出其独特的特性,如具有空缺的金属位点,可与溶剂吸附材料结合,从而大大提高材料的吸附效果。同时,由于构成MOFs的有机配体和金属离子种类繁多,可以通过改变金属离子与有机配体的结构种类及二者之间的化学配位形式、有机配体的配位长度及结构修饰、合成材料的条件及应用方法等,使形成的MOFs的化学结构多种多样,从而具有不同的应用功能[12]。根据分子轨道理论,在MOFs中,有机配体构成了其电子的HOMO能级,而金属中心或金属簇构成了其LUMO能级,两能级间存在带隙,在一定条件下MOFs的金属中心和有机配体之间可以存在电荷迁移。并且相比于传统无机催化剂,MOFs还具有如下优点:具有超高的比表面积;具有灵活可调的孔道结构和带隙;同时MOFs中金属中心和配体间存在多种电荷转移形式以便于调节载流子行为[13]。以上特点和优势使MOFs在催化、生物、传感、气体储存、分子探针等方面有着广泛的应用[14-18]。
以负载在载体上、分散的金属原子为特征的单原子催化剂(single-atom catalysts,SACs)表现出相当的原子利用率和可控配位环境的特性[19-21],对诸多反应表现出优异的催化活性和很高的选择性[22],引起了人们广泛的关注。随着SACs的发展,化学家们认识到催化中心配位环境的结构对催化性能具有重要的影响。在大多数情况下,SACs的中心金属原子通过与来自载体材料的氮、硫、氧的配位相互作用,或金属-金属键等相互作用固定在载体上,固定的方式、紧密程度等均通过影响配位环境的方式产生不同的催化性能。近年来,通过对配位原子、配位数的改变,SACs的催化性能得到显著提高,这为SACs的进一步发展提供了新的机遇,如Ma等通过优化Niガ的配位微环境从而得到Ni1-S/UiO-66-NH2,其表现出优异的光催化制氢活性,高达原始MOF的270倍[23]。基于配位化学的认识,金属单原子基于配位键与载体上的锚定位点结合,金属中心周围的配位原子必然对其催化活性、选择性和稳定性有影响,通过改变金属中心的配位环境,在相同光催化环境下分析其催化活性,能够分析配位环境对配合物性能的影响[24]。
亚甲基蓝(MB)是一种广泛应用于纺织印染工业的染料,其降解性差且毒性较强。随着工业的发展,排放的MB废水越来越多,这不仅破坏水体环境还威胁人的生命安全,因此研究优良的催化剂以高效处理MB具有重要的现实意义。另一方面,MB具有较好的紫外吸收性质,也具有肉眼可见的蓝色,特别适合作为光降解过程中的污染物降解指针化合物,可以通过其光催化降解的速率来分析光催化条件以及催化剂性能的影响因素。Liu等基于MB的光降解过程报道了Cu-MOF的光催化降解性质[25]。因此,我们基于以前进行的Cuギ配合物光降解性质研究的工作,设计并合成了新型的Cuギ配合物,并进一步探究其配位环境对MB溶液的光降解性质的影响和作用机理。通过合成桥联吡啶类配体2,6-二(4′-吡啶基)-4-甲基苯胺(L),并将其单独或与间苯二甲酸(H2IPA)共同使用,与一水合醋酸铜分别合成了配位聚合物{[(Cu(OAc)2)2(L)]·3CH3CN}n(1)和{[Cu(IPA)(L)(H2O)]2·H2IPA·H2O}n(2),分析所得产物的不同配位环境对基于铜中心的类Fenton光催化反应的活性影响,探索配合物的结构、性质与金属原子配位环境之间的关联情况。通过MB溶液在可见光条件下的光催化降解实验对2个配合物作为光降解过程催化剂的活性进行对比,并通过与具有[CuO3]配位环境的HKUST-1催化效果对比,发现具有Cu—N配位环境的配合物1和2的催化效果优于只有Cu—O配位环境的HKUST-1。实验结果证明了金属原子的配位环境对其光催化性能有重要的影响,对配合物的光催化降解研究具有一定的指导意义。
1 实验部分
1.1 仪器和试剂
二氯甲烷、乙腈、水合肼、1,4-二氧六环等溶剂均为分析纯,未经纯化直接使用;三苯基膦、四(三苯基膦)氯化钯、吡啶-4-硼酸、碳酸铯、间苯二甲酸、一水合醋酸铜等金属盐和试剂为市售试剂,未经纯化直接使用。碳酸铯在使用前放置烘箱中烘干1 h,HKUST-1、2,6-二(4′-吡啶基)-4-甲基苯胺按照文献方法合成[26-27]。
红外光谱使用Nicolet IS50傅里叶变换红外光谱仪(KBr压片)测定。元素分析使用Perkin-Elemental 2400元素分析仪测定。电感耦合等离子质谱(ICP-MS)使用iCAP PQ质谱仪测定。光降解实验用光源为CEL-LPH120型低压汞灯光源系统,UV-Vis吸收光谱使用Hitachi UH4150型紫外可见分光光度计测试获得数据。
1.2 配合物1的合成
在试管中将含有醋酸铜(41.9 mg,0.21 mmol)的10 mL乙腈溶液铺于溶解了配体L(26.1 mg,0.1 mmol)的二氯甲烷溶液(10 mL)上,室温下静置至有绿色晶体析出,取出合适的晶体进行X射线单晶衍射分析,剩余部分继续反应至结晶完全(约需1周),过滤并用少量二氯甲烷-乙腈混合液洗涤,得到1的绿色晶体。IR(KBr,cm-1):3 488(m),3 393(m),3 074(w),2 360(m),1 610(s),1 450(s),1 364(m),1 071(m),845(m),685(m)。Cu2C29H33N5O8的元素分析(%,括号内为理论值):C,49.36(49.22);H,4.72(4.66);N,9.87(9.90)。
1.3 配合物2的合成
在试管中加入醋酸铜(21.0 mg,0.11 mmol)、配体L(26.1 mg,0.1 mmol)和 间 苯 二 甲 酸(16.6 mg,0.1 mmol),通过程序升温至180℃,维持96 h后逐步在144 h内降至室温。过滤并用少量二氯甲烷-乙腈混合液洗涤,得到2的蓝色晶体。IR(KBr,cm-1):3 401(m),3 356(m),3 076(w),2 341(m),1 628(s),1 433(s),1 221(m),1 019(m),804(m),682(m)。Cu2C58H50N6O15的元素分析(%,括号内为理论值):C,59.12(58.14);H,4.26(4.21);N,7.12(7.01)。
1.4 光催化降解实验
分别称量20 mg的1、2、HKUST-1与醋酸铜的固体,在100 mL质量浓度为20 mg·L-1的MB溶液中加入0.5 mL的30%H2O2溶液。超声振荡使其混合均匀,置于低压汞灯下搅拌,每间隔7.5 min取样,使用紫外分光光度计测其在664 nm处的吸光度,至吸光度为0时作为反应终止时间。以At/A0为纵坐标(At和A0分别为t时刻所测吸光度和初始吸光度),以测试时间t为横坐标作图进行比较。
1.5 配体L以及配合物1和2的晶体结构测定
选取合适尺寸的单晶,用Bruker公司的SMART APEX CCD单晶衍射仪,配体L、配合物1、2分别在293(2)、173(2)、293(2)K下,利用石墨单色化MoKα辐射(λ=0.071 073 nm)以φ-ω扫描方式收集衍射点,数据经经验吸收校正后使用SHELXTL软件包,采用直接法解出晶体结构,全部非氢原子坐标及各向异性热参数用全矩阵最小二乘法修正。非水分子上的氢原子的坐标由理论加氢方法得到,水分子上的氢原子坐标通过傅里叶合成方法确定,配合物1的晶体的结构解析及精修通过SHELXTL-2014软件包完成,配合物2的通过Olex2 1.2完成。晶体学数据列于表1,部分键长和键角列于表2,氢键参数则列于表3。
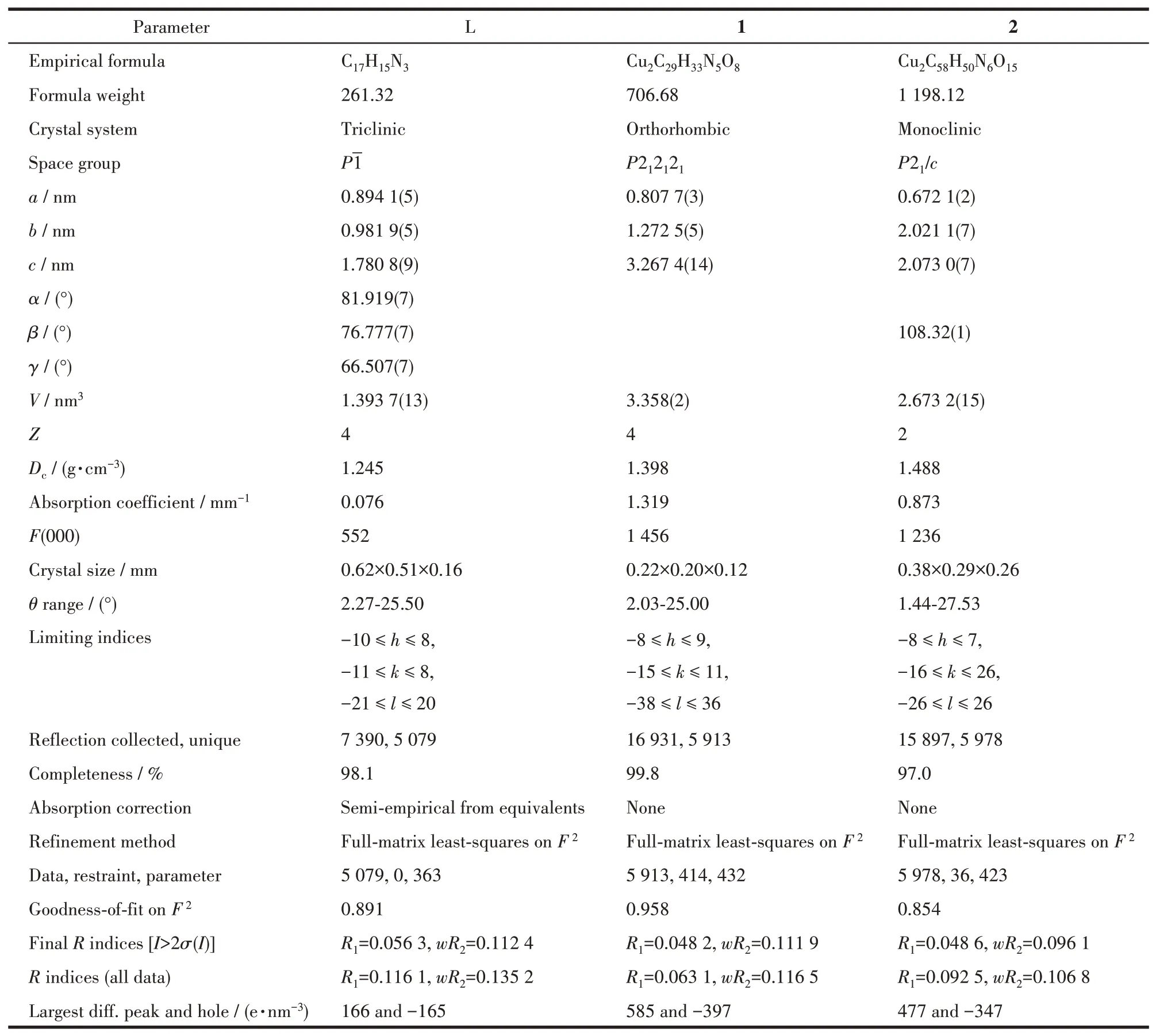
表1 配体L、配合物1和2的晶体学数据Table 1 Crystallographic data of ligand L,complexes 1 and 2
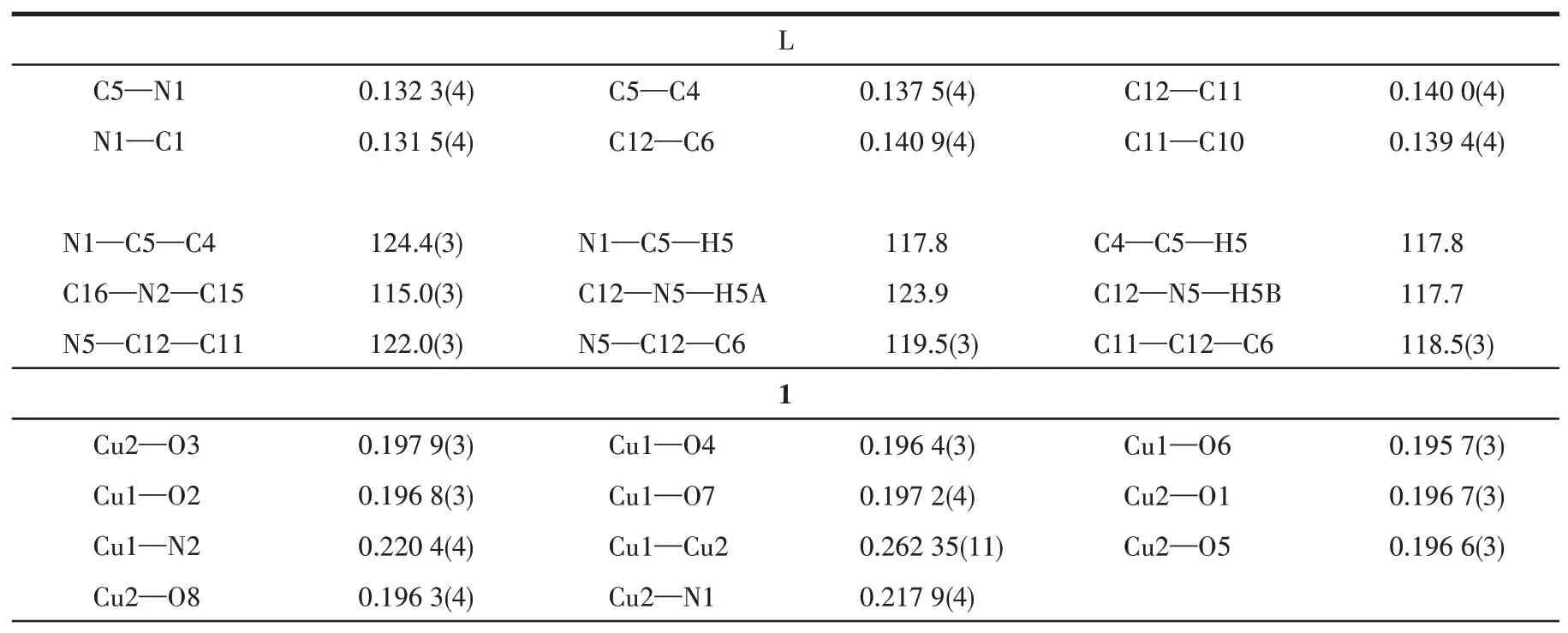
表2 配体L、配合物1和2的部分键长(nm)与键角(°)Table 2 Selected bond lengths(nm)and bond angles(°)for ligand L,complexes 1 and 2
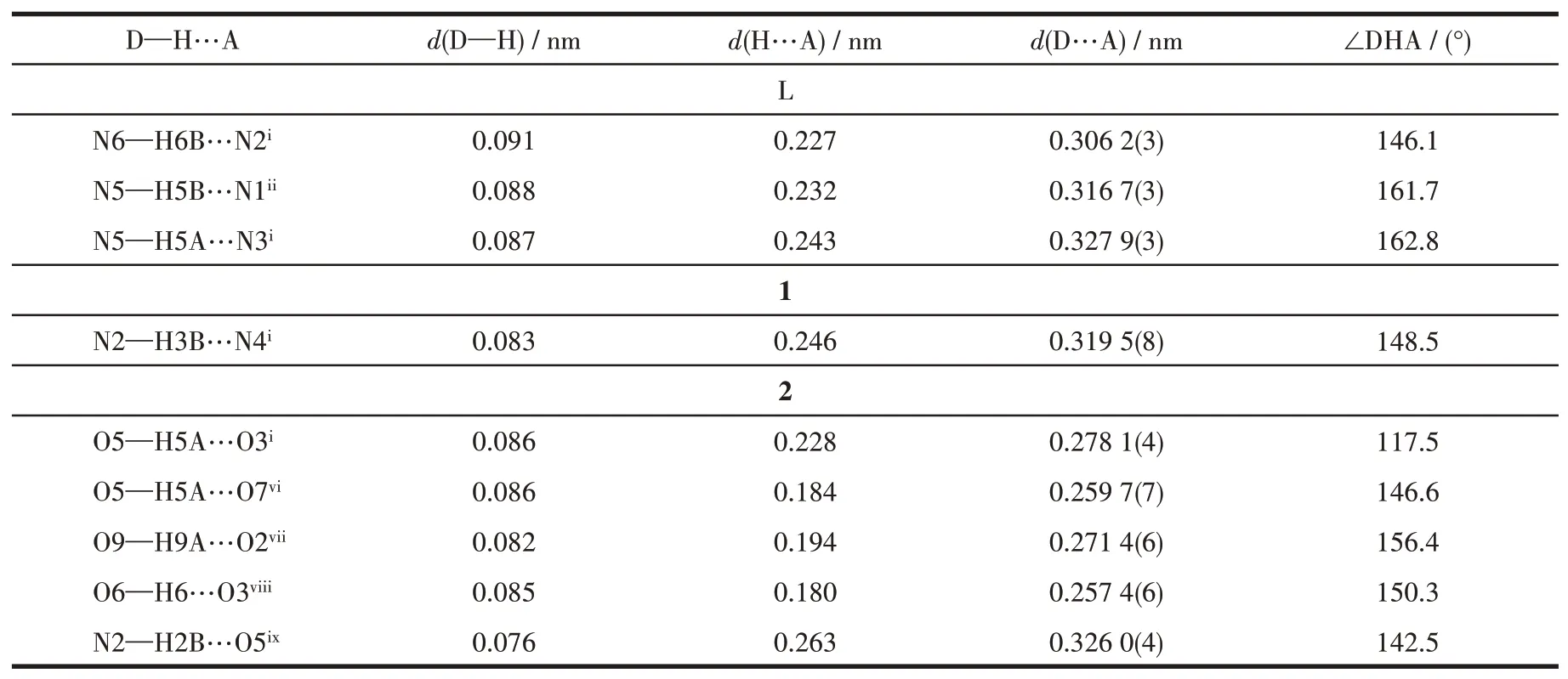
表3 配体L、配合物1和2的氢键参数Table 3 Hydrogen bond parameters for ligand L,complexes 1 and 2
CCDC:2178802,L;2178799,1;2178801,2。
2 结果与讨论
2.1 配体L的晶体结构
配体L结晶于三斜晶系P1ˉ空间群(图1a),其晶态下是多个通过氢键连接的2,6-二(4′-吡啶基)-4-甲基苯胺分子,如图1b所示。
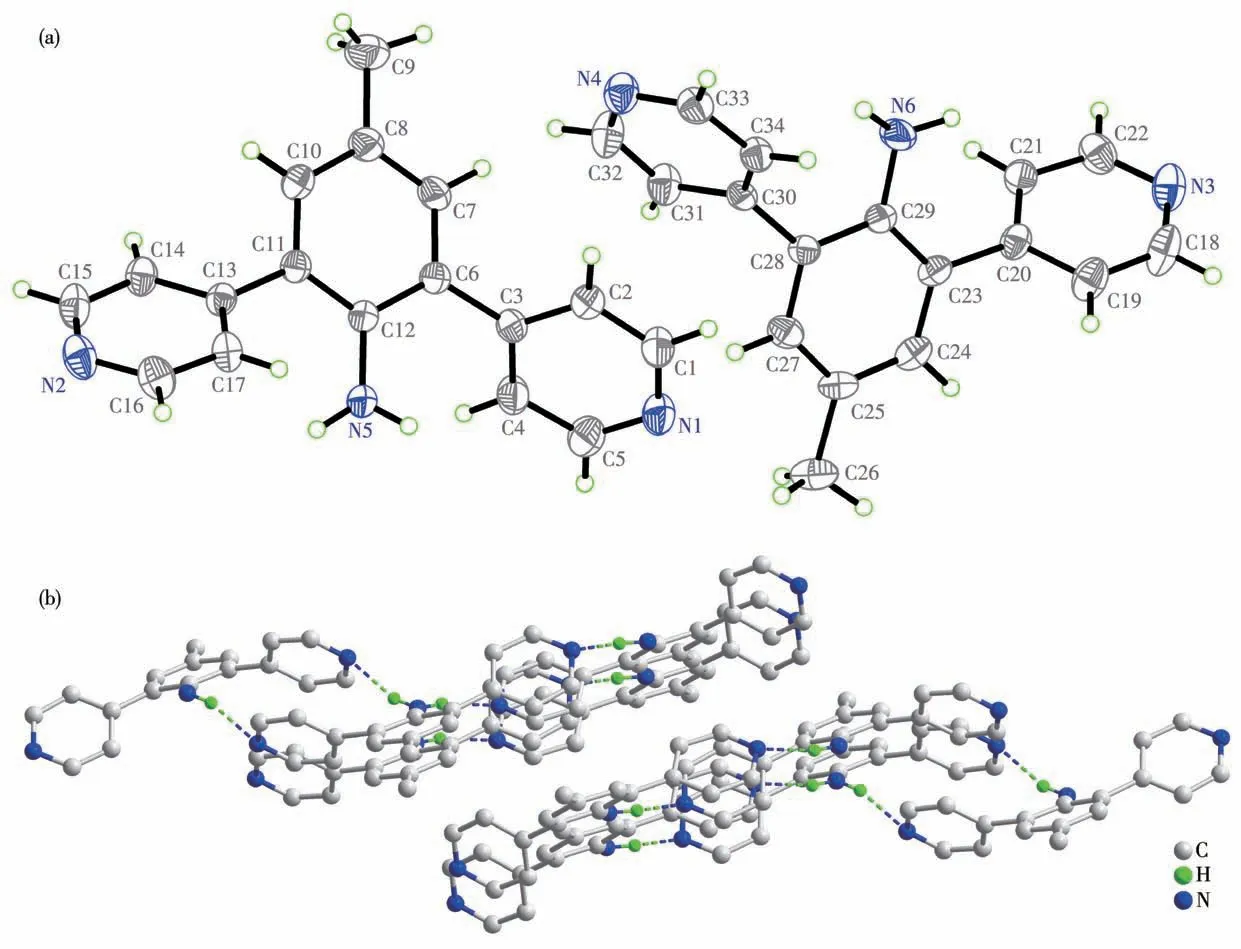
图1 配体L的椭球概率水平30%的不对称结构单元(a)和氢键连接的空间结构(b)Fig.1 Asymmetric structural unit with an ellipsoid probability level of 30%(a)and spatial structure linked by hydrogen bonds(b)of ligand L
2.2 配合物1的晶体结构
配合物1结晶于正交晶系P212121空间群,一个不对称结构单元中包含1个配体L、2个Cuギ离子和4个醋酸根离子(图2a)。如图2b所示,中心铜离子周围有1个氮原子、1个铜离子和4个氧原子,2个铜离子被4个醋酸根离子连接形成[Cu2N2O8]的双核簇结构。相邻的铜簇被配体分子连接形成一维折线形的长链结构。Cu1—N2和Cu2—N1的键长分别为0.220 4(4)和0.217 9(4)nm,Cu—O键长在0.195 7(3)~0.197 9(3)nm范围内,配体上2个吡啶环之间的平面夹角为20.44°,苯环和N1与N2所在的吡啶环之间的夹角均为41.45°。如图3所示,配合物中游离的乙腈分子通过氢键与配位聚合物长链相连接,这些氢键将溶剂分子固定在一维长链上,使得晶体中的溶剂分子较为稳定地存在于长链之间,形成了图4所示的结构。
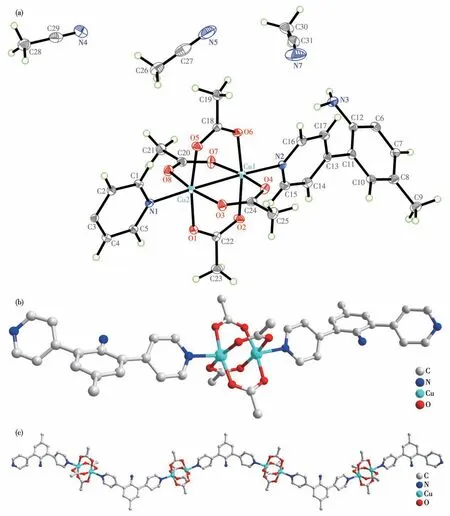
图2 配合物1的结构:(a)椭球概率水平30%的不对称结构单元;(b)Cuギ的配位环境;(c)一维折线结构Fig.2 Structure of complex 1:(a)asymmetric structural unit with an ellipsoid probability level of 30%;(b)coordination environment of Cuギ;(c)1D broken line structure
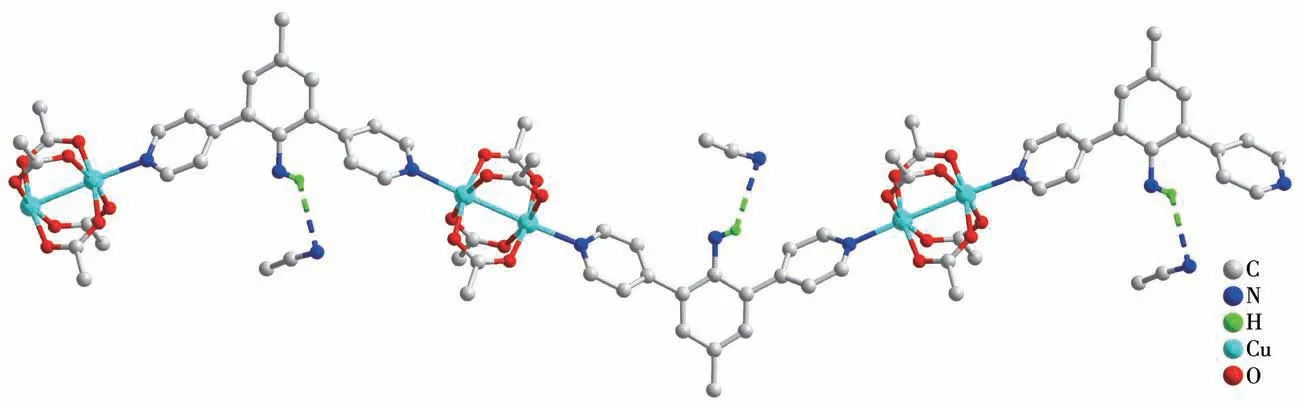
图3 配合物1的一维长链上以氢键相连的溶剂分子Fig.3 Solvent molecules linked with 1D chain in complex 1 by hydrogen bonds
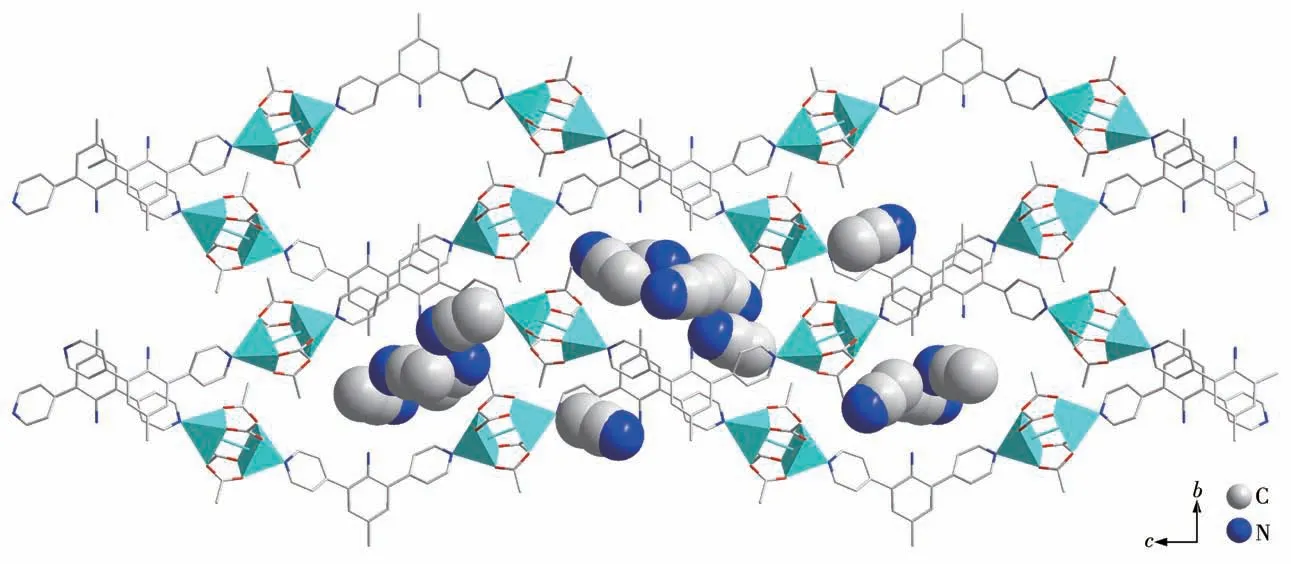
图4 沿a轴观察到的配合物1中的溶剂分子Fig.4 Solvent molecules in complex 1 viewed along the a-axis
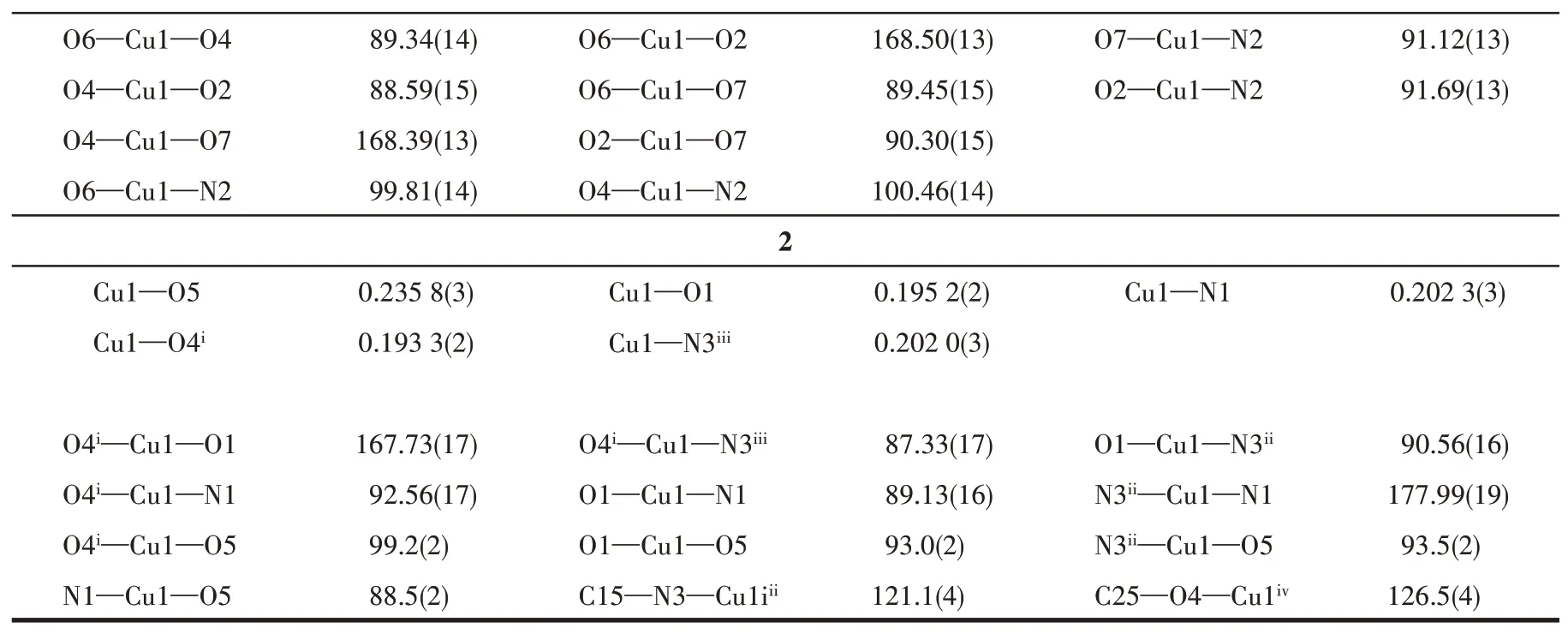
续表2
2.3 配合物2的晶体结构
配合物2结晶于单斜晶系P2/n空间群,其不对称结构单元包含1个配体L分子、1个铜离子、1个间苯二甲酸根离子和1个水分子(图5a)。如图5b所示,中心铜离子被3个氧原子和2个氮原子包裹,处于[CuN2O3]配位环境的中心。Cu1—O5键长为0.235 0(3)nm,Cu1—N1和Cu1—N3iii的键长分别为0.202 3(3)和0.202 0(3)nm。如图6所示,相邻的2个铜离子被2个配体L与2个IPA2-离子连接围成一个环状结构单元,结构单元之间通过铜中心相互连接形成二维网状结构。相邻的网状结构之间存在氢键(N2—H2B…O5ix),通过这些氢键的相互作用堆积形成三维结构,如图7所示。
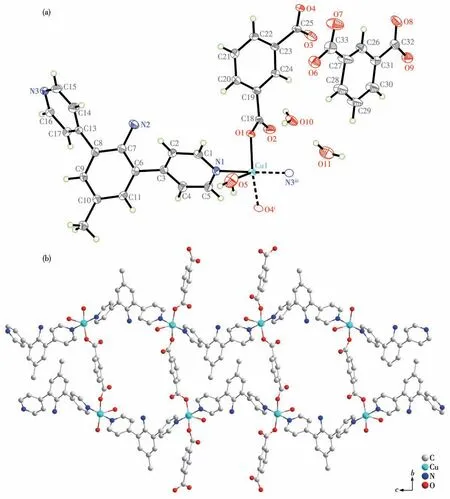
图5 配合物2的椭球概率水平30%的不对称结构单元(a)及其二维结构(b)Fig.5 Asymmetric structural unit with an ellipsoid probability level of 30%(a)and 2D structure(b)of complex 2
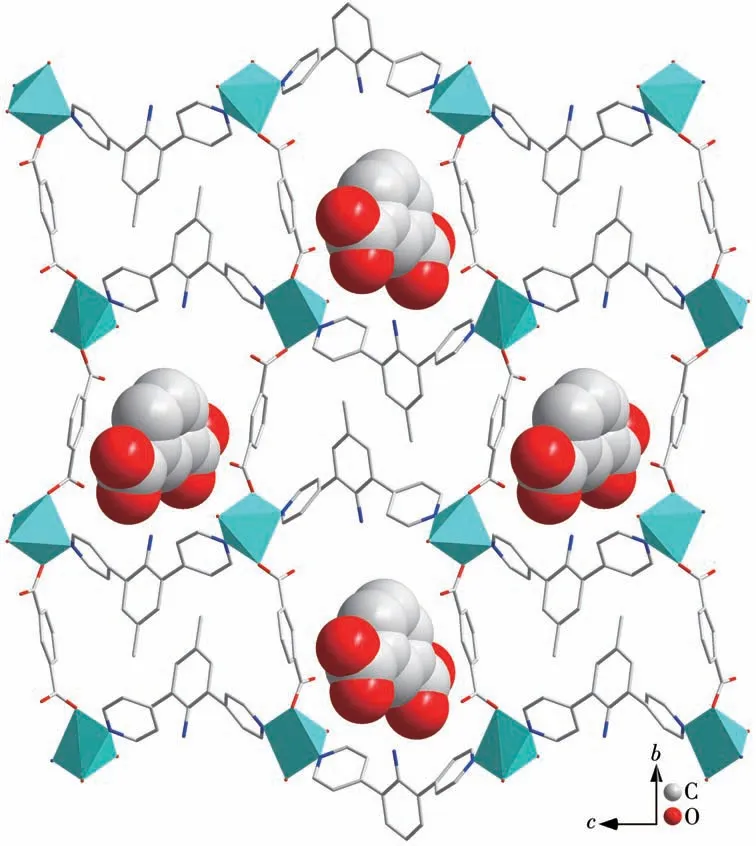
图6 沿a轴观察到的配合物2中环内的IPA2-离子Fig.6 IPA2-ions in the ring of complex 2 viewed along the a-axis
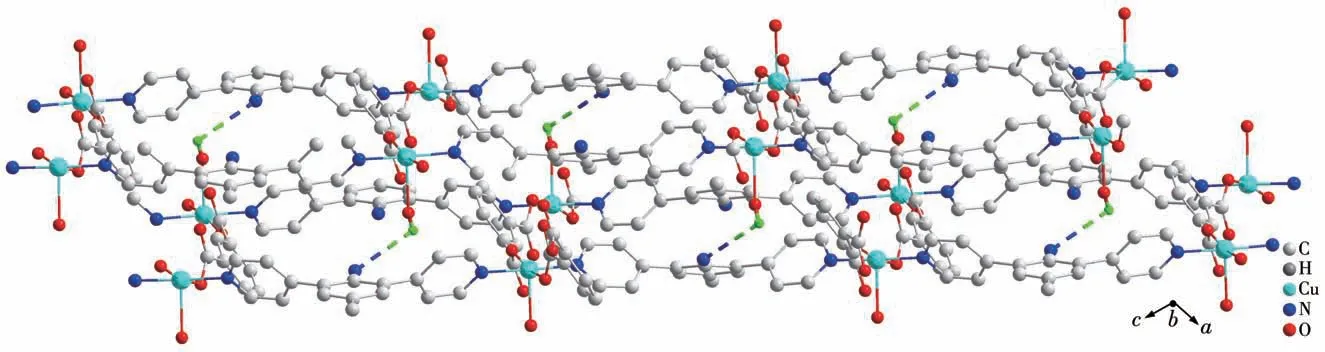
图7 沿b轴观察到的配合物2通过氢键相连的两个环状分子Fig.7 Two cyclic molecules connected by hydrogen bonds in complex 2 viewed along the b-axis
2.4 配合物1和2的UV-Vis光谱
以BaSO4为参考测量了配合物在200~800 nm范围内的紫外可见漫反射(UV-Vis DRS)光谱。如图8所示,除了516和492 nm附近的吸收边缘外,也可以检测到配合物1和2在558~800 nm和522~754 nm区域内的其它吸收带,这表明基于MOFs的光催化剂具有很强的可见光捕获能力。半导体的禁带宽度(HOMO与LUMO的能级差,Eg)通过以下公式计算:αhν=A(hν-Eg)1/2,其中α、h、ν、Eg和A分别是吸收系数、普朗克常数、入射光子频率、半导体禁带宽度(带隙)和常数。根据上述公式得到的曲线的线性区域外推切线的x轴截距,得到配合物1和2的Eg分别为2.92和2.70 eV(图9)。
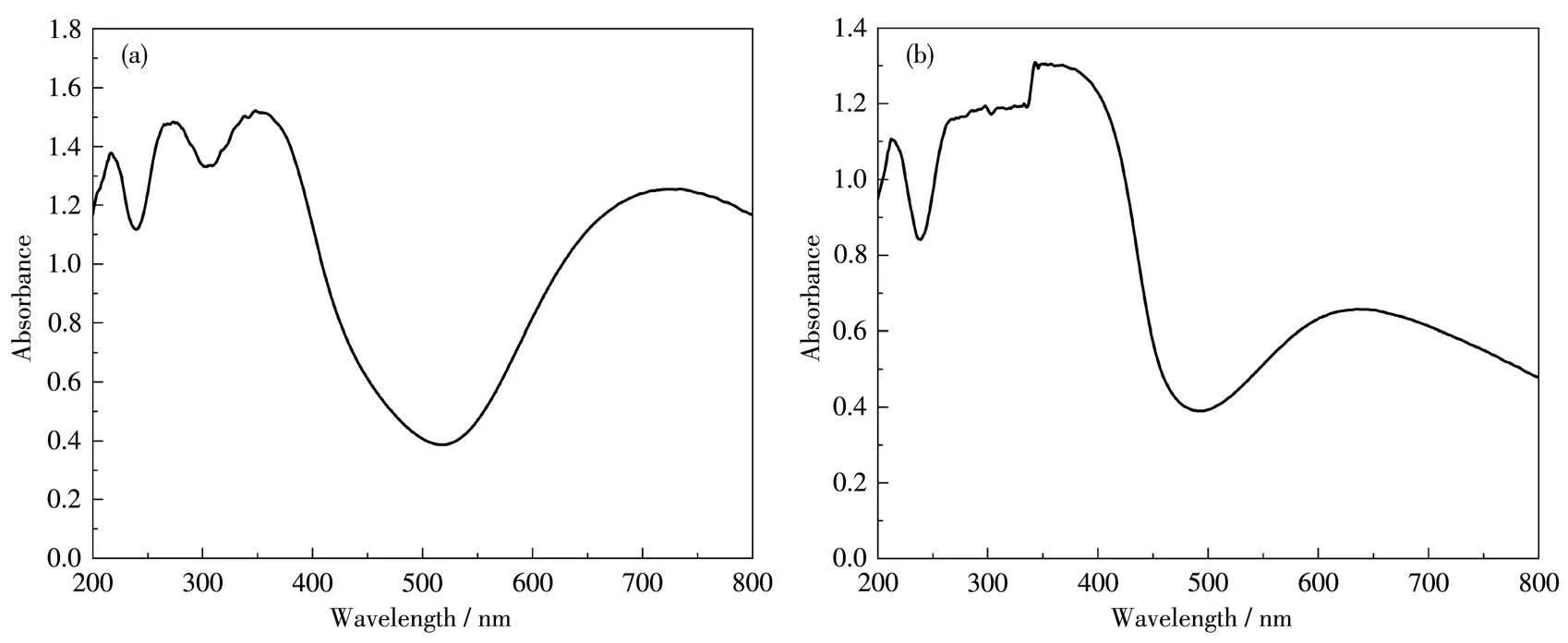
图8 配合物1(a)和2(b)的UV-Vis DRS谱图Fig.8 UV-Vis DRS spectra of complexes 1(a)and 2(b)
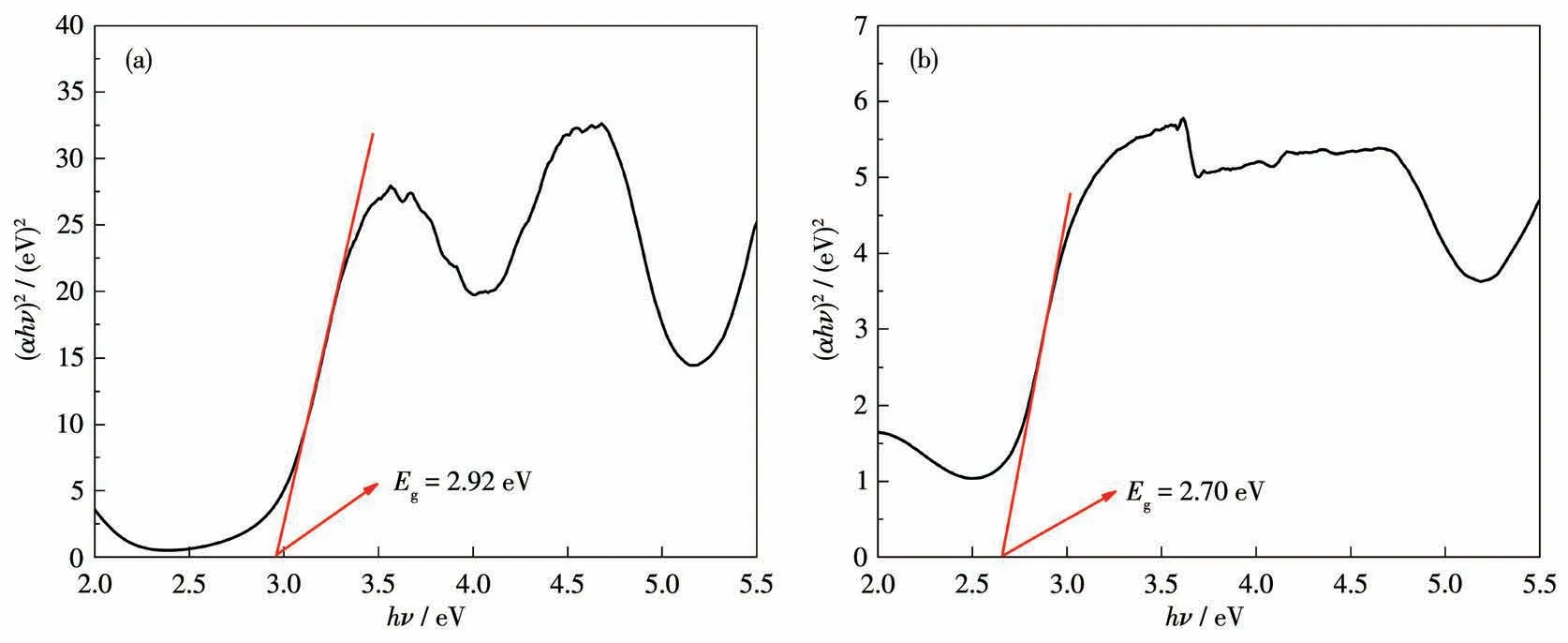
图9 配合物1(a)和2(b)的禁带宽度Fig.9 Band gaps of complexes 1(a)and 2(b)
2.5 配合物1和2及HKUST-1对MB的光催化降解性质
据文献报道,铜基MOFs或者配合物具有光催化降解有机物的性质[28],同时考虑到不同配位环境的配合物有不同的催化性质,我们猜测配合物1和2在溶液中有可能具有不同的光催化活性。因此,我们采用染料MB对配合物1和2进行了光催化降解活性的探究,并与纯醋酸铜和HKUST-1作为光催化剂的体系进行了对比。以MB的最大UV-Vis吸收峰(664 nm)作为检测的基准,通过该处的吸光度的变化表征其光催化效果,如图10所示。通过测试每次取样后MB的吸光度与初始吸光度的比值计算其降解效率,结果显示配合物1和2在反应15 min后分别能达到93%和69%的降解效率,二者均具有比HKUST-1和醋酸铜更好的催化效果,这说明我们合成的配合物均有光催化降解效果,且通过调整中心金属原子的配位环境能够改变其光催化的效率。同时配合物2在光催化降解方面的活性强于配合物1。考虑到MOFs比醋酸铜拥有更稳定的性质和可回收利用的特性,因此我们对配合物1和2进行了重复实验。如图11所示,经过5次循环以后配合物1和2在60 min内仍可以催化降解MB完全。通过ICP-MS对5次光催化反应后来自催化剂的金属离子进行检测。配合物1和2催化后的MB水溶液中Cuギ的质量浓度分别为0.849和1.282 mg·L-1。因此,配合物1和2中金属离子的损失率分别为2.36%和5.83%(表4),这表明2个配合物在MB光降解过程中保持稳定。通过循环前后的XRD图(图12a和12b)可以看出,配合物1较好地保持了其晶相,而配合物2存在微量的分解,形成了CuO的粉末衍射峰[29]。这说明配合物1和2有着较好的稳定性和可重复利用性。为了了解配合物1和2对MB的光催化降解机理[30],在不同的清除剂如叔丁醇(TBA,·OH清除剂)、三乙醇胺(TEOA,h+清除剂)和苯醌(BQ,·O2-清除剂)存在下进行了光催化降解实验。如图13所示,当BQ、TEOA和TBA存在时,对于配合物1和2,MB的降解效率分别下降到了91.3%、55.2%、37.1%和87.9%、61.4%、41.3%。实验结果表明,·OH是主要的反应物种,h+和·O2-对MB的降解有一定的贡献。根据上述实验结果推测了光催化机理。当光催化剂在可见光(能量不低于2.92、2.70 eV)下被激发时,电子从价带激发到导带,在价带中留下h+。光激发的h+直接与染料分子反应分解成小分子,或与OH-反应生成·OH用于进一步的氧化反应。生成的e-与O2反应生成·O2-或与H2O2生成·OH,然后直接氧化染料产生CO2、H2O或其他小分子。
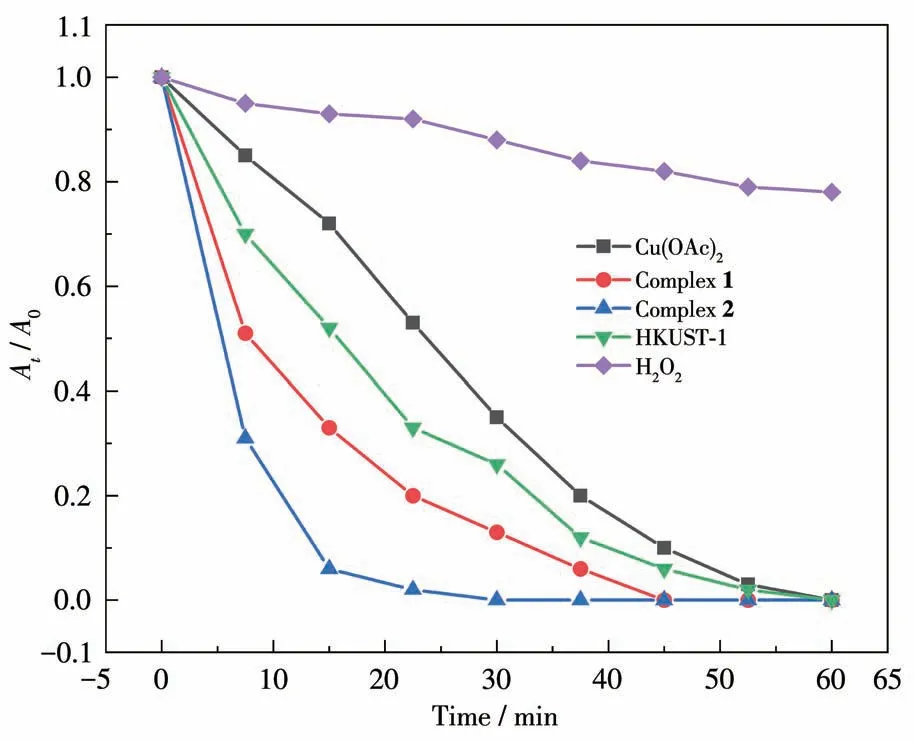
图10 配合物1、2和HKUST-1与醋酸铜对MB光催化降解的效果对比Fig.10 Comparison of the effects of complexes 1,2,and HKUST-1 and copper acetate on the catalytic photodegradation of MB
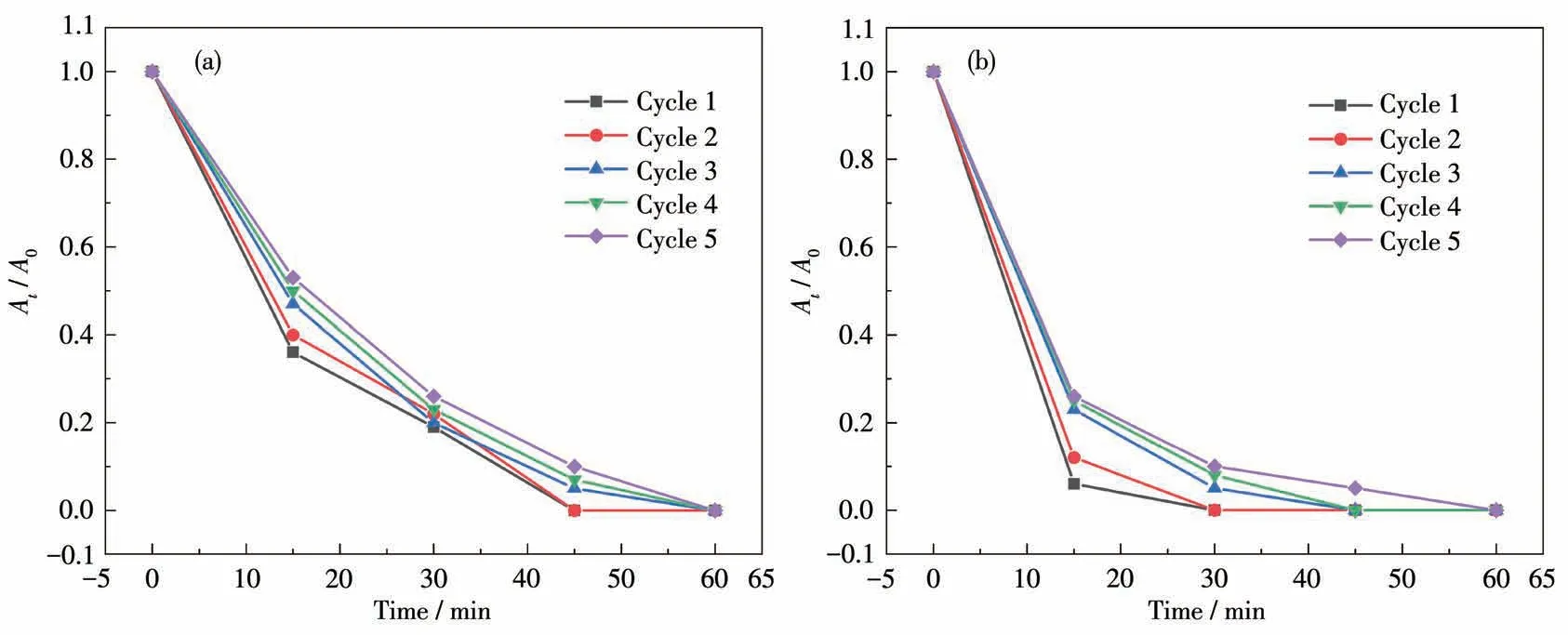
图11 配合物1(a)和2(b)的循环测试Fig.11 Cyclic testing of coordination complexes 1(a)and 2(b)
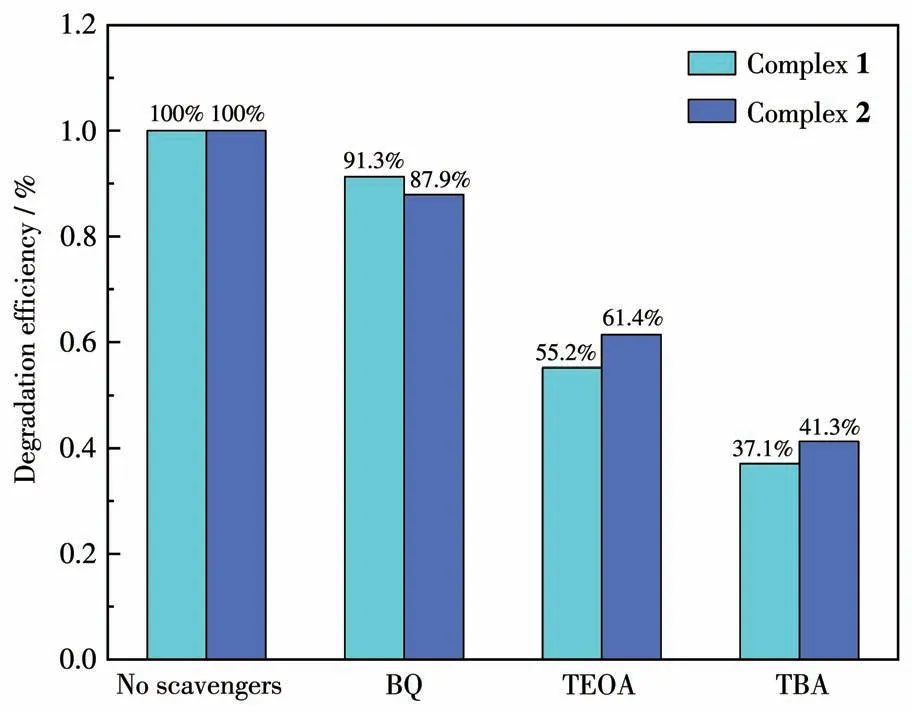
图13 在清除剂BQ、TEOA和TBA的存在下配合物1和2降解MB的催化效率Fig.13 Catalytic efficiency of complexes 1 and 2 for MB degradation in the presence of scavengers BQ,TEOA,and TBA

表4 ICP-MS测定的光催化后MB水溶液中铜离子的质量浓度Table 4 Copper ion mass concentration in MB aqueous solution after photocatalysis determined by ICP-MS*
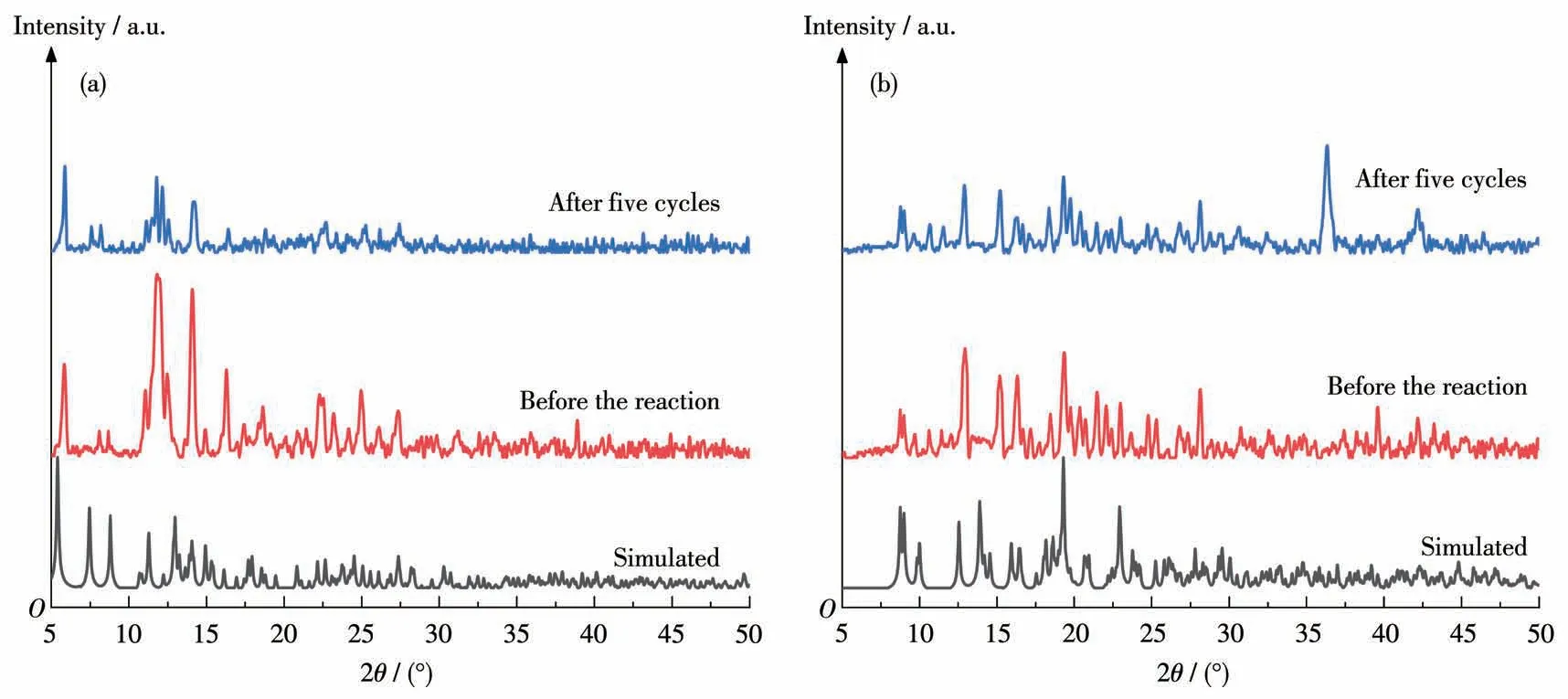
图12 配合物1(a)和2(b)在光催化之前和循环五次之后的XRD图Fig.12 XRD patterns of complexes 1(a)and 2(b)before the photocatalysis and after five cycles
通过对比实验可以证实,金属离子的配位环境对配合物的光催化性能有着较大的影响,对比不同配位环境的配合物1、2和HKUST-1,配合物1和2因存在键长更长的Cu—N、Cu—O键而表现出比HKUST-1更好的催化效果,更长的键长意味着反应过程中该键更容易断裂从而有更好的催化活性。且由于这2种催化剂有更窄的带隙,在可见光下很容易被激发形成电子和空穴,而电子和空穴会扩散到催化剂表面,与吸附在催化剂表面的电子受体或电子供体发生氧化还原反应,形成光催化反应中的活性基团,引发一系列化学反应。多次循环实验证明配合物1和2仍具有很好的催化活性,反应后的ICP-MS和XRD的测试也表明催化剂有着较好的稳定性,可多次重复利用。
3 结论
通过对比配合物1、2、HKUST-1和醋酸铜的光催化实验的结果,发现在金属离子周围组织良好的光敏单元和邻近的催化位点对于提高配合物电荷分离效率以及促进光催化性能至关重要。配合物1和2中铜氮氧协同的配位结构、HKUST-1中的铜氧配位结构均比无配体约束的醋酸铜盐的催化活性要高得多,意味着这些被配体分散固定的光敏单元大大加速了电荷的转移,提高了催化效率。同时配合物1和2中的氮-铜-氧簇的三元配位结构提供了比HKUST-1中的铜-氧二元配位结构更好的催化位点,这意味着其三元结构可能更容易促进铜离子对双氧水类Fenton反应的催化。

