一种席夫碱Al3+荧光探针的制备及细胞成像应用
陈 曦李思媛王 元吴伟娜*,陈 忠*,
(1河南理工大学化学化工学院,焦作454000)
(2江西科技师范大学材料与机电学院,南昌330013)
0 引言
铝是地球上储量第三大的金属(约占地球重量的8%)。因其具有低密度、抗腐蚀和导热快等优点,铝制品被人们大量制造及使用,从而导致环境、生物体内Al3+过量残留[1]。研究表明,当人体摄入过高含量的Al3+时,会引发许多器官功能障碍,导致相关疾病,如痴呆症、贫血、阿尔茨海默病、骨关节炎等[2-3];在水体中过量蓄积的Al3+同样会导致水生生物的死亡。因此,对环境、生物体内Al3+的快速检测尤为重要[4-6]。
目前,Al3+的测定方法主要有原子吸收光谱法、离子色谱法、电感耦合等离子体法等[7]。其中,荧光探针检测法因具有操作简单快捷、可视性强、识别作用专一性强、灵敏度高、响应时间短、可进行活体分析和在线监测等优点而备受关注[8]。因此,针对Al3+的荧光探针取得了一定进展[9-10],现有探针通常利用萘[11-13]、氟硼二吡咯(BODIPY)[14]、香豆素[15-16]或罗丹明[17-18]作为荧光团,辅以连接基和识别位点构建。然而,这些荧光基团由于较大的分子量与复杂的合成步骤,在检测生物性能与成本上受到一定的限制。相比之下,席夫碱类化合物简便易得[19],是目前Al3+探针研究的热点。席夫碱结构中的碳氮双键(C=N)可以与Al3+配位,从而阻止了C=N的异构化,使得体系荧光增强而实现检测[20-21]。此外,因Al3+具有较高的离子水化能,可在缓冲体系中检测Al3+且应用于细胞成像的席夫碱荧光探针数量有限。
基于此,我们通过一步缩合反应,高效制备了一例席夫碱类荧光探针1(图1)。在DMSO/H2O(2∶8,V/V)体系中,探针1可特异性与Al3+配位,导致体系荧光显著增强,同时伴随明显的颜色改变。探针1对Al3+检测灵敏度高,检出限低至1.44 μmol·L-1。通过核磁滴定、质谱分析和理论计算研究了探针与Al3+的配位模式和荧光传感机理,并将其应用于活细胞内Al3+的检测。
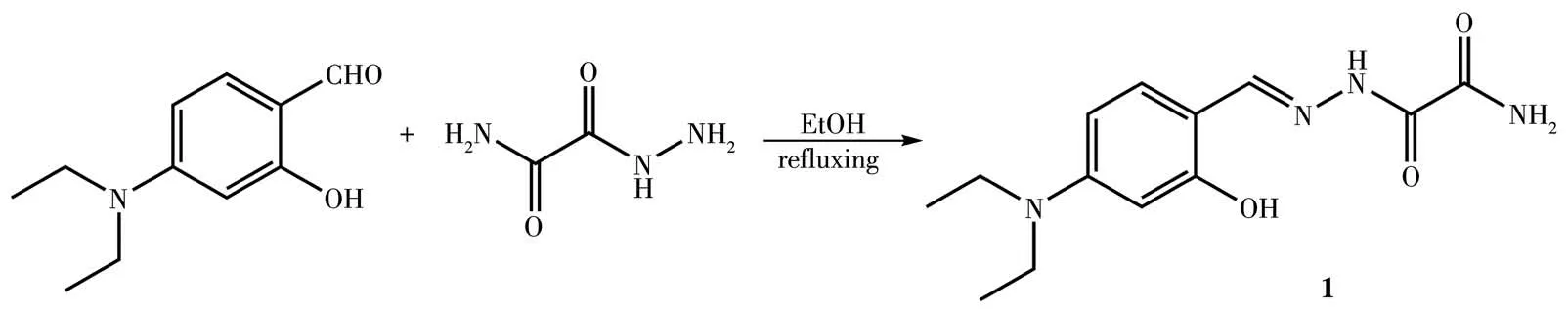
图1 探针1的合成路径Fig.1 Synthetic route of probe 1
1 实验部分
1.1 试剂和仪器
所有用于实验合成的试剂都可以通过商业公司进行购买并直接使用,无需进一步的处理与纯化。光谱性质测试中,所有溶剂如二甲亚砜(DMSO)等为光谱纯试剂,购自Macklin公司,水为MILIPORE处理过的超纯水。元素分析在Vario EL元素分析仪上进行。NMR谱在Bruker AV400 NMR核磁共振仪上测得。荧光光谱在Varian CARY Eclipse分光光度计上测定。电喷雾电离质谱(ESI-MS)在Bruker Daltonics Esquire 6000质谱仪上获得。在Zeiss Leica倒置落射荧光/反射激光共聚焦扫描显微镜上获得荧光图像。pH值用PHS-3精密pH计记录。荧光光谱数据用Origin软件包处理。
1.2 探针1的合成
将0.193 g(1 mmol)4-(二乙氨基)水杨醛和0.103 g(1 mmol)奥肼以100 mL无水乙醇溶解。在250 mL圆底烧瓶内加热回流,90℃下反应4 h,点板监测反应过程。反应完成后,冷却至室温,有黄色固体析出,抽滤得到产物并用无水乙醇洗涤,得到黄色固体。1H NMR(400 MHz,DMSO-d6):δ12.13(s,1H,NH),11.31(d,J=15.15 Hz,1H,OH),8.51(d,J=5.05 Hz,1H,CH=N),8.26(s,1H,NH2),7.39(s,1H,NH2),7.15~7.99(dd,J=6.07 Hz,2H,NH2),6.26(m,3H,Aryl-H),3.33~3.38(d,J=9.02 Hz,4H,2CH2),1.08~1.11(t,J=6.76 Hz,6H,2CH3)。13C NMR(101 MHz,DMSO-d6):δ162.26,160.37,156.29,152.85,150.92,132.37,106.68,104.25,97.85,44.28,12.99。C13H18N4O3元素分析计算值(%):C 56.10,H 6.52,N 20.13;实验值(%):C 56.18;H 6.28;N 20.24。ESI-MS:m/z=279.151 4[M+H]+。
1.3 探针1的光谱性能测试
将探针1溶于DMSO制得1 mmol·L-1的探针储备液。探针1的Al3+荧光滴定实验检测体系为DMSO-H2O(2∶8,V/V,pH=7.4)。移取20 μL的探针储备 液,加 入 适 量Al(NO3)3水 溶 液(1 mmol·L-1),用DMSO定容至5 mL,充分混匀后进行荧光测试。
1.4 金属离子选择性实验
金属离子选择性及Al3+与碱金属、碱土金属的竞争性实验都在上述DMSO-H2O体系中进行。将AgNO3、Al(NO3)3、Ca(NO3)2、Cd(NO3)2、Co(NO3)2、CrCl3、Cu(NO3)2、Fe(NO3)3、HgCl2、KNO3、Mg(NO3)2、MnCl2、NaNO3、Ni(NO3)2、Pb(NO3)2、Zn(NO3)2分别溶解,配制成浓度为1 mmol·L-1的金属储备液。激发波长为390 nm,狭缝宽度为5 nm。
在探针1对常见金属离子选择性实验中,向2 mL的DMSO-H2O体系中加入20 μL浓度为1 mmol·L-1的探针1溶液到比色皿中,依次分别加入60 μL Al3+(1 mmol·L-1)和60 μL其 它 常 见 金 属 离 子(1 mmol·L-1),测定495 nm处的荧光强度。在Al3+识别实验中,在2 mL的DMSO-H2O体系中,取20 μL浓度为1 mmol·L-1探针1到比色皿中,用微量进样器不断加入Al3+溶液,测定495 nm处的荧光强度。在竞争实验中,向2 mL DMSO-H2O体系中加入20 μL浓度 为1 mmol·L-1的 探 针1溶 液 和60 μL浓 度 为1 mmol·L-1的Al(NO3)3水溶液,然后再分别加入80 μL浓度为1 mmol·L-1的阳离子溶液:Ag+、Ca2+、Cd2+、Co2+、Cr3+、Fe3+、Hg2+、K+、Mg2+、Mn2+、Na+、Ni2+、Pb2+、Zn2+,充分混合后,记录光谱。
1.5 细胞毒性和成像实验
选用Hela细胞为研究对象,在培养有Hela细胞的培养皿中分别加入浓度为0、10、20、30和40 μmol·L-1的探针1,37℃下培养24 h后,通过MTT法测定细胞活力。
将探针1(20 μmol·L-1)孵育的Hela细胞加入到含有10%胎牛血清的Dulbecco改良Eagle培养基(DMEM)中培养30 min,用空白培养基清洗3次,除去过量探针,进行荧光共聚焦成像。加入20 μmol·L-1的Al3+,在37℃培养30 min后,再次进行荧光成像。
2 结果与讨论
2.1 探针1对常见金属离子识别
首先,我们测定了探针1与常见金属离子的荧光响应。在DMSO-H2O(2∶8,V/V,pH=7.4)的溶液中,探针1(20 μmol·L-1)在390 nm激发波长下无荧光。当加入Al3+后,在495 nm处峰值明显升高,体系荧光强度增加。且在365 nm的紫外灯下,肉眼可观察到溶液由无色变为蓝绿色(图2a插图)。除Zn2+能够引起探针溶液荧光轻微增强(约为加Al3+时强度的1/8),其它离子如Ag+、Ca2+、Cd2+、Co2+、Cr3+、Fe3+、Hg2+、K+、Mg2+、Mn2+、Na+、Ni2+和Pb2+,对探针荧光发射无影响。故该探针可实现对Al3+的选择性识别。可以作为开启型Al3+荧光探针。
其次,测定了探针1与Al3+的反应时间,如图2b所示。实验结果显示,将探针1溶解到DMSO-H2O体系,加入60 μmol·L-1的Al3+溶液后,其495 nm处的荧光强度随时间的增加明显增强,20 min后荧光强度达到峰值。因此,探针1对Al3+的响应时间为20 min。
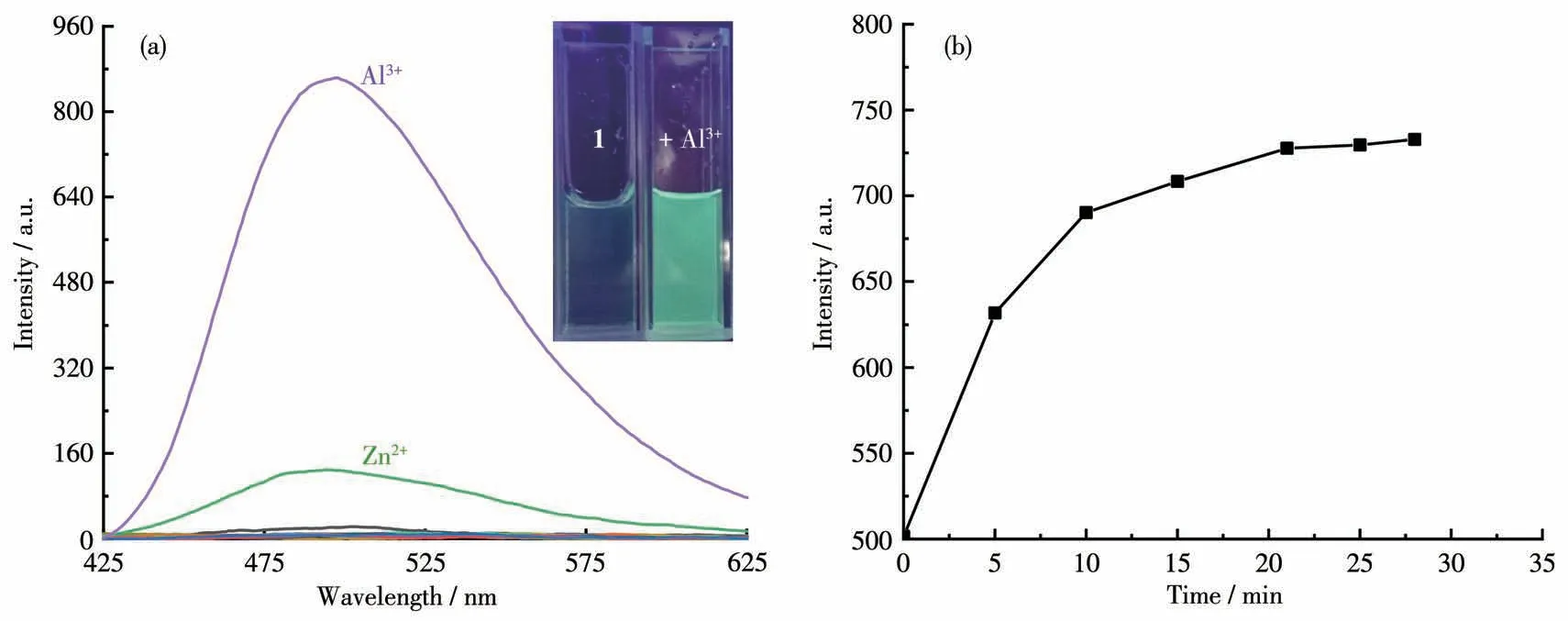
图2 (a)探针1在无金属离子和加入60 μmol·L-1不同金属离子后495 nm处的荧光强度;(b)探针1加入60 μmol·L-1 Al3+后495 nm处荧光强度随时间变化的曲线Fig.2(a)Fluorescence intensity of probe 1 before and after addition of 60 μmol·L-1 different metal ions;(b)Time-dependent fluorescence intensity of probe 1 at 495 nm upon treatment with 60 μmol·L-1 Al3+
2.2 探针1对溶液中的Al3+的识别
我们测试了不同的Al3+加入量(每次加入2 μL)对探针1的荧光光谱的影响,结果如图3所示。荧光光谱图表明,随着Al3+加入量的增大,探针1在495 nm处的荧光强度上升。当加入40 μmol·L-1的Al3+时,495 nm处的荧光强度升为最高;将Al3+浓度继续增加至60 μmol·L-1,荧光强度也基本保持不变。测试了探针1与Al3+反应后的荧光强度与Al3+浓度的关系。如图3插图所示,经过线性拟合可得线性回归方程:y=25.908 66+19.748 88x,R2=0.991 94,说明探针可以定量检测Al3+。经计算得出检出限LOD=3σ/k=1.44 μmol·L-1(σ指空白标准偏差,k是线性方程的斜率),这远远低于世界卫生组织规定的Al3+最高允许水平(7.41 mmol·L-1)[22]。
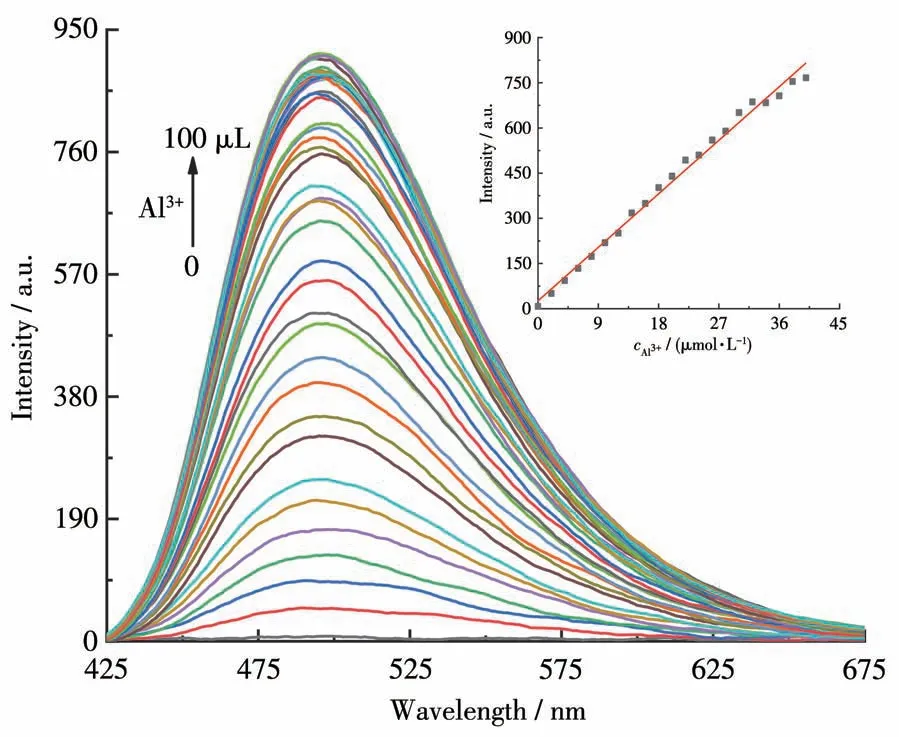
图3 加入不同浓度的Al3+后探针1的荧光光谱Fig.3 Fluorescence spectra of probe 1 upon addition of Al3+with different concentrations
2.3 探针分子的抗干扰能力
探针分子在实际应用中容易受到多种因素的荧光强度干扰。如图4所示,向探针1-Al3+体系内分别加入60 μL浓度为1 mmol·L-1的Ag+、Ca2+、Cd2+、Co2+、Cr3+、Fe3+、Hg2+、K+、Mg2+、Mn2+、Na+、Ni2+、Pb2+、Zn2+,其均对体系荧光发射无明显影响。这一结果说明探针1对Al3+的检测具有较强的抗干扰能力。
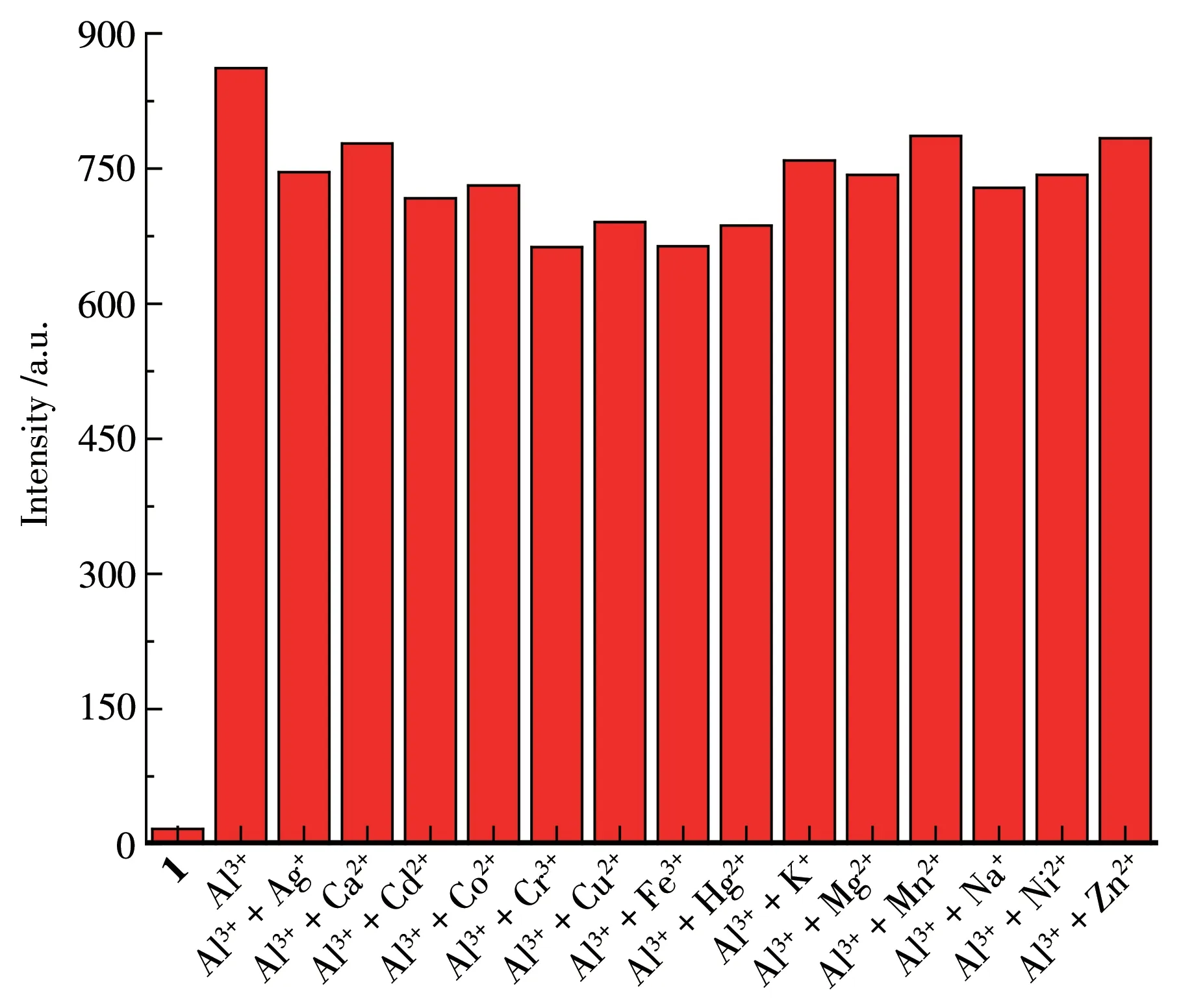
图4 竞争离子存在下探针1识别Al3+的荧光响应Fig.4 Fluorescence response of probe 1 to Al3+with competition ions
2.4 探针1对Al3+的识别机理
通过ESI-MS实验分析了探针1与Al3+的反应模式。取1 mg探针溶解在2 mL CH3OH溶液,加入Al(NO3)32 mg,混合20 min后进行ESI-MS测试。如图5a所示,1+Al3+在m/z321.120 6处出现了新峰,与[Al(1-H)(OH)]+(计算值321.117 9,1+Al3+)相对应。而m/z=335.137 0、349.110 1和417.098 9处的峰归属于溶剂化离子[Al(1-H)(OCH3)]+(计算值335.137 9)、[Al(1-H-NH2+OCH3)(OCH3)]+(计算值350.137 9)和[Al(1-H-NH2)(OCH3)(NO3)](计算值416.142 1)。
为了获得更多关于配合物的信息,我们进行了1H NMR测试。取5 mg探针溶于0.6 mL的DMSOd6中,再加入含5 mg Al(NO3)3的DMSO-d6溶液,等待20 min后进行1H NMR测试,谱图见图5b。随着Al3+的加入,1的OH质子峰消失,说明探针1的羟基脱氢与Al3+配位。同时,探针1的CH=N、NH2和Ar-H质子峰向低场区轻微位移,证实探针1分子中的亚氨基氮原子以及羰基氧原子参与了配位。根据以上实验结果,推断1通过ONO给体与Al3+结合,结合模式如图6所示。
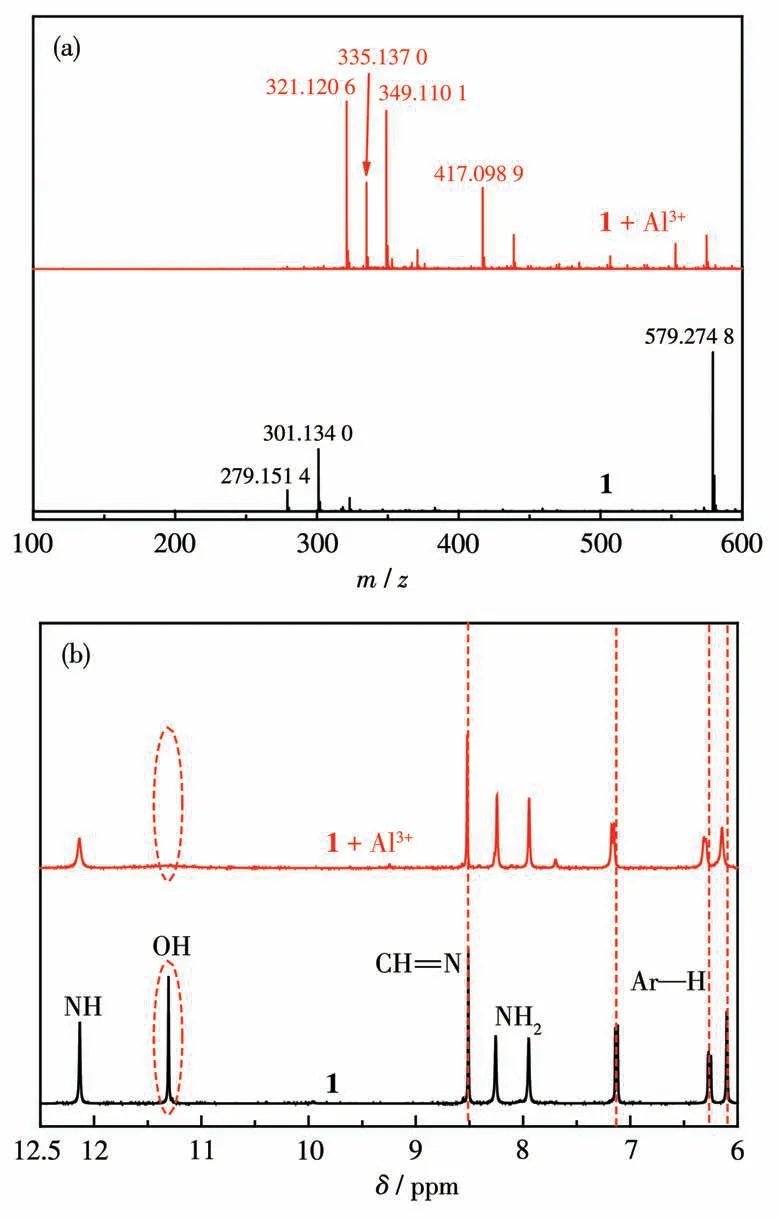
图5 探针1和1+Al3+的(a)ESI-MS谱图和(b)1H NMR谱图(DMSO-d6)Fig.5(a)ESI-MS and(b)1H NMR spectra(DMSO-d6)of 1 and 1+Al3+

图6 探针1与Al3+离子反应的可能机理Fig.6 Proposed reaction mechanism of 1 with Al3+ion
为了进一步研究探针1与Al3+的配位行为,我们用Gaussian 09程序包和B3LYP交换函数进行密度泛函理论(DFT)计算。如图7所示,探针1的HOMO集中在席夫碱部分,而LUMO主要位于吡嗪基上,这与其微弱的荧光相一致。探针1的C=N异构化在配合物中被抑制,这是导致荧光增强的原因。配合物形成后,电子云扩展到了包括HOMOs和LUMOs在内的整个探针中,这也支持了这一事实。1+Al3+的HOMO和LUMO之间的能量差为3.14 eV,低于探针1中HOMO和LUMO的能量差(3.56 eV)。结果表明,1与Al3+形成的配合物比1更稳定。
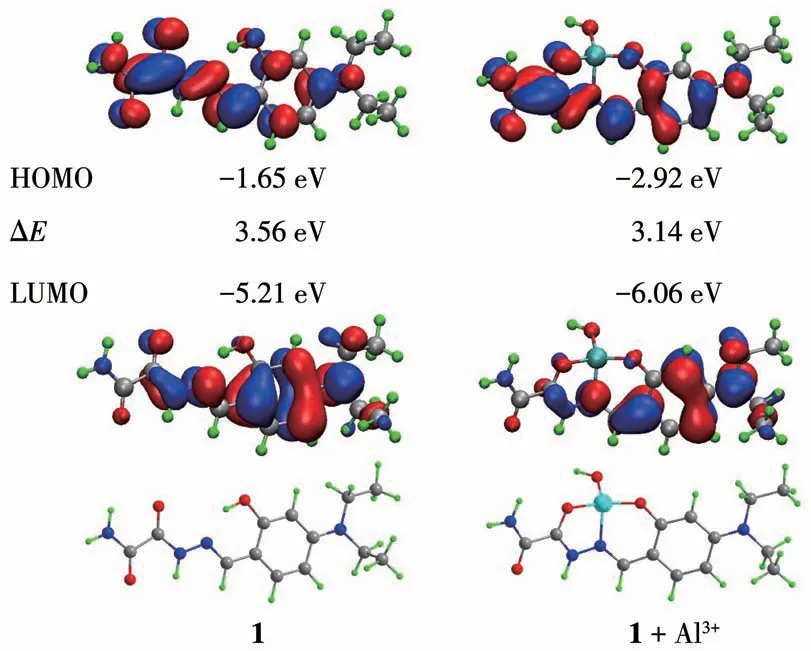
图7 探针1和1+Al3+的优化结构和分子轨道排布Fig.7 Optimized structures and HOMO/LUMO of 1 and 1+Al3+
2.5 探针1检测细胞中Al3+
为了评价探针1检测生物细胞中Al3+的性能,首先进行了探针1的细胞毒性实验。具体实验内容为将浓度为0~40 μmol·L-1的探针1分别孵育到Hela细胞中24 h,检测Hela细胞的存活率,如图8所示。实验结果表明,孵育24 h,探针1浓度为40 μmol·L-1时80%的细胞存活,说明探针1细胞毒性较低。
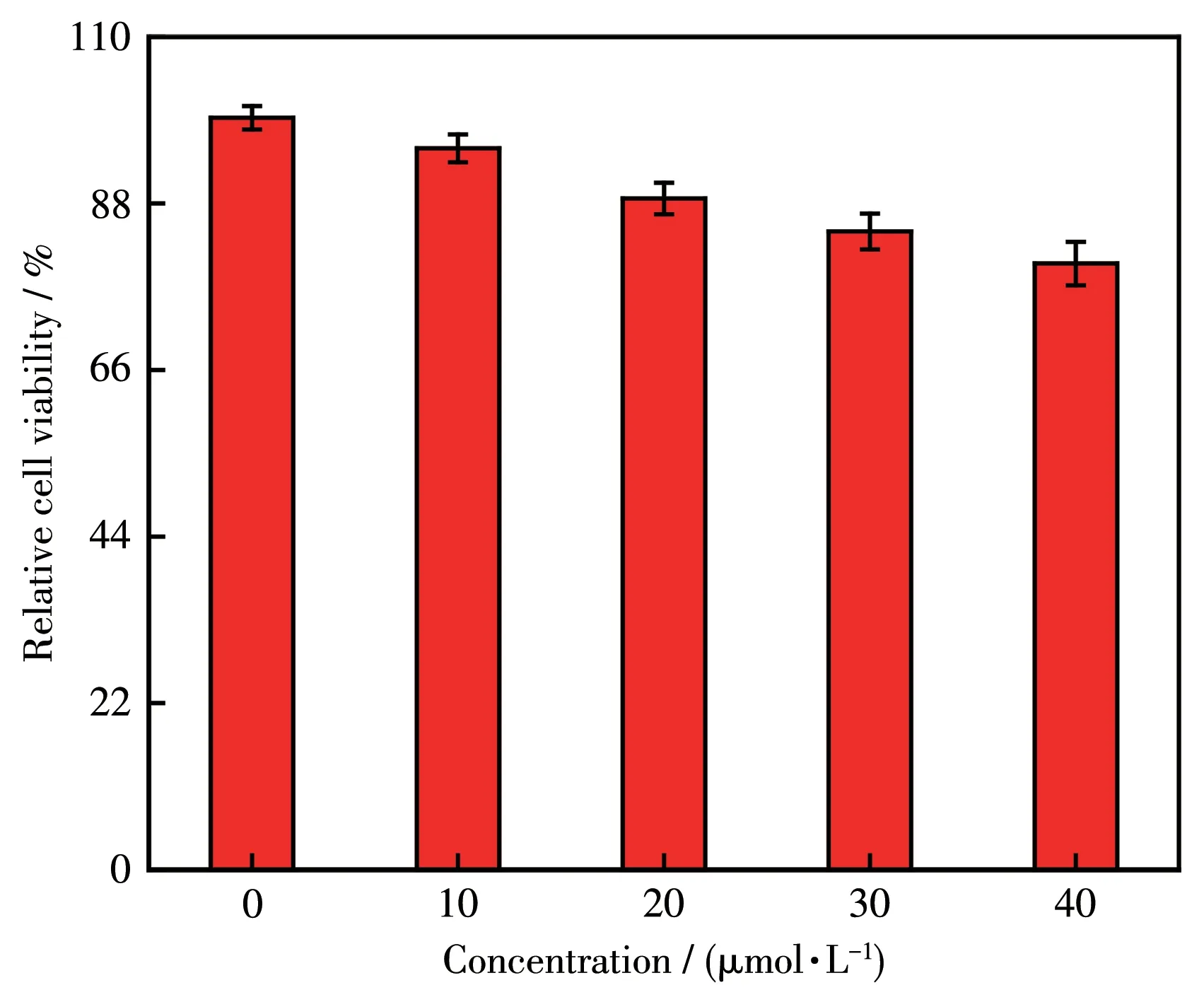
图8 MTT法测定的探针1对Hela细胞的毒性Fig.8 Toxicity of probe 1 to Hela cells using the MTT assay
之后,我们测试了探针1对细胞中Al3+的成像。37℃下,将10 μmol·L-1探针1与Hela细胞孵育30 min,绿色通道弱荧光(图9a);在相同的条件下补加10 μmol·L-1的Al3+,继续孵育30 min后Hela细胞内绿色通道荧光显著增强,如图9d所示。因此,探针1能够高效检测细胞中Al3+的存在。
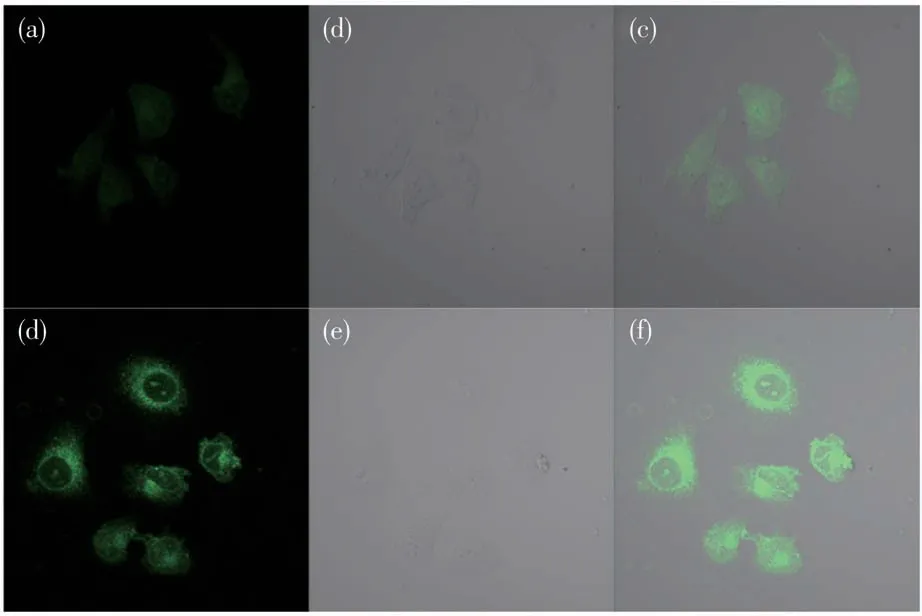
图9 Hela细胞共聚焦荧光图像:(a、b、c)37℃下,10 μmol·L-1探针1孵化Hela细胞30 min;(d、e、f)继续加入10 μmol·L-1 Al3+,37℃孵化该细胞30 minFig.9 Confocal fluorescence images of Hela cells:(a,b,c)Hela cells incubated with 10 μmol·L-1 of probe 1 for 30 min at 37℃;(d,e,f)the cells with probe 1 incubated with 10 μmol·L-1 Al3+for another 30 min at 37℃
3 结论
以4-(二乙氨基)水杨醛和奥肼缩合,合成了一种非常简单的席夫碱类荧光探针1,该探针对Al3+具有良好的识别作用,受其他金属离子干扰影响较弱。在DMSO/H2O(2/8,V/V,pH=7.40)溶液中形成配合物,可引起体系荧光增强,且使溶液颜色由无色变为蓝绿色,可以用于Al3+的裸眼识别检测。结合NMR研究表明,配位位点为1中的酚羟基氧原子、亚氨基氮原子以及羰基氧原子。所制备的席夫碱探针1合成简单、对Al3+选择性好、检测灵敏度高,并且能在细胞内实现Al3+的荧光成像,因此在传感器研制方面具有潜在的应用价值。

