乙型脑炎病毒疫苗研究进展
张福良,马圣明,邢月腾,曹金泽,刘 芳
(安阳工学院,河南 安阳 455000)
作为一种疫苗可预防的疾病,世卫组织建议在乙型脑炎构成公共卫生问题的所有国家(地区)进行常规免疫接种,并竭力实现最高的疫苗接种覆盖率。Amicizia等,Sunwoo等和Yang等的研究表明在成功开展了针对儿童的乙型脑炎疫苗接种的国家中,发病率显著下降[1-3]。实际上,Campbell等调查显示在建立了高质量疫苗接种程序的国家(例如日本和韩国)中,该疾病的发病率估计为每10万人0.003,而在疫苗接种覆盖率不足的地区(例如柬埔寨、印度尼西亚和马来西亚)发病率为每10万人中3.7[4]。目前全球范围内使用的乙脑疫苗主要有三种:鼠脑灭活疫苗、细胞灭活疫苗和乙脑减毒活疫苗。鼠脑灭活疫苗曾是生产最广泛、国际上应用最广的疫苗,但是由于担心疫苗的不良影响(包括急性扩散性脑脊髓炎)而不再使用。
1 鼠源性乙脑灭活疫苗
20世纪50年代日本成功研制了全球第一种乙型脑炎病毒鼠脑疫苗,系由JEV中山株(Nakayama strain)感染小鼠大脑而产生的灭活疫苗(JE-VAX; Biken Institute),也是目前惟一获得WHO批准并且商品化的人用乙型脑炎灭活疫苗。Heffelfinger等和Ishikawa等指出在几个亚洲国家的全国疫苗接种计划中实施以后可以产生大约90%防控效果,使得日本脑炎感染率明显减少[5-6]。1989年以来,又生产了另一种基于Beijing-1株的小鼠乙型脑炎病毒灭活疫苗,该疫苗可以引发更强和更广的保护性免疫应答。但这些疫苗也产生一些常见的不良反应,如红斑、肿胀、压痛、发热、头痛和头晕等,且被怀疑与严重急性弥漫性脑脊髓炎和超敏反应有关;此外由于生产成本高、缺乏长期免疫效果,在急需疫苗的贫困农村地区不实用,因而促使了更安全的疫苗的开发,例如灭活的Vero细胞培养衍生疫苗和减毒活疫苗。出于安全考虑,2005年日本政府暂时取消了使用灭活的小鼠脑灭活疫苗进行常规免疫的建议,同时建议新一代疫苗逐渐取代灭活的小鼠脑源性疫苗。
2 细胞源性乙脑灭活疫苗
通过更加严格的生产过程生产的细胞源性乙脑灭活疫苗已经取代组织灭活疫苗。迄今为止,已经生产了不同的细胞培养来源的灭活疫苗。其中,基于减毒乙型脑炎疫苗株SA 14-14-2适应Vero细胞生产的以氢氧化铝为佐剂、甲醛灭活的IC51疫苗(Valneva Scotland Limited生产,美国和欧洲命名为IXIARO®,澳大利亚和新西兰命名为JESPECT®)于2009年首次获得许可,并通过技术协议转让给Biological E Limited于2012年在印度以JEEV®的身份获得许可,此后在其他亚洲国家也获得许可。IXIARO®疫苗是唯一在美国和欧洲获得许可并可以购买的日本脑炎疫苗,已被批准用于2个月以上的儿童。初次接种疫苗采取间隔28天肌注两次,对于有疾病风险的成年人,建议在初次免疫后第二年内增加剂量,2个月至36个月的儿童剂量减半。
其他基于Vero细胞生产的灭活疫苗包括Beijing-1疫苗株灭活疫苗(Biken公司生产的JEBIK®V 和 Kaketsuken生产的 ENCEVAC®在日本获得许可)、Beijing P3株灭活疫苗(JEVAC™,辽宁成大生物技术有限公司生产,在中国获得许可)以及印度乙型脑炎病毒基因III型Kolar-821564XY株(JENVAC®,Bharat Biotech制造并在印度获得许可)。这些疫苗目前在国际上的使用分布有限,IC51疫苗(IXIARO®)已经获得有关安全性和免疫原性的大量数据。Roberts等对疫苗3期试验研究数据指出,IC51具有非常好的安全性,类似于安慰剂[7]。Erra在成人和儿童中的临床试验中还表明,接种两倍剂量IC51疫苗可诱导针对JEV基因型I-IV的高中和抗体滴度和高血清转化率[8]。Pato等研究表明在成年人中,初次免疫后观察到疫苗保护作用会逐渐下降,基础免疫1~2年后给予加强免疫可导致中和抗体滴度明显提升,并且加强免疫后6年以内> 95%的病例存在持续保护性免疫[9]。Okada等对JEBIK®V和ENCEVAC®疫苗的研究表明成人单剂注射后血清转化率为86.8%,三剂接种后儿童血清转化率为100%[10]。据Yun等报道,约有14%的病例发生了严重的不良事件,但与疫苗本身无关,只是发生了一次高热惊厥[11]。Liu 等指出在中国,1967年开始生产和使用基于仓鼠原代肾细胞(Primary hamster cell,PHK)培养生产的灭活疫苗,使用的是乙型脑炎病毒北京P3毒株,副作用相对较小且容易制造,疗效在76%到90%之间[12]。
3 SA 14-14-2减毒活疫苗
减毒活疫苗似乎真正给乙型脑炎病毒疫苗开发带来了广阔前景,因为活病毒颗粒建立疫苗免疫应答所需的病毒剂量更少,也使得疫苗价格更便宜,这使得乙型脑炎防控更容易。20世纪80年代,一种基于SA 14-14-2毒株的减毒活疫苗开始在中国以及随后在亚洲其他国家被开发并批准用于人类,其商品名为CD.JEVAX™(成都生物制品研究所,中国)。Yu等证明 SA 14-14-2减毒株被具有遗传稳定性、高度免疫原性,在小鼠中无神经毒力并且在蚊子中不能复制[13]。Gromowski等研究指出SA14-14-2毒株致弱的分子基础可能是E蛋白中的6个氨基酸和NS基因中的3个氨基酸突变造成[14]。
自从获得许可以来,已经有数百万人接种了减毒活SA 14-14-2疫苗,该疫苗已在中国广泛使用,根据国家疫苗接种计划的建议,该疫苗适用于8月龄的儿童,2岁时加强剂量接种。韩国(自1999年起)、尼泊尔(自2001年起)、印度(自2006年起)和泰国(自2007年起)也已推荐使用该疫苗。由于减毒SA 14-14-2活疫苗具有很高的免疫原性,因此一些国家在国家疫苗接种计划中加入了单一剂量的疫苗。
Torresi等指出在中国、尼泊尔和韩国的儿童中进行的临床试验表明,即使在单剂量接种后,这种减毒活疫苗也具有很高的免疫原性和功效,在中国成人和儿童中,血清转化率在94%至100%之间,功效为85~98%[15]。此外,Ohrr等证明对以前接受过两剂和三剂灭活的鼠脑灭活疫苗的儿童接种的SA 14-14-2减毒疫苗是安全的,可显著提高抗体水平[16]。
4 嵌合减毒活疫苗
一 种 名 为 IMOJEV®或JE-CV(Chimer VAX™-JE, Sanofi Pasteur, France)的基因工程减毒活疫苗,已于2010年首次注册并在多个国家获得了用于儿童和成人预防日本脑炎的许可证。该疫苗毒株是用SA 14-14-2疫苗株的prM-E基因替换了黄热病病毒(Yellow fever virus, YFV)疫苗株YFV-17D的相应基因。Guirakhoo和Monath等研究证实这种嵌合疫苗在遗传上稳定,在小鼠和非人类灵长类动物接种后可以诱导免疫保护[17-18]。Chokephaibulkit等进一步研究证明毒株致弱的分子基础是JEV SA 14-14-2毒株的E蛋白包含至少四个氨基酸残基的突变,这是病毒神经毒力表型所必需的[19]。
Feroldi等在对成人和儿童进行的几项II期和III期研究中证明了嵌合毒株的免疫原性和安全性,特别是疫苗免疫原性的随机对照III期研究表明,在接种后28天,成人和儿童单剂量接种这种嵌合疫苗诱导的血清转化率分别大于99%和95%。此外,当将嵌合疫苗作为一种强化疫苗接种之前已经接种过一次灭活疫苗或减毒疫苗的儿童时,乙脑嵌合疫苗是有效的。加强疫苗接种诱导的中和和交叉中和抗体对不同野生型的JEV基因型I-IV株具有保护作用,95.7%和97.9%的病例免疫后持续5年以上[20]。
5 其他疫苗
目前,几种候选疫苗仍处于研发的各个阶段,主要包括:重组蛋白疫苗、重组/嵌合病毒疫苗和DNA疫苗等。基本上,所有这些疫苗都含有JEV E糖蛋白,该蛋白具有大多数病毒中和表位,是较好的免疫原。
5.1 基于重组蛋白的乙型脑炎病毒疫苗
已知乙型脑炎病毒的E蛋白对于诸如受体结合和融合的各种功能很重要,并且能够诱导免疫保护。该蛋白质在不同的表达系统中以多种形式表达,在以小鼠为动物模型试验中中测试了E蛋白的免疫原性,其中,大肠杆菌和杆状病毒表达系统是常用于此目的的两种表达载体。
5.2 基于重组病毒的乙型脑炎病毒疫苗
重组病毒在疫苗开发中很重要,已经使用了许多重组病毒,每个重组病毒都有自己独特的功能。能够同时诱导体液免疫应答和细胞免疫应答是所有重组/嵌合疫苗的共同特征。在重组病毒策略中,外源性抗原以类似于自然感染的方式被宿主免疫系统呈递并加工,许多病毒已用于生产乙型脑炎病毒疫苗,包括痘病毒、麻疹病毒、腺病毒、黄热病毒。
5.3 DNA疫苗
近年来,质粒DNA疫苗由于能够诱导产生广泛的免疫应答而受到了广泛关注,包括诱导抗体产生、产生CD4+辅佐细胞和CD8+CTL以及对一系列病毒感染提供保护。此外,质粒DNA疫苗也是有效的、安全的、且易于生产,并且不会干扰其他黄病毒或疫苗载体已经存在的抗体。在质粒DNA疫苗免疫中,将编码有效抗原或其部分的DNA置于细菌质粒之中,该质粒在强真核启动子的控制下通过不同的途径(如肌肉或皮下)给药,然后将质粒内吞,由MHC-I类分子进行内源性抗原呈递产生CD8+ CTL反应;除此之外,APC对可溶性抗原的摄取还导致通过MHC-II类分子呈递产生CD4+Th反应。在过去的几年中,已经开发出使用结构和非结构基因的针对乙型脑炎病毒的DNA疫苗,并已在具有不同功效的动物模型中对其进行了评估。
1998年首个乙型脑炎病毒质粒DNA疫苗产生,命名为pcDNA3JEME,其中整合了病毒的E基因和PrM基因,Konishi等证明免疫小鼠后产生了中和抗体,其中70%的小鼠在致死性挑战后存活下来,CTL和B细胞反应均被激活,并在免疫小鼠的脾细胞中持续长达6周[21]。后来,Chai等进一步研究发现单次肌肉注射可提供保护作用,从而保护小鼠免受致命性攻击[22]。Ashok等评估缺少信号肽的编码E蛋白的DNA疫苗的免疫原性实验表明,在不产生抗病毒抗体的情况下,可以保护免疫复合物免受攻击[23]。Kaur等进一步试验表明颗粒形式的质粒DNA可以增强的小鼠免疫原性[24]。
尽管各种针对乙型脑炎病毒的疫苗开发方法已经进行了尝试,这些针对乙型脑炎病毒的新型疫苗虽然在实验室中显示出了良好前景,但遗憾的是,它们在临床中均尚未成功,因此,还需要对此进行进一步深入、详尽的评价。
目前,乙型脑炎病毒疫苗接种策略和深入的研究是未来开发成功的乙型脑炎病毒疫苗所需要的,Kumar等提出了乙型脑炎病毒疫苗开发战略流程(图1)[25]。此外,还需要广泛的关注和探索一些新的候选疫苗,迫切需要开发新一代疫苗,以有效地防控乙型脑炎。
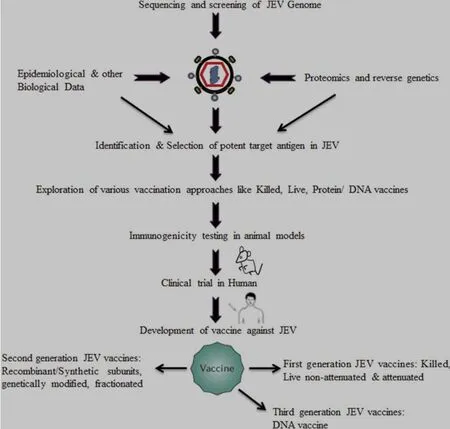
图1 JEV疫苗开发战略流程[25]

