国产利妥昔单抗治疗弥漫大B细胞淋巴瘤的临床疗效和安全性
王倩 杨宇娟 张慈现 付杰
221000 江苏省徐州市中心医院血液科,江苏徐州
弥漫大B细胞淋巴瘤是成人非霍奇金淋巴瘤中发病率最高的类型[1]。1997年,原研利妥昔单抗被美国食品药物管理局(FDA)批准用于弥漫大B 细胞淋巴瘤的一线治疗,与环磷酰胺、蒽环类、长春碱类和糖皮质激素联用,可显著提高治疗效果[2]。原研利妥昔单抗价格昂贵,在国内难以推广,仿制品的上市为弥漫大B细胞淋巴瘤患者提供了更多的治疗选择。本研究回顾性分析国产利妥昔单抗治疗弥漫大B细胞淋巴瘤的临床疗效和安全性,报告如下。
资料与方法
回顾性分析2019年5月-2021年10月江苏省徐州市中心医院血液科收治的43 例弥漫大B 细胞淋巴瘤患者的临床资料,诊断标准参考2016年WHO 血液淋巴瘤分类诊断标准和《中国弥漫大B 细胞淋巴瘤诊断与治疗指南(2013 版)》,采用2014年Lugano 分期标准,预后评估采用国际预后指数评分(IPI)[3]。根据治疗药物不同分为观察组(21例)与对照组(22例)。两组间临床资料比较,差异无统计学意义(P>0.05),具有可比性。见表1。本研究经过医院伦理委员会批准。
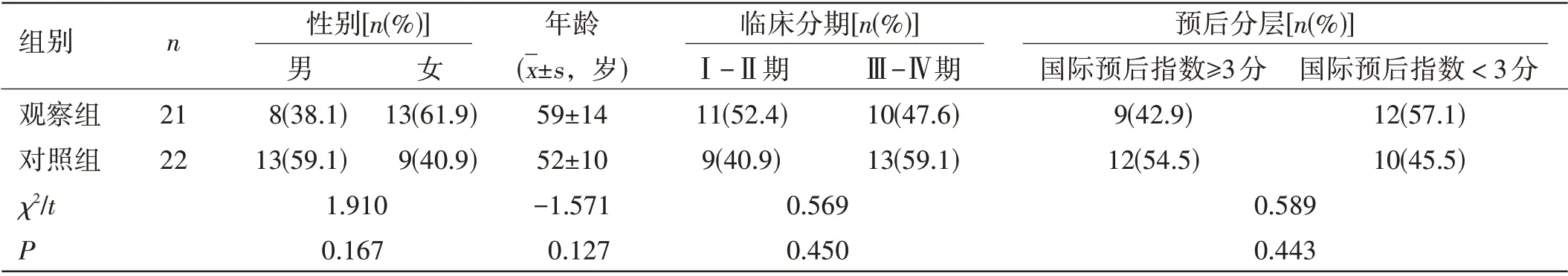
表1 两组患者临床资料比较
纳入标准:①患者经组织病理学、影像学检查确诊为弥漫大B 细胞淋巴瘤;②患者有联合化疗指征;③患者无过敏史;④患者及其家属均知情同意本研究,并签署研究知情同意书。
排除标准:①严重心、肝、肾等脏器功能不全者;②合并严重心脑血管疾病者;③合并其他部位恶性肿瘤者;④合并精神类疾病者;⑤妊娠及哺乳期妇女。
方法:两组患者均采用R/H-CHOP 方案(原研/国产利妥昔单抗、环磷酰胺、蒽环类、长春碱类、糖皮质激素)治疗。环磷酰胺(生产厂家:江苏恒瑞医药股份有限公司;批准文号:国药准字H32020856)静脉滴注,750 mg/m2,第1 天;长春新碱(生产厂家:浙江海正药业股份有限公司;批准文号:国药准字H20043326)静脉滴注,1.4 mg/m2,第1 天;表柔比星(生产厂家:浙江海正药业股份有限公司;批准文号:国药准字H20183145)静脉滴注,60 mg/m2,第1 天;泼尼松(生产厂家:天津力生制药股份有限公司;批准文号:国药准字H12020123)口服60 mg/m2,第1~5 天。观察组使用国产利妥昔单抗(生产厂家:上海复宏汉霖生物制药有限公司;批准文号:国药准字S20190021)静脉滴注,375 mg/m2;对照组使用原研利妥昔单抗(生产厂家:Roche Diagnostics GmbH;批准文号:国药准字SJ20170002)静脉滴注,375 mg/m2。CHOP 方案前1 d。静脉滴注利妥昔单抗时应进行心电监测,若无输液反应,每30 min 可增加100 mg 静脉滴注,滴注前应提前使用解热镇痛药和抗组胺药物,如出现严重不良反应则需暂停滴注,甚至停药。每21 d 为1 个疗程。本研究患者均治疗2~8个疗程。
观察指标:①治疗效果,疗效评价采用2014年Lugano 会议修订标准,每2~4 个疗程后进行影像学检查以评价疗效。疗效评价标准包括完全缓解(CR)、部分缓解(PR)、疾病稳定(SD)、疾病进展(PD)。客观缓解率(ORR)=(CR+PR)例数/总例数×100%。②安全性,根据NCI/NIH 常见毒性标准3.0 版本进行分级,不良反应包括血液学不良反应及非血液学不良反应,血液学不良反应主要为血小板减少和白细胞减少,非血液学不良反应包括转氨酶升高、胃肠道反应、感染、发热。
统计学方法:数据均用SPSS 20.0 统计学软件予以处理;计数资料以[n(%)]表示,比较采用χ2检验;计量资料以(±s)表示,比较采用t检验;P<0.05为差异有统计学意义。
结 果
两组患者治疗效果比较:两组患者ORR 比较,差异无统计学意义(P>0.05)。见表2。
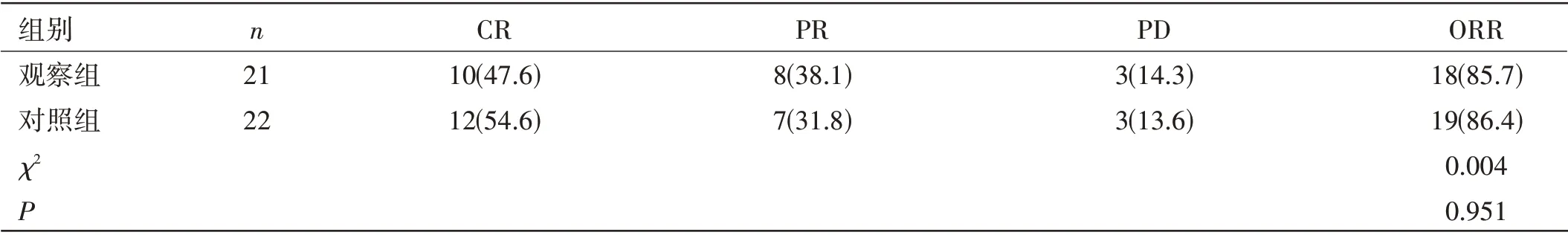
表2 两组患者治疗效果比较[n(%)]
两组患者安全性比较:两组患者白细胞减少、血小板减少、转氨酶升高、胃肠道反应、感染、发热发生率比较,差异无统计学意义(P>0.05)。见表3。
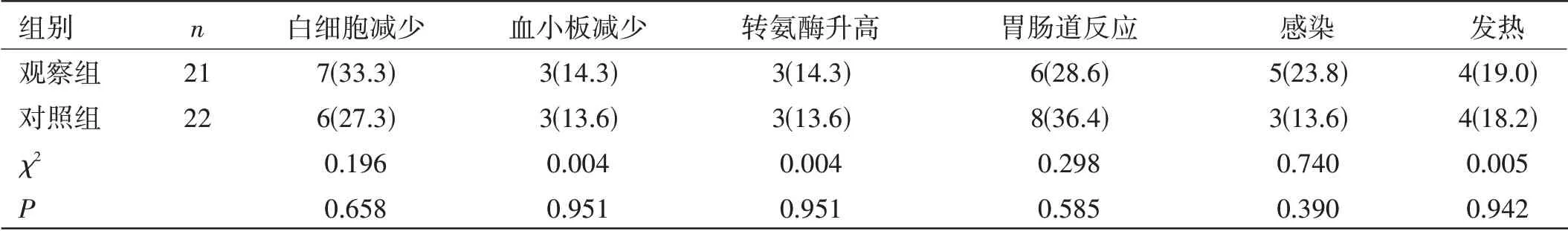
表3 两组患者不良反应发生情况比较[n(%)]
讨 论
弥漫大B细胞淋巴瘤在成人非霍奇金淋巴瘤中约占30%~40%,多数为原发性弥漫大B 细胞淋巴瘤,也有部分由惰性淋巴瘤进展或转化而来[4-5]。利妥昔单抗是一种人鼠嵌合型抗CD20 单克隆抗体,通过补体依赖的细胞毒作用和抗体依赖的细胞毒作用有效清除恶性B 细胞以达疗效。R-CHOP 是公认治疗弥漫大B 细胞淋巴瘤患者的一线方案,多项临床试验表明,该方案可显著提高患者的治疗效果[6-8]。
汉利康在上市前与美罗华抗进行了一项Ⅲ期临床试验,共有400 例弥漫大B 细胞淋巴瘤患者纳入研究并被随机分配至国产组和原研组,均接受6周期的利妥昔单抗联合CHOP 方案化疗,结果表明两组的疗效及安全性差异均无统计学意义。但是,在真实世界中尚缺乏对国产利妥昔单抗疗效和安全性的临床研究[9-10]。本研究共纳入43 例患者,其中21 例为国产组,22 例为原研组,采用R/H-CHOP 方案化疗,结果表明两组患者均获得了良好的疗效,差异无统计学意义,与报告数据类似。
R-CHOP 方案使得50%~60%的患者在化疗后获得较好的疗效,但仍有部分患者预后相对较差。Chiappella A 等[11]临床实验结果显示,自体造血干细胞移植能提高初治高危弥漫大B 细胞淋巴瘤患者2年的无进展生存期(PFS)。王希等[12]研究表明,增强免疫化疗序贯自体移植能提高年轻高危患者的5年PFS 和总生存期。本研究中亦有4例患者至2022年4月已完成4 疗程R-CHOP 方案,3 例达CR,1 例为PR,下一步拟行自体造血干细胞移植。
虽然R-CHOP 方案疗效肯定,但在治疗过程中仍有患者发生了不良反应,本研究结果显示,国产利妥昔单抗同样具有良好的安全性,两组差异无统计学意义,未出现因严重不良反应而中断化疗者。
我国目前仍属于发展中国家,本研究显示,国产利妥昔单抗治疗弥漫大B细胞淋巴瘤的疗效与安全性良好,与原研产品相近,且价格较低,为患者提供了更多的治疗选择。然而,本研究的观察时间尚短,病例数尚少,仍需进一步累积更多病例及长期随访以观察疗效。

